Carcinoma de Orofaringe na Radioterapia Moderna
O delineamento de volume alvo no carcinoma de orofaringe exige domínio preciso da anatomia regional, dos padrões de disseminação tumoral e do status do HPV. A orofaringe abrange quatro subsítios — tonsilas, base de língua, palato mole e parede faríngea posterior — e a grande maioria dos tumores que ali surgem são carcinomas de células escamosas. O vírus HPV transformou o panorama desta doença: tumores HPV-positivos apresentam prognóstico significativamente superior ao dos HPV-negativos, o que levou a revisões no estadiamento AJCC com sistemas separados para cada grupo.
Apesar da relevância prognóstica do HPV, a de-escalação terapêutica fora de ensaios clínicos não é recomendada. Estudos como o NRG Oncology RTOG 1016 e o De-ESCALaTE HPV confirmaram que substituir cisplatina por cetuximabe em pacientes HPV-positivos resultou em desfechos inferiores. O estudo NRG-HN002, por sua vez, avaliou pacientes p16-positivos não tabagistas com doença locorregionalmente avançada, explorando abordagens de de-escalação em cenários muito selecionados. Na prática, a testagem viral deve ser realizada em todos os pacientes com carcinoma de orofaringe, mas o tratamento padrão segue sendo radioterapia com quimioterapia concomitante baseada em cisplatina. Para uma visão ampla sobre volumes e campos em diferentes localizações, confira nosso guia completo sobre delineamento de volume alvo.
Anatomia e Padrões de Disseminação da Orofaringe
A orofaringe é um espaço cuboide delimitado anteriormente pela cavidade oral, superiormente pela nasofaringe e inferiormente pela laringe e hipofaringe. Consiste em quatro subsítios: tonsilas, base de língua, palato mole e parede faríngea, com a maioria dos casos originando-se nas tonsilas e na base de língua. Uma característica que torna o planejamento da radioterapia particularmente desafiador é a rica drenagem linfática da região: linfonodos cervicais estão comumente envolvidos já na apresentação inicial, mesmo em tumores de estadio T precoce.
A disseminação submucosa é frequente e segue padrões previsíveis conforme o subsítio. Tumores tonsilares podem estender-se anterolateralmente ao longo do músculo constritor faríngeo em direção ao trígono retromolar e, em estádios avançados, invadir as lâminas pterigoides. Já os tumores de base de língua tendem a progredir anteriormente em direção à língua oral, inferiormente para o sulco glossotonsilar, valécula e espaço pré-epiglótico. Tumores do palato mole podem crescer superiormente em direção à nasofaringe e às lâminas pterigoides, enquanto tumores da parede faríngea apresentam risco de lesões skip, exigindo margens generosas tanto cranial quanto caudalmente. Esses padrões de disseminação determinam diretamente o desenho do CTV subclínico.
Investigação Diagnóstica Relevante para o Delineamento
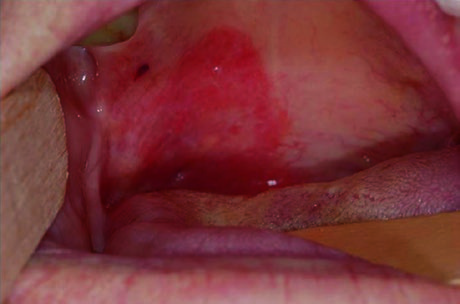
O delineamento do GTV primário é mais bem definido pela combinação de exames de imagem e exame físico. A extensão mucosa e superficial do tumor é avaliada por inspeção visual, palpação e nasofibrolaringoscopia. Registros fotográficos no momento da consulta ou simulação são valiosos, pois documentam extensão mucosa que pode não aparecer nos exames de imagem — especialmente envolvimento do palato mole e extensão para linha média, como ilustrado na figura clínica acima.
A TC contrastada continua sendo o principal exame de diagnóstico, mas a RM e o PET/CT possuem papéis bem definidos e complementares:
- RM T1 pré-contraste: ideal para avaliação de planos gordurosos e sinal da medula óssea, ajudando a distinguir tumor de tecido normal.
- RM T1 pós-contraste: essencial para delinear a extensão anterior de tumores de base de língua e avaliar invasão perineural. Sem essa sequência, a extensão anterior pode ser subestimada em vários milímetros.
- RM T2 fat-sat: avalia linfonodos retrofaríngeos (RP) e extensão em tecido mole nos espaços parafaríngeo e pré-epiglótico. Os linfonodos RP são notoriamente difíceis de avaliar apenas por TC.
- FDG-PET/CT: fornece informação metabólica complementar, podendo identificar extensão tumoral não vista na TC ou RM. Contudo, apresenta baixa resolução espacial e sensibilidade limitada para metástases linfonodais de pequeno volume — um linfonodo suspeito sem captação de FDG não deve ser considerado necessariamente livre de doença. Essa limitação é particularmente relevante na avaliação dos linfonodos retrofaríngeos e de pequenos linfonodos do nível II alto.
Simulação e Localização Diária
O paciente deve ser posicionado em decúbito dorsal com extensão cervical, utilizando apoio de cabeça e máscara termoplástica de 5 pontos (Aquaplast) que imobilize cabeça, pescoço e ombros. Mordedor ou protetor bucal pode ser inserido para reprodutibilidade diária e afastamento do palato da dose. Os pacientes são orientados a não deglutir durante a aquisição da tomografia e durante o tratamento, já que movimentos de deglutição alteram a posição da orofaringe em relação à imobilização.
A simulação por TC com contraste intravenoso utiliza espessura de corte ≤ 3 mm, cobrindo desde o vértice do crânio até a carina. Essa extensão generosa é necessária para englobar tanto a possível extensão cranial do tumor quanto os campos cervicais baixos. O isocentro é posicionado tipicamente nas cartilagens aritenoides, facilitando o casamento de um campo anteroposterior cervical baixo convencional com os campos de IMRT quando essa estratégia for adotada.
Imagens de RM e PET podem ser registradas ou fusionadas com a TC de simulação. Usar a máscara de imobilização durante o PET melhora a acurácia da fusão, embora durante a RM isso possa impossibilitar o uso de bobinas dedicadas de cabeça e pescoço. Na prática do Memorial Sloan Kettering Cancer Center (MSKCC), a verificação diária de imagem é feita com kV 2D e cone-beam CT diário montados no acelerador linear. Alternativas aceitáveis incluem cone-beam semanal com kV diário, imagens kV ortogonais (ExacTrac) ou TC por MV (TomoTherapy).
Esquemas de Dose IMRT para Orofaringe
Existem vários esquemas de dose válidos. Na abordagem sequencial preferida no MSKCC, a dose total na doença macroscópica é de 70 Gy. A escolha entre as técnicas depende do status HPV, da extensão da doença e da disponibilidade de quimioterapia concomitante.
Para tumores HPV-positivos (técnica sequencial), as regiões subclínicas recebem 30 Gy em frações de 2 Gy na primeira fase. A região subclínica é rigorosamente avaliada com RM, TC contrastada e PET/CT para confirmar ausência de doença macroscópica antes de prosseguir. Segue-se cone-down para a doença macroscópica com 40 Gy em frações de 2 Gy, totalizando 70 Gy. Quando um campo cervical baixo AP é casado aos campos de IMRT, a região cervical baixa recebe 30 Gy em frações de 2 Gy. Conforme publicado por Tsai et al. do MSKCC, essa abordagem de dose eletiva reduzida baseia-se na avaliação cuidadosa das regiões subclínicas por múltiplas modalidades de imagem.
Para tumores HPV-negativos (técnica sequencial), a fase inicial entrega 60 Gy em frações de 2 Gy à doença macroscópica, com 54 Gy simultâneos em frações de 1,8 Gy a todas as regiões subclínicas. Segue-se cone-down de 10 Gy em frações de 2 Gy à doença macroscópica, completando os 70 Gy. O campo cervical baixo casado recebe 50 Gy em frações de 2 Gy. Note que as doses eletivas neste cenário são consideravelmente maiores que no protocolo HPV-positivo — reflexo do comportamento biológico mais agressivo desses tumores. Doses eletivas reduzidas só devem ser consideradas quando combinadas com quimioterapia concomitante baseada em cisplatina.
O boost integrado simultâneo (SIB) é outra técnica amplamente utilizada: 70 Gy (2 Gy/fração) na doença macroscópica, 56 Gy (1,6 Gy/fração) nas regiões subclínicas de alto risco e 50–52,5 Gy (1,43–1,5 Gy/fração) nas de baixo risco. Esta abordagem deve ser empregada somente com quimioterapia concomitante, pois as doses por fração reduzidas nas regiões subclínicas dependem do efeito radiossensibilizador da quimioterapia para controle adequado da doença microscópica. Protocolos como RTOG 0022 (hipofracionamento acelerado) e RTOG 1016 oferecem esquemas fracionados alternativos.
Volumes Alvo para Doença Macroscópica
O delineamento dos volumes alvo para doença macroscópica segue diretrizes bem definidas. O GTV inclui toda a doença macroscópica visível ao exame clínico e de imagem. Para o sítio primário, isso representa o tumor conforme visualizado na TC, RM e PET/CT. Para linfonodos, todos os suspeitos são incluídos: maiores que 1 cm no menor eixo, necróticos, com realce ou captação de FDG. Existe flexibilidade para linfonodos borderline — aqueles apenas marginalmente suspeitos podem receber dose intermediária de 60–66 Gy em vez dos 70 Gy da doença macroscópica franca.
| Volume | Definição e Descrição |
|---|---|
| GTV70 | Primário: toda a doença macroscópica definida por exame clínico e imagem. Linfonodos: todos os suspeitos (>1 cm, necróticos, com realce ou FDG-ávidos). Linfonodos borderline podem receber dose menor (60–66 Gy). |
| CTV70 | Em áreas de excelente visualização, GTV pode igualar-se ao CTV (sem margem adicional). Em situações de incerteza quanto à extensão tumoral, CTV = GTV + 3–5 mm. |
| PTV70 | CTV + 3–5 mm, dependendo da acurácia do setup diário e da disponibilidade de guia por imagem (CBCT diário permite margens menores). |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 2.1)
A decisão entre margem zero e margem de 3–5 mm do GTV para o CTV70 depende fundamentalmente da qualidade da visualização tumoral. Em tumores de tonsila bem definidos na TC contrastada, por exemplo, uma expansão mínima pode ser suficiente. Já em tumores de base de língua com extensão anterior mal definida, os 5 mm completos são prudentes, e a fusão com RM T1 pós-contraste torna-se indispensável.
Volumes Alvo para Doença Subclínica
Como diretriz geral, o CTV do sítio primário deve englobar o GTV + 1 cm, descontando barreiras anatômicas à disseminação como ar, osso e pele. Esse princípio simples se desdobra em orientações específicas para cada subsítio, baseadas nos padrões de disseminação descritos anteriormente.
| Subsítio / Volume | Definição e Descrição |
|---|---|
| Tonsila — CTV subclínico | Margem adequada de ~1 cm ao tumor primário. Inclusão altamente recomendada das lâminas pterigoides em doença avançada. Considerar cobertura do trígono retromolar ipsilateral se houver suspeita de disseminação anterolateral pelo constritor faríngeo. |
| Base de língua — CTV subclínico | Sulco glossotonsilar, valécula e espaço pré-epiglótico. Margem mucosa de pelo menos 1 cm ao redor do tumor; anteriormente pode estender-se à língua oral. RM é essencial para delineamento da extensão anterior do tumor. |
| Palato mole — CTV subclínico | Palato mole inteiro, aspecto superior dos pilares tonsilares + fossa, nasofaringe adjacente superiormente até as lâminas pterigoides. Em tumores avançados, considerar fossa pterigopalatina; se envolvida, é necessária avaliação de base de crânio por RM. Cobertura anterior adequada pode exigir parte do palato duro. |
| Parede faríngea — CTV subclínico | Margens superior e inferior generosas dado o risco de lesões skip. Em tumores avançados, considerar extensão do CTV cranialmente para nasofaringe e caudalmente para hipofaringe. |
| Linfonodos cervicais eletivos | Regiões linfonodais podem receber 54 Gy (1,8 Gy/fx), 54,12 Gy (1,64 Gy/fx), 56 Gy (1,6 Gy/fx) ou 59,4 Gy (1,8 Gy/fx) conforme alto ou baixo risco. Pescoço N0: níveis II–IV bilaterais e retrofaríngeos laterais; no MSKCC, IB e V não são tratados rotineiramente exceto se macroscopicamente envolvidos (exceção: extensão para cavidade oral justifica IB). Pescoço N+: retrofaríngeos e retroestiloides até a base do crânio; linfonodos baixos macroscópicos: considerar cobertura supraclavicular. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 2.2)
O manejo da cobertura linfonodal merece atenção particular. Para tumores T1–T2 N0–N1 tonsilares bem lateralizados, sem extensão para base de língua ou palato mole, o tratamento ipsilateral é aceitável. Esse cenário é detalhado a seguir.
Tratamento Ipsilateral de Tonsilas Bem Lateralizadas
Para tumores tonsilares T1–T2, N0–N1, bem lateralizados (pelo menos 1 cm lateral à linha média), sem extensão para base de língua ou palato mole, o tratamento unilateral do pescoço é aceitável. A localização bem lateral torna o risco de drenagem linfática contralateral suficientemente baixo para justificar a omissão do pescoço oposto. Nestes casos, a extensão superior da cobertura para o pescoço N-negativo pode iniciar no processo transverso de C1 ou quando o ventre posterior do digástrico começa a cruzar a veia jugular interna.
Na prática do MSKCC, independentemente do estádio, a região subclínica ipsilateral em tumores tonsilares quase sempre se estende superiormente para incluir a lâmina pterigoide ipsilateral. Essa abordagem garante cobertura adequada contra disseminação superior oculta, mesmo em casos aparentemente confinados à tonsila. Além disso, o CTV subclínico inclui a base de língua ipsilateral e o palato mole ipsilateral, respeitando a anatomia de drenagem linfática da fossa tonsilar.
No lado N-positivo, a cobertura estende-se até a base do crânio, incluindo os linfonodos retrofaríngeos e retroestiloides. Essa extensão é fundamental porque a presença de doença linfonodal macroscópica aumenta substancialmente o risco de disseminação para estações linfonodais mais craniais. Quando o tumor cruza a linha média na língua oral, a cobertura bilateral do nível IB deve ser considerada, dado o padrão de drenagem linfática cruzada nessa região. Em contrapartida, no pescoço N-negativo, o MSKCC não inclui rotineiramente o nível IB, a menos que haja extensão macroscópica para a cavidade oral.
Exemplos Clínicos Representativos
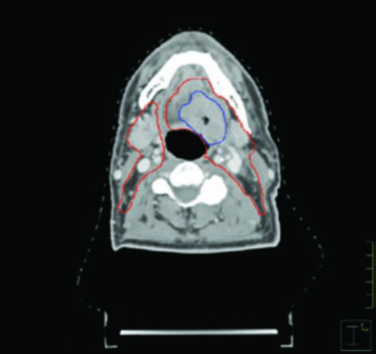
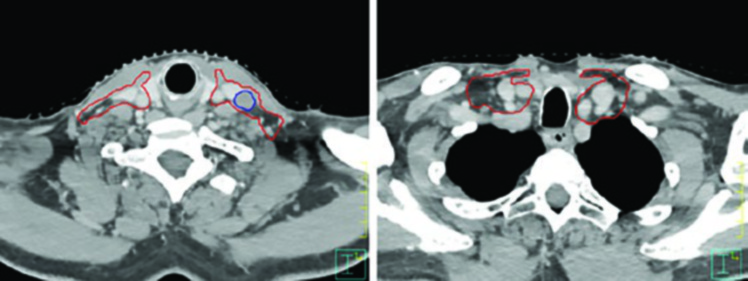
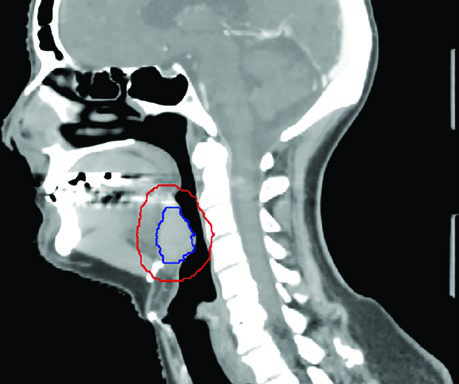
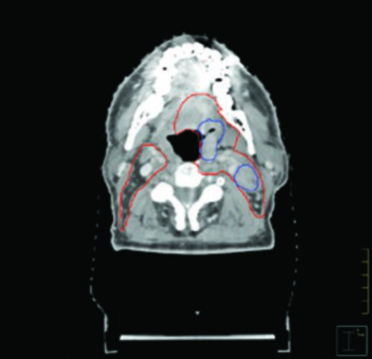
As figuras deste capítulo ilustram casos reais que exemplificam os princípios de delineamento discutidos. O caso de carcinoma tonsilar HPV-negativo cT4N2 demonstra a necessidade de cobertura até as lâminas pterigoides e inclusão do nível IB ipsilateral por invasão da língua oral. Note como o GTV (azul) e o CTV (vermelho) se adaptam às barreiras anatômicas, respeitando osso e ar enquanto se expandem generosamente em direção aos tecidos moles.
O caso de base de língua HPV-positivo cT4N1 ilustra a cobertura até a base do crânio no lado N-positivo e a extensão do CTV para considerar cobertura do nível IB bilateral quando o tumor cruza a linha média. A visão sagital demonstra de forma particularmente clara a importância da cobertura do espaço pré-epiglótico nos tumores de base de língua — uma área frequentemente subestimada por planejadores menos experientes.
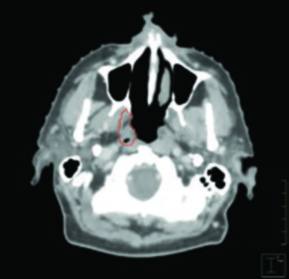
Já o caso de carcinoma tonsilar HPV-positivo cT2N0 tratado unilateralmente mostra como, mesmo no cenário de tratamento ipsilateral, a cobertura se estende superiormente até a lâmina pterigoide ipsilateral. A cobertura linfonodal inicia no processo transverso de C1, englobando a base de língua e o palato mole ipsilaterais sem cruzar a linha média.
Considerações Práticas no Planejamento
A seleção do esquema fracionado e da técnica de tratamento depende de múltiplos fatores clínicos e logísticos. O boost integrado simultâneo oferece a vantagem operacional de tratar em uma única fase, reduzindo o tempo total de tratamento e simplificando a logística de planejamento. Porém, exige atenção redobrada à dose por fração nas regiões subclínicas — as doses de 1,6 Gy e 1,43–1,5 Gy por fração são biologicamente menos eficazes que as frações convencionais de 1,8–2 Gy, dependendo da radiossensiblização pela quimioterapia para compensar. A técnica sequencial, por outro lado, permite avaliar a resposta durante o tratamento e ajustar o volume do cone-down com base em imagens intermediárias.
Na avaliação dos linfonodos suspeitos, a decisão entre prescrever 70 Gy ou uma dose intermediária (60–66 Gy) depende do grau de suspeita. Linfonodos francamente positivos — necróticos, com extensão extracapsular ou fortemente captantes — recebem dose plena. Aqueles borderline em tamanho ou captação podem receber doses intermediárias. Essa estratégia permite reduzir a toxicidade nas estruturas adjacentes sem comprometer o controle local.
A fusão de imagens multimodalidade merece atenção especial. O PET realizado com máscara de imobilização melhora a precisão da fusão com a TC de simulação, mas a RM com máscara pode restringir o uso de bobinas dedicadas, comprometendo a qualidade da imagem justamente onde ela é mais necessária. Na minha experiência, a solução mais prática é realizar a RM sem máscara usando bobina dedicada e registrar as imagens com base em referências anatômicas, aceitando uma incerteza ligeiramente maior na fusão em troca de resolução superior nos tecidos moles da orofaringe.
Artigos sobre subsítios adjacentes complementam esta discussão com fronteiras anatômicas e volumes compartilhados: confira o delineamento em nasofaringe, o câncer de laringe, a hipofaringe e o câncer de cavidade oral — todas localizações que compartilham drenagem linfática e podem afetar decisões de cobertura no carcinoma de orofaringe.


![Imagem fundida PET/TC com captação de [89Zr]girentuximab em massa renal posterior](https://rtmedical.com.br/wp-content/uploads/2026/05/article10_pet-600x403.jpg)