Carcinoma de Orofaringe en la Radioterapia Actual
La delineación del volumen blanco en el carcinoma de orofaringe requiere un conocimiento preciso de la anatomía regional, los patrones de diseminación tumoral y el estado del VPH. La orofaringe comprende cuatro subsitios — amígdalas, base de lengua, paladar blando y pared faríngea posterior — y la gran mayoría de los tumores son carcinomas de células escamosas. El virus del papiloma humano ha transformado radicalmente el panorama de esta enfermedad: los tumores VPH-positivos presentan un pronóstico significativamente superior, lo que llevó al American Joint Committee on Cancer a establecer sistemas de estadificación separados para cada grupo.
A pesar de la importancia pronóstica del VPH, la de-escalación terapéutica fuera de ensayos clínicos no está recomendada. Los estudios NRG Oncology RTOG 1016 y De-ESCALaTE HPV demostraron que sustituir cisplatino por cetuximab en pacientes VPH-positivos resultó en desenlaces inferiores. El estudio NRG-HN002 exploró la de-escalación en una población altamente seleccionada de pacientes p16-positivos no fumadores con enfermedad locorregionalmente avanzada. En la práctica habitual, la determinación viral debe realizarse en todos los pacientes con carcinoma orofaríngeo, pero el tratamiento estándar sigue siendo la radioterapia con quimioterapia concomitante basada en cisplatino. Para una visión global sobre volúmenes y campos en distintas localizaciones, consulte nuestra guía completa sobre delineación del volumen blanco.
Anatomía y Patrones de Diseminación
La orofaringe es un espacio cuboidal limitado anteriormente por la cavidad oral, superiormente por la nasofaringe e inferiormente por la laringe y la hipofaringe. Se compone de cuatro subsitios: amígdalas, base de lengua, paladar blando y pared faríngea, con la mayoría de los casos originándose en las amígdalas y la base de lengua. Lo que hace que la planificación de radioterapia sea particularmente exigente es el rico drenaje linfático de la región: los ganglios cervicales se encuentran comúnmente comprometidos en la presentación inicial, incluso en tumores de estadio T temprano.
La extensión submucosa es frecuente y sigue patrones predecibles según el subsitio. Los tumores amigdalinos pueden extenderse anterolateralmente a lo largo del músculo constrictor faríngeo hacia el trígono retromolar y, en estadios avanzados, invadir las láminas pterigoideas. Los tumores de base de lengua tienden a progresar anteriormente hacia la lengua oral e inferiormente hacia el surco glosoamigdalino, valécula y espacio preepiglótico. Los tumores del paladar blando pueden crecer superiormente hacia la nasofaringe y las láminas pterigoideas, mientras que los tumores de la pared faríngea presentan riesgo de lesiones salteadas (skip), exigiendo márgenes generosos tanto craneal como caudalmente. Estos patrones de diseminación determinan directamente el diseño del CTV subclínico.
Estudio Diagnóstico para la Delineación
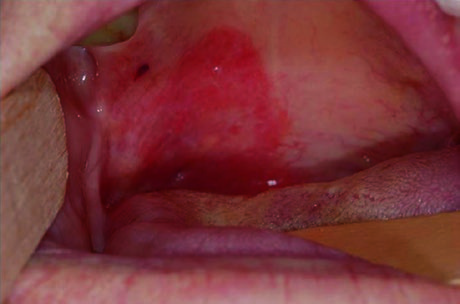
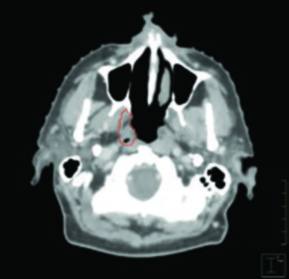
La delineación del GTV primario se define mejor mediante la combinación de imágenes y examen físico. La extensión mucosa y superficial se evalúa por inspección visual, palpación y endoscopia fibróptica. El registro fotográfico en el momento de la consulta o simulación resulta valioso, ya que documenta extensión mucosa que puede no evidenciarse en las imágenes — especialmente el compromiso del paladar blando y la extensión hacia la línea media, como se ilustra en la fotografía clínica superior.
La TC contrastada sigue siendo la imagen principal, pero la RM y el PET/TC tienen roles complementarios bien definidos:
- RM T1 precontraste: ideal para evaluar planos grasos y señal de médula ósea, ayudando a distinguir tumor de tejido normal.
- RM T1 poscontraste: esencial para delinear la extensión anterior de tumores de base de lengua y evaluar invasión perineural. Sin esta secuencia, la extensión anterior puede subestimarse en varios milímetros.
- RM T2 fat-sat: evalúa ganglios retrofaríngeos (RP) y extensión en tejido blando en los espacios parafaríngeo y preepiglótico. Los ganglios RP son notoriamente difíciles de evaluar solo por TC.
- FDG-PET/TC: aporta información metabólica complementaria y puede identificar extensión tumoral no visible en TC o RM. Sin embargo, su baja resolución espacial y limitada sensibilidad para metástasis ganglionares de bajo volumen la hacen insuficiente por sí sola — un ganglio sospechoso sin captación de FDG no debe considerarse necesariamente libre de enfermedad. Esta limitación es particularmente relevante al evaluar ganglios retrofaríngeos y pequeños ganglios del nivel II alto.
Simulación y Localización Diaria
El paciente se posiciona en decúbito supino con extensión cervical, utilizando soporte cefálico y máscara termoplástica de 5 puntos (Aquaplast) que inmovilice cabeza, cuello y hombros. Se puede insertar un mordedor o protector bucal para reproducibilidad diaria y para desplazar el paladar de la distribución de dosis. Los pacientes reciben instrucciones de no deglutir durante la adquisición de la tomografía ni durante el tratamiento, ya que los movimientos de deglución desplazan la orofaringe respecto a la inmovilización.
La simulación por TC con contraste intravenoso utiliza espesor de corte ≤ 3 mm cubriendo desde el vértex craneal hasta la carina. Esta extensión generosa es necesaria para abarcar tanto la posible extensión craneal del tumor como los campos cervicales bajos. El isocentro se posiciona típicamente a nivel de los cartílagos aritenoides, facilitando el acoplamiento de un campo anteroposterior cervical bajo convencional con los campos de IMRT cuando se adopta esta estrategia.
Las imágenes de RM y PET pueden registrarse o fusionarse con la TC de simulación. El uso de la máscara de inmovilización durante el PET mejora la precisión de la fusión, aunque durante la RM puede impedir el uso de bobinas dedicadas de cabeza y cuello. En el MSKCC, la verificación diaria de imagen se realiza con kV 2D e cone-beam CT diario montados en el acelerador lineal. Alternativas aceptables incluyen cone-beam semanal con kV diario, imágenes kV ortogonales (ExacTrac) o TC por MV (TomoTherapy).
Esquemas de Dosis IMRT en Orofaringe
Existen múltiples esquemas de dosis válidos. En el MSKCC, el enfoque preferido utiliza una técnica secuencial con dosis total a la enfermedad macroscópica de 70 Gy. La elección entre técnicas depende del estado VPH, la extensión de la enfermedad y la disponibilidad de quimioterapia concomitante.
Para tumores VPH-positivos (técnica secuencial), las regiones subclínicas reciben 30 Gy en fracciones de 2 Gy en la primera fase. La región subclínica se evalúa rigurosamente con RM, TC contrastada y PET/TC para confirmar ausencia de enfermedad macroscópica antes de continuar. Sigue un cone-down a la enfermedad macroscópica con 40 Gy en fracciones de 2 Gy, totalizando 70 Gy. Si se utiliza un campo cervical bajo AP acoplado, este recibe 30 Gy en fracciones de 2 Gy. Como publicaron Tsai et al. del MSKCC, este enfoque de dosis electiva reducida se basa en la evaluación cuidadosa de las regiones subclínicas mediante múltiples modalidades de imagen.
Para tumores VPH-negativos (técnica secuencial), la fase inicial entrega 60 Gy en fracciones de 2 Gy a la enfermedad macroscópica, con 54 Gy simultáneos en fracciones de 1,8 Gy a todas las regiones subclínicas. Sigue un cone-down de 10 Gy en fracciones de 2 Gy, completando los 70 Gy totales. El campo cervical bajo acoplado recibe 50 Gy en fracciones de 2 Gy. Note que las dosis electivas aquí son considerablemente mayores que en el protocolo VPH-positivo — reflejando el comportamiento biológico más agresivo de estos tumores. Las dosis electivas reducidas solo deben considerarse con quimioterapia concomitante basada en cisplatino.
El boost integrado simultáneo (SIB) es otra técnica bien establecida: 70 Gy (2 Gy/fracción) a enfermedad macroscópica, 56 Gy (1,6 Gy/fracción) a regiones subclínicas de alto riesgo y 50–52,5 Gy (1,43–1,5 Gy/fracción) a bajo riesgo. Solo debe emplearse con quimioterapia concomitante, ya que las dosis por fracción reducidas en los volúmenes subclínicos dependen del efecto radiosensibilizante de la quimioterapia para un control adecuado de la enfermedad microscópica. Protocolos como RTOG 0022 (hipofraccionamiento acelerado) y RTOG 1016 ofrecen opciones de fraccionamiento adicionales.
Volúmenes Blanco para Enfermedad Macroscópica
La delineación del GTV para enfermedad macroscópica sigue directrices específicas. El GTV incluye toda la enfermedad visible al examen clínico y por imágenes: el tumor según TC, RM y PET/TC en el sitio primario, y todos los ganglios sospechosos (mayores de 1 cm en eje corto, necróticos, con realce o captación de FDG) en las cadenas ganglionares. Existe flexibilidad para ganglios limítrofes — aquellos solo marginalmente sospechosos pueden recibir dosis intermedias de 60–66 Gy en lugar de los 70 Gy prescritos a la enfermedad macroscópica franca.
| Volumen | Definición y Descripción |
|---|---|
| GTV70 | Primario: toda enfermedad macroscópica definida por examen clínico e imagen. Ganglios: todos los sospechosos (>1 cm, necróticos, con realce o FDG-ávidos). Ganglios limítrofes pueden recibir dosis menor (60–66 Gy). |
| CTV70 | En áreas de excelente visualización, GTV puede igualarse al CTV (sin margen adicional). Donde existe incertidumbre sobre la extensión tumoral, CTV = GTV + 3–5 mm. |
| PTV70 | CTV + 3–5 mm según la precisión del setup diario y la disponibilidad de guía por imagen (CBCT diario permite márgenes menores). |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 2.1)
La decisión entre margen cero y expansión de 3–5 mm del GTV al CTV70 depende fundamentalmente de la calidad de visualización del tumor. Para tumores amigdalinos bien definidos en la TC contrastada, una expansión mínima puede ser suficiente. Para tumores de base de lengua con extensión anterior mal definida, los 5 mm completos son prudentes, y la fusión con RM T1 poscontraste se vuelve indispensable.
Volúmenes Blanco para Enfermedad Subclínica
Como directriz general, el CTV del sitio primario debe abarcar el GTV + 1 cm, descontando barreras anatómicas a la diseminación como aire, hueso y piel. Este principio simple se traduce en recomendaciones específicas por subsitio, informadas por los patrones de diseminación descritos anteriormente.
| Subsitio / Volumen | Definición y Descripción |
|---|---|
| Amígdala — CTV subclínico | Margen adecuado de ~1 cm al tumor primario. Inclusión altamente recomendada de láminas pterigoideas en enfermedad avanzada. Considerar cobertura del trígono retromolar ipsilateral si se sospecha diseminación anterolateral por el constrictor faríngeo. |
| Base de lengua — CTV subclínico | Surco glosoamigdalino, valécula y espacio preepiglótico. Margen mucoso de al menos 1 cm alrededor del tumor primario, pudiendo extenderse anteriormente hacia la lengua oral. La RM es esencial para la delineación precisa de la extensión anterior. |
| Paladar blando — CTV subclínico | Paladar blando completo, aspecto superior de los pilares amigdalinos y fosa, nasofaringe adyacente superiormente hasta las láminas pterigoideas. En tumores avanzados, considerar la fosa pterigopalatina; si está comprometida, se requiere evaluación de base de cráneo por RM. La cobertura anterior adecuada puede requerir parte del paladar duro. |
| Pared faríngea — CTV subclínico | Márgenes superior e inferior generosos por el riesgo de lesiones salteadas (skip). En tumores avanzados, considerar extensión del CTV cranealmente a nasofaringe y caudalmente a hipofaringe. |
| Ganglios cervicales electivos | Las regiones ganglionares pueden recibir 54 Gy (1,8 Gy/fx), 54,12 Gy (1,64 Gy/fx), 56 Gy (1,6 Gy/fx) o 59,4 Gy (1,8 Gy/fx) según alto o bajo riesgo. Cuello N0: niveles II–IV bilaterales y retrofaríngeos laterales; en MSKCC, IB y V no se tratan rutinariamente salvo compromiso macroscópico (excepción: extensión macroscópica a cavidad oral justifica IB). Cuello N+: retrofaríngeos y retroestiloideos hasta base de cráneo; ganglios macroscópicos bajos: considerar cobertura supraclavicular. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 2.2)
El manejo de la cobertura ganglionar electiva merece atención particular. Para tumores amigdalinos T1–T2 N0–N1 bien lateralizados, sin extensión a base de lengua ni paladar blando, el tratamiento ipsilateral es aceptable. Este escenario se detalla a continuación.
Tratamiento Ipsilateral en Tumores Amigdalinos Lateralizados
Para tumores amigdalinos T1–T2, N0–N1, bien lateralizados (al menos 1 cm lateral a la línea media), sin extensión a base de lengua ni paladar blando, el tratamiento unilateral del cuello es aceptable. La localización bien lateral hace que el riesgo de drenaje linfático contralateral sea suficientemente bajo para justificar la omisión del cuello opuesto. En estos casos, el extremo superior de cobertura para el cuello N-negativo puede iniciar en la apófisis transversa de C1 o donde el vientre posterior del digástrico comienza a cruzar la vena yugular interna.
En la práctica del MSKCC, independientemente del estadio, la región subclínica ipsilateral en tumores amigdalinos casi siempre se extiende superiormente para incluir la lámina pterigoidea ipsilateral. Este enfoque garantiza cobertura adecuada contra diseminación superior oculta, incluso en casos aparentemente confinados a la fosa amigdalina. Además, el CTV subclínico incluye la base de lengua ipsilateral y el paladar blando ipsilateral, respetando la anatomía de drenaje linfático de la fosa amigdalina.
En el lado N-positivo, la cobertura se extiende hasta la base del cráneo, incluyendo los ganglios retrofaríngeos y retroestiloideos. Esta extensión es fundamental porque la presencia de enfermedad ganglionar macroscópica aumenta sustancialmente el riesgo de diseminación a estaciones ganglionares más craneales. Cuando el tumor cruza la línea media hacia la lengua oral, debe considerarse la cobertura bilateral del nivel IB dado el patrón de drenaje cruzado en esta región. Por el contrario, en el cuello N-negativo, el MSKCC no incluye rutinariamente el nivel IB salvo que exista extensión macroscópica a la cavidad oral.
Ejemplos Clínicos Representativos
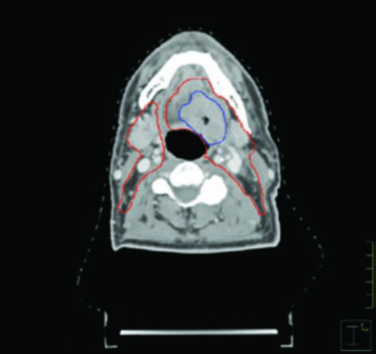
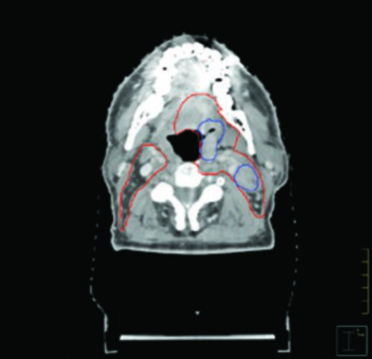
Las figuras de este capítulo ilustran casos reales que ejemplifican los principios de delineación discutidos. El caso de carcinoma amigdalino VPH-negativo cT4N2 demuestra la necesidad de cobertura hasta las láminas pterigoideas e inclusión del nivel IB ipsilateral por invasión de la lengua oral. Observe cómo el GTV (azul) y el CTV (rojo) se adaptan a las barreras anatómicas, respetando hueso y aire mientras se expanden generosamente hacia los tejidos blandos.
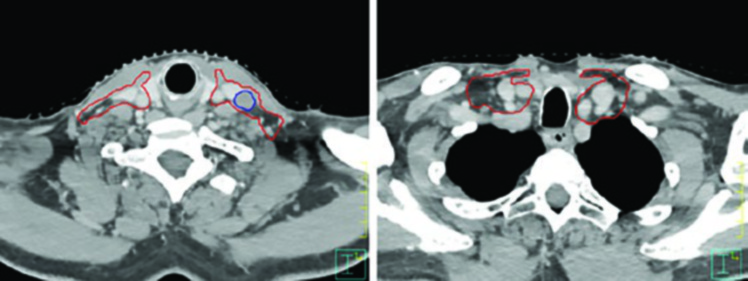
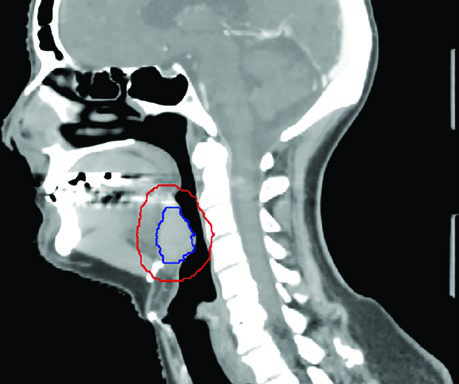
El caso de base de lengua VPH-positivo cT4N1 ilustra la cobertura hasta la base del cráneo en el lado N-positivo y la extensión del CTV para considerar cobertura bilateral del nivel IB cuando el tumor cruza la línea media. La vista sagital demuestra con particular claridad la importancia de la cobertura del espacio preepiglótico en tumores de base de lengua — un área frecuentemente subestimada por planificadores menos experimentados.
El caso de carcinoma amigdalino VPH-positivo cT2N0 tratado unilateralmente muestra cómo, incluso en el escenario de tratamiento ipsilateral, la cobertura se extiende superiormente hasta la lámina pterigoidea ipsilateral. La cobertura ganglionar inicia en la apófisis transversa de C1, abarcando la base de lengua y el paladar blando ipsilaterales sin cruzar la línea media.
Consideraciones Prácticas en la Planificación
La elección del esquema de fraccionamiento y la técnica de tratamiento depende de múltiples factores clínicos y logísticos. El boost integrado simultáneo ofrece la ventaja operativa de tratar en una sola fase, reduciendo el tiempo total de tratamiento y simplificando la logística de planificación. Sin embargo, exige atención rigurosa a la dosis por fracción en los volúmenes subclínicos — las dosis de 1,6 Gy y 1,43–1,5 Gy por fracción son biológicamente menos eficaces que las fracciones convencionales de 1,8–2 Gy, dependiendo del efecto radiosensibilizante de la quimioterapia para compensar. La técnica secuencial, por otro lado, permite evaluar la respuesta durante el tratamiento y ajustar el volumen del cone-down basándose en imágenes intermedias.
En la evaluación de ganglios sospechosos, la decisión entre prescribir 70 Gy o una dosis intermedia (60–66 Gy) depende del grado de sospecha. Los ganglios francamente positivos — necróticos, con extensión extracapsular o intensamente captantes — reciben dosis plena. Aquellos solo limítrofes en tamaño o avidez pueden recibir dosis intermedias. Esta estrategia permite reducir la toxicidad en las estructuras adyacentes sin comprometer el control local.
La fusión de imágenes multimodalidad merece atención especial. El PET adquirido con máscara de inmovilización mejora la precisión de la fusión con la TC de simulación, pero la RM con máscara puede limitar el uso de bobinas dedicadas, comprometiendo la calidad de imagen precisamente donde más se necesita. En la experiencia práctica, la solución más pragmática consiste en realizar la RM sin máscara usando bobina dedicada y registrar las imágenes por referencias anatómicas, aceptando una incertidumbre ligeramente mayor en la fusión a cambio de una resolución superior en los tejidos blandos de la orofaringe.
Para orientación detallada sobre subsitios adyacentes, consulte nuestros artículos sobre delineación en nasofaringe, cáncer de laringe, hipofaringe y cáncer de cavidad oral — todas localizaciones que comparten vías de drenaje linfático y pueden influir en las decisiones de cobertura del carcinoma de orofaringe.




