Los tumores de glándulas salivales mayores — parótida, submandibular y sublingual — representan un desafío particular para la planificación de radioterapia postoperatoria. Su cercanía con nervios craneales, la base del cráneo y los espacios profundos cervicales exige una delineación precisa del volumen blanco y una evaluación rigurosa de la diseminación perineural. En este artículo detallamos los principios de imagen, las definiciones de GTV, CTV y PTV, los puntos de referencia del lecho quirúrgico y las particularidades de cada glándula, siguiendo las guías actuales de planificación conformacional e IMRT.
Principios de Imagen para Tumores de Glándulas Salivales
Todo paciente con cáncer de glándula salivar debe someterse a tomografía computarizada (TC) con contraste intravenoso o resonancia magnética (RM) de la región de cabeza y cuello, cubriendo desde la base del cráneo hasta las clavículas. La RM ofrece un contraste de tejidos blandos superior a la TC, lo que facilita la identificación del margen tumoral, la extensión profunda y el patrón de infiltración en el parénquima glandular.
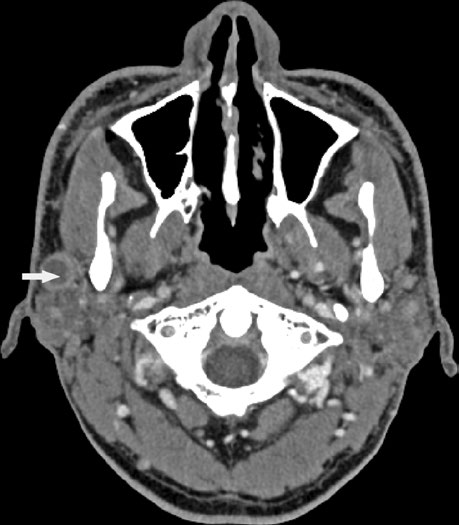
Las imágenes ponderadas en T1 proporcionan una evaluación excelente de los márgenes tumorales. Al agregar secuencias T1 con saturación grasa y contraste, la diseminación perineural, la invasión ósea y la infiltración meníngea se visualizan con mayor claridad. En la práctica, se recomienda fusionar la TC de simulación con la RM diagnóstica, combinando la precisión geométrica de la primera con la resolución de contraste de la segunda.
La simulación por TC con contraste debe realizarse siempre que el tumor primario esté in situ, para guiar la delineación del volumen tumoral macroscópico (GTV). Cortes de 3 mm y uso de máscara termoplástica garantizan reproducibilidad posicional.
El flujo de fusión entre TC de simulación y RM diagnóstica merece énfasis como paso esencial en la práctica actual. La TC proporciona la referencia geométrica para el cálculo de dosis, mientras la RM delinea con mayor precisión la interfaz entre tumor y tejidos normales — particularmente en tumores del lóbulo profundo de la parótida, donde la distinción entre parénquima glandular y músculo pterigoideo puede ser sutil. Siempre que sea posible, la RM debe incluir secuencias axiales y coronales con supresión de grasa y gadolinio, ya que estas secuencias revelan patrones de infiltración que pasan desapercibidos en la TC convencional.
Para una visión general completa sobre delineación de volúmenes blanco en radioterapia, consulte nuestra guía completa sobre delineación de volumen blanco.
Volúmenes Blanco en la Enfermedad Macroscópica
La definición precisa del GTV es el punto de partida de toda planificación. Para tumores de parótida o submandibular, el GTV70 incluye toda la enfermedad macroscópica identificada en el examen físico y por imagen. Los ganglios cervicales con eje corto igual o mayor a 1 cm, o aquellos con centro necrótico, también deben incluirse en este volumen.
Tabla de Volúmenes Blanco — Enfermedad Macroscópica
La siguiente tabla resume las definiciones y márgenes recomendados para la región de enfermedad macroscópica.
| Volumen blanco | Definición y descripción |
|---|---|
| GTV70 | Parótida o submandibular: toda la enfermedad macroscópica en examen físico e imagen. Ganglios cervicales ≥ 1 cm en eje corto o con centro necrótico. Dosis sugerida: 2 Gy/fracción hasta 70 Gy. |
| CTV70 | GTV70 + 5 mm de margen. Alternativamente, el CTV70 puede ser equivalente al GTV70 cuando el médico tiene certeza del blanco. Para ganglios pequeños pero sospechosos (< 1 cm), considerar 63–66 Gy. |
| PTV70 | Margen específico de la institución, típicamente CTV70 + 3–5 mm. Márgenes menores con guía por imagen (IGRT). |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition
Un punto que merece atención: los ganglios con diámetro menor a 1 cm en eje corto pero con características sospechosas en imagen pueden recibir una dosis intermedia de 63 a 66 Gy. Este enfoque equilibra el control local con la preservación de los tejidos normales adyacentes.
Lecho Quirúrgico de la Parótida y Volúmenes Subclínicos de Alto Riesgo
En el escenario postoperatorio, el CTV60 debe englobar el lecho quirúrgico de la parótida o submandibular y toda la extensión del GTV original. Los puntos de referencia anatómicos bien definidos orientan esta delineación y reducen el riesgo de omisión de enfermedad subclínica.
Para el lecho quirúrgico de la parótida, los límites recomendados son: anterior — músculo masetero; lateral — tejidos blandos del cuello; medial — apófisis estiloides en profundidad, pudiendo extenderse a la grasa parafaríngea según la extensión de la parótida; posterior — hueso mastoideo. Estos límites deben ajustarse caso por caso: tumores profundos exigen la inclusión del espacio parafaríngeo, mientras que lesiones superficiales pueden tener volúmenes más conservadores.
Para la glándula submandibular, todo el lecho quirúrgico debe incluirse con todos los cambios postoperatorios. La glándula submandibular contralateral sirve como referencia anatómica para guiar la delineación. Se debe motivar al cirujano a dejar clips metálicos siempre que sea posible para facilitar la localización del lecho.
La enfermedad residual o márgenes positivos requieren un boost de 6 a 10 Gy sobre la región afectada. En la experiencia clínica, esta escalada de dosis marca una diferencia sustancial en el control local, especialmente en histologías agresivas.
Tabla de Volúmenes Subclínicos de Alto Riesgo
Esta tabla detalla los criterios para la delineación de los volúmenes subclínicos de alto riesgo y la irradiación ganglionar electiva.
| Volumen blanco | Definición y descripción |
|---|---|
| CTV60 | Parótida o submandibular: debe englobar todo el GTV o el lecho quirúrgico en pacientes postoperatorios. Puntos de referencia anatómicos detallados en el texto. Boost de 6–10 Gy para enfermedad residual o margen positivo. Incluir trayecto neural cuando exista invasión perineural. |
| CTV50 | N+: Irradiar electivamente el cuello ipsilateral (niveles Ib–V) a 50 Gy; puede omitirse el nivel V. N0: Incluir al menos niveles Ib–III/IV para tumores de alto grado o T3–4. El carcinoma adenoide quístico y el carcinoma de células acinares típicamente no requieren irradiación ganglionar electiva (bajo riesgo de diseminación linfática). Cuello contralateral: Considerar cuando exista preocupación clínica, tanto para parótida como para submandibular. |
| PTV60 | Margen específico de la institución, típicamente CTV60 + 3–5 mm. Márgenes reducidos con IGRT. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition
Espacio Parafaríngeo y Anatomía de la Base del Cráneo
El espacio parafaríngeo es una región predominantemente grasa que se extiende desde la base del cráneo hasta el hueso hioides. Los tumores de parótida grandes o con extensión profunda requieren su inclusión en el CTV60. Posterolateral a la apófisis estiloides se encuentra el espacio retrostiloideo, que puede contener ganglios linfáticos y también debe incorporarse al volumen de tratamiento.
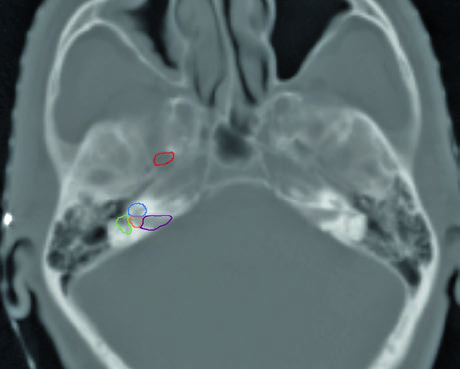
La delineación de las estructuras de la base del cráneo debe realizarse con ventana ósea en la TC. Las principales referencias incluyen: el foramen oval (rojo), la cóclea (azul), el vestíbulo (naranja), el conducto auditivo interno (violeta) y los canales semicirculares (verde). Identificar correctamente estas estructuras es fundamental para garantizar una cobertura neural adecuada sin irradiar excesivamente estructuras sensibles como la cóclea.
En la práctica diaria, recomiendo delinear estas estructuras como órganos en riesgo antes de expandir el CTV hacia la base del cráneo. Esto permite evaluar objetivamente las relaciones dosis-volumen y tomar decisiones conscientes sobre cuánta cobertura es realmente necesaria frente al costo en toxicidad auditiva o neural. Un enfoque similar se aplica en la delineación de tumores de cavidad nasal y senos paranasales, donde la base del cráneo también juega un papel central.
Diseminación Perineural: Evaluación y Cobertura del CTV
La diseminación perineural es uno de los mayores desafíos en la planificación de glándulas salivales. Cuando está presente, el CTV debe expandirse para incluir el trayecto completo de los nervios afectados — frecuentemente hasta la base del cráneo.
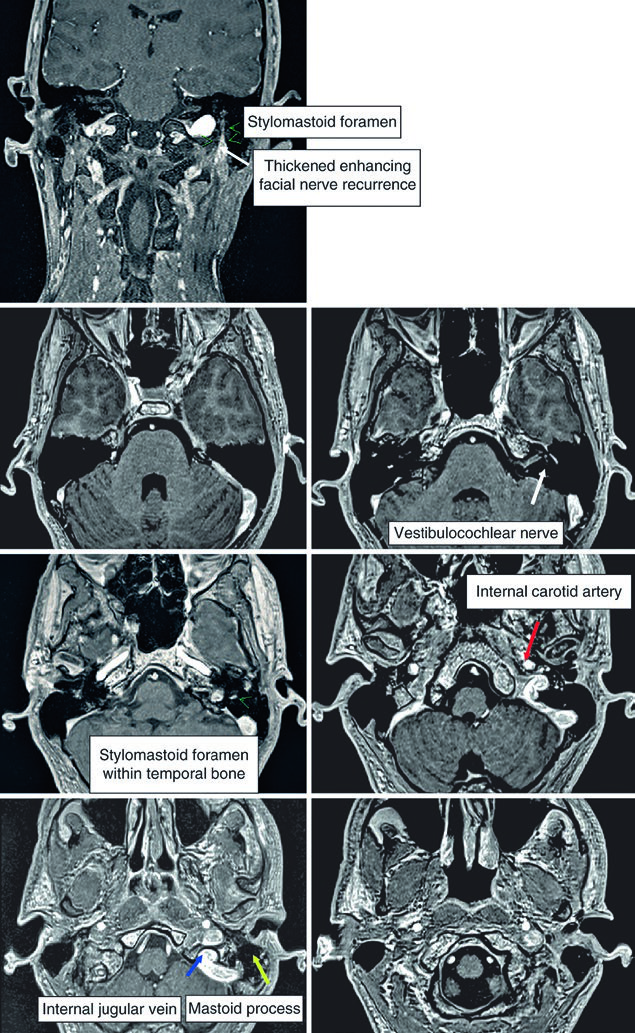
Para tumores de parótida, deben incluirse: el nervio facial, el nervio glosofaríngeo y la rama V3 del trigémino. En casos con diseminación extensa, la cobertura puede necesitar extenderse hasta la caverna de Meckel. El trayecto intratemporal del nervio facial merece atención especial — recorre el canal facial desde el conducto auditivo interno hasta el foramen estilomastoideo. Cuando existe compromiso directo o la histología es carcinoma adenoide quístico, la inclusión de este trayecto es obligatoria.
Para tumores submandibulares y sublinguales, los nervios hipogloso y lingual deben incluirse en el volumen. La extensión hasta la caverna de Meckel es especialmente importante en el carcinoma adenoide quístico, dada su conocida predilección por la invasión perineural. En estos casos también puede ser necesario incluir el nervio facial. Esta complejidad en la cobertura neural es comparable a la planificación de tumores de nasofaringe, donde el trayecto de los nervios craneales también determina las expansiones del CTV.
Irradiación Ganglionar Electiva en Glándulas Salivales
La decisión sobre irradiación ganglionar electiva depende del estado ganglionar, el grado histológico y la histología específica. Para pacientes con ganglios clínicamente positivos (N+), el cuello ipsilateral — niveles Ib a V — debe recibir 50 Gy de dosis electiva. La omisión del nivel V puede considerarse en casos seleccionados, especialmente cuando el análisis riesgo-beneficio favorece la preservación del plexo braquial.
Para pacientes clínicamente N0, el enfoque varía significativamente según la histología. Los tumores de alto grado o estadio T3–T4 justifican irradiación electiva de los niveles Ib a III (pudiendo extenderse al nivel IV). El carcinoma adenoide quístico y el carcinoma de células acinares son excepciones notables: debido al bajo riesgo de diseminación linfática, la irradiación ganglionar electiva típicamente no está indicada en estos subtipos. Esta particularidad es una de las razones por las que la clasificación histológica precisa resulta tan crítica antes de la planificación.
El tratamiento del cuello contralateral sigue siendo controvertido. Debe considerarse cuando exista preocupación clínica significativa — tumores que cruzan la línea media, extensión al espacio parafaríngeo contralateral o histología agresiva con múltiples ganglios positivos ipsilaterales.
Un aspecto práctico frecuentemente pasado por alto es la correlación entre el grado histológico y el riesgo de metástasis ganglionar oculta. Los carcinomas mucoepidermoides de alto grado, carcinomas ductales salivares y carcinomas indiferenciados presentan tasas de metástasis regional que justifican la inclusión de al menos los niveles Ib a IV en el CTV50, incluso en cuellos clínicamente negativos. En contraste, el carcinoma adenoide quístico — a pesar de su comportamiento localmente agresivo con predilección por invasión perineural — raramente metastatiza a ganglios regionales al momento del diagnóstico, haciendo la irradiación ganglionar electiva prescindible en la mayoría de los casos de este subtipo.
La decisión sobre la extensión de la cobertura ganglionar también debe considerar la localización del tumor primario. Los tumores de parótida drenan predominantemente a los ganglios intraparotídeos y a los niveles II y III, mientras que los tumores submandibulares tienen acceso directo al nivel I y frecuentemente comprometen los niveles II y III. Esta diferencia topográfica influye en el diseño de los campos electivos y debe incorporarse a la discusión multidisciplinaria pretratamiento.
Principios similares de cobertura ganglionar se aplican en la delineación del carcinoma de orofaringe y otros subsitios de cabeza y cuello.
Compromiso Cutáneo y Óseo en la Planificación
La infiltración dérmica y el compromiso óseo son hallazgos que modifican sustancialmente la planificación. Cuando existe evidencia clínica o radiológica de infiltración cutánea, la piel debe incluirse como estructura blanco utilizando bolus para garantizar dosis adecuada en la superficie. En casos con derrame tumoral perioperatorio, la cicatriz quirúrgica también se incorpora al volumen de tratamiento.
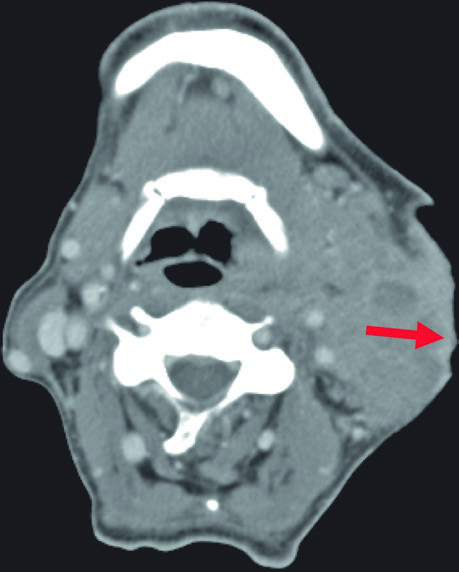
El compromiso óseo requiere evaluación específica en ventana ósea de la TC. La imagen muestra reacción perióstica en la cara posterior de la rama mandibular izquierda, sugiriendo compromiso directo. Al confirmarse, la estructura ósea debe incorporarse al CTV con margen adecuado.
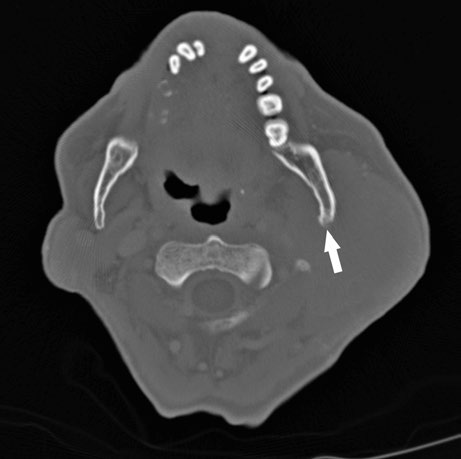
Estos hallazgos refuerzan la importancia de un estudio de imagen completo antes de la simulación. La combinación de ventana de tejidos blandos y ventana ósea en la misma TC garantiza que ninguna extensión tumoral pase desapercibida. En mi experiencia, la integración de hallazgos de RM — especialmente secuencias con supresión de grasa — con la TC de simulación mejora considerablemente la confianza en la delineación de estos casos complejos.
Planificación Postoperatoria de la Glándula Submandibular
Los tumores submandibulares presentan consideraciones específicas para la delineación postoperatoria. Todo el lecho quirúrgico debe incluirse junto con todos los cambios postoperatorios visibles en la TC de simulación. La glándula submandibular contralateral intacta sirve como guía anatómica invaluable para definir los límites del CTV.
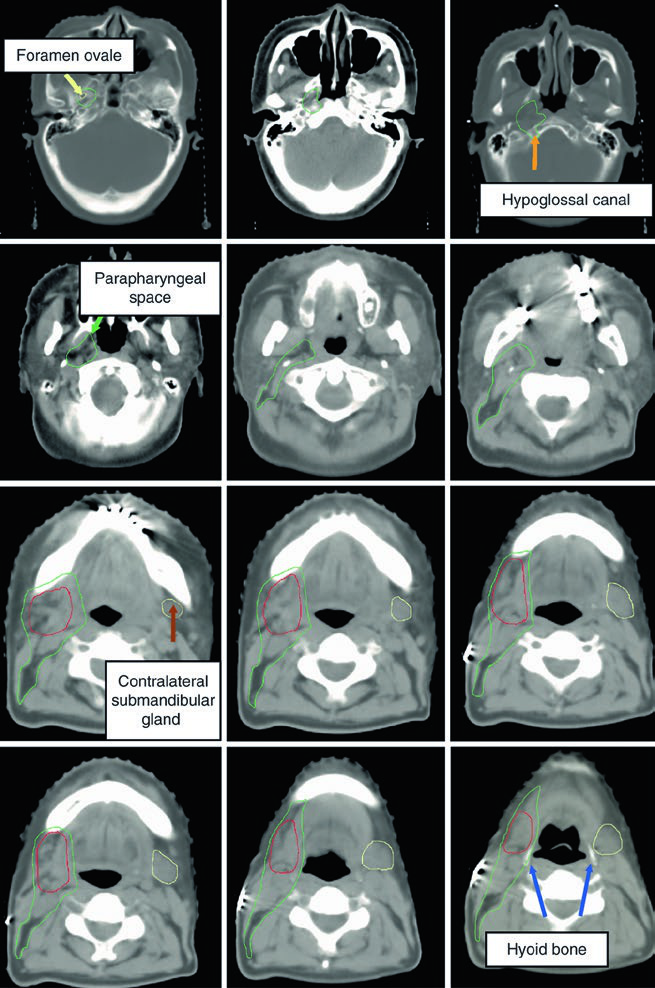
El trayecto del nervio lingual merece atención particular. Se origina de la rama mandibular (V3) del nervio trigémino en el foramen oval, desciende profundamente al músculo pterigoideo lateral y discurre entre el músculo pterigoideo medial y la rama mandibular, dirigiéndose a la cara medial de la glándula submandibular antes de terminar en la lengua. Cuando el nervio lingual o el nervio hipogloso están comprometidos, el CTV debe extenderse hasta la base del cráneo — especialmente en el carcinoma adenoide quístico.
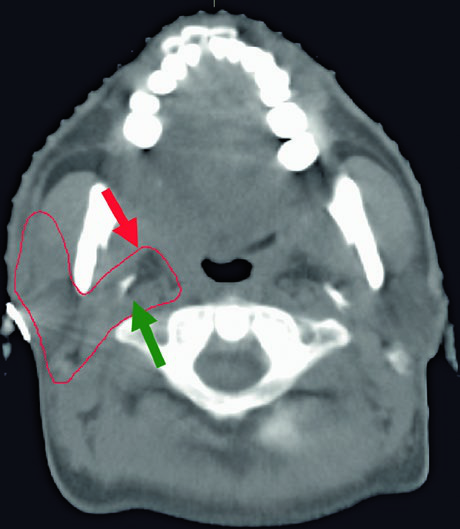
La imagen muestra un caso de carcinoma mucoepidermoide de alto grado cT1N1M0 de la submandibular derecha, con el CTV60–66 (rojo) cubriendo el lecho quirúrgico y el CTV50–54 (verde) englobando estaciones ganglionares ipsilaterales y el espacio parafaríngeo hasta la base del cráneo. Este enfoque garantiza cobertura adecuada incluso en tumores de estadio temprano pero alto grado.
El Nervio Glosofaríngeo y Su Relevancia en la Delineación
El nervio glosofaríngeo (IX par craneal) sale de la base del cráneo por el foramen yugular y desciende por el cuello anterolateral a la arteria carótida interna, medial a la apófisis estiloides. Termina en ramos para la faringe. Su identificación es relevante porque, en tumores de parótida con diseminación perineural, el trayecto de este nervio puede necesitar incluirse en el CTV.
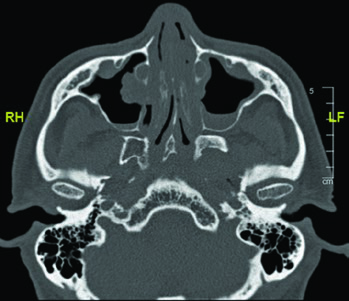
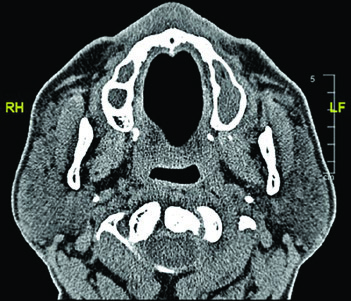
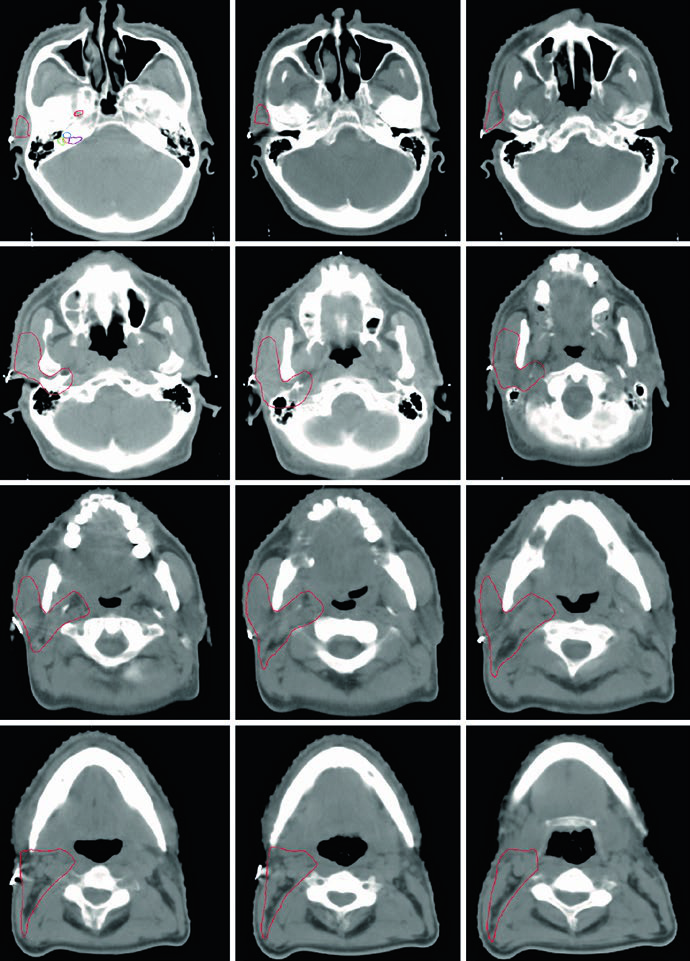
Las imágenes de TC demuestran el trayecto del nervio glosofaríngeo en diferentes cortes axiales. El nervio puede identificarse posterolateral a la apófisis estiloides, descendiendo junto a la carótida interna. La marcación oval roja en los cortes muestra la localización esperada del nervio a lo largo de su recorrido cervical. El último corte utiliza ventana de tejidos blandos para mejor visualización de las relaciones entre el nervio y los vasos cervicales.
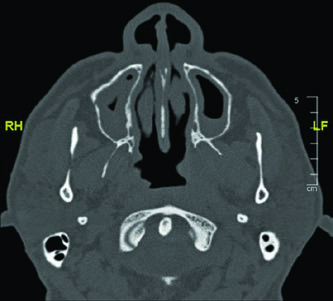
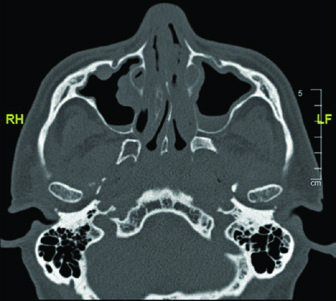
El dominio de esta anatomía es especialmente relevante al planificar la irradiación de carcinomas adenoides quísticos de parótida, dado su fuerte tendencia a seguir las vainas neurales. La inclusión del trayecto completo — desde el foramen yugular hasta los ramos faríngeos — garantiza que la diseminación subclínica a lo largo del nervio glosofaríngeo sea adecuadamente cubierta. Un enfoque similar de mapeo neural se discute en el contexto de primario oculto en cabeza y cuello.
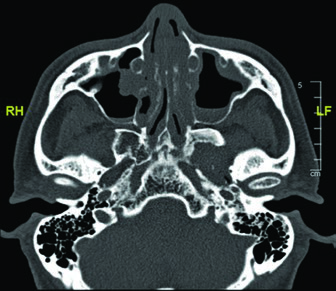
El papel de los clips quirúrgicos no puede subestimarse. Sin clips, el radioterapeuta depende exclusivamente de los cambios postoperatorios visibles en la TC de simulación — que pueden ser ambiguos en las primeras semanas tras la cirugía. Clips posicionados en los límites del lecho quirúrgico, en los márgenes más cercanos y a lo largo del trayecto de nervios disecados proporcionan información que ningún estudio de imagen por sí solo puede replicar. Esta colaboración entre cirujano y radioterapeuta, iniciada en el intraoperatorio, es lo que diferencia una delineación adecuada de una excelente.
En resumen, la planificación radioterápica de las glándulas salivales mayores demanda una evaluación imagenológica minuciosa, conocimiento anatómico detallado de la base del cráneo y los espacios profundos cervicales, y comprensión de los patrones de diseminación perineural específicos de cada histología. La colaboración estrecha entre cirujano y radioterapeuta — con colocación de clips y descripción operatoria detallada — mejora sustancialmente la calidad de la delineación. Para la referencia completa sobre volúmenes blanco en radioterapia, consulte nuestra guía completa sobre delineación de volumen blanco.