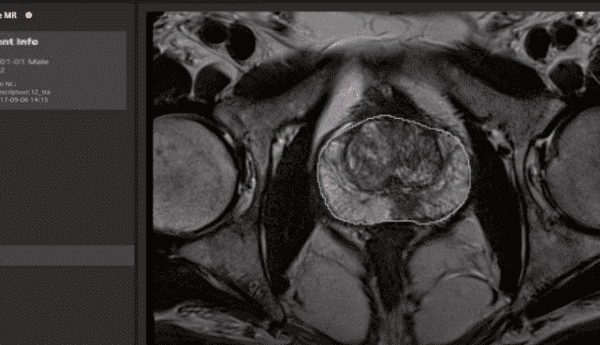
Glândulas salivares maiores — parótida, submandibular e sublingual — representam sítios desafiadores para o planejamento radioterápico pós-operatório. A proximidade com nervos cranianos, a base do crânio e espaços profundos do pescoço exige delineamento preciso do volume-alvo e avaliação criteriosa da disseminação perineural. Neste artigo, detalhamos os princípios de imagem, as definições de GTV, CTV e PTV, os marcos anatômicos do leito cirúrgico e as particularidades de cada glândula, conforme as diretrizes mais atuais de planejamento conformacional e IMRT.
Princípios de Imagem para Tumores de Glândulas Salivares
Todo paciente com câncer de glândula salivar deve realizar tomografia computadorizada (TC) com contraste endovenoso ou ressonância magnética (RM) da região de cabeça e pescoço, cobrindo desde a base do crânio até as clavículas. A RM oferece contraste de partes moles superior à TC, o que facilita a identificação da margem tumoral, da extensão profunda e do padrão de infiltração no parênquima glandular.
As imagens ponderadas em T1 proporcionam excelente avaliação das margens tumorais. Com a adição de sequências T1 com saturação de gordura e contraste, a disseminação perineural, a invasão óssea e a infiltração meníngea tornam-se mais evidentes. Na prática, a fusão entre a TC de simulação e a RM diagnóstica é altamente recomendada, pois combina a precisão geométrica da TC com a resolução de contraste da RM.
A simulação por TC com contraste endovenoso deve ser realizada sempre que o tumor primário estiver in situ, auxiliando no delineamento do volume tumoral macroscópico (GTV). Cortes de 3 mm e uso de máscara termoplástica garantem reprodutibilidade posicional.
A fusão de imagem entre TC de simulação e RM diagnóstica merece destaque como passo essencial na prática atual. A TC fornece a referência geométrica para o cálculo de dose, enquanto a RM delineia com maior precisão a interface entre tumor e tecidos normais — particularmente em tumores do lobo profundo da parótida, onde a distinção entre parênquima glandular e músculo pterigoideo pode ser sutil. Sempre que possível, a RM deve incluir sequências axiais e coronais com supressão de gordura e gadolínio, pois essas sequências revelam padrões de infiltração que passam despercebidos na TC convencional.
Para uma visão geral completa sobre delineamento de volumes-alvo em radioterapia, confira nosso guia completo sobre delineamento de volume alvo.
Volumes-Alvo na Doença Macroscópica
A definição precisa do GTV é o ponto de partida de todo planejamento. Para tumores de parótida ou submandibular, o GTV70 engloba toda a doença macroscópica identificada em exame físico e por imagem. Linfonodos cervicais com eixo curto maior ou igual a 1 cm, ou aqueles com centro necrótico, também devem ser incluídos nesse volume.
Tabela de Volumes-Alvo — Doença Macroscópica
A tabela a seguir resume as definições e margens recomendadas para a região de doença macroscópica.
| Volume-alvo | Definição e descrição |
|---|---|
| GTV70 | Parótida ou submandibular: toda doença macroscópica em exame físico e imagem. Linfonodos cervicais ≥ 1 cm no eixo curto ou com centro necrótico. Dose sugerida: 2 Gy/fração até 70 Gy. |
| CTV70 | GTV70 + 5 mm de margem. Alternativamente, o CTV70 pode ser equivalente ao GTV70 quando o médico tem certeza sobre o alvo. Para linfonodos pequenos mas suspeitos (< 1 cm), considerar dose de 63–66 Gy. |
| PTV70 | Margem específica da instituição, tipicamente CTV70 + 3–5 mm. Margens menores quando houver guiamento por imagem (IGRT). |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition
Um ponto que merece atenção: linfonodos com diâmetro abaixo de 1 cm no eixo curto, mas com características suspeitas na imagem, podem receber uma dose intermediária de 63 a 66 Gy. Essa abordagem equilibra controle local e preservação de tecidos normais adjacentes.
Leito Cirúrgico da Parótida e Volumes Subclínicos de Alto Risco
No cenário pós-operatório, o CTV60 deve englobar o leito cirúrgico da parótida ou submandibular e toda a extensão do GTV original. Marcos anatômicos bem definidos orientam esse delineamento e reduzem o risco de omissão de doença subclínica.
Para o leito cirúrgico da parótida, os limites recomendados são: anterior — músculo masseter; lateral — tecidos moles do pescoço; medial — processo estiloide em profundidade, podendo estender-se à gordura parafaríngea conforme a extensão da parótida; posterior — osso mastoide. Esses marcos devem ser ajustados caso a caso: tumores profundos exigem inclusão do espaço parafaríngeo, enquanto lesões superficiais podem ter volumes mais conservadores.
Para a glândula submandibular, o leito cirúrgico inteiro deve ser incluído, com todas as alterações pós-operatórias. A glândula submandibular contralateral serve como referência anatômica para guiar o delineamento. O cirurgião deve ser encorajado a deixar clipes metálicos sempre que possível, facilitando a localização do leito.
Doença residual ou margens positivas demandam um boost de 6 a 10 Gy sobre a região acometida. Na experiência clínica, essa escalada de dose faz diferença substancial no controle local, especialmente em histologias agressivas.
Tabela de Volumes Subclínicos de Alto Risco
Esta tabela detalha os critérios para delineamento dos volumes de alto risco subclínico e irradiação nodal eletiva.
| Volume-alvo | Definição e descrição |
|---|---|
| CTV60 | Parótida ou submandibular: deve englobar todo o GTV ou o leito cirúrgico nos pacientes pós-operatórios. Marcos anatômicos detalhados no texto. Boost de 6–10 Gy para doença residual ou margem positiva. Incluir percurso de nervos quando houver invasão perineural. |
| CTV50 | N+: Irradiar eletivamente o pescoço ipsilateral (níveis Ib–V) a 50 Gy; pode-se omitir o nível V. N0: Incluir ao menos níveis Ib–III/IV para tumores de alto grau ou T3–4. Carcinoma adenoide cístico e carcinoma de células acinares tipicamente não requerem irradiação nodal eletiva (baixo risco de disseminação linfática). Pescoço contralateral: Considerar quando houver preocupação clínica, tanto para parótida quanto para submandibular. |
| PTV60 | Margem específica da instituição, tipicamente CTV60 + 3–5 mm. Margens menores se IGRT disponível. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition
Espaço Parafaríngeo e Anatomia da Base do Crânio
O espaço parafaríngeo é uma região predominantemente preenchida por gordura que se estende da base do crânio ao osso hioide. Tumores de parótida grandes ou com extensão profunda exigem sua inclusão no CTV60. Posterolateral ao processo estiloide encontra-se o espaço retrostiloide, que pode conter linfonodos e também deve ser incorporado ao volume de tratamento.
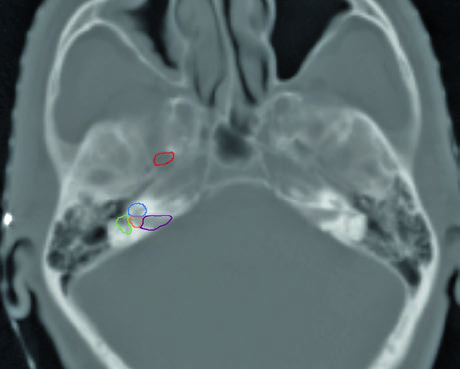
O delineamento das estruturas da base do crânio deve ser realizado com janela óssea na TC. As principais referências incluem: o forame oval (vermelho), a cóclea (azul), o vestíbulo (laranja), o canal auditivo interno (violeta) e os canais semicirculares (verde). Identificar corretamente essas estruturas é fundamental para garantir cobertura adequada do trajeto neural sem irradiar excessivamente estruturas sensíveis como a cóclea.
Na prática diária, recomendo delinear essas estruturas como órgãos de risco antes de expandir o CTV em direção à base do crânio. Isso permite avaliar objetivamente a relação dose-volume e tomar decisões conscientes sobre quanto de cobertura é realmente necessário versus o custo em toxicidade auditiva ou neural. Essa abordagem é semelhante à utilizada no delineamento de tumores da cavidade nasal e seios paranasais, onde a base do crânio também desempenha papel central.
Disseminação Perineural: Avaliação e Cobertura do CTV
A disseminação perineural é um dos maiores desafios no planejamento de glândulas salivares. Quando presente, o CTV deve ser expandido para incluir o trajeto completo dos nervos acometidos — frequentemente até a base do crânio.
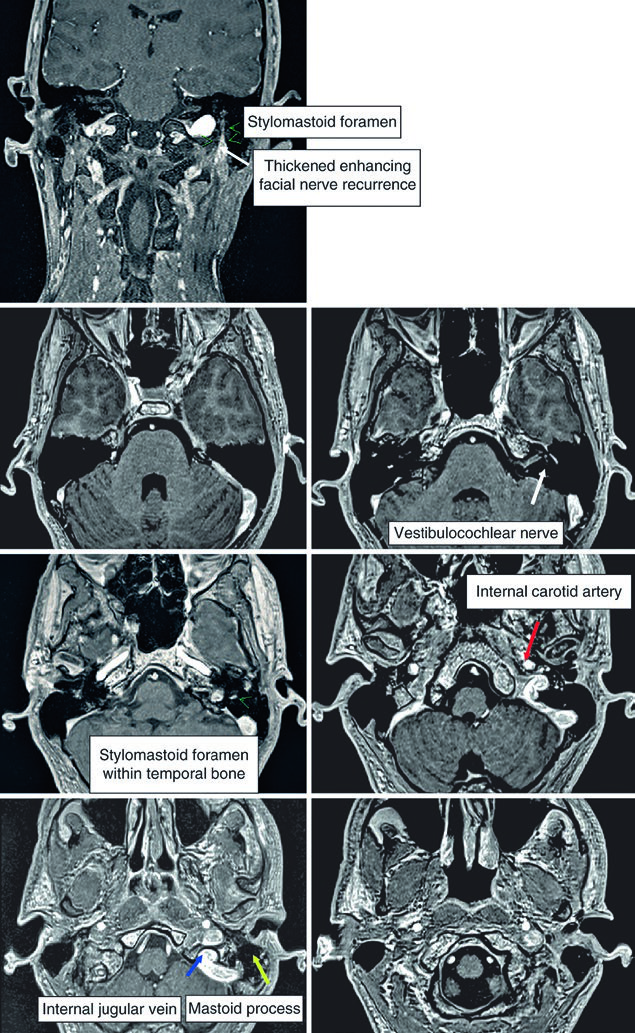
Para tumores de parótida, devem ser incluídos: o nervo facial, o nervo glossofaríngeo e o ramo V3 do trigêmeo. Em casos com disseminação extensa, a cobertura pode precisar estender-se até a caverna de Meckel. O trajeto intratemporal do nervo facial merece atenção especial — ele percorre o canal facial desde o canal auditivo interno até o forame estilomastoideo. Quando há envolvimento direto ou quando a histologia é carcinoma adenoide cístico, a inclusão desse trajeto é mandatória.
Para tumores submandibulares e sublinguais, os nervos hipoglosso e lingual devem ser incluídos no volume. A extensão até a caverna de Meckel torna-se especialmente importante no carcinoma adenoide cístico, dada sua conhecida predileção por invasão perineural. Pode ser necessário incluir também o nervo facial nesses casos. Essa complexidade na cobertura neural é comparável ao planejamento de tumores de nasofaringe, onde o trajeto de nervos cranianos também dita as expansões do CTV.
Irradiação Nodal Eletiva nas Glândulas Salivares
A decisão sobre irradiação nodal eletiva depende do status linfonodal, do grau histológico e da histologia específica. Para pacientes com linfonodos clinicamente positivos (N+), o pescoço ipsilateral — níveis Ib a V — deve receber 50 Gy de dose eletiva. A omissão do nível V pode ser considerada em casos selecionados, especialmente quando a análise de risco-benefício favorece a preservação do plexo braquial.
Para pacientes clinicamente N0, a abordagem muda significativamente conforme a histologia. Tumores de alto grau ou estadiamento T3–T4 justificam irradiação eletiva dos níveis Ib a III (podendo estender-se ao nível IV). O carcinoma adenoide cístico e o carcinoma de células acinares são exceções notáveis: devido ao baixo risco de disseminação linfática, a irradiação nodal eletiva tipicamente não é indicada nesses subtipos. Essa particularidade é uma das razões pelas quais a classificação histológica precisa é tão crítica antes do planejamento.
O tratamento do pescoço contralateral permanece controverso. Deve-se considerar essa abordagem quando houver preocupação clínica significativa — tumores que cruzam a linha média, extensão para o espaço parafaríngeo contralateral ou histologia agressiva com múltiplos linfonodos positivos ipsilaterais.
Um aspecto prático frequentemente negligenciado é a correlação entre o grau histológico e o risco de metástase nodal oculta. Carcinomas mucoepidermoides de alto grau, carcinomas ductais salivares e carcinomas indiferenciados apresentam taxas de metástase regional que justificam a inclusão de pelo menos os níveis Ib a IV no CTV50, mesmo em pescoços clinicamente negativos. Em contraste, o carcinoma adenoide cístico — apesar de seu comportamento localmente agressivo com propensão à invasão perineural — raramente metastatiza para linfonodos regionais no momento do diagnóstico, tornando a irradiação nodal eletiva dispensável na maioria dos casos desse subtipo.
A decisão sobre extensão da cobertura nodal deve considerar também a localização do tumor primário. Tumores de parótida drenam predominantemente para os linfonodos intraparotídeos e para os níveis II e III, enquanto tumores submandibulares têm acesso direto ao nível I e frequentemente envolvem os níveis II e III. Essa diferença topográfica influencia o desenho dos campos eletivos e deve ser incorporada à discussão multidisciplinar pré-tratamento.
Princípios semelhantes de cobertura nodal são aplicados no delineamento do carcinoma de orofaringe e em outros sítios de cabeça e pescoço.
Envolvimento de Pele e Osso no Planejamento
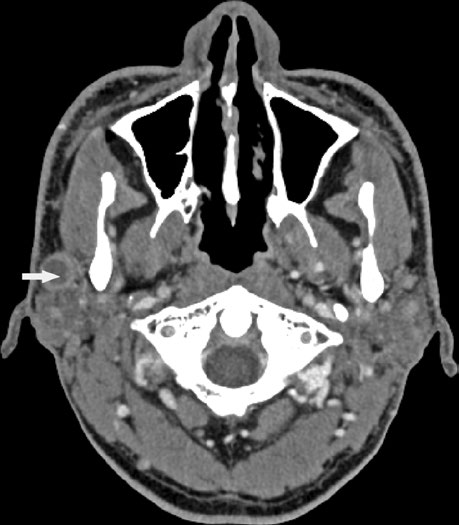
A infiltração dérmica e o comprometimento ósseo são achados que modificam substancialmente o planejamento. Quando há evidência clínica ou radiológica de infiltração cutânea, a pele deve ser incluída como estrutura-alvo, utilizando bolus para garantir dose adequada na superfície. Em casos com derramamento tumoral perioperatório, a cicatriz cirúrgica também entra no volume de tratamento.
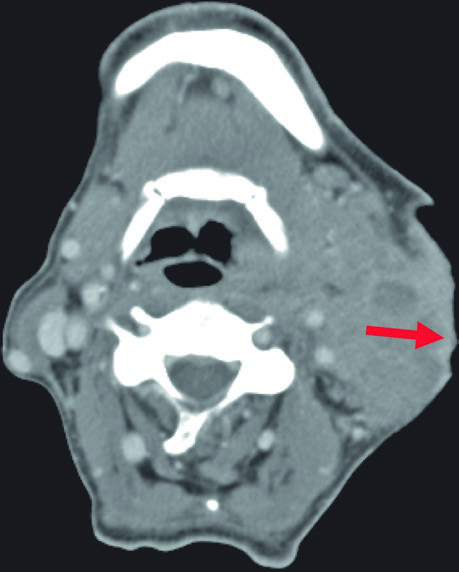
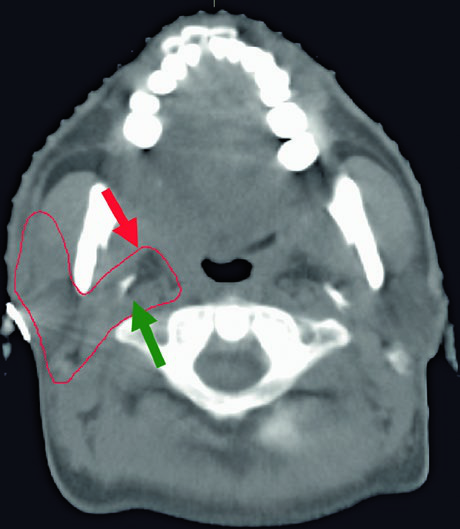
O comprometimento ósseo exige avaliação específica em janela óssea na TC. A imagem ao lado mostra reação periosteal na face posterior do ramo mandibular esquerdo, sugerindo envolvimento direto. Quando confirmado, a estrutura óssea deve ser incorporada ao CTV com margem adequada.
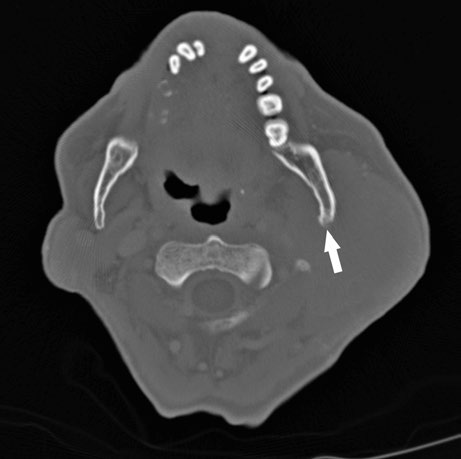
Esses achados reforçam a importância de um estudo de imagem completo antes da simulação. A combinação de janela de partes moles e janela óssea na mesma TC garante que nenhuma extensão tumoral passe despercebida. Na minha experiência, a integração de achados de RM — especialmente sequências com supressão de gordura — com a TC de simulação melhora consideravelmente a confiança no delineamento desses casos complexos.
Planejamento Pós-operatório da Glândula Submandibular
Os tumores submandibulares apresentam considerações específicas para o delineamento pós-operatório. O leito cirúrgico inteiro deve ser incluído, juntamente com todas as alterações pós-operatórias visíveis na TC de simulação. A glândula submandibular contralateral intacta serve como guia anatômico inestimável para definir os limites do CTV.
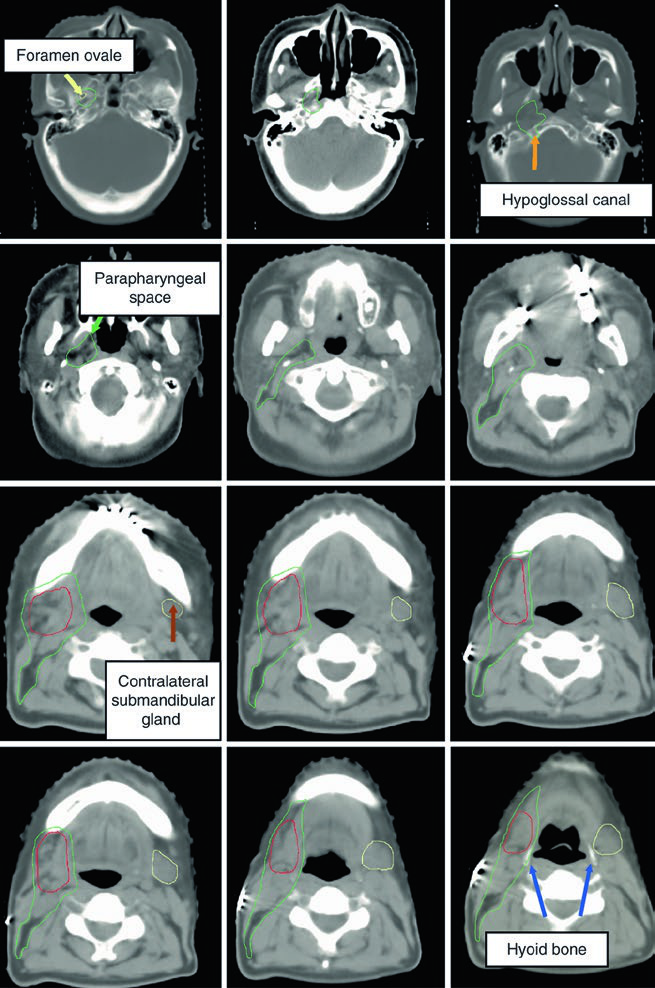
O trajeto do nervo lingual merece atenção particular. Ele se origina do ramo mandibular (V3) do trigêmeo no forame oval, desce profundamente ao músculo pterigoideo lateral e cursa entre o músculo pterigoideo medial e o ramo mandibular, dirigindo-se à face medial da glândula submandibular antes de terminar na língua. Quando o nervo lingual ou o nervo hipoglosso estão envolvidos, o CTV deve ser estendido até a base do crânio — especialmente no carcinoma adenoide cístico.
A imagem mostra um caso de carcinoma mucoepidermoide de alto grau cT1N1M0 da submandibular direita, com o CTV60–66 (vermelho) cobrindo o leito cirúrgico e o CTV50–54 (verde) englobando estações nodais ipsilaterais e o espaço parafaríngeo até a base do crânio. Essa abordagem garante cobertura adequada mesmo em tumores de estádio inicial mas alto grau.
O Nervo Glossofaríngeo e Sua Relevância no Delineamento
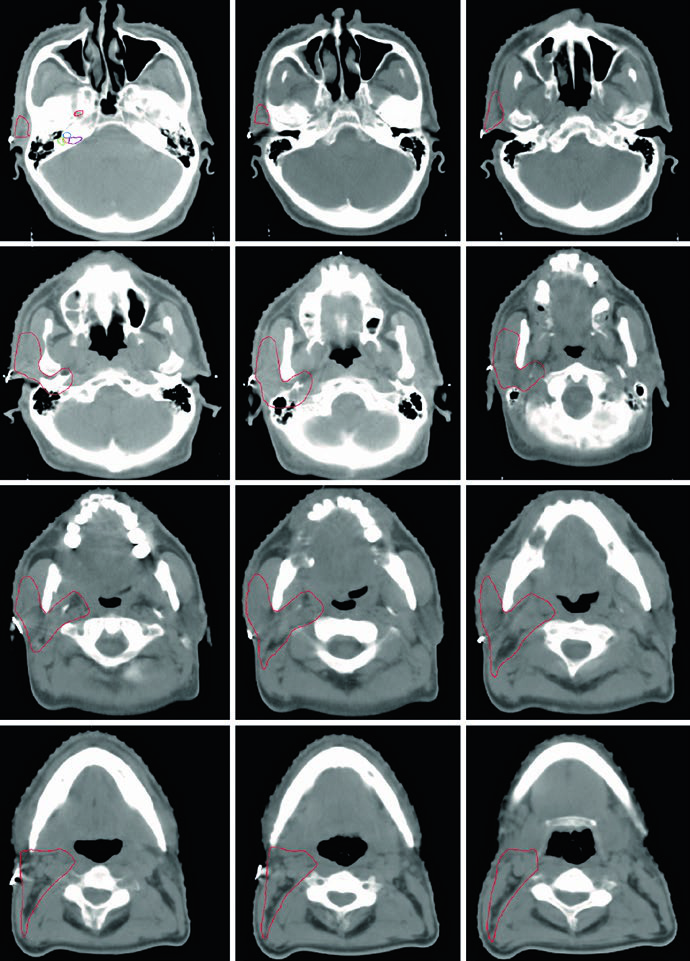
O nervo glossofaríngeo (IX par craniano) sai da base do crânio pelo forame jugular e desce pelo pescoço anterolateral à artéria carótida interna, medial ao processo estiloide. Termina em ramos para a faringe. Sua identificação é relevante porque, em tumores de parótida com disseminação perineural, o percurso desse nervo pode precisar ser incluído no CTV.
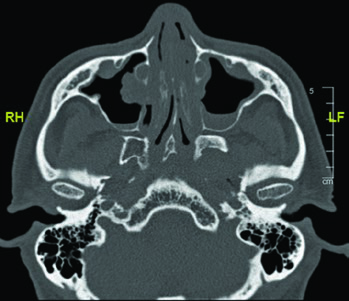
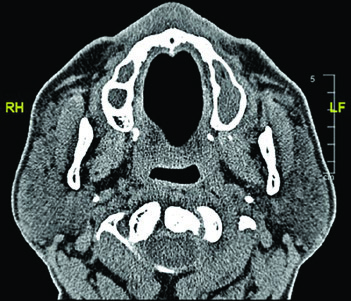
As imagens da TC demonstram o trajeto do nervo glossofaríngeo em diferentes cortes axiais. O nervo pode ser identificado posterolateral ao processo estiloide, descendo junto à carótida interna. A marcação oval vermelha nos cortes mostra a localização esperada do nervo ao longo de seu percurso cervical. O último corte utiliza janela de partes moles para melhor visualização das relações entre o nervo e os vasos cervicais.
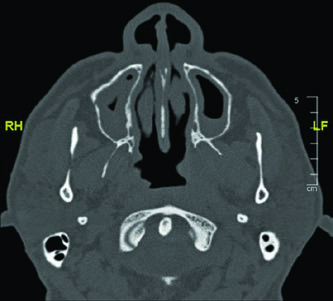
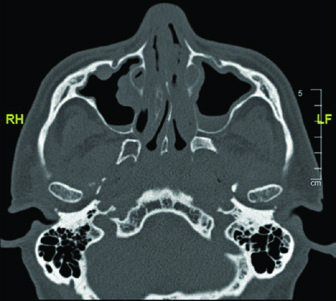
O domínio dessa anatomia é especialmente relevante quando se planeja irradiar carcinomas adenoides císticos da parótida, pois esse subtipo tem forte tendência a seguir bainhas neurais. A inclusão do percurso completo — do forame jugular até os ramos faríngeos — garante que a disseminação subclínica ao longo do nervo glossofaríngeo seja adequadamente coberta. Uma abordagem semelhante de mapeamento neural é discutida no contexto de primário oculto em cabeça e pescoço.
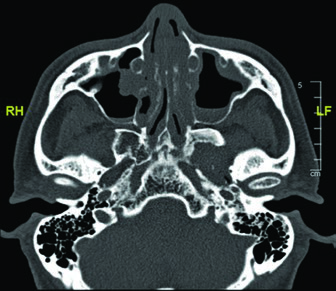
O papel dos clipes cirúrgicos não pode ser subestimado. Na ausência de clipes, o radioterapeuta depende exclusivamente das alterações pós-operatórias visíveis na TC de simulação — que podem ser ambíguas nas primeiras semanas após a cirurgia. Clipes posicionados nos limites do leito cirúrgico, nas margens mais próximas e ao longo do trajeto de nervos dissecados fornecem informação que nenhum exame de imagem sozinho consegue replicar. Essa colaboração entre cirurgião e radioterapeuta, iniciada no intraoperatório, é o que diferencia um delineamento adequado de um excelente.
Em resumo, o planejamento radioterápico das glândulas salivares maiores demanda avaliação minuciosa por imagem, conhecimento anatômico detalhado da base do crânio e dos espaços profundos cervicais, e compreensão dos padrões de disseminação perineural específicos de cada histologia. A colaboração estreita entre cirurgião e radioterapeuta — com colocação de clipes e descrição operatória detalhada — melhora substancialmente a qualidade do delineamento. Para a referência completa sobre volumes-alvo em radioterapia, consulte nosso guia completo sobre delineamento de volume alvo.