En Este Artículo
- 1. Qué es TSET y Por Qué Monte Carlo Marca la Diferencia
- 2. Simulación Monte Carlo de los Haces Utilizados en TSET
- 3. Validación de Haces en la Geometría de Entrega TSET
- 4. Uniformidad de Dosis y Distribuciones en el Paciente
- 5. Monte Carlo en Braquiterapia: Más Allá del TG-43
- 6. Herramientas de Cálculo MC para Braquiterapia
- 7. El Papel de la Imagen en la Asignación de Tejidos para MC
Qué es TSET y Por Qué Monte Carlo Marca la Diferencia
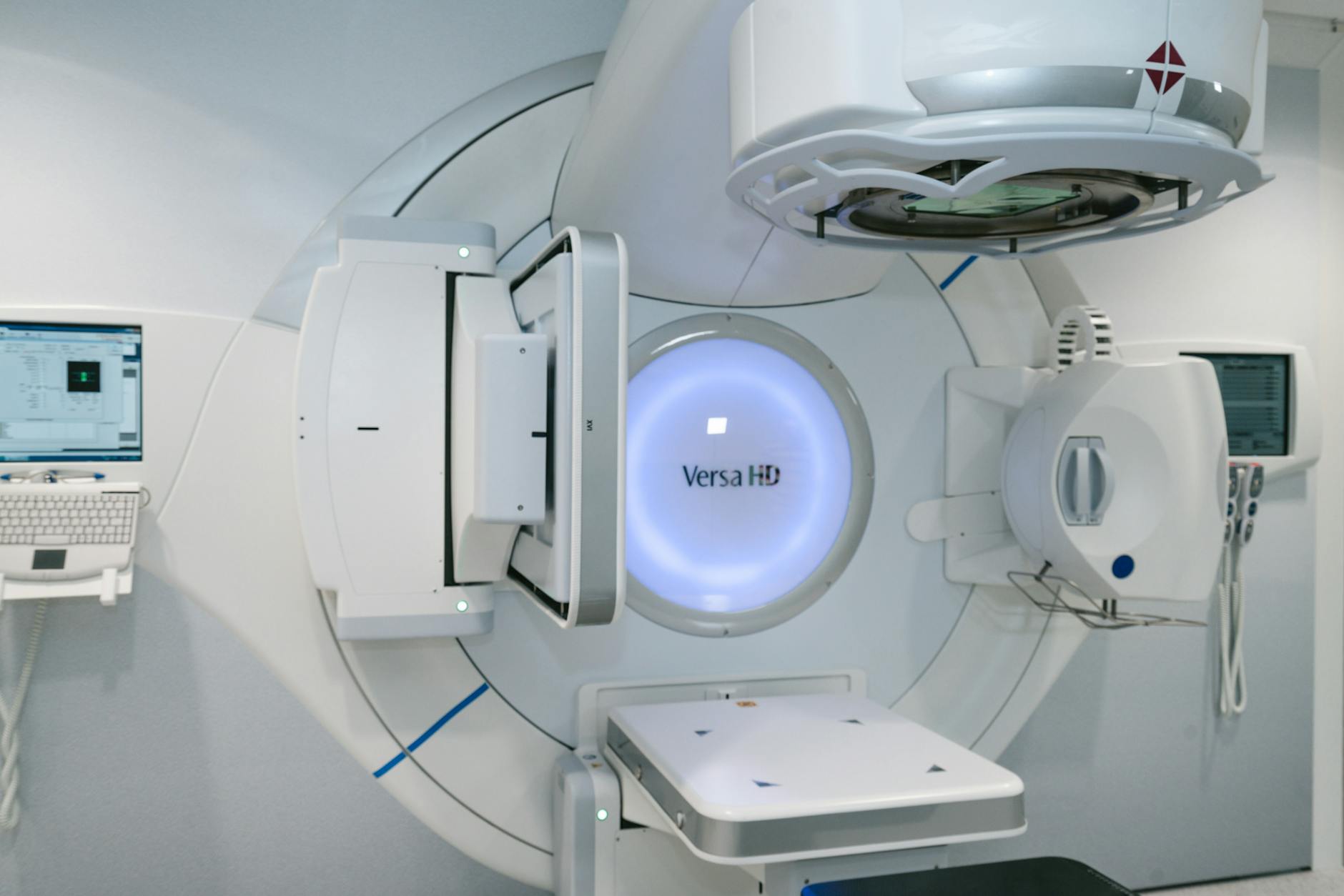
La irradiación total de piel con electrones (TSET) sigue siendo uno de los tratamientos más eficaces para el linfoma cutáneo de células T (micosis fungoide). En la práctica, se trata de un procedimiento especial que exige modificaciones en el equipo y una geometría de campo fuera de lo convencional — campos compuestos de aproximadamente 200 cm de altura por 80 cm de ancho, con SSDs nominales entre 300 y 500 cm.
Guía completa de la serie: para ver el panorama general y los artículos relacionados, vuelve a la guía completa sobre Monte Carlo en radioterapia.
El método Monte Carlo aportó a este escenario algo que décadas de dosimetría experimental no pudieron ofrecer: la visualización completa de las distribuciones de dosis en la piel del paciente, incluyendo análisis DVH a diferentes profundidades. Históricamente, la información de dosis provenía de películas, TLDs y cámaras de ionización en fantomas — datos útiles pero fundamentalmente limitados.
La energía nominal del haz de electrones más utilizada varía entre 4 y 9 MeV. Según las recomendaciones del AAPM Report 23, la dosis máxima debe ocurrir en la superficie, el nivel del 80% de la dosis prescrita necesita estar a una profundidad superior a 0,4 cm, y la dosis debe caer por debajo del 20% a 2 cm de profundidad. Para una visión integral, consulte nuestra guía completa sobre Técnicas de Monte Carlo en Radioterapia.
Simulación Monte Carlo de los Haces Utilizados en TSET
La simulación de haces para TSET utiliza el sistema EGSnrc, partiendo de la geometría detallada del cabezal del LINAC. Ding et al. modelaron haces de 6 MeV a partir de aceleradores Varian Clinac 21EX y Varian TrueBeam — dos máquinas con enfoques de simulación distintos.
Para el Clinac 21EX, la simulación comienza con electrones saliendo de la ventana de vacío. La energía y el tamaño del spot del haz se ajustan para obtener la mejor concordancia entre mediciones y cálculos. Para el TrueBeam, el punto de partida son archivos de phase-space proporcionados directamente por Varian, registrados en el plano justo encima de los colimadores x-y — sin necesidad de ajuste.
Los parámetros estándar del EGSnrc se utilizan en las simulaciones: $AE = ECUT = 0,521$ MeV, $AP = PCUT = 0,010$ MeV, sin forzamiento de interacción fotónica y sin dispersión Rayleigh. Los haces simulados, almacenados en archivos phase-space a SSD = 100 cm, alimentan el código DOSXYZnrc para los cálculos de dosis posteriores.
Un hallazgo particularmente relevante: Ding et al. no observaron aumento significativo de la dosis de bremsstrahlung a distancias extendidas, contradiciendo el valor de hasta 5% reportado por Das et al. La dosis de bremsstrahlung para un haz de 6 MeV quedó entre 0,5% y 1% para SSDs de 100 a 700 cm. Para más detalles sobre modelado de haces de electrones, consulte nuestro artículo sobre cálculo de dosis en paciente y aplicaciones en electrones.
Validación de Haces en la Geometría de Entrega TSET
Validar la simulación en la geometría real de tratamiento es un paso obligatorio. La técnica emplea campos duales rotacionales: el paciente se coloca sobre una plataforma giratoria, mientras una placa de acrílico transparente (90 cm × 200 cm) funciona como degradador de haz, reduciendo la energía de los electrones y aumentando la dispersión.
Las mediciones de validación se realizaron con dosímetros nanoDot (tecnología OSL de LANDAUER) sobre un fantoma cilíndrico equivalente a agua (29 cm de diámetro, 30 cm de longitud) cubierto con dos capas de bolus de 5 mm. Los dosímetros se colocaron en la superficie del fantoma y entre las capas de bolus.
La comparación entre perfiles de dosis medidos y calculados en la placa dispersora mostró una concordancia excelente. Los perfiles son muy sensibles al tamaño de campo. Para el campo de 40 × 40 cm², la dosis en los bordes es menor que para 36 × 36 cm² porque ambos campos duales contribuyen en el centro, mientras que en los extremos solo contribuye un campo.
Uniformidad de Dosis y Distribuciones en el Paciente
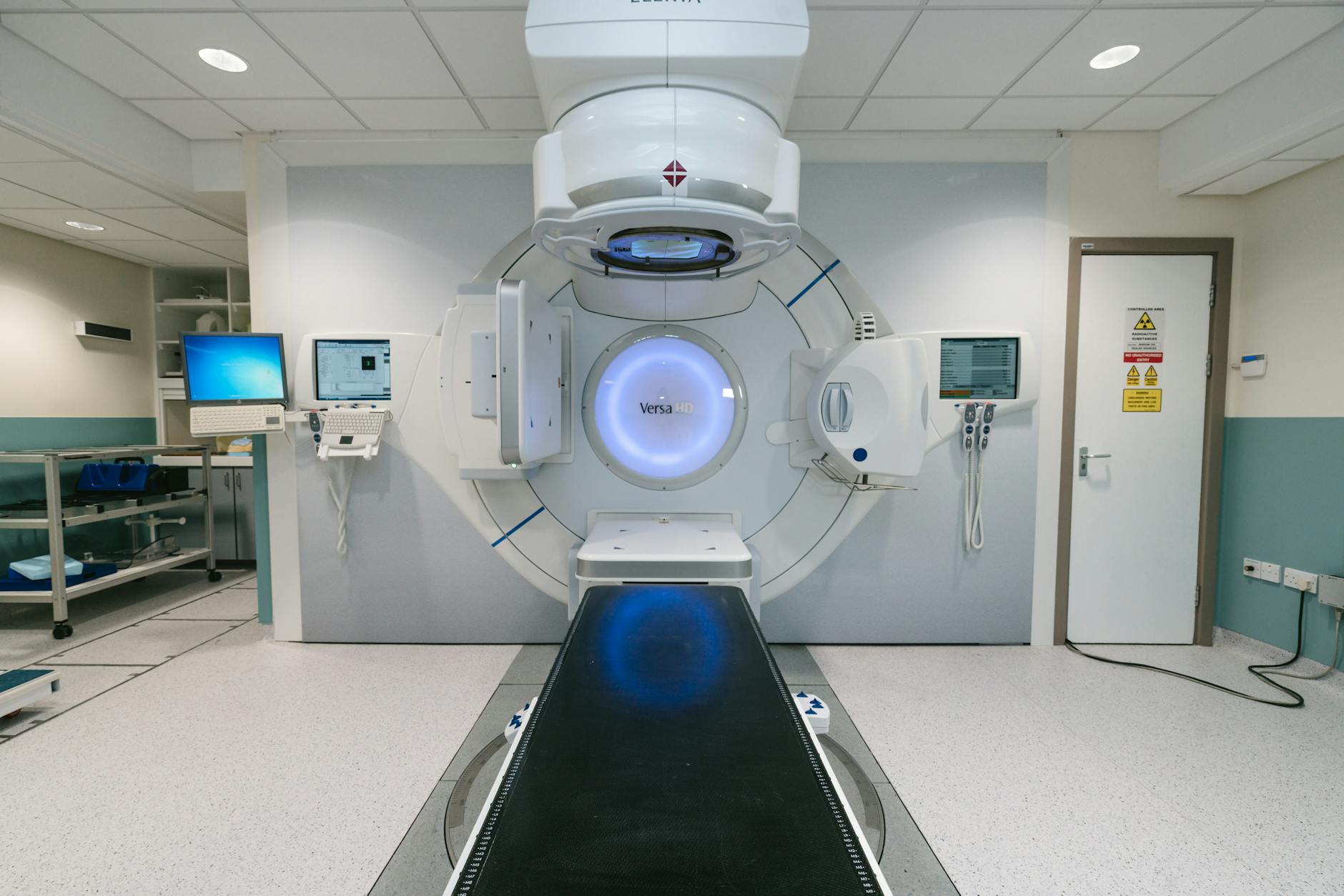
El torso humano se asemeja a una forma ovalada, y esta geometría irregular tiene consecuencias directas en la distribución de dosis. Simulaciones Monte Carlo en un fantoma cilíndrico ovalado (eje largo de 40 cm, eje corto de 20 cm) revelan dosis significativamente menores en las superficies del eje corto — correspondientes a las regiones anterior y posterior del torso.
El espesor de la placa degradadora influye directamente en la cobertura de dosis en profundidad. Simulaciones con placas de 3 mm, 9 mm y sin placa muestran que el máximo de dosis ocurre en la superficie incluso sin la placa, gracias a la incidencia de electrones desde múltiples direcciones durante la rotación. Basándose en los resultados Monte Carlo, Ding et al. recomiendan una placa de 3 mm con campo de 40 × 40 cm² para una cobertura óptima.
Las distribuciones de dosis en anatomía real del paciente (basadas en CT) muestran variaciones de dosis cutánea superiores al 20%, consistentes con mediciones in vivo. Los análisis DVH en tres intervalos de profundidad — 0–5 mm, 5–10 mm y 10–15 mm — proporcionan información que ningún método experimental puede obtener con tal detalle.
Monte Carlo en Braquiterapia: Más Allá del TG-43
El formalismo TG-43 fue un hito en la dosimetría de braquiterapia. Sin embargo, sus simplificaciones se vuelven problemáticas en situaciones específicas. La superposición de distribuciones de dosis de fuente única ignora la atenuación intersemillas (ISA), las heterogeneidades tisulares y los efectos de blindaje del aplicador.
| Sitio Anatómico | Energía Fuente | Absorción | Atenuación | Blindaje | Dispersión | Breakdown Dosis=Kerma |
|---|---|---|---|---|---|---|
| Próstata | Alta | N | N | N | N | N |
| Próstata | Baja | Y | Y | Y | N | N |
| Mama | Alta | N | N | N | Y | N |
| Mama | Baja | Y | Y | Y | N | N |
| GYN | Alta | N | N | Y | N | N |
| Piel | Alta | N | N | Y | Y | N |
| Pulmones | Alta | N | N | N | Y | Y |
| Ojos | Alta | N | N | Y | Y | Y |
| Ojos | Baja | Y | Y | Y | Y | N |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022), Table 16.1, adaptada de Rivard et al.
Para fuentes de baja energía, el coeficiente de absorción másica de energía $\mu_{en}/\rho$ varía significativamente entre tejidos por la dependencia aproximada de $Z^{3-4}$ de la sección eficaz fotoeléctrica. Bajo equilibrio de partículas cargadas, $D_{tejido}/(\mu_{en}/\rho)_{tejido} = D_{agua}/(\mu_{en}/\rho)_{agua}$, lo que significa que la dosis en tejido puede diferir sustancialmente de la dosis en agua.
El impacto clínico es concreto. Carrier et al. demostraron, en un estudio retrospectivo de 28 pacientes con cáncer de próstata implantados con $^{125}$I, una reducción promedio del 7% en el $D_{90}$ al considerar ISA y heterogeneidades tisulares. Las calcificaciones intraprostáticas pueden causar reducciones del $D_{90}$ de hasta un 25%. Para implantes mamarios con $^{103}$Pd, las reducciones oscilan entre 4% y 35%. Para más detalles, consulte nuestro artículo sobre haces de electrones y modelado de fuentes en braquiterapia.
Herramientas de Cálculo MC para Braquiterapia
Diversas plataformas de cálculo Monte Carlo han sido desarrolladas para dosimetría de braquiterapia específica por paciente. Cada una aporta un enfoque distinto para resolver el mismo problema fundamental.
| Herramienta | Motor MC | Tamaño Voxel | Tiempo de Cálculo | Incertidumbre Estadística |
|---|---|---|---|---|
| MCPI | GEPTS | 2 mm³ | ~1 min | 2% |
| PTRAN_CT | EGSnrc (correlated sampling) | 2 mm³ | ~3 s | 2% |
| BrachyDose | EGSnrc | 2 mm³ | ~30 s | <2% |
| ALGEBRA | GEANT4 | 2 mm³ | 6–12 min | 2% |
| egs_brachy | EGSnrc (egs++) | 2 mm³ (próstata) / 1 mm³ (ojo) | 13–39 s | 2% |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
PTRAN_CT merece mención especial por su implementación de correlated sampling: las historias de fotones se construyen primero en agua homogénea y luego se recalculan los pesos de las partículas para la geometría heterogénea, aumentando la eficiencia por factores de 2 a 40.
egs_brachy, como aplicación moderna del EGSnrc, se distribuye como software libre y de código abierto, con una biblioteca verificada de geometrías de fuentes, aplicadores y fantomas. Los tiempos de simulación oscilan entre 13 y 39 segundos para alcanzar un 2% de incertidumbre promedio en la dosis del blanco.
El Papel de la Imagen en la Asignación de Tejidos para MC
La precisión del cálculo Monte Carlo depende directamente de la correcta asignación de secciones eficaces de fotones vóxel a vóxel. La tomografía computarizada (CT) proporciona datos de atenuación convertibles en densidad electrónica o másica.
Para fuentes de baja energía, la CT de doble energía (DECT) puede proporcionar estimaciones más precisas de la composición elemental de los tejidos. La resonancia magnética, con su excelente contraste en tejidos blandos, ofrece alternativas para contornear el volumen blanco.
Landry et al. investigaron la sensibilidad de las distribuciones de dosis a la composición tisular para implantes de próstata con $^{125}$I y mama con $^{103}$Pd. Dos composiciones elementales de la próstata resultaron en variaciones del 3,5% en el $D_{w,m,90\%}$. Para mama, la variabilidad en la composición tisular produjo variaciones de dosis de hasta un 10%. Estos números refuerzan que la asignación precisa de tejidos no es solo un detalle técnico — es un factor determinante en la precisión dosimétrica.
El avance continuo de estas técnicas apunta hacia un futuro donde el cálculo Monte Carlo será herramienta de rutina en la planificación de braquiterapia. Para más información, consulte nuestra guía completa sobre técnicas de Monte Carlo en radioterapia.