Radioterapia definitiva para cáncer ginecológico: por qué la IMRT transformó el estándar
La radioterapia definitiva para tumores ginecológicos con útero intacto exige una delineación precisa de volúmenes blanco y restricciones rigurosas de dosis a órganos en riesgo. La IMRT se ha consolidado como el abordaje estándar en este escenario, respaldada por múltiples ensayos fase II y estudios controlados que demuestran eficacia equivalente a las técnicas convencionales con un perfil de toxicidad significativamente mejor — especialmente gastrointestinal, hematológica y de fracturas pélvicas. Protocolos fase III como el NRG-GY006 ya incorporan la IMRT como tratamiento estándar, reflejando su amplia aceptación. Para una visión completa del tema, consulte nuestra guía completa sobre delineación de volúmenes blanco.
Sin embargo, la aplicación de IMRT en pacientes con útero intacto es más compleja que en el escenario posoperatorio. La movilidad de los blancos y los órganos en riesgo es considerablemente mayor, la intensidad del tratamiento es más alta — con quimioterapia concurrente seguida de braquiterapia y/o refuerzos nodales —, y las dosis totales entregadas son superiores. La dosis en tejido normal se convierte en un factor crítico tanto para la tolerancia al tratamiento como para el riesgo de complicaciones tardías de alto grado.
Evaluación clínica y estadificación por imagen
Toda paciente debe someterse a historia clínica completa y examen físico detallado, con atención especial al examen pélvico: tamaño y localización del tumor, extensión vaginal, compromiso uretral, parametrial y/o de pared lateral. Si la paciente no tolera un examen ambulatorio adecuado, puede ser necesario el examen bajo anestesia.
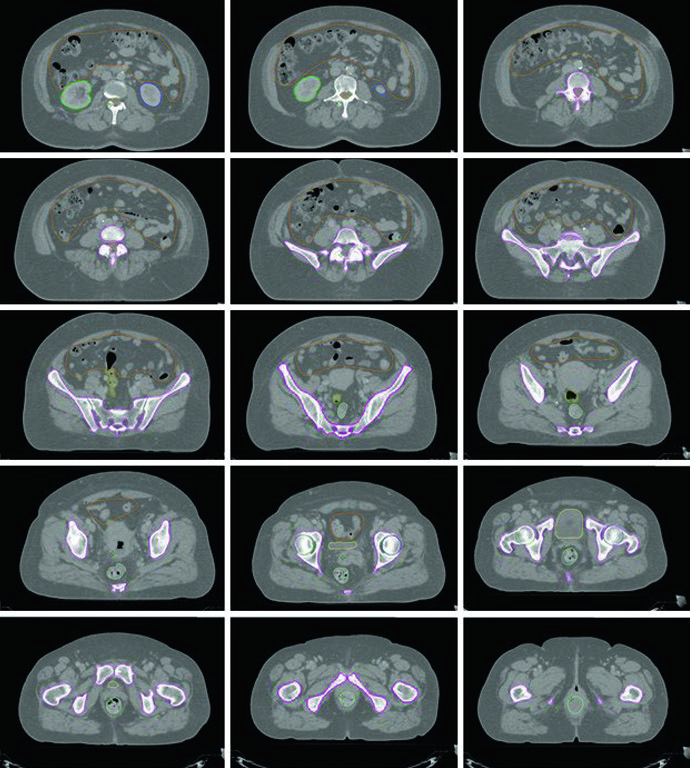
La resonancia magnética con contraste dinámico es el método óptimo para detectar invasión cervical y miometrial, con precisión del 85–93%, y ha demostrado superioridad sobre la TC y el examen físico para determinar tamaño tumoral y extensión de la invasión. Para la evaluación de metástasis ganglionares, la RM presenta sensibilidad del 27–66% con especificidad del 73–94% en pacientes estadificadas quirúrgicamente. Cuando está disponible, el PET/TC es preferible, con sensibilidad y especificidad de 50–100% y 87–100%, respectivamente.
La estadificación radiológica con PET/TC de cuerpo entero se recomienda para pacientes con enfermedad FIGO estadio IB o superior, dada su mayor sensibilidad comparada con la TC sola, y ahora es admisible para fines de estadificación FIGO. La FIGO ha publicado sistemas de estadificación para cánceres cervical, endometrial y ovárico, complementados por los sistemas TNM del AJCC.
Simulación por TC y preparación para planificación
La simulación por TC debe obtenerse con la paciente en posición supina con cuna de inmovilización personalizada para minimizar errores de posicionamiento. Los cortes deben tener espesor ≤3 mm. Dos detalles prácticos merecen atención: el grado de llenado vesical y rectal en la simulación debe replicar idealmente lo que se observará durante el tratamiento diario.
El tratamiento puede realizarse con vejiga cómodamente llena o vacía. Se recomienda mantener consistencia en el estado de llenado vesical entre simulación y tratamiento diario. La vejiga vacía tiende a ser más reproducible y reduce la variación absoluta del volumen vesical. La vejiga llena puede desplazar asas intestinales del campo de tratamiento, mejorando la dosimetría intestinal. La preparación intestinal con enema permite lograr un recto vacío en la simulación.
La simulación con contraste intravenoso se recomienda, ya que la vasculatura pélvica sirve como referencia para la localización ganglionar — salvo contraindicación médica. Marcadores fiduciales colocados antes de la simulación o marcadores radiopacos en el ápex vaginal e introito al momento de la simulación mejoran la delineación de volúmenes. Las pacientes con enfermedad que compromete la mitad distal de la vagina deben recibir RT inguinal bilateral; en ese caso, la simulación puede realizarse en posición de «piernas de rana» para minimizar toxicidad en pliegues cutáneos.
Principios de delineación de volúmenes blanco
La fusión del PET/TC pretratamiento con la TC de simulación se recomienda para asistir la delineación del GTV. Se han publicado guías internacionales de consenso para contorneo en casos definitivos de cérvix, y están disponibles casos de muestra interactivos en plataformas educativas como eContour.
Un estudio con RM usando partículas de óxido de hierro inyectadas demostró que el 95% de los ganglios pélvicos (ilíaco común, ilíaco interno, ilíaco externo medial y anterior, y obturadores) se ubican dentro de 7 mm de la vasculatura pélvica. Los ganglios inguinales, sin embargo, deben delinearse usando un abordaje de compartimento anatómico dada la mayor variabilidad de ubicación respecto a los vasos.
Problemas frecuentes en ensayos multicéntricos incluyen: margen inadecuado alrededor de la vasculatura con CTV demasiado cercano a los vasos, cobertura insuficiente alrededor de la vasculatura ilíaca interna inferior y posterior, cobertura insuficiente alrededor de la vasculatura obturadora inferior y anterolateral, cobertura presacra insuficiente y extensión innecesaria del CTV hacia las concavidades sacras.
Definición de volúmenes según protocolo NRG-GY006
| Volumen | Definición |
|---|---|
| GTV | Toda enfermedad macroscópica visible, evaluada por información clínica, examen físico, estudios radiográficos, examen endoscópico y biopsias |
| CTV1 | GTV + cérvix + útero |
| CTV2 | Parametrios y tercio superior de la vagina (mitad superior si la vagina está clínicamente comprometida) |
| CTV3 | Ganglios ilíacos comunes, ilíacos externos, ilíacos internos y presacros. Borde superior en bifurcación aórtica (≈ L4–L5). Presacros hasta S2–S3. Ilíacos externos hasta el tope de las cabezas femorales. Margen de 7 mm alrededor de los vasos, excluyendo hueso, músculo e intestino |
| CTV_boost | Ganglios pélvicos macroscópicos; incluye parametrio si se indica refuerzo parametrial |
| ITV | CTV1 delineado en TC con vejiga llena y vacía, combinados |
| PTV1 | CTV1 + 15 mm de expansión uniforme |
| PTV2 | CTV2 + 10 mm de expansión uniforme |
| PTV3 | CTV3 + 5 mm de expansión uniforme |
| PTV4 | ITV + 7 mm de expansión uniforme |
| PTV_boost | CTV_boost + 5 mm de expansión uniforme |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 21.1, protocolo NRG-GY006)
Órganos en riesgo y restricciones de dosis
Los OARs estándar incluyen intestino, recto, médula ósea, vejiga y cabezas femorales. Para pacientes con campo extendido, se agregan riñones bilaterales, médula espinal, duodeno e hígado. Estudios de modelado NTCP han establecido restricciones validadas para intestino y médula ósea en pacientes con cáncer cervical tratadas con quimiorradioterapia.
| OAR | Parámetro dosimétrico | Protocolo | Variación aceptable |
|---|---|---|---|
| Espacio intestinal | V45 (cc) | ≤200 | ≤250 |
| Espacio intestinal | DMax (Gy) | ≤59,4 | ≤62,1 |
| Espacio intestinal | D30% (Gy) | ≤40 | ≤50 |
| Recto | D50% (Gy) | ≤45 | ≤54 |
| Recto | D60% (Gy) | ≤30 | ≤50 |
| Recto | DMax (Gy) | ≤50 | ≤55 |
| Médula ósea | Dmean (Gy) | ≤27 | ≤29 |
| Médula ósea | V10 (%) | ≤85,5 | ≤90 |
| Médula ósea | V20 (%) | ≤66 | ≤75 |
| Vejiga | D50% (Gy) | ≤45 | ≤55 |
| Vejiga | DMax (Gy) | ≤50 | ≤57,5 |
| Cabezas femorales | D15% (Gy) | ≤30 | ≤50 |
| Cabezas femorales | DMax (Gy) | ≤50 | ≤55 |
| Riñones (campo extendido) | D50% (Gy) | ≤18 | ≤20 |
| Médula espinal (campo extendido) | D0,03cc (Gy) | ≤45 | ≤47,5 |
| Duodeno (campo extendido) | D0,03cc (Gy) | ≤56 | ≤60 |
| Duodeno (campo extendido) | D50% (Gy) | ≤40 | ≤50 |
| Hígado (campo extendido) | D50% (Gy) | ≤25 | ≤30 |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 21.2, protocolo NRG-GY006)
La IMRT ha demostrado reducir la toxicidad GI y hematológica, y puede mejorar la toxicidad urinaria reportada por la paciente. El PET/TC puede segmentar subregiones activas de médula ósea donde la acumulación de dosis se correlaciona con mayores tasas de toxicidad hematológica. Preservar la médula metabólicamente activa con IMRT redujo la neutropenia y mejoró la tolerancia a la quimioterapia en ensayos clínicos prospectivos.
Evaluación del plan y entrega guiada por imagen
Al menos el 95% del PTV debe recibir el 100% de la dosis prescrita, y ≥99% del PTV debe recibir al menos el 90% de la prescripción. El máximo de dosis debe ocurrir dentro del PTV, y las áreas que superen el 100% fuera del PTV deben minimizarse. Los flujos de planificación basados en conocimiento ayudan a lograr dosimetría óptima en planes de IMRT complejos.
Las pacientes tratadas con arreglos de haces convencionales deben realizar imágenes al menos semanales con portales MV. La imagen ósea diaria con kV o CBCT facilita la reducción de márgenes de planificación a 5 mm alrededor del CTV nodal. Las pacientes con IMRT deben recibir CBCT al menos semanal — idealmente cada fracción — para verificar variaciones en la posición del blanco por cambios en el llenado rectal, vesical o movimiento uterino.
Cáncer cervical: delineación y prescripción de dosis
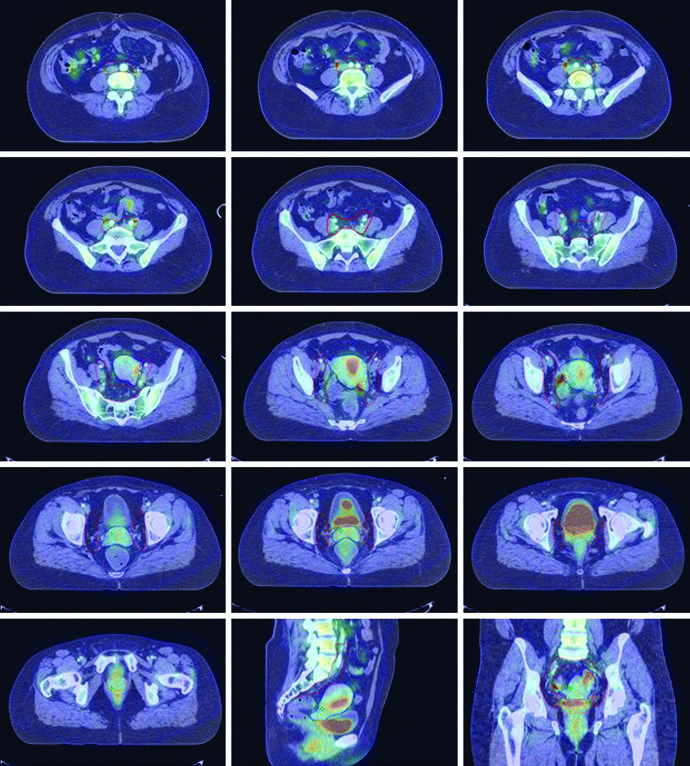
La diseminación linfática regional del cáncer cervical sigue un patrón escalonado: los ganglios paracervicales drenan hacia los obturadores, ilíacos internos e ilíacos externos, seguidos por los ilíacos comunes y paraaórticos. Las pacientes con lesiones que comprometen la vagina distal están en riesgo de metástasis inguinales.
Cuando los ganglios paraaórticos están comprometidos, se debe emplear una técnica de campo extendido, extendiendo el borde craneal del CTV superiormente hasta el interespacio L1/L2 o 3 cm craneal al ganglio más superior comprometido. Los PTVs se crean para cada CTV y el PTV final es la combinación de todos. Se utilizan expansiones diferenciales CTV-PTV para cada componente basadas en el grado de movimiento orgánico interno e incertidumbre de posicionamiento.
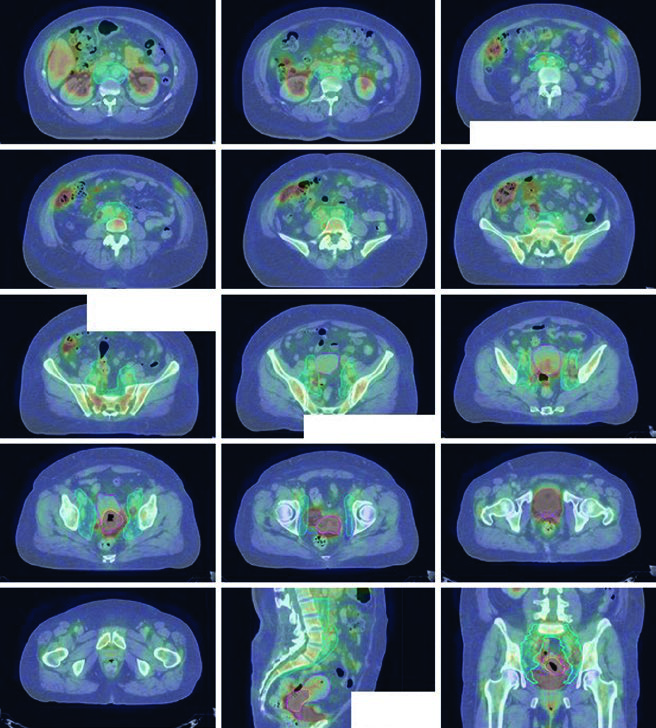
La prescripción de dosis típica es 45 Gy en 25 fracciones para la pelvis ganglio-negativa, o 47,6 Gy en 28 fracciones si hay enfermedad nodal, con boost integrado simultáneo (SIB) a ganglios comprometidos hasta 59,4 Gy. La dosis del boost nodal y/o la dosis por fracción pueden requerir reducción para respetar la tolerancia intestinal. Un refuerzo parametrial puede agregarse a criterio médico para compromiso parametrial, siempre que ese lado no reciba SIB dentro del campo de refuerzo. Los campos AP/PA convencionales para refuerzo parametrial incluyen articulaciones sacroilíacas (borde superior), fondo del agujero obturador (borde inferior) y músculo obturador interno (bordes laterales) con bloque de línea media de 4–5 cm. Prescripción típica: 6–10 Gy en 3–5 fracciones. El boost de braquiterapia es estándar hacia el final o después de completar la EBRT. Para profundizar sobre braquiterapia, consulte nuestro artículo dedicado sobre braquiterapia guiada por imagen.
Cáncer vaginal: abordaje y planificación
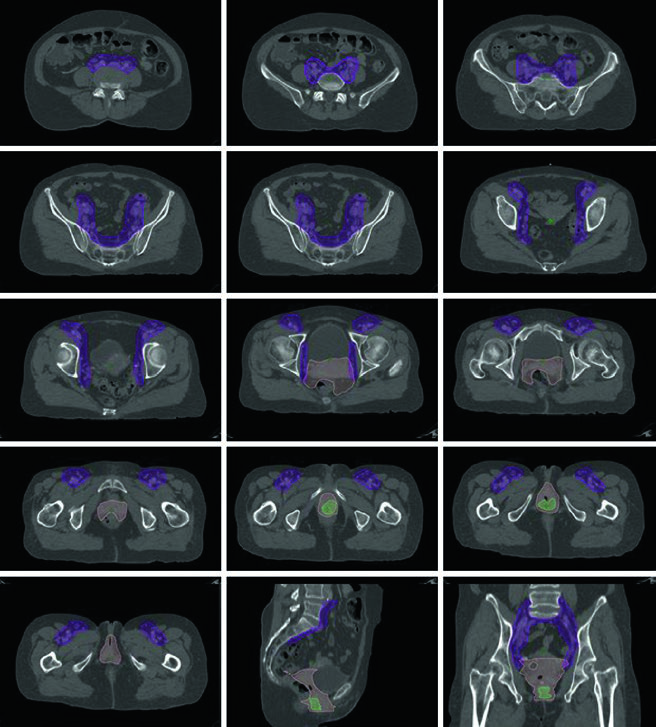
Los tumores primarios vaginales son relativamente raros — cualquier tumor que comprometa el cérvix o la vulva se clasifica como cáncer cervical o vulvar, respectivamente. Faltan datos prospectivos específicos para guiar el manejo del cáncer vaginal, y el abordaje recomendado es individualizado, frecuentemente siguiendo las guías de cáncer cervical.
Para enfermedad estadio I, la RT definitiva con EBRT y braquiterapia es una excelente opción, aunque la cirugía definitiva es alternativa para pacientes seleccionadas con enfermedad no voluminosa, distal y no uretral. Para estadios II-IVA, la quimiorradiación definitiva es estándar. La EBRT pélvica estándar debe cubrir toda la vagina. Las pacientes con enfermedad en la mitad distal de la vagina deben recibir RT inguinal bilateral.
Los marcadores fiduciales temporales pueden delinear el ápex vaginal e introito en la simulación por TC. La prescripción típica de EBRT es 45 Gy en 25 fracciones para pelvis y toda la vagina, seguida de boost de braquiterapia (por ejemplo, 6 Gy × 4 fracciones). Para más sobre el manejo del cáncer de vulva con IMRT, consulte nuestro artículo dedicado.
Cáncer endometrial: anatomía, diseminación y volúmenes
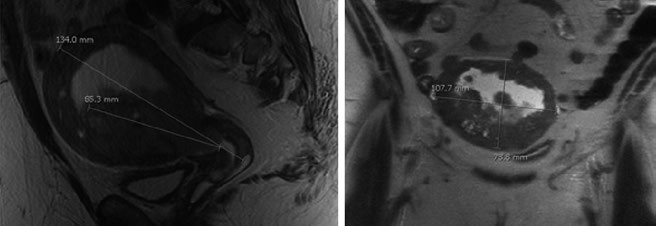
El útero está delimitado anteriormente por la vejiga y posteriormente por el recto, cubierto por reflexiones peritoneales, y se divide en fondo, istmo y cérvix. La pared uterina consiste en una capa muscular lisa externa (miometrio) y una capa interna de epitelio glandular (endometrio). Está soportado por cinco ligamentos: ancho, redondo, cardinal, uterosacro y vesicouterino.
Las áreas ganglionares en riesgo incluyen ganglios obturadores, ilíacos externos, ilíacos internos, ilíacos comunes y paraaórticos. Las lesiones del fondo uterino pueden diseminarse directamente a ganglios paraaórticos. La incidencia de compromiso ganglionar pélvico y paraaórtico varía según categorías de riesgo (bajo, medio y alto), tamaño tumoral y profundidad de invasión, según definido en el estudio GOG-33.
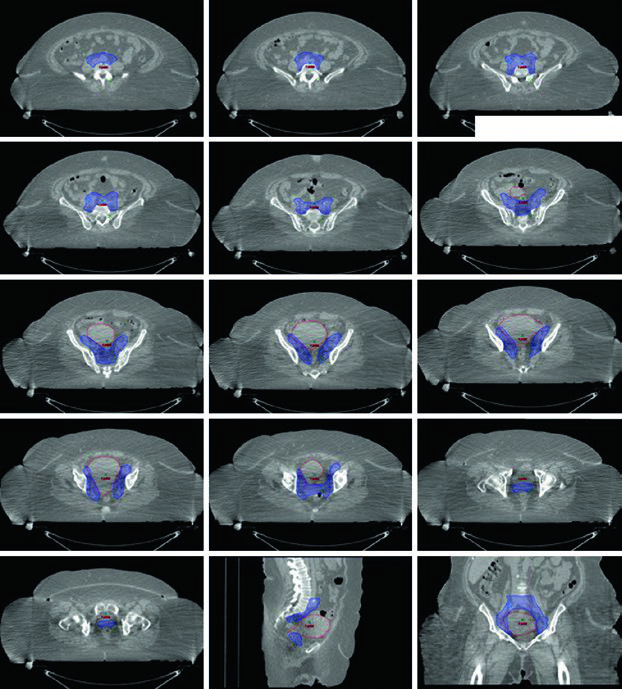
La histerectomía es el tratamiento estándar para candidatas quirúrgicas, con consideración de RT adyuvante basada en factores de riesgo patológicos. Para pacientes clínicamente inoperables, el tratamiento estándar es RT definitiva con braquiterapia, con o sin EBRT. La EBRT sola puede considerarse para pacientes inelegibles o que rechacen la braquiterapia. Las pacientes con enfermedad recurrente también son candidatas a EBRT.
Para EBRT + braquiterapia, la dosis estándar de EBRT es 45 Gy en 25 fracciones. Para EBRT sola, la RT pélvica puede seguirse de boost cone-down al útero y cérvix. La SBRT puede considerarse si la braquiterapia no es factible.
La delineación sigue los principios del cáncer cervical. El GTV incluye toda enfermedad macroscópica. El CTV se divide en CTV1 (GTV + útero entero), CTV2 (tejidos paravaginales/parametriales + 3 cm de vagina proximal) y CTV3 (igual al escenario posoperatorio). Con compromiso vaginal del tercio distal, los ganglios inguinales deben contornearse continuamente desde los ilíacos externos hasta 2 cm caudal a la unión safeno-femoral. Con compromiso paraaórtico, campo extendido según la Tabla 21.1. Expansiones diferenciales: PTV1 = 15 mm, PTV2 = 7–10 mm, PTV3 = 5–7 mm. Un boost adicional de 5–15 Gy puede agregarse para enfermedad nodal macroscópica o compromiso parametrial, con SIB o abordaje secuencial.
Para conocer tecnologías más recientes en este contexto, consulte nuestro artículo sobre tecnologías avanzadas en radioterapia ginecológica. El escenario posoperatorio se aborda en detalle en nuestro artículo dedicado sobre RT ginecológica posoperatoria.




