Radioterapia definitiva para câncer ginecológico: por que a IMRT mudou o jogo
A radioterapia definitiva para tumores ginecológicos com útero intacto exige delineamento preciso de volumes-alvo e órgãos de risco. A IMRT se consolidou como abordagem padrão nesse cenário, com múltiplos ensaios fase II e estudos controlados demonstrando eficácia equivalente às técnicas convencionais e perfil de toxicidade significativamente melhor — especialmente gastrointestinal, hematológica e de fraturas pélvicas. Na prática, protocolos fase III como o NRG-GY006 já incorporam a IMRT como tratamento-padrão, o que reflete a aceitação ampla da técnica. Para uma visão completa do tema, confira nosso guia completo sobre delineamento de volumes-alvo.
Entretanto, a aplicação da IMRT em pacientes com útero intacto é mais complexa que no cenário pós-operatório. A mobilidade dos alvos e dos órgãos de risco é consideravelmente maior, a intensidade do tratamento é mais alta — com quimioterapia concomitante seguida de braquiterapia e/ou boosts nodais —, e as doses totais entregues são superiores. A dose em tecido normal se torna fator crítico tanto para tolerância ao tratamento quanto para risco de complicações tardias de alto grau.
Avaliação clínica e estadiamento por imagem
Toda paciente deve passar por história clínica completa e exame físico detalhado, com atenção especial ao exame pélvico: tamanho e localização do tumor, extensão vaginal, envolvimento uretral, parametrial e/ou da parede lateral. Se a paciente não tolerar exame ambulatorial adequado, exame sob anestesia pode ser necessário.
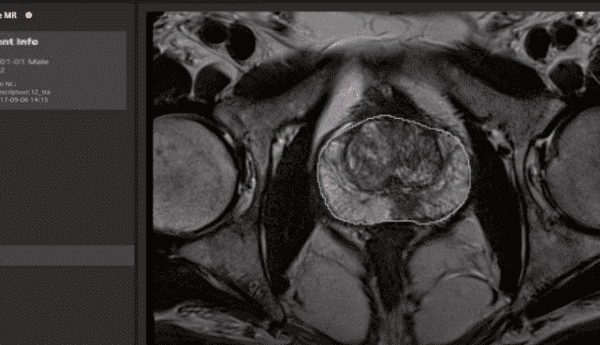
A ressonância magnética com contraste dinâmico é o método ideal para detectar invasão cervical e miometrial, com acurácia de 85–93%, e demonstrou superioridade sobre a TC e o exame físico na determinação do tamanho tumoral e extensão da invasão. Para avaliação de metástases linfonodais, a RM apresenta sensibilidade de 27–66% com especificidade de 73–94% em pacientes estadiadas cirurgicamente. Quando disponível, o PET/CT é preferível, com sensibilidade e especificidade de 50–100% e 87–100%, respectivamente.
O estadiamento radiológico com PET/CT de corpo inteiro é recomendado para pacientes com doença FIGO estágio IB ou superior, dada sua maior sensibilidade em relação à TC isolada, e agora é admissível para fins de estadiamento FIGO. A FIGO publicou sistemas de estadiamento específicos para cânceres cervical, endometrial e ovariano, além dos sistemas TNM do AJCC.
Simulação por TC e preparo para planejamento
A simulação por TC deve ser obtida com a paciente em posição supina, com berço de imobilização customizado para minimizar erros de posicionamento. Os cortes devem ter espessura ≤3 mm. Dois detalhes práticos merecem atenção especial: o grau de enchimento vesical e retal na simulação deve replicar o que se observará durante o tratamento diário.
O tratamento pode ser realizado com bexiga confortavelmente cheia ou vazia. Recomenda-se manter consistência no estado de enchimento vesical entre simulação e tratamento diário. Bexiga vazia tende a ser mais reprodutível e reduz a variação absoluta do volume vesical. Já bexiga cheia pode deslocar alças intestinais do campo de tratamento, melhorando a dosimetria intestinal. Para limpeza retal, pode-se usar enema para obter reto vazio na simulação.
A simulação com contraste intravenoso é recomendada, pois a vasculatura pélvica serve como referência para localização dos linfonodos — salvo contraindicação médica. Marcadores fiduciais colocados antes da simulação ou marcadores radiopacos no ápice vaginal e introito no momento da simulação ajudam a melhorar o delineamento dos volumes. Pacientes com doença envolvendo a metade distal da vagina devem receber RT inguinal bilateral; nesse caso, a simulação pode ser realizada na posição “pernas de rã” para minimizar toxicidade em dobras cutâneas.
Princípios de delineamento de volumes-alvo
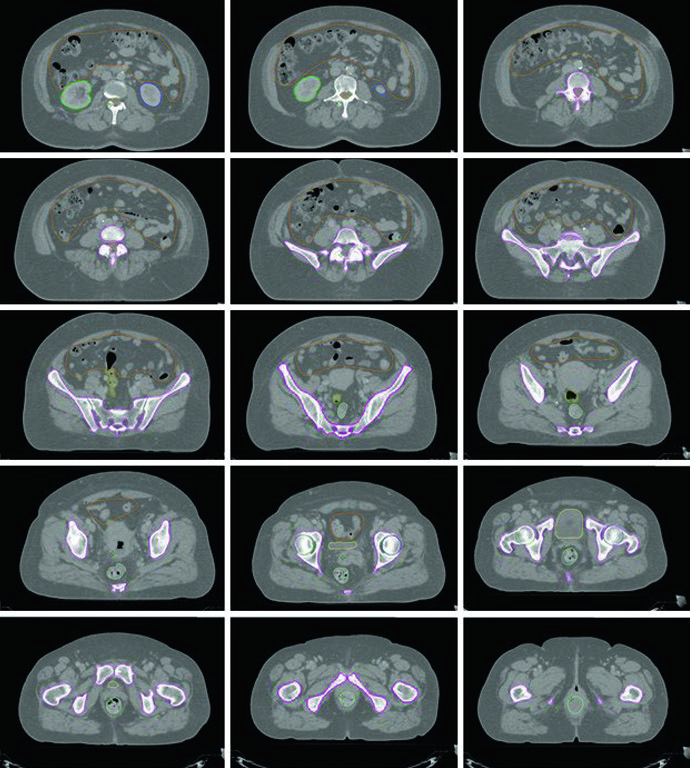
A fusão do PET/CT pré-tratamento com a TC de simulação é recomendada para auxiliar no delineamento do volume tumoral bruto (GTV). Diretrizes internacionais de consenso para contorno em casos de cérvice definitiva já foram publicadas, e casos-amostra interativos estão disponíveis em plataformas educacionais como o eContour.
Um estudo com RM usando partículas de óxido de ferro injetadas demonstrou que 95% dos linfonodos pélvicos (ilíaco comum, ilíaco interno, ilíaco externo medial e anterior, e obturatórios) estão localizados dentro de 7 mm da vasculatura pélvica. Já os linfonodos inguinais devem ser delineados usando abordagem de compartimento anatômico, dada a maior variabilidade de localização em relação aos vasos.
Problemas frequentes observados em ensaios multicêntricos incluem: margem inadequada ao redor da vasculatura (CTV próximo demais dos vasos), cobertura insuficiente ao redor da vasculatura ilíaca interna inferior e posterior na pelve, cobertura insuficiente ao redor da vasculatura obturadora inferior e anterolateral, cobertura insuficiente da região pré-sacral e extensão desnecessária do CTV nas concavidades sacrais.
Definição de volumes segundo o protocolo NRG-GY006
| Volume | Definição |
|---|---|
| GTV | Toda doença macroscópica visível, avaliada por informação clínica, exame físico, estudos radiográficos, exame endoscópico e biópsias |
| CTV1 | GTV + cérvice + útero |
| CTV2 | Paramétrios e terço superior da vagina (ou metade superior se vagina clinicamente envolvida) |
| CTV3 | Linfonodos ilíacos comuns, ilíacos externos, ilíacos internos e pré-sacrais. Borda superior na bifurcação aórtica (≈ L4–L5). Pré-sacrais até S2–S3. Ilíacos externos até o topo das cabeças femorais. Margem de 7 mm ao redor dos vasos, excluindo osso, músculo e intestino |
| CTV_boost | Linfonodos pélvicos macroscópicos; inclui paramétrio se boost parametrial indicado |
| ITV | CTV1 delineado em TC com bexiga cheia e vazia, combinados |
| PTV1 | CTV1 + 15 mm de expansão uniforme |
| PTV2 | CTV2 + 10 mm de expansão uniforme |
| PTV3 | CTV3 + 5 mm de expansão uniforme |
| PTV4 | ITV + 7 mm de expansão uniforme |
| PTV_boost | CTV_boost + 5 mm de expansão uniforme |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 21.1, protocolo NRG-GY006)
Órgãos de risco e restrições de dose
Os OARs padrão incluem intestino, reto, medula óssea, bexiga e cabeças femorais. Para pacientes tratadas com campo estendido, acrescentam-se rins bilaterais, medula espinhal, duodeno e fígado. Estudos de modelagem de probabilidade de complicação em tecido normal (NTCP) estabeleceram restrições validadas para intestino e medula óssea em pacientes com câncer cervical tratadas com quimiorradioterapia.
| OAR | Parâmetro dosimétrico | Protocolo | Variação aceitável |
|---|---|---|---|
| Espaço intestinal | V45 (cc) | ≤200 | ≤250 |
| Espaço intestinal | DMax (Gy) | ≤59,4 | ≤62,1 |
| Espaço intestinal | D30% (Gy) | ≤40 | ≤50 |
| Reto | D50% (Gy) | ≤45 | ≤54 |
| Reto | D60% (Gy) | ≤30 | ≤50 |
| Reto | DMax (Gy) | ≤50 | ≤55 |
| Medula óssea | Dmean (Gy) | ≤27 | ≤29 |
| Medula óssea | V10 (%) | ≤85,5 | ≤90 |
| Medula óssea | V20 (%) | ≤66 | ≤75 |
| Bexiga | D50% (Gy) | ≤45 | ≤55 |
| Bexiga | DMax (Gy) | ≤50 | ≤57,5 |
| Cabeças femorais | D15% (Gy) | ≤30 | ≤50 |
| Cabeças femorais | DMax (Gy) | ≤50 | ≤55 |
| Rins (campo estendido) | D50% (Gy) | ≤18 | ≤20 |
| Medula espinhal (campo estendido) | D0,03cc (Gy) | ≤45 | ≤47,5 |
| Duodeno (campo estendido) | D0,03cc (Gy) | ≤56 | ≤60 |
| Duodeno (campo estendido) | D50% (Gy) | ≤40 | ≤50 |
| Fígado (campo estendido) | D50% (Gy) | ≤25 | ≤30 |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 21.2, protocolo NRG-GY006)
A IMRT demonstrou reduzir toxicidade GI e hematológica, e pode melhorar toxicidade urinária relatada pela paciente. O PET/CT pode ser usado para segmentar sub-regiões ativas de medula óssea, onde acúmulo de dose correlaciona-se com maiores taxas de toxicidade hematológica. Poupar medula metabolicamente ativa com IMRT reduziu neutropenia e melhorou tolerância à quimioterapia em ensaios clínicos prospectivos.
Avaliação do plano e entrega guiada por imagem
O padrão de qualidade é que pelo menos 95% do PTV receba 100% da dose prescrita, e ≥99% do PTV receba ao menos 90% da prescrição. O máximo de dose deve ocorrer dentro do PTV, e áreas >100% fora do PTV devem ser minimizadas. Fluxos de planejamento baseados em conhecimento (knowledge-based planning) auxiliam na otimização dosimétrica em planos de IMRT mais complexos.
Pacientes tratadas com arranjos de feixes convencionais devem realizar imagem ao menos semanal com portais MV. Imagem óssea diária com kV ou CBCT permite redução das margens de planejamento para 5 mm ao redor do CTV nodal. Pacientes tratadas com IMRT devem realizar CBCT ao menos semanal — e idealmente a cada fração — para verificar variações na posição do alvo por mudanças no enchimento retal, vesical ou movimento uterino.
Câncer cervical: delineamento e prescrição de dose
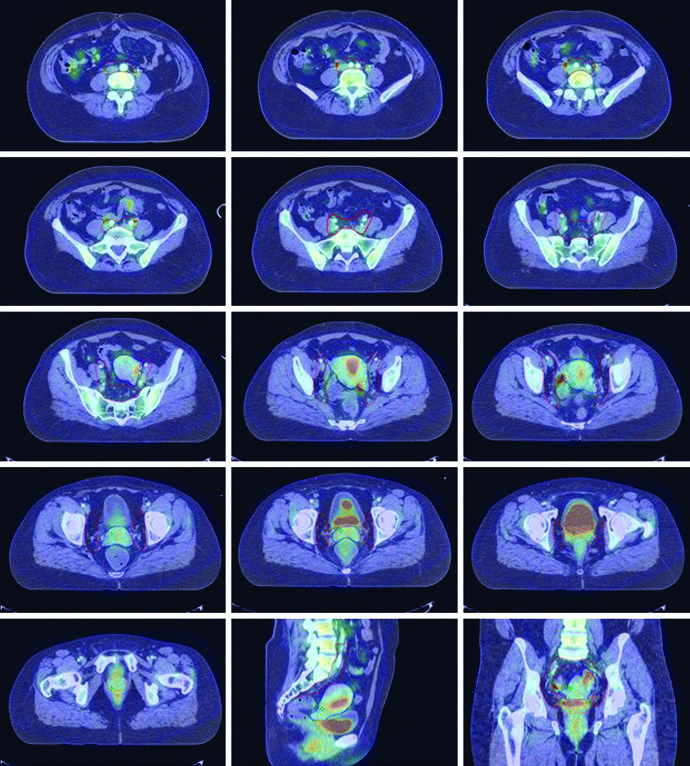
A disseminação linfática regional do câncer cervical segue padrão escalonado: linfonodos paracervicais drenam para obturatórios, ilíacos internos e ilíacos externos, seguidos por ilíacos comuns e para-aórticos. Pacientes com lesões envolvendo a vagina distal estão sob risco de metástases inguinais.
Se linfonodos para-aórticos estiverem envolvidos, deve-se empregar técnica de campo estendido, estendendo a borda cranial do CTV superiormente até o interespaço L1/L2 ou 3 cm cranial ao linfonodo mais superior envolvido. Os PTVs são criados para cada CTV e o PTV final é a combinação de todos. Expansões diferenciais CTV-PTV são utilizadas para cada componente baseadas no grau de movimento orgânico interno e incerteza de posicionamento.
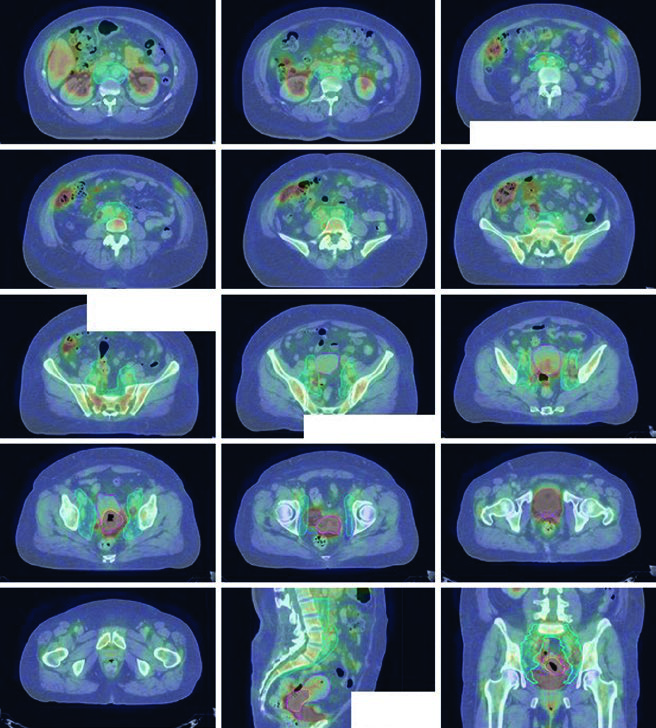
A prescrição de dose típica é 45 Gy em 25 frações para a pelve linfonodo-negativa, ou 47,6 Gy em 28 frações se houver doença nodal, com boost integrado simultâneo (SIB) para linfonodos envolvidos até 59,4 Gy. A dose do boost nodal e/ou dose por fração pode precisar de redução para respeitar a tolerância intestinal. Boost parametrial pode ser adicionado a critério médico para envolvimento parametrial, desde que aquele lado não receba SIB dentro do campo de boost. Campos AP/PA convencionais para boost parametrial incluem articulações sacroilíacas (borda superior), fundo do forame obturador (borda inferior) e músculo obturador interno (bordas laterais) com bloco de linha média de 4–5 cm. Prescrição típica do boost parametrial: 6–10 Gy em 3–5 frações. Boost de braquiterapia é padrão ao final ou após a EBRT. Para aprofundamento sobre braquiterapia, confira nosso artigo dedicado sobre braquiterapia guiada por imagem.
Câncer vaginal: abordagem e planejamento
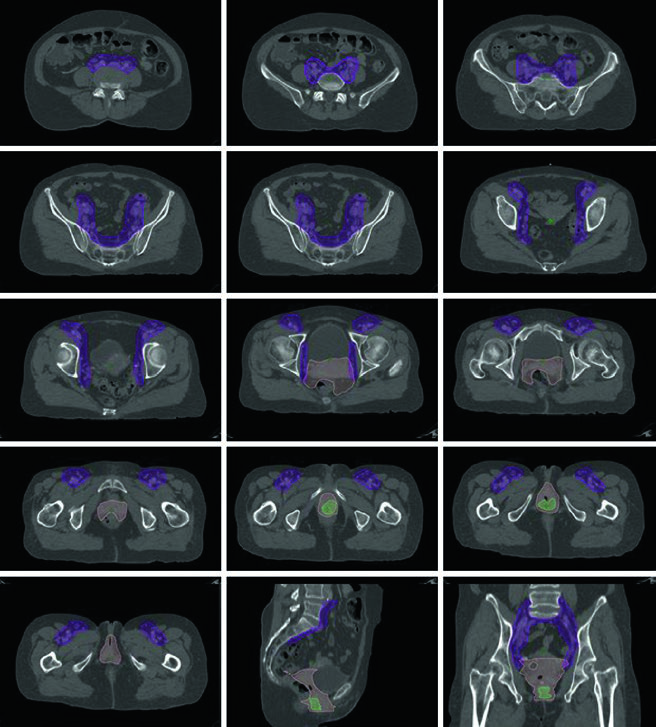
Tumores primários vaginais são relativamente raros — qualquer tumor que envolva cérvice ou vulva é classificado como câncer cervical ou vulvar, respectivamente. Faltam dados prospectivos específicos para orientar o manejo do câncer vaginal, e a abordagem recomendada é individualizada, frequentemente seguindo as diretrizes de câncer cervical.
Para doença estágio I, a RT definitiva com EBRT e braquiterapia é excelente opção, embora cirurgia definitiva seja alternativa para pacientes selecionadas com doença não-volumosa, distal e não-uretral. Para estágios II-IVA, quimiorradioterapia definitiva é padrão. A EBRT pélvica padrão deve cobrir toda a vagina. Pacientes com doença na metade distal da vagina devem receber RT inguinal bilateral.
Marcadores fiduciais temporários podem delinear ápice vaginal e introito na simulação por TC. A prescrição típica de EBRT é 45 Gy em 25 frações para pelve e toda a vagina, seguida de boost de braquiterapia (por exemplo, 6 Gy × 4 frações). Para mais detalhes sobre o tratamento do câncer de vulva com IMRT, confira nosso artigo dedicado.
Câncer endometrial: anatomia, disseminação e volumes
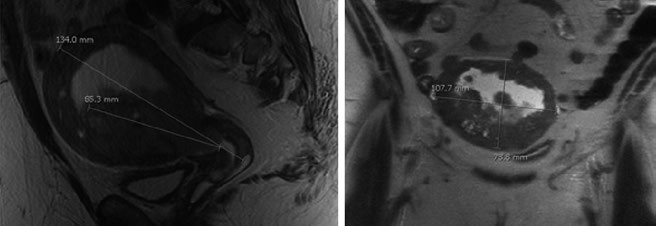
O útero é delimitado anteriormente pela bexiga e posteriormente pelo reto, coberto por reflexões peritoneais, e divide-se em fundo, istmo e cérvice. A parede uterina consiste em camada muscular lisa externa (miométrio) e camada interna de epitélio glandular (endométrio). O útero é sustentado por cinco ligamentos: largo, redondo, cardinal, uterossacral e vesicouterino.
As áreas nodais em risco incluem linfonodos obturatórios, ilíacos externos, ilíacos internos, ilíacos comuns e para-aórticos. Lesões envolvendo o fundo uterino podem se disseminar diretamente para linfonodos para-aórticos. A incidência de envolvimento nodal pélvico e para-aórtico varia conforme categorias de risco (baixo, médio e alto), tamanho tumoral e profundidade de invasão, conforme definido pelo estudo GOG-33.
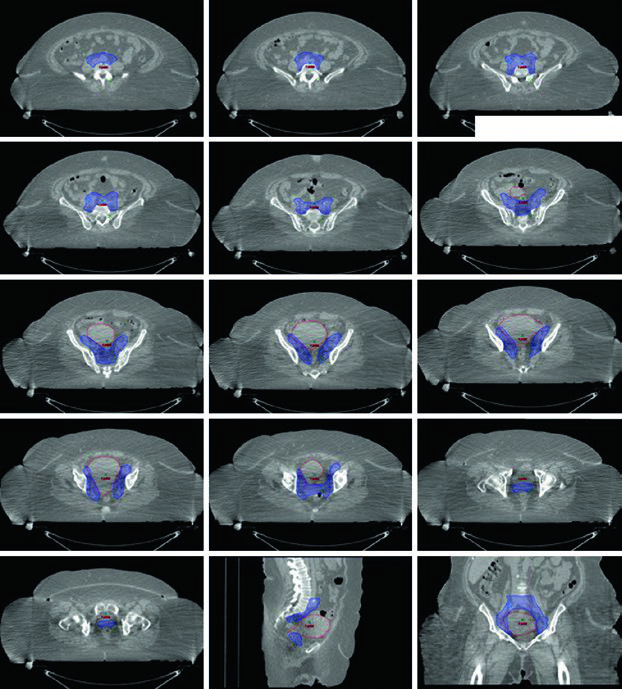
A histerectomia é tratamento-padrão para candidatas cirúrgicas, com consideração de RT adjuvante baseada em fatores de risco patológicos. Para pacientes clinicamente inoperáveis, o tratamento-padrão é RT definitiva com braquiterapia, com ou sem EBRT. EBRT isolada pode ser considerada para pacientes inelegíveis ou que recusem braquiterapia. Pacientes com doença recorrente também são candidatas a EBRT.
Para EBRT + braquiterapia, a dose padrão de EBRT é 45 Gy em 25 frações. Para pacientes tratadas com EBRT isolada, RT pélvica pode ser seguida de boost cone-down no útero e cérvice. SBRT pode ser considerada se a paciente não puder receber braquiterapia.
O delineamento é similar à RT pélvica para câncer cervical. O GTV inclui toda doença macroscópica. O CTV se divide em CTV1 (GTV + útero inteiro), CTV2 (tecidos paravaginais/parametriais + 3 cm da vagina proximal) e CTV3 (igual ao cenário pós-operatório). Se a vagina distal (terço inferior) estiver envolvida, linfonodos inguinais devem ser contornados continuamente dos ilíacos externos até 2 cm caudal à junção safeno-femoral. Com envolvimento para-aórtico, campo estendido similar ao da Tabela 21.1. Expansões diferenciais: PTV1 = 15 mm, PTV2 = 7–10 mm, PTV3 = 5–7 mm. Boost adicional de 5–15 Gy pode ser adicionado para doença nodal macroscópica ou envolvimento parametrial, com SIB ou abordagem sequencial.
Para conhecer tecnologias mais recentes aplicadas neste contexto, confira nosso artigo sobre tecnologias avançadas na radioterapia ginecológica. O cenário pós-operatório é abordado em detalhes no nosso artigo dedicado sobre RT ginecológica pós-operatória.