Princípios das Técnicas Avançadas em Ginecologia
Os resultados do tratamento de tumores ginecológicos locorregionalmente avançados continuam aquém do ideal. Toxicidades hematológicas e gastrointestinais comprometem a entrega completa do esquema terapêutico em uma parcela significativa das pacientes. Duas frentes de desenvolvimento se impõem: intensificar o tratamento quando possível e reduzir a toxicidade de forma consistente.
A radioterapia de intensidade modulada (IMRT) consolidou-se como modalidade padrão tanto no tratamento definitivo quanto no pós-operatório de câncer cervical e endometrial. Ainda existe alguma controvérsia sobre a implementação rotineira, dado o volume limitado de dados prospectivos e randomizados, mas a prática clínica já incorporou a técnica de forma ampla. A IMRT com guia de imagem diário (IG-IMRT) melhora a localização dos alvos e dos órgãos em risco (OARs), viabilizando planos mais conformais sem comprometer as doses tumoricidas.
Esse progresso técnico não se limita à conformação do feixe. O replanejamento adaptativo corrige mudanças na anatomia tumoral e da paciente ao longo do curso de tratamento. A IMRT com preservação de medula óssea (BM-IMRT) reduz a toxicidade hematológica — um problema clínico real quando se administra quimioterapia concomitante à base de cisplatina. A SBRT oferece uma alternativa de boost para pacientes inelegíveis ou que recusam braquiterapia, além de possibilitar reirradiação de áreas previamente tratadas. A terapia com prótons pode diminuir toxicidade graças à queda de dose distal rápida, embora dados comparativos de alta qualidade permaneçam escassos.
Para uma visão abrangente do delineamento de volume alvo em diversas localizações anatômicas, consulte nosso guia completo sobre delineamento de volume alvo e campos na radioterapia.
Guia de Imagem na Radioterapia Ginecológica
A IMRT permite planejamentos sofisticados e conformais que reduzem o volume irradiado. Contudo, essa vantagem exige delineação precisa das estruturas-alvo e dos OARs, além de gerenciamento adequado da movimentação orgânica e da incerteza de posicionamento. Os órgãos pélvicos se movem tanto entre frações quanto durante a entrega de cada fração individual.
A IG-IMRT associou-se a melhora tanto na toxicidade hematológica quanto gastrointestinal em comparação à IMRT isolada. Três abordagens de guia de imagem merecem destaque na prática clínica:
- kV ortogonal diário: imagens kV no momento do tratamento alinham a anatomia óssea à posição inicial da simulação CT. Método acessível, mas não captura variações de tecido mole.
- Cone-beam CT (CBCT) diário: permite identificar o estado de enchimento retal e vesical em comparação à simulação. Com expansão de PTV baseada em modelo de forma e guia diário por CBCT, a cobertura do alvo dentro da isodose de 95% demonstra-se excelente.
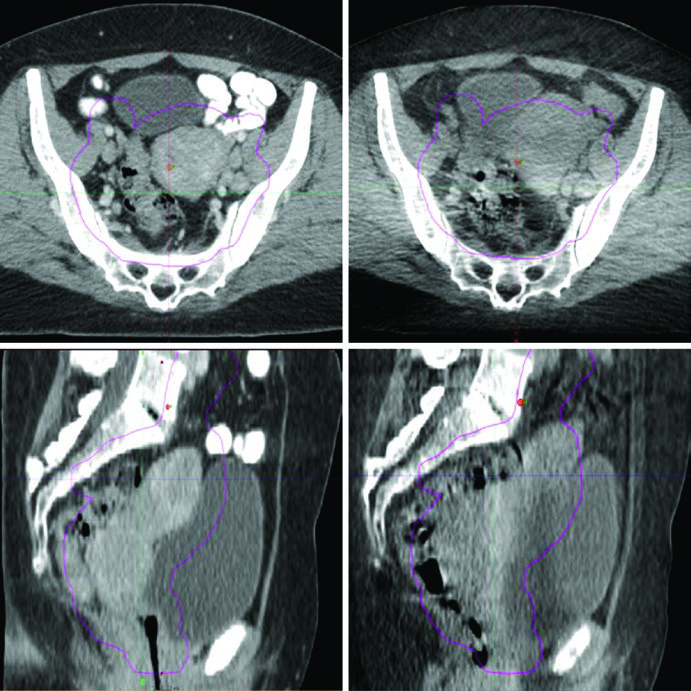
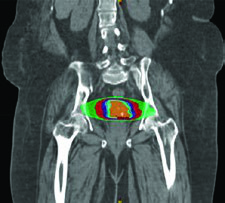
- Monitoramento da variação: a Figura 24.1 ilustra um caso real em que mudanças no enchimento vesical e retal deslocaram o fundo uterino para fora do PTV — exatamente o tipo de evento que o CBCT pré-tratamento detecta e permite corrigir.
Na prática diária, o CBCT oferece o melhor equilíbrio entre informação anatômica e viabilidade logística. A dose adicional de imagem é clinicamente aceitável quando comparada ao risco de subdosagem tumoral por deslocamento não detectado.
IMRT com Preservação de Medula Óssea
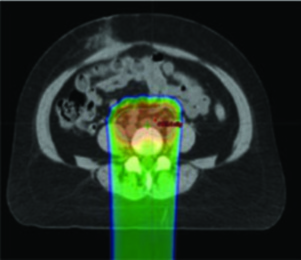
A IMRT pode ser empregada especificamente para preservar medula óssea em pacientes submetidas a RT pélvica, e essa estratégia demonstrou reduzir toxicidade hematológica de forma significativa. Quem trabalha com quimiorradiação concomitante sabe que citopenias prolongadas atrasam ciclos, comprometem dose-intensidade e ocasionalmente levam à hospitalização. Preservar medula ativa é uma resposta concreta a esse problema.
Diversas abordagens foram implementadas e validadas clinicamente:
IG-IMRT baseada em PET/CT envolve contornar os ossos pélvicos e definir medula ativa como regiões com SUV acima do SUV médio intraósseo, aplicando então restrições de dose à medula. As restrições publicadas, baseadas em modelagem NTCP, seguem a seguinte hierarquia:
| Estrutura | Tipo de Restrição | Dose Média | V10 (%) | V20 (%) |
|---|---|---|---|---|
| Medula óssea pélvica | Soft constraint | ≤27 Gy | ≤85,5% | ≤66% |
| Medula óssea pélvica | Hard constraint | ≤29 Gy | ≤90% | ≤75% |
| Medula óssea ativa | Soft constraint | ≤28,5 Gy | ≤90% | ≤70% |
| Medula óssea ativa | Hard constraint | ≤30 Gy | ≤90% | ≤75% |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition — restrições baseadas em modelagem NTCP (Rose et al.)
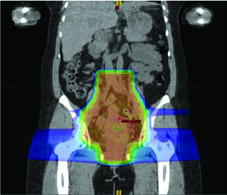
Quando PET/CT não está disponível, duas alternativas funcionam bem. Uma abordagem baseada em atlas é viável e reprodutível entre centros. A outra opção delimita medula óssea como as regiões de baixa densidade dentro dos ossos no CT de simulação, aplicando as mesmas restrições de dose. Ambas reduzem toxicidade hematológica de forma mensurável, mesmo sem a informação funcional do PET.
Essa estratégia é particularmente relevante para quem trata câncer cervical com quimiorradiação concomitante. A redução de citopenias permite manter a intensidade de dose da cisplatina semanal, o que tem impacto direto no controle tumoral. Detalhes sobre o delineamento dos volumes pélvicos podem ser encontrados nos artigos sobre radioterapia definitiva em ginecologia e tratamento pós-operatório ginecológico.
Replanejamento Adaptativo na Pelve
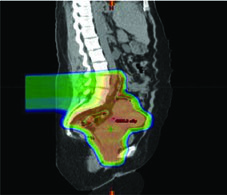
O replanejamento adaptativo divide-se em três categorias principais: offline (entre frações), online (imediatamente antes de uma fração) e em tempo real (durante a entrega). Cada uma responde a cenários clínicos diferentes, e a escolha depende da infraestrutura disponível e do grau de variação anatômica esperado.
Plano-do-dia (plan-of-the-day): gera uma biblioteca de planos paciente-específicos correspondendo a diferentes volumes-alvo e configurações de movimentação orgânica. Antes de cada fração, o CBCT seleciona o plano mais similar à configuração do dia. Essa estratégia é elegante porque não exige replanejamento em tempo real, mas demanda investimento inicial na criação da biblioteca.
Replanejamento programado: pode ser feito com RM semanal. Registro deformável de imagem modela a dose acumulada nos alvos e OARs. Na prática, funciona bem para pacientes que perdem peso progressivamente ou cujos tumores regridem significativamente durante o tratamento.
A radioterapia adaptativa offline deve ser considerada para pacientes com perda de peso significativa ou mudança substancial no tamanho tumoral. Uma nova simulação pode ser necessária se o replanejamento não puder ser realizado com as imagens adquiridas na sala de tratamento. Sistemas avançados de planejamento permitem monitoramento automatizado de dose e métricas dose-volume que podem ser revisadas offline para orientar a decisão de replanificar.
Na radioterapia adaptativa online, a variação no enchimento do reto e da bexiga desloca tanto os alvos quanto os OARs de maneiras que a simulação CT inicial não captura. Tecnologias emergentes integram CBCT iterativo para cálculo de dose e replanejamento diário, ou utilizam RM para replanejamento online. A plataforma MR-Linac representa o exemplo mais avançado dessa categoria, combinando imagem em tempo real com adaptação do plano na mesma sessão.
Terapia com Prótons em Tumores Ginecológicos
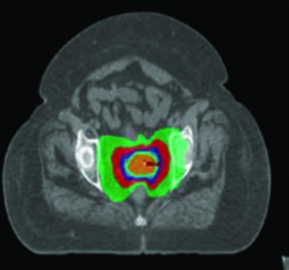
A terapia com prótons aproveita um build-up de dose relativamente gradual e uma queda de dose abrupta distal ao alvo em comparação com fótons. Essa propriedade física fundamental permite reduzir a dose nos OARs — especialmente distais aos campos de tratamento — e diminuir a dose integral, preservando cobertura adequada dos alvos.
Cenários em que prótons podem oferecer vantagem sobre IMRT incluem tratamento de linfonodos para-aórticos e reirradiação. Estudos dosimétricos e clínicos iniciais mostram melhora na dose em estruturas normais adjacentes, incluindo intestino, bexiga e medula óssea. Prótons também permitem melhor preservação ovariana em mulheres pré-menopáusicas — por exemplo, poupando um ovário com dose média inferior a 15 Gy.
Para o tratamento definitivo, a dosimetria-alvo deve ser idêntica à utilizada com fótons, corrigida pela efetividade biológica relativa (RBE) assumida de 1,1 para prótons. O delineamento de GTV e CTV segue os mesmos princípios do capítulo de EBRT definitiva. Os PTVs são específicos por feixe, baseados na incerteza de alcance. Um cuidado fundamental: evitar arranjos de feixe que coloquem estruturas críticas no campo distal ao alvo.
A terapia com prótons pode ser considerada como alternativa de boost para pacientes que não podem receber braquiterapia. Prótons apresentam vantagens dosimétricas em bexiga, intestino, cabeças femorais e reto em comparação ao VMAT. O CTV de boost pode ser determinado por RM obtida após 3 semanas de quimiorradiação, administrando-se então 30 Gy/Gy equivalente em 5 frações em substituição à braquiterapia. Entretanto, evidência prospectiva de alta qualidade ainda é insuficiente, e a relação entre dosimetria melhorada e redução clinicamente significativa de toxicidade permanece sem comprovação definitiva.
SBRT para Câncer Cervical
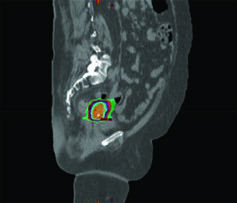
No câncer cervical locorregionalmente avançado, o padrão de tratamento combina EBRT fracionada diária com cisplatina concomitante seguida de boost com braquiterapia, alcançando dose EQD2 final de 80 a 95 Gy no alvo. A SBRT surge como modalidade especializada que entrega doses altas em 1 a 5 frações, exigindo visualização precisa do alvo, delineação acurada de tumor e OARs, e posicionamento de alta fidelidade com guia de imagem.
Os linfonodos podem receber boost com SBRT. A técnica também se aplica ao cenário de reirradiação para doença recorrente ou tratamento de sítios limitados de metástase. Algumas pacientes não são candidatas à braquiterapia por comorbidades graves, e outras recusam o procedimento — incluindo pacientes em risco de transtorno de estresse pós-traumático.
A SBRT permite entrega conformal de boost em alta dose, mas resultados recentes exigem cautela. Um ensaio fase II investigando SBRT (28 Gy em 4 frações) como substituto da braquiterapia foi encerrado prematuramente por toxicidade maior que a esperada e taxas de controle local, sobrevida livre de progressão e sobrevida global inferiores ao previsto em 2 anos. Braquiterapia permanece o padrão de tratamento para pacientes elegíveis.
Para pacientes que definitivamente não receberão braquiterapia, um esquema de 5 frações (por exemplo, 27,5 Gy em 5 frações) após 45 Gy na pelve pode ser considerado, resultando em EQD2 de 80 Gy (α/β = 10). A determinação de dose e fracionamento deve considerar o tamanho do alvo, RT prévia na área e tolerância dos OARs adjacentes. Para regime de 5 frações, a dose por fração situa-se tipicamente na faixa de 4 a 8 Gy, embora frações de 8 a 15 Gy também tenham sido reportadas. A EQD2 total deve ser calculada para a área tratada. Para entender melhor a SBRT em outros cenários, confira nosso artigo dedicado sobre SBRT em cabeça e pescoço.
SBRT no Câncer de Endométrio
A SBRT tem sido considerada como modalidade alternativa para entrega de boost no cenário pós-operatório do câncer endometrial. Linfonodos também podem receber boost com SBRT. Reirradiação ou SBRT dirigida a metástases representam indicações adicionais.
Uma série retrospectiva avaliou pacientes com focos recorrentes, persistentes ou oligometastáticos tratados com dose mediana de 24 Gy (variação de 10 a 50 Gy) em mediana de 4 frações (variação de 1 a 6). Os resultados mostraram taxas de controle local de 80% em 1 ano e 68% em 3 anos, com controle mais favorável em tumores menores. O perfil de segurança foi aceitável: taxa de toxicidade grau ≥2 de 4,3%, com apenas um evento grau 3 e nenhuma toxicidade grau 4 ou 5.
Esses dados justificam a SBRT como opção razoável em pacientes selecionados, mas séries retrospectivas têm limitações inerentes. A decisão clínica deve ponderar tamanho tumoral, localização em relação a estruturas previamente irradiadas e dose cumulativa. Para mais informações sobre o tratamento da braquiterapia ginecológica, consulte nosso artigo sobre braquiterapia guiada por imagem.
Considerações Práticas e Integração Clínica
A escolha entre estas tecnologias avançadas não segue uma receita única. O cenário clínico determina a melhor abordagem: IG-IMRT com preservação de medula óssea é praticamente obrigatória quando se administra quimiorradiação concomitante; replanejamento adaptativo se justifica em tratamentos longos com anatomia variável; prótons podem ser considerados quando estruturas críticas estão em posição desfavorável ou em cenários de reirradiação; SBRT preenche a lacuna quando braquiterapia não é viável.
O que une todas essas estratégias é a necessidade de infraestrutura de imagem robusta e equipe treinada em delineamento preciso. Sem CBCT ou RM de qualidade, as vantagens da IMRT conformal se perdem. Sem restrições de dose bem definidas para medula óssea, a toxicidade hematológica persiste. Sem guia de imagem rigoroso, a SBRT se torna perigosa.
A radioterapia ginecológica avançada exige integração entre física médica, dosimetria e oncologia clínica em cada decisão de tratamento. Os dados atuais sustentam benefícios dosimétricos claros para estas técnicas, mas a tradução em resultados clínicos superiores depende da execução cuidadosa em cada etapa do processo. Para compreender o contexto completo do delineamento ginecológico, explore o guia completo sobre delineamento de volume alvo e campos na radioterapia, além dos artigos sobre câncer de vulva e IMRT.