Orofaringe en Radioterapia: Lo Que Cambia con el VPH
El carcinoma de orofaringe comprende tumores primarios de las amígdalas, base de lengua, paladar blando y pared posterior de la faringe. La abrumadora mayoría son carcinomas escamosos, y el gran cambio de los últimos años ha sido el reconocimiento del rol del virus del papiloma humano (VPH). Los tumores VPH-positivos presentan pronóstico superior — dato tan relevante que el AJCC adoptó sistemas de estadificación separados para tumores VPH-positivos y VPH-negativos.
A pesar del mejor pronóstico, la de-escalación terapéutica basada únicamente en el estado del VPH no debe realizarse fuera de ensayos clínicos. Estudios como el NRG Oncology RTOG 1016 y el De-ESCALaTE HPV demostraron que reemplazar cisplatino por cetuximab en tumores VPH-positivos resultó en desenlaces inferiores. La prueba viral debe realizarse en todos los pacientes con carcinoma de orofaringe, sin excepción. Para una visión completa de la delineación en todos los sitios anatómicos, consulte nuestra guía completa sobre delineación de volumen blanco y configuración de campos.
Anatomía y Patrones de Diseminación
La orofaringe es un espacio cuboidal delimitado anteriormente por la cavidad oral, superiormente por la nasofaringe, e inferiormente por la laringe e hipofaringe. Cuatro subsitios la componen: amígdalas, base de lengua, paladar blando y pared faríngea. En la práctica, la mayoría de los casos surgen en las amígdalas y la base de lengua.
Un punto clínicamente crucial: la orofaringe posee drenaje linfático rico. Los ganglios cervicales están comúnmente involucrados incluso en estadios tempranos. La planificación radioterápica necesita reflejar esta realidad anatómica, garantizando cobertura ganglionar adecuada desde el inicio.
Estudio Diagnóstico para Delineación del Volumen Blanco
La delineación del GTV del sitio primario depende de una combinación juiciosa de imágenes y examen físico. Ningún estudio resuelve todo por sí solo — cada modalidad tiene su rol específico.
La extensión mucosa y superficial de la enfermedad se evalúa mejor mediante inspección visual, palpación y nasofibrolaringoscopia. La documentación fotográfica al momento de la consulta o simulación ayuda a registrar extensión mucosa que puede no verse bien en las imágenes — un detalle que marca la diferencia real en el contorneo.
La TC con contraste sigue siendo la base de la imagen diagnóstica, pero la RM y el PET/TC tienen roles bien definidos:
| Modalidad | Indicación Principal | Limitación |
|---|---|---|
| TC con contraste | Imagen diagnóstica estándar; base para simulación | Resolución de tejidos blandos inferior a la RM |
| RM T1 pre-contraste | Evaluación de planos grasos y señales de médula ósea | Artefactos de movimiento |
| RM T1 con contraste | Extensión anterior de tumores de base de lengua; invasión perineural | Puede sobreestimar el volumen tumoral |
| RM T2 fat-sat | Ganglios retrofaríngeos; extensión en espacio parafaríngeo y pre-epiglótico | Artefactos de susceptibilidad |
| FDG-PET/TC | Información metabólica complementaria; detecta extensión tumoral no vista en TC/RM | Resolución espacial baja; baja sensibilidad para metástasis ganglionares pequeñas |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Capítulo 2)
Un punto que merece destacarse: la ausencia de captación de FDG en un ganglio morfológicamente sospechoso no debe considerarse tranquilizadora. El PET tiene sensibilidad limitada para metástasis ganglionares de pequeño volumen.
Simulación y Localización Diaria
El paciente se posiciona en decúbito supino con soporte de cabeza y cuello extendido. La inmovilización se realiza con máscara termoplástica de 5 puntos (Aquaplast) que debe cubrir cabeza, cuello y hombros adecuadamente. Puede insertarse un bloqueador de mordida y/o protector bucal. Instrucción fundamental: el paciente no debe deglutir durante las adquisiciones ni durante el tratamiento.
La simulación por TC con contraste IV utiliza espesor de corte ≤3 mm, cubriendo desde el vértice del cráneo hasta la carina. El isocentro se posiciona típicamente en los cartílagos aritenoides. Un campo cervical anterior bajo convencional AP puede emparejarse a los campos de IMRT.
Las imágenes de RM y PET pueden registrarse o fusionarse a la TC de simulación. El uso de la máscara de inmovilización durante el PET mejora la precisión de la fusión, pero durante la RM puede impedir el uso de bobina dedicada de cabeza y cuello — un trade-off práctico que el equipo debe considerar caso por caso.
En el Memorial Sloan Kettering Cancer Center (MSKCC), la guía por imagen diaria utiliza kV 2D montada en el acelerador lineal y cone-beam CT diario. Alternativas incluyen kV semanal con kV diario, sistema ExacTrac (kV ortogonal) o MV CT en TomoTherapy.
Esquemas de Dosis y Fraccionamiento con IMRT
Existen múltiples abordajes de tratamiento. En el MSKCC, la técnica preferida es secuencial, con dosis total a la enfermedad macroscópica de 70 Gy. Las diferencias surgen según el estado del VPH:
Tumores VPH-positivos (Técnica Secuencial — MSKCC)
La región subclínica recibe 30 Gy en fracciones de 2 Gy, seguida por cone down a la enfermedad macroscópica recibiendo 40 Gy en fracciones de 2 Gy. La región subclínica se evalúa rigurosamente con RM, TC con contraste y PET/TC para asegurar la ausencia de enfermedad macroscópica oculta. Si un campo cervical bajo AP se empareja a los campos IMRT, el cuello bajo recibe 30 Gy en fracciones de 2 Gy.
Tumores VPH-negativos (Técnica Secuencial — MSKCC)
La fase inicial entrega 60 Gy en fracciones de 2 Gy a la enfermedad macroscópica, con tratamiento simultáneo de 54 Gy en fracciones de 1,8 Gy a todas las regiones subclínicas. Sigue cone down de 10 Gy en fracciones de 2 Gy a la enfermedad macroscópica. El cuello bajo recibe 50 Gy en fracciones de 2 Gy. Dosis electivas reducidas solo deben considerarse con quimioterapia concomitante basada en cisplatino.
Boost Integrado Simultáneo (SIB)
Otra técnica ampliamente utilizada: enfermedad macroscópica 70 Gy (2 Gy/fracción), dosis subclínica de alto riesgo 56 Gy (1,6 Gy/fracción), dosis subclínica de bajo riesgo 50–52,5 Gy (1,43–1,5 Gy/fracción). Esta técnica solo debe considerarse con quimioterapia concomitante. Otros esquemas incluyen RTOG 0022 y RTOG 1016.
| Esquema | Enfermedad Macroscópica | Subclínica Alto Riesgo | Subclínica Bajo Riesgo | Observación |
|---|---|---|---|---|
| Secuencial VPH+ | 70 Gy (30+40 Gy, 2 Gy/fx) | 30 Gy (2 Gy/fx) | 30 Gy cuello bajo | Cone down tras 30 Gy |
| Secuencial VPH− | 70 Gy (60+10 Gy, 2 Gy/fx) | 54 Gy (1,8 Gy/fx) | 50 Gy cuello bajo | SIB parcial en fase 1 |
| SIB | 70 Gy (2 Gy/fx) | 56 Gy (1,6 Gy/fx) | 50–52,5 Gy (1,43–1,5 Gy/fx) | Requiere QT concomitante |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Capítulo 2, Sección 2.5.1)
Volúmenes Blanco para Enfermedad Macroscópica
El GTV70 incluye toda la enfermedad macroscópica definida por examen clínico e imagen en el sitio primario, además de todos los ganglios sospechosos (>1 cm, necróticos, con realce o FDG-ávidos). Ganglios limítrofes sospechosos pueden recibir dosis inferior a 70 Gy — por ejemplo, 60–66 Gy.
| Volumen Blanco | Definición y Descripción |
|---|---|
| GTV70 | Primario: toda enfermedad macroscópica por examen clínico e imagen. Ganglios: todos los sospechosos (>1 cm, necróticos, realce, FDG-ávidos). Ganglios limítrofes: 60–66 Gy |
| CTV70 | En áreas de excelente visualización: GTV70 = CTV70 (sin margen). Con incertidumbre: CTV70 = GTV70 + 3–5 mm |
| PTV70 | CTV70 + 3–5 mm según precisión del setup diario y disponibilidad de guía por imagen |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 2.1)
Volúmenes Blanco Subclínicos
Como directriz general, el CTV del sitio primario debe englobar el GTV70 + 1 cm, restando barreras anatómicas a la diseminación (aire, hueso, piel). A partir de ahí, cada subsitio requiere atención específica:
Amígdala
Asegure margen adecuado (~1 cm) al tumor primario. En enfermedad avanzada, incluya las placas pterigoides. Considere incluir el trígono retromolar ipsilateral si se sospecha diseminación anterolateral a lo largo del músculo constrictor faríngeo.
Base de Lengua
El CTV subclínico debe cubrir el surco glosoamigdalino, la valécula y el espacio pre-epiglótico. Asegure margen mucoso de al menos 1 cm alrededor del tumor primario de base de lengua — anteriormente, esto puede extenderse a la lengua oral. La RM es muy útil para delineación precisa de la extensión anterior del tumor.
Paladar Blando
Cubra todo el paladar blando, aspecto superior de los pilares amigdalinos y fosa, nasofaringe adyacente superiormente hasta la placa pterigoidea. En primarios avanzados, considere la fosa pterigopalatina. Si la fosa pterigopalatina está comprometida, evaluación de la base del cráneo con RM es obligatoria. Asegure cobertura anterior adecuada, que puede requerir parte del paladar duro.
Pared Faríngea
Márgenes superior e inferior generosos, dada la posibilidad de lesiones skip. En tumores avanzados, considere extender el CTV cranealmente para incluir la nasofaringe y caudalmente para incluir la hipofaringe.
Ganglios Electivos
En casos N0, las áreas en riesgo incluyen niveles II–IV bilaterales y ganglios retrofaríngeos laterales. En el MSKCC, los niveles IB y V no se tratan rutinariamente, a menos que estén macroscópicamente comprometidos. La excepción: extensión macroscópica a cavidad oral, cuando los ganglios IB pasan a considerarse en riesgo.
En casos N+, los ganglios retrofaríngeos y retroestiloideos deben cubrirse superiormente hasta la base del cráneo. Con compromiso macroscópico de ganglios bajos, considere cobertura del espacio supraclavicular.
Para tumores de amígdala T1–2, N0–N1, bien lateralizados (≥1 cm de la línea media), sin extensión a base de lengua o paladar blando: el tratamiento ipsilateral del cuello es aceptable. La extensión superior de la cobertura para el cuello N0 puede iniciar en el proceso transverso de C1 o donde el vientre posterior del digástrico cruza la vena yugular interna.
| Subsitio Primario | CTV Subclínico — Puntos Clave |
|---|---|
| Amígdala | GTV + ~1 cm; placas pterigoides en enfermedad avanzada; trígono retromolar si extensión anterolateral sospechada |
| Base de lengua | Surco glosoamigdalino, valécula, espacio pre-epiglótico; margen mucoso ≥1 cm; RM para extensión anterior |
| Paladar blando | Paladar blando entero, pilares amigdalinos superiores, nasofaringe adyacente; fosa pterigopalatina si avanzado |
| Pared faríngea | Márgenes generosos sup/inf (lesiones skip); nasofaringe craneal e hipofaringe caudal si avanzado |
| Ganglios electivos (N0) | Niveles II–IV bilaterales + retrofaríngeos laterales; IB solo con extensión oral |
| Ganglios electivos (N+) | Retrofaríngeos/retroestiloideos hasta base del cráneo; supraclavicular si ganglios bajos comprometidos |
| Amígdala lateralizada T1-2 N0-N1 | Cuello ipsilateral aceptable; cobertura superior desde C1 |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 2.2)
Consideraciones Prácticas y Casos Ilustrativos
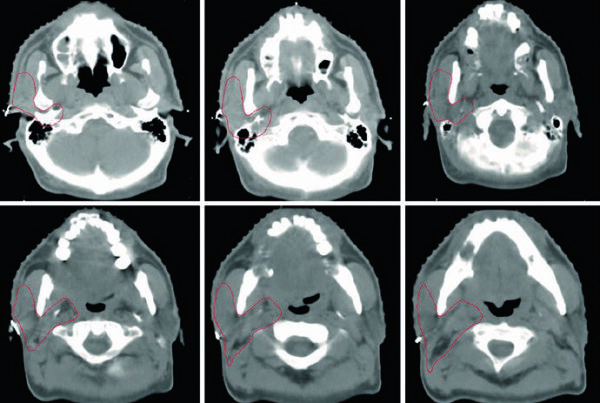
El capítulo presenta seis casos representativos que ilustran la aplicación práctica de estos principios:
Un paciente con carcinoma escamoso VPH-negativo cT4N2 de amígdala izquierda demuestra la necesidad de cobertura hasta las placas pterigoides e inclusión ipsilateral del nivel IB debido a invasión de lengua oral. Un caso de carcinoma VPH-positivo cT4N1 de base de lengua ilustra la cobertura hasta la base del cráneo en el lado N+ y la consideración de IB bilateral cuando el tumor cruza la línea media en la lengua oral.
La cobertura del espacio pre-epiglótico se demuestra en tumores de base de lengua — estructura anatómica que frecuentemente alberga extensión subclínica y que puede pasar desapercibida sin RM dedicada.
Un caso de amígdala cT1N1 VPH-positiva con ganglios bajos muestra la inclusión del espacio supraclavicular. Y el caso de amígdala cT2N0 VPH-positiva bien lateralizada demuestra que la radiación ipsilateral es viable, con cobertura ganglionar iniciando en el proceso transverso de C1, sin necesidad de tratar nivel IB. En el MSKCC, para tumores de amígdala independiente del estadio, la región subclínica ipsilateral casi siempre se extiende superiormente para incluir la placa pterigoidea ipsilateral.
Estos ejemplos refuerzan que no existe una receta única — cada decisión de contorneo equilibra la extensión anatómica del tumor, el estado ganglionar y el VPH para definir la cobertura óptima. El dominio de los patrones de drenaje linfático cervical y los espacios parafaríngeos es esencial para planificar con seguridad y precisión.