SBRT para Cáncer de Cabeza y Cuello: Indicaciones y Selección de Pacientes
La radioterapia estereotáctica corporal (SBRT) para cáncer de cabeza y cuello ofrece control local duradero en pacientes que no toleran tratamientos radicales prolongados. En centros de alto volumen, la SBRT administra dosis ablativas de 40–50 Gy en solo 5 fracciones, dos veces por semana, reduciendo drásticamente el tiempo de tratamiento sin sacrificar la eficacia oncológica. La técnica elimina los volúmenes microscópicos tradicionales y trabaja con márgenes de PTV de solo 3 mm.
El cáncer avanzado de cabeza y cuello (CCC) afecta predominantemente a pacientes de edad avanzada y, pese a tratamientos multimodales agresivos, los resultados siguen siendo desfavorables. Pacientes ancianos con buen estado general pueden optar por radioterapia radical de alta dosis para maximizar el control tumoral, aunque aceptando mayores tasas de toxicidad y morbilidad. En pacientes frágiles, la decisión contra un curso prolongado de radioterapia requiere ponderar múltiples factores de forma individual.
Estos factores incluyen la preferencia del paciente, aspectos tumorales como la morbilidad esperada de la progresión frente al riesgo del tratamiento y la probabilidad de un resultado exitoso, la expectativa de vida influida por edad y comorbilidades, la tolerancia al tratamiento agresivo según el estado funcional, y factores no relacionados con el paciente — distancia al hospital, disponibilidad de apoyo social, financiero y psicológico. El análisis conjunto de estas variables determina si la SBRT es el abordaje más apropiado.
Históricamente, la SBRT para cabeza y cuello fue considerada principalmente para escenarios de reirradiación. Sin embargo, la evidencia creciente sugiere que su mayor valor puede residir en pacientes no irradiados previamente. Cuando el tiempo extendido de tratamiento y recuperación de una terapia radical convencional — que puede extenderse 6–7 semanas con quimioterapia concurrente — resulta indeseable o irrealista para determinados pacientes, la SBRT logra un control local duradero con un curso acortado y perfil de efectos secundarios aceptable. Para una visión integral de todas las regiones anatómicas cubiertas en esta serie, consulte nuestra guía completa sobre delineación de volumen blanco.
Simulación e Imagen: TC con Doble Contraste y Fusión con RM
La delineación precisa del GTV es la piedra angular de la seguridad en la SBRT de cabeza y cuello. A diferencia de la radioterapia convencional — donde pequeñas imprecisiones en la delineación se compensan parcialmente con márgenes generosos — en la SBRT cada milímetro importa. Las fotografías intraorales que documenten hallazgos del examen clínico pueden complementar la información de imagen, y la revisión neurorradiológica ayuda a esclarecer la extensión tumoral y localizar órganos en riesgo radiosensibles.
La TC de simulación con contraste intravenoso es obligatoria para la definición precisa de volúmenes. La fusión con RM de simulación mejora sustancialmente la visualización de la enfermedad macroscópica — las secuencias T1 con gadolinio, T1 con supresión grasa y T2 son particularmente útiles para diferenciar tumor de tejido normal adyacente. Cuando la RM no está disponible — ya sea por incompatibilidad con dispositivos implantados o limitaciones logísticas — la TC de simulación con doble contraste (160 mL en vez de los habituales 80 mL) resulta una alternativa eficaz.
Un ejemplo práctico de este abordaje: una paciente de 79 años con carcinoma epidermoide T1N1 de base de lengua tuvo visualización inadecuada del GTV con contraste simple (80 mL) en la TC de simulación. El GTV era prácticamente indistinguible del tejido circundante. Con doble contraste (160 mL), la misma paciente obtuvo excelente definición tumoral, permitiendo una delineación confiable. Esta técnica simple puede viabilizar la SBRT en centros donde la RM de simulación no está disponible de forma rutinaria.
Las obturaciones dentales que generan artefacto y comprometen la visualización del blanco deben retirarse antes de la SBRT. Un caso reportado ejemplifica bien este problema: un paciente frágil de 87 años con marcapasos incompatible con RM presentaba artefacto severo por obturación dental que afectaba gravemente la visualización del blanco en el surco gingivobucal mandibular izquierdo. La extracción dental posibilitó la delineación adecuada del GTV. Alternativamente, las obturaciones metálicas pueden reemplazarse por materiales no metálicos antes de la simulación.
Inmovilización y Márgenes de PTV en la SBRT de Cabeza y Cuello
La máscara termoplástica de cinco puntos combinada con CBCT diario permite una inmovilización reproducible y la reducción de los márgenes de PTV a solo 3 mm. Esta combinación constituye uno de los pilares de seguridad de la SBRT: la máscara garantiza la reproducibilidad del posicionamiento, mientras el CBCT verifica la posición antes de cada fracción.
La toxicidad se minimiza adicionalmente al eliminar los volúmenes microscópicos convencionales abarcativos. En la SBRT de cabeza y cuello, el CTV de alta dosis es simplemente igual al GTV, sin expansión para enfermedad microscópica. Este enfoque difiere radicalmente de la radioterapia convencional de cabeza y cuello, donde expansiones de CTV de 5–10 mm son habituales y volúmenes electivos extensos son la norma.
La precisión del posicionamiento verificada por CBCT diario, con correspondencia tanto ósea como de tejidos blandos, justifica estos márgenes estrechos. La correspondencia debe incluir ambos tipos de referencia — solo hueso no es suficiente, dada la potencial movilidad de los tejidos blandos respecto a las estructuras óseas. Un programa robusto de garantía de calidad debe sustentar todo el proceso: el centro de los autores emplea un test de alineación de isocentro Winston-Lutz modificado para asegurar tolerancia dentro de 2,5 mm. Como el número de CBCTs en 5 fracciones es mínimo, los intentos de reducir la dosis del CBCT tienen escaso valor y no deben impedir la obtención de imágenes de alta calidad.
Volúmenes Blanco y Prescripción de Dosis en la SBRT
La prescripción estándar para el GTV oscila entre 40 y 50 Gy en 5 fracciones, dos veces por semana, con 45 Gy como la dosis prescrita con mayor frecuencia. La literatura de SBRT para cabeza y cuello reporta prescripciones en el rango de 35–50 Gy en 3–8 fracciones. A diferencia de la radioterapia convencional, no se utiliza expansión de CTV de alta o baja dosis a partir del GTV — el concepto de volumen microscópico peritumoral se elimina por completo.
La siguiente tabla resume las definiciones de volúmenes blanco utilizadas en la SBRT de cabeza y cuello según lo propuesto por los autores:
| Volumen Blanco | Definición y Descripción |
|---|---|
| GTV40–50 | Primario: toda enfermedad macroscópica en el examen físico e imagen, incluyendo secuencias T1-gadolinio, T1 con supresión grasa y T2 de RM. Fusión de TC de simulación con contraste y RM. Si la RM no es posible, usar TC con doble contraste. Ganglios cervicales: con centro necrótico o PET-ávidos. |
| CTV40–50 | Con delineación precisa del GTV, este volumen es igual al GTV40–50. |
| PTV35–40 | CTV40–50 (equivalente al GTV40–50) + 3 mm, con CBCT diario. |
| CTV35–40 | Ganglios sospechosos (redondeados, con realce). |
| PTV30–35 | CTV35–40 + 3 mm si cerca de otros volúmenes de alta dosis con buena correspondencia en CBCT; si no es posible, CTV35–40 + 5 mm. |
| CTV25 | Cadenas ganglionares de alto riesgo inmediatamente adyacentes a los volúmenes de tratamiento, donde la reirradiación por recidiva regional sería difícil. |
| PTV25 | CTV25 + 3–5 mm. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 3.1)
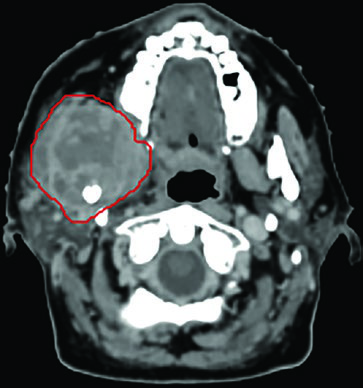
Los puntos calientes deben ubicarse dentro del GTV y lejos de los órganos en riesgo. Un índice de conformidad de 1,1 entre GTV y PTV35–40/PTV40–50 es deseable — valores muy por encima de 1,1 indican irradiación excesiva de tejido normal, mientras que valores muy cercanos a 1,0 pueden comprometer la robustez del plan. La cobertura del blanco debe comprometerse cuando existe proximidad a estructuras neurológicas críticas como el plexo braquial, las vías ópticas, el cerebro y el tronco encefálico. Sin embargo — y este es un punto crucial — la dosis a la arteria carótida no debe comprometer la cobertura del blanco, excepto en escenarios de reirradiación.
El CTV microscópico (CTV25) merece atención especial. No es una expansión del GTV como en la radioterapia convencional, sino un volumen independiente que cubre cadenas ganglionares de alto riesgo inmediatamente adyacentes a los volúmenes de tratamiento. Su inclusión es particularmente importante donde la reirradiación por recidiva regional en esa zona sería difícil o imposible. El PTV de dosis reducida (PTV35–40) se crea con una expansión uniforme de 3 mm del GTV/CTV de alta dosis, manteniendo la filosofía de márgenes mínimos viabilizados por la máscara de 5 puntos y el CBCT diario.
Casos Clínicos: Versatilidad de la SBRT en Escenarios Complejos
La fortaleza de la SBRT de cabeza y cuello reside en su adaptabilidad a escenarios clínicos complejos. Los siguientes casos, documentados por Keilty y colaboradores, ilustran esta versatilidad en pacientes de distintos rangos etarios y presentaciones tumorales.
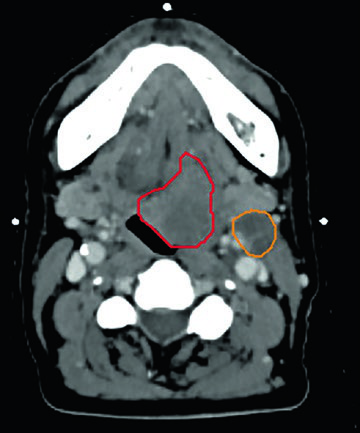
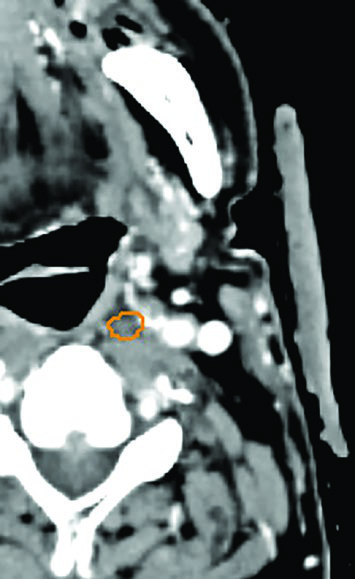
Tumor irresecable de seno piriforme. Una paciente de 73 años con carcinoma epidermoide T1N3 del seno piriforme izquierdo que comprimía la vena yugular interna optó contra un curso prolongado de radioterapia. Recibió 50 Gy en 5 fracciones al GTVn (volumen ganglionar, naranja) y 40 Gy en 5 fracciones al GTVp (volumen primario, rojo), dos fracciones semanales. La cobertura del blanco no se comprometió para preservar la arteria carótida — consistente con la recomendación de que la carótida no debe limitar la dosis al blanco en el escenario no reirradiado. A los 2 años, sin evidencia de enfermedad.
CCC extenso de cavidad oral. Una mujer de 65 años presentó un carcinoma epidermoide de cavidad oral de 6,9 por 4,0 cm, extendiéndose desde la base del cráneo por la fosa infratemporal hasta el espacio masticatorio y la mandíbula derecha, causando fractura patológica y trismo con apertura bucal de apenas 1,5 cm. Pese a la extensión tumoral considerable, recibió 45 Gy en 5 fracciones. El resultado fue notable: cuatro años después, podía abrir la boca 4 cm y permanecía libre de enfermedad. Este caso demuestra el potencial de control local duradero incluso en tumores voluminosos.
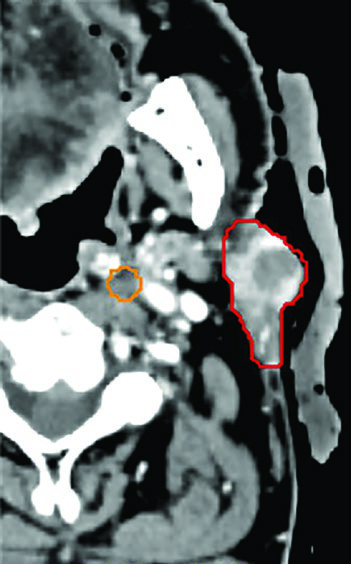
CCC con cáncer concomitante potencialmente mortal. Un paciente de 66 años con obstrucción de vena cava superior por masa pulmonar de células no pequeñas de 10 cm. Radioterapia paliativa y quimioterapia estabilizaron la enfermedad pulmonar durante 18 meses. La investigación de disfagia dolorosa reveló una masa de 3 cm en la base de lengua izquierda que cruzaba la línea media y un ganglio nivel II izquierdo de 3,3 cm. La nasofaringoscopia flexible mostró extensión hacia la valécula con desplazamiento epiglótico. Este carcinoma T2N1 de base de lengua fue tratado con 45 Gy en 5 fracciones — el GTVp (rojo), GTVn45 (naranja) y GTVn40 (verde) fueron delineados individualmente. Tras la SBRT, inició terapia sistémica de segunda línea para el pulmón. Sin evidencia de enfermedad de cabeza y cuello a los 18 meses, tolerando todas las texturas alimentarias sin dolor.
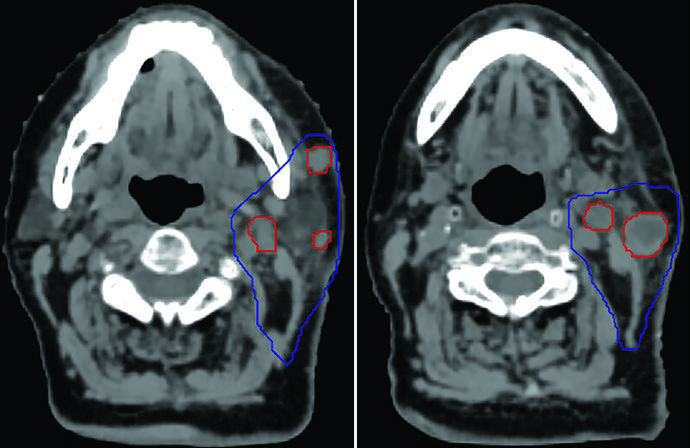
Recidiva en centenaria. Una paciente de 100 años con carcinoma epidermoide cutáneo recidivó en la parótida y ganglios cervicales. El GTV45 (rojo) englobó la enfermedad macroscópica, mientras el CTVn25 (azul) cubrió la cadena ganglionar de alto riesgo de recaída. Permaneció bien durante 6 meses, luego recidivó regionalmente tanto dentro como fuera del campo de baja dosis — demostrando una limitación inherente de la SBRT cuando se necesitan volúmenes electivos extensos pero no se incluyen. Consulte también nuestro artículo dedicado a la delineación en cáncer de laringe para comparaciones con abordajes convencionales de cabeza y cuello.
Enfermedad oligometastásica adyacente al plexo braquial. Una paciente de 55 años con metástasis solitaria irresecable de cáncer colorrectal en la fosa supraclavicular. El nódulo de 6 cm fue tratado con 45 Gy en 5 fracciones, dos veces por semana. La planificación empleó RM de simulación para diferenciar el GTV (rojo) del plexo braquial (azul) — una diferenciación crucial que sería imposible solo con TC, dada la densidad similar de ambas estructuras. La masa recidivó 3 años después en el cuello izquierdo.
Tumor primario de parótida. Un paciente de 91 años con parálisis del nervio facial secundaria a carcinoma poco diferenciado de parótida izquierda (rojo) y dos ganglios retrofaríngeos (naranja) recibió 50 Gy en 5 fracciones, dos veces por semana. Alcanzó respuesta clínica completa con recuperación de la función del nervio facial. Un ectropión paralítico menor del ojo sería tratado con cantotomía y cantopexia. Sin evidencia de enfermedad a los 6 meses — un resultado llamativo considerando la edad y el grado tumoral.
Evaluación de la Respuesta y Seguimiento por Imagen Post-SBRT
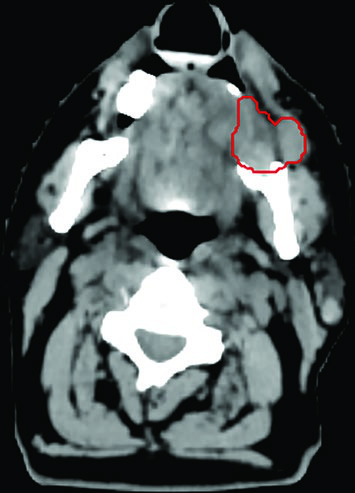
La tasa de regresión tras SBRT de cabeza y cuello es variable, y la respuesta máxima frecuentemente se alcanza más allá de los plazos tradicionales — típicamente después de 3 meses. Esta cinética lenta exige cautela al interpretar los estudios de imagen postratamiento y paciencia antes de considerar un rescate.
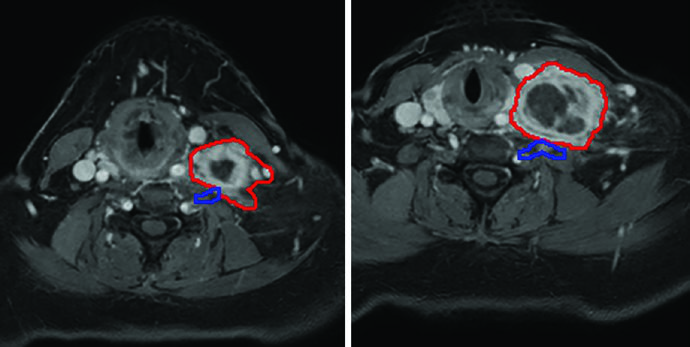
Un caso ilustrativo es el de una paciente de 83 años, tratada quirúrgicamente 3 años antes por carcinoma epidermoide de lengua derecha, que presentó una masa dolorosa ganglionar nivel II derecho profunda a la parótida, extendiéndose al espacio parafaríngeo y la vaina carotídea. No era candidata a quimiorradiación radical y recibió 45 Gy en 5 fracciones, dos veces por semana. La delineación del GTV (rojo) fue asistida por fusión TC-RM, con la TC a la izquierda y la RM a la derecha en la misma pantalla de planificación.
A pesar de la mejoría del dolor, la RM a los 4 meses mostró posible progresión en T1 pero respuesta en T2 — hallazgos discordantes que podrían conducir a una decisión prematura de rescate si se interpretan aisladamente. A los 9 meses, la RM demostró estabilidad de la enfermedad y la paciente estaba libre de dolor. Este caso refuerza que la evaluación multiparamétrica y la paciencia son esenciales en el seguimiento post-SBRT.
Consideraciones Prácticas y Seguridad en la SBRT de Cabeza y Cuello
La SBRT de cabeza y cuello exige un equipo multidisciplinario altamente experimentado compuesto por físicos médicos, dosimetristas y técnicos de radioterapia. Este no es un procedimiento para centros de bajo volumen — la curva de aprendizaje es pronunciada y los riesgos de toxicidad severa en caso de fallo técnico son significativos en esta región anatómica.
La garantía de calidad rigurosa sustenta la seguridad del tratamiento. El test de alineación de isocentro Winston-Lutz modificado asegura tolerancia de 2,5 mm — un valor que debe mantenerse en cada sesión. El CBCT diario con correspondencia en hueso y tejidos blandos es imperativo; como ya se mencionó, el número reducido de CBCTs en una SBRT de 5 fracciones hace irrelevante cualquier preocupación por dosis adicional de imagen.
En la práctica, la eliminación de los volúmenes microscópicos convencionales es una de las mayores ventajas de la SBRT en esta región. Con delineación precisa del GTV y márgenes de PTV de solo 3 mm — viabilizados por la máscara de 5 puntos y el CBCT diario — los tejidos normales adyacentes reciben dosis sustancialmente menores que con la radioterapia convencional fraccionada. Para detalles sobre delineación en otros subsitios de cabeza y cuello, consulte nuestros artículos sobre nasofaringe, orofaringe e hipofaringe.
Los resultados clínicos documentados por Keilty y colaboradores demuestran que la SBRT puede lograr control local duradero incluso en pacientes muy ancianos con tumores avanzados. La paciente de 65 años con tumor extenso de cavidad oral de casi 7 cm permaneció libre de enfermedad durante 4 años; el paciente de 91 años con carcinoma poco diferenciado de parótida alcanzó respuesta completa con recuperación de la función facial. Estos desenlaces refuerzan el papel de la SBRT como herramienta terapéutica valiosa para pacientes que, de otra manera, recibirían únicamente cuidados paliativos convencionales con menor expectativa de control local.




