Anatomia e Padrões de Disseminação dos Tumores Sinonasais
Os tumores sinonasais representam um desafio único no planejamento radioterápico. A cavidade nasal e os seios paranasais estão interconectados por múltiplos óstios e separados apenas por septos finos — o que facilita a extensão local para cavidades adjacentes. Essa anatomia interligada exige atenção redobrada no delineamento dos volumes alvo.
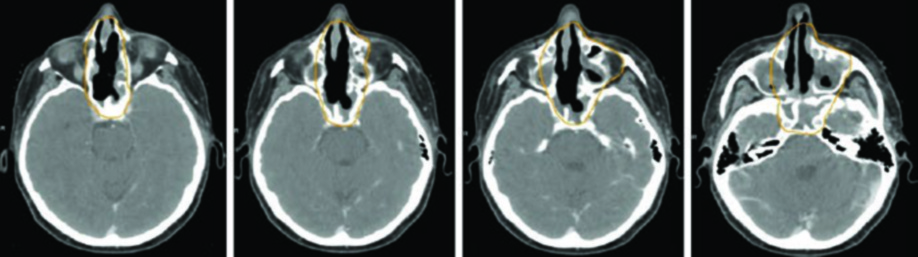
A diversidade histológica é marcante. Carcinoma espinocelular, adenocarcinoma de glândula salivar menor, carcinoma adenoide cístico, estesioneuroblastoma (ENB), carcinoma sinonasal indiferenciado (SNUC), carcinoma neuroendócrino de pequenas células (SNEC), melanomas e carcinoma NUT de linha média — cada subtipo apresenta comportamento biológico distinto e exige adaptações no volume de tratamento.
Alguns padrões de disseminação merecem atenção especial. ENB, SNUC e SNEC surgem na cavidade nasal superior e invadem facilmente a lâmina cribriforme em direção à fossa craniana anterior. Essas regiões precisam ser incluídas no volume alvo. Já os cânceres do seio maxilar podem invadir a cavidade nasal pela parede medial porosa, a gengiva maxilar pela parede lateral do antro, a fossa infratemporal ou pterigopalatina por extensão posterior, ou a órbita por extensão superior direta ou via seios etmoidais.
A invasão perineural é outro ponto crítico. Quando há envolvimento de nervos cranianos, é fundamental cobrir o nervo afetado até a base do crânio. Metástases skip microscópicas são comuns nessa via, e recidivas ao longo de nervos podem ser difíceis de resgatar. Para carcinomas adenoides císticos, a cobertura de nervos cranianos é fortemente recomendada mesmo sem invasão perineural patológica confirmada.
Volumes Alvo e Doses de Prescrição
O delineamento dos volumes alvo em tumores sinonasais segue princípios bem definidos, mas exige flexibilidade diante da proximidade de estruturas críticas. As tabelas a seguir resumem as definições e doses recomendadas.
Volumes para doença macroscópica
| Volume | Definição | Dose |
|---|---|---|
| GTV70 | Toda doença macroscópica ao exame físico e imagem (TC e RM). PET auxilia na extensão tumoral. RM identifica invasão perineural oculta ao PET | 70 Gy (1,8–2 Gy/fração) |
| CTV70 | Geralmente idêntico ao GTV70. Margem de 3–5 mm quando há incerteza na delineação. Pode ser 0 mm próximo a estruturas críticas — GTV pode igualar CTV | 70 Gy |
| PTV70 | CTV70 + 3–5 mm dependendo da incerteza de setup. Reduzido para 1 mm adjacente a tronco encefálico e quiasma óptico | 70 Gy |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 7.1)
Volumes para regiões subclínicas de alto e baixo risco
| Volume | Definição |
|---|---|
| CTV60–66 | Regiões de alto risco para doença microscópica. Pós-operatório: inclui leito de ressecção, áreas de extensão nodal e todos os sítios pré-operatórios de doença. Considerar cobertura de todo o leito pós-operatório e retalho. Definitivo: expansão de 5–10 mm no tumor primário cobrindo o subsítio anatômico, respeitando barreiras anatômicas. CTV66 para margens positivas ou extensão extranodal (6 Gy em 3 frações sequenciais) |
| CTV50–54 | Regiões subclínicas de baixo risco, incluindo pescoço não violado ou cobertura profilática de nervos cranianos |
| PTV60–66 | CTV60–66 + 3–5 mm. Pode ser reduzido para 1 mm adjacente a estruturas normais críticas |
| PTV50–54 | CTV50–54 + 3–5 mm dependendo da incerteza de setup e técnica de guiamento por imagem |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 7.2)
Na prática, a proximidade com estruturas como tronco encefálico, quiasma óptico e nervos ópticos faz com que as margens de PTV sejam frequentemente reduzidas para 1 mm nessas interfaces. Essa compressão de margens é aceitável, desde que haja guiamento por imagem diário de alta qualidade. Para uma visão abrangente de como essas estratégias se encaixam no planejamento geral, confira nosso guia completo sobre delineamento de volume alvo e configuração de campos.
Avaliação Diagnóstica para Delineamento
A definição precisa dos volumes alvo começa com uma avaliação diagnóstica minuciosa. Revisão detalhada da história pré-operatória, exame neurológico com ênfase em nervos cranianos, imagens pré e pós-operatórias, relatório cirúrgico e laudo patológico — tudo é necessário.
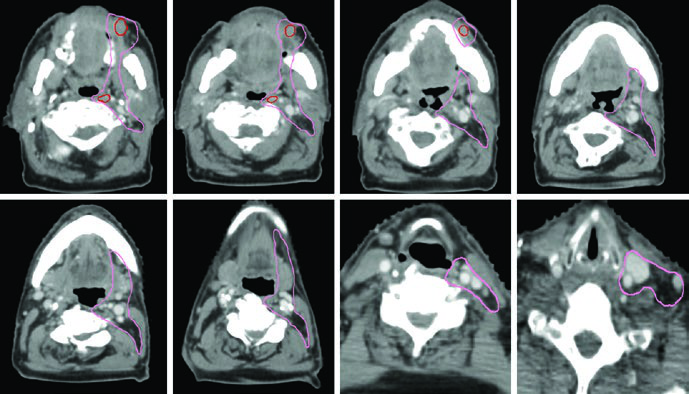
Além da endoscopia com fibra óptica, imagens diagnósticas de alta qualidade são críticas para a localização tumoral. Cada modalidade de imagem tem seu papel específico:
A TC de alta resolução dos seios paranasais com contraste IV e cortes finos de 1–2 mm é ideal para visualizar erosão cortical óssea precoce. A RM com contraste IV e sequências com supressão de gordura, em cortes finos, é superior para avaliar extensão em partes moles, extensão intracraniana, invasão perineural e envolvimento dos forames e canais dos nervos cranianos. O PET/CT complementa o estadiamento ao identificar linfonodos suspeitos e doença metastática.
Simulação e Localização Diária
A simulação deve ser realizada com o paciente em decúbito dorsal, com suporte de cabeça e pescoço estendido, usando máscara termoplástica de cinco pontos (Aquaplast) que imobilize cabeça, pescoço e ombros. Uma prancha de tração de ombros pode ser utilizada para rebaixar os ombros fora do caminho do feixe.
Bloqueador de mordida ajuda a empurrar a língua inferiormente, afastando-a da nasofaringe de alta dose. Pacientes com muitas restaurações metálicas se beneficiam de um protetor bucal customizado para absorver elétrons secundários e reduzir a mucosite. A TC de simulação deve usar cortes de até 3 mm com contraste IV, cobrindo do vértice da cabeça até a carina. O isocentro fica tipicamente posicionado nas aritenoides.
Para casos pós-operatórios, marcadores radiopacos nas cicatrizes cirúrgicas auxiliam na delineação do leito tumoral. A guia por imagem diária — idealmente com cone beam CT (CBCT) alinhado ao osso — é fundamental. Imagens kV diárias com CBCT semanal também são adequadas.
Delineamento de Volumes e Planejamento por Subsítio
O GTV deve ser delineado usando todas as informações clínicas relevantes de endoscopia, TC, RM e PET. O CTV de alto risco deve cobrir todos os sítios iniciais de doença e regiões potenciais de disseminação subclínica. Todas as imagens pré-operatórias devem ser avaliadas para garantir que o volume tumoral inicial esteja coberto.
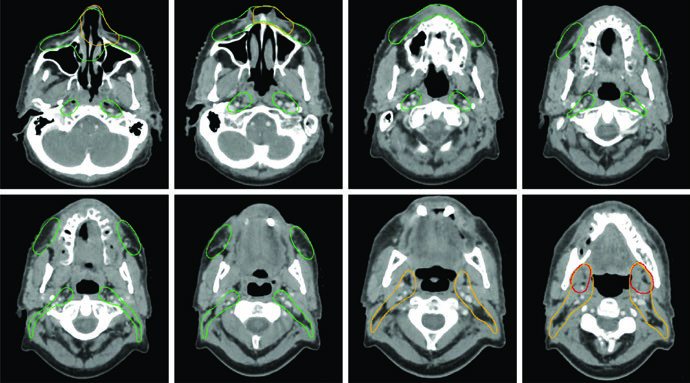
A RM deve ser usada em todos os casos para auxiliar o delineamento, exceto quando contraindicada. Carcinomas adenoides císticos são altamente neurotrópicos, portanto os volumes devem cobrir nervos aferentes e eferentes locais até a base do crânio. ENB surge na cavidade nasal superior e tende a invadir a lâmina cribriforme e fossa craniana anterior precocemente.
A tabela abaixo detalha as considerações anatômicas específicas por subsítio para delineamento do CTV primário.
| Subsítio | Direção | Considerações para Delineamento |
|---|---|---|
| Seio maxilar (CEC) | Superior | Assoalho orbital/base do crânio. RM coronal útil para assoalho orbital. Extensão intracraniana: margem dural de 5 mm |
| Inferior | Palato duro com margem mínima de 10 mm ao redor da doença macroscópica inicial | |
| Medial | Septo nasal para casos lateralizados. Extensão medial além do septo: considerar cobertura de toda a cavidade nasal | |
| Lateral | Fossa infratemporal incluindo espaço mastigatório. Extensão lateral: considerar cobertura ao longo do músculo temporal | |
| Posterior | Fossa pterigopalatina e base do crânio, incluindo fissura infraorbital. Envolvimento posterior: cobrir cursos de CN V2/V3 até a caverna de Meckel | |
| Nervos | Ramos de CN V2, nervo infraorbital e nervos palatinos maiores | |
| Cavidade nasal (CEC, ENB, SNUC, SNEC, melanoma) | Superior | Lâmina cribriforme (se intacta) ou enxerto dural. Margem dural de 5 mm quando cribriforme envolvida ou extensão intracraniana macroscópica |
| Inferior | Palato duro | |
| Medial | Incluir toda a cavidade nasal | |
| Lateral | Parede medial do seio maxilar ipsilateral para casos localizados | |
| Posterior | Lâminas pterigoides, fossa pterigopalatina, seio etmoidal e seio esfenoidal | |
| Nervos | Ramos de CN I, CN V1 e CN V2 incluindo nervos nasociliar e nasopalatino | |
| Seio etmoidal | Superior | Conforme cavidade nasal |
| Inferior | Margem de 10 mm na extensão tumoral inicial. Tumores iniciais: corneto inferior aceitável. Tumores avançados: incluir palato duro | |
| Medial/Lateral | Cavidade nasal, seios etmoidais e seio maxilar ipsilateral. Violação da lâmina papirácea: incluir reto medial | |
| Posterior | Base do crânio e seio esfenoidal. Linfonodos retrofaríngeos se envolvimento da nasofaringe ou N1 | |
| Nervos | Ramos de CN V1 e CN V2. Inervação parassimpática via nervo vidiano |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 7.3)
Situações especiais merecem destaque. O SNEC tem alto risco de doença metastática e pode ser tratado com fracionamento padrão ou 45 Gy em 30 frações BID, podendo omitir cobertura nodal eletiva. Melanoma mucoso nasal também tem alto risco metastático — tumores grandes recebem fracionamento padrão, enquanto tumores pequenos podem ser tratados com 30–36 Gy em frações de 6 Gy duas vezes por semana, limitados ao sítio primário.
Irradiação Cervical Eletiva e Planejamento
A irradiação nodal eletiva deve ser considerada caso a caso. Linfonodos eletivos fazem sentido para ENB e carcinoma espinocelular avançado, especialmente quando a origem é o seio maxilar ou quando há envolvimento de áreas com suprimento linfático extenso — nasofaringe, mucosa, pele, bochecha, nariz anterior, gengiva maxilar ou crista alveolar.
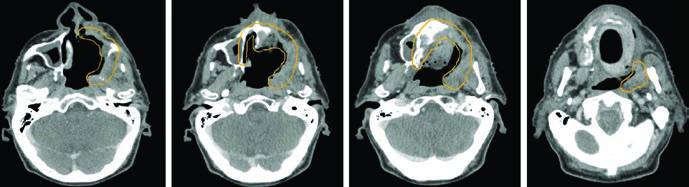
A drenagem nodal regional segue padrões previsíveis: linfonodos retrofaríngeos e níveis IB–IV. O nível V deve ser incluído quando há envolvimento da nasofaringe. Cobertura de linfonodos faciais deve ser considerada para tumores da cavidade nasal. A maioria dos tumores primários são estruturas de linha média, justificando irradiação nodal bilateral. A exceção são cânceres do seio maxilar, que recebem irradiação nodal unilateral.
A abordagem cirúrgica (degloving de face média, rinotomia lateral, ressecção craniofacial ou ressecção endoscópica) influencia diretamente o desenho do campo. Quando uma ressecção craniofacial foi realizada, o enxerto frontal deve ser incluído no volume alvo. Marcadores fiduciais cirúrgicos auxiliam na delineação do leito tumoral.
Para o planejamento propriamente dito, a equipe do Memorial Sloan-Kettering Cancer Center preconiza uma abordagem sequencial de cone-down. O plano inicial (30 frações) utiliza dose-painting para entregar 54 Gy (1,8 Gy/fração) às regiões subclínicas de baixo risco e 60 Gy (2 Gy/fração) às regiões subclínicas de alto risco. Em seguida, um plano cone-down (5 frações) entrega 10 Gy adicionais exclusivamente à doença macroscópica, totalizando 70 Gy em 35 frações.
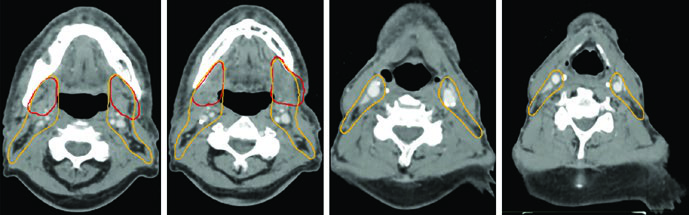
Os tumores sinonasais exigem do radioterapeuta um conhecimento profundo da anatomia da base do crânio, dos forames e canais nervosos, e das vias de disseminação local e regional. A fusão de TC e RM, revisão cuidadosa do relatório cirúrgico e estadiamento por PET/CT compõem a base para um delineamento de qualidade. Cada histologia tem suas particularidades — desde a neurotroficidade do carcinoma adenoide cístico até o comportamento agressivo do SNUC com invasão cribriforme precoce. A atenção a esses detalhes separa um planejamento adequado de um planejamento verdadeiramente eficaz.