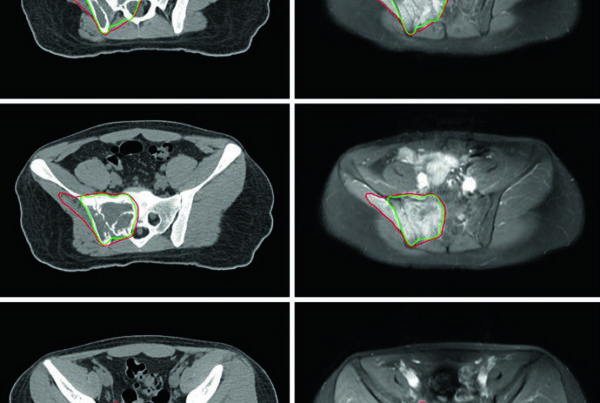
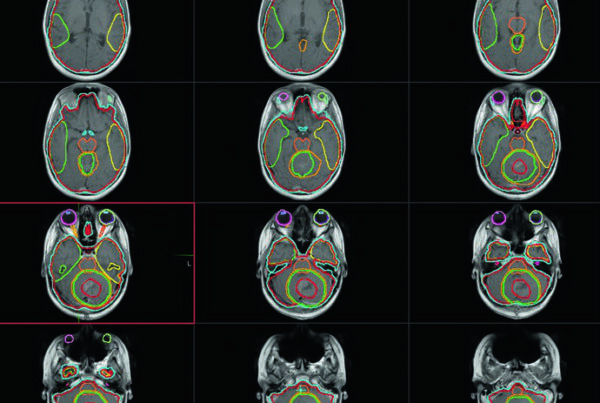
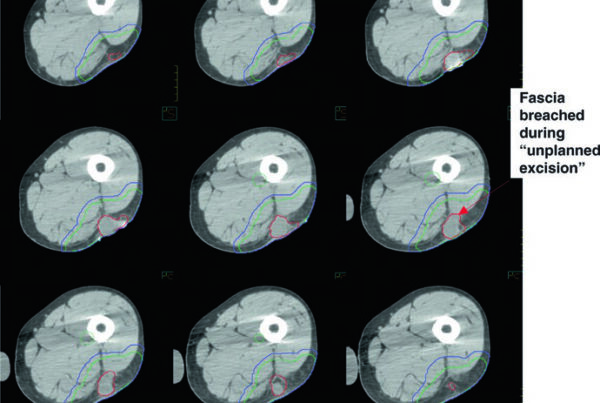
O planejamento do câncer de mama inicial descrito neste capítulo gira em torno de três exigências técnicas: campos tangenciais bem construídos, dose homogênea dentro da mama e delimitação rigorosa do leito cirúrgico quando há indicação de boost ou de APBI. Os autores percorrem o fluxo completo, desde a revisão de mamografia, ultrassom e patologia até a simulação, o posicionamento, o contorno dos volumes e a avaliação do coração e dos pulmões. Para uma visão mais ampla do tema, consulte nosso guia completo sobre delineamento de volume alvo e campos na radioterapia.
Câncer de mama inicial: princípios gerais do planejamento
No capítulo, a técnica padrão para radioterapia adjuvante é a radioterapia conformada tridimensional com compensação adequada. Essa compensação pode ser feita com a técnica field-in-field e, quando necessário, com feixes de energia mista, sempre com a meta de manter a dose homogênea no tecido mamário. O mesmo trecho acrescenta um ponto decisivo para a rotina: o mais alto nível de evidência favorece a irradiação de mama inteira em esquema hipofracionado, o que transforma a homogeneidade do plano em requisito central, e não em detalhe periférico.
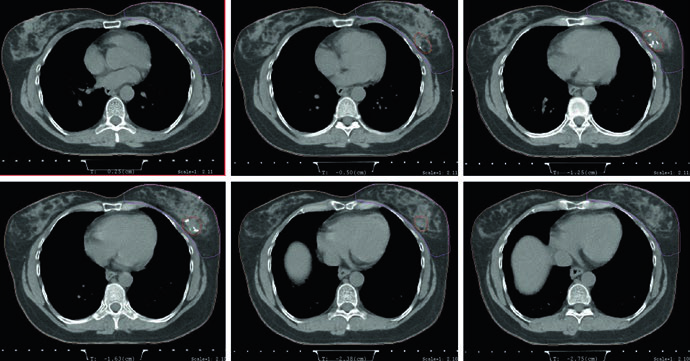
Essa abertura do capítulo é pragmática. Ela não separa planejamento e delineamento como tarefas independentes, porque a cobertura homogênea da mama depende da forma como o volume é desenhado e da maneira como os tangentes são compensados. Ao citar 3D CRT e IMRT como possibilidades técnicas, o texto não sugere que uma modalidade substitui automaticamente a outra. O recado é outro: qualquer técnica escolhida precisa preservar o mesmo objetivo geométrico e dosimétrico, com cobertura uniforme da mama e controle consciente da dose que alcança coração e pulmões.
As figuras de planejamento deixam esse raciocínio concreto. O exemplo supino mostra tangentes com field-in-field para homogeneidade e um pequeno bloqueio por MLC para proteção cardíaca. Na mesma legenda, a prescrição aparece de forma direta: 42,4 Gy em frações de 2,65 Gy, seguidos de boost com elétrons na cavidade da lumpectomia até 10 Gy em frações de 2,5 Gy. O capítulo, portanto, não trata a compensação como um refinamento opcional. Ela já integra a técnica padrão desde o início do plano.
Outro ponto relevante é a disciplina do escopo. O texto não se dispersa para doença localmente avançada nem para cenários nodais extensos. O foco fica na mama inteira, no leito cirúrgico e nos ajustes de setup que mantêm o tratamento reproduzível. Isso é útil porque evita que o caso inicial seja carregado por margens arbitrárias ou por rotinas emprestadas de outros contextos clínicos.
Imagem, cirurgia e patologia antes da tomografia
Antes da radioterapia, o capítulo pede revisão cuidadosa do exame físico, das imagens pré-operatórias e da patologia. Todas as pacientes devem ter mamografia no diagnóstico, e o ultrassom aparece como complemento frequente. A ressonância magnética tem indicação limitada na doença inicial, mas pode estar disponível em alguns casos; quando estiver, deve ser revisada antes do planejamento para ajudar tanto nas margens da mama inteira quanto no direcionamento preciso do boost e da APBI.
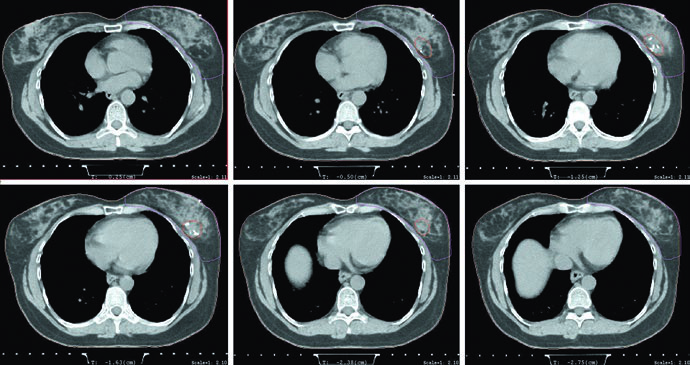
O texto também organiza a sequência cirúrgica e anatomopatológica. A biópsia guiada por imagem costuma confirmar o diagnóstico. Para carcinoma ductal in situ, a recomendação citada é lumpectomia ou excisão segmentar isolada. Para doença invasiva inicial, o capítulo aponta lumpectomia associada à biópsia do linfonodo sentinela. A revisão da patologia vem logo depois, com um critério de margem bem definido: ausência de tumor na tinta para doença invasiva e 2 mm para DCIS puro, conforme o consenso SSO-ASTRO de 2016 mencionado pelos autores.
Os clipes cirúrgicos recebem uma observação extremamente prática. O capítulo diz que é preferível, embora não obrigatório, que o cirurgião os coloque no momento da cirurgia para ajudar na delimitação do leito tumoral e na localização radiográfica antes da entrega da dose. A utilidade desses clipes cresce ainda mais quando a indicação considerada é APBI. Sem eles, o planejador depende muito mais do seroma, das diferenças do tecido glandular e da comparação com a mama contralateral.
Essa etapa prévia explica por que o texto insiste tanto na revisão de toda a imagem disponível antes de abrir o planejamento. O leito de lumpectomia não deve ser tratado como um volume deduzido apenas pela tomografia de simulação. O capítulo pede explicitamente a leitura integrada de mamografia, ultrassom e ressonância quando disponível. Em outras palavras, o delineamento correto começa antes da primeira linha de contorno no console.
Tomografia de simulação, posição supina, prona e DIBH
Na simulação para mama inteira, o capítulo recomenda tomografia com espessura de corte menor ou igual a 3 mm, em posição supina ou prona. Para APBI, a exigência fica mais estreita: cortes de 1,5 a 2 mm através da cavidade de lumpectomia podem melhorar a definição desse volume. Não é um detalhe burocrático. É a diferença entre aceitar uma cavidade apenas presumida e enxergar melhor o alvo que depois orientará a expansão de CTV e PTV.
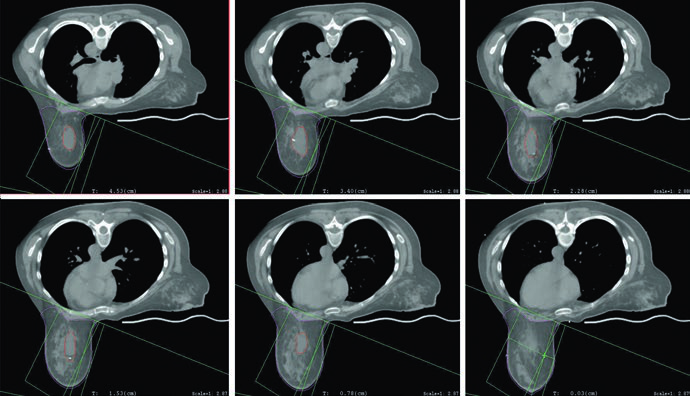
Quando a opção é pelo setup supino, a paciente deve ficar em prancha mamária com os braços acima da cabeça. Se o tumor é à esquerda, o texto recomenda considerar respiração profunda em inspiração mantida, a técnica de DIBH, para reduzir a dose no coração. O verbo usado importa. O capítulo não transforma DIBH em ritual obrigatório para todos os casos à esquerda, mas deixa claro que a redução da dose cardíaca deve entrar no raciocínio do planejador sempre que esse recurso estiver disponível e for reproduzível.
A posição prona ganha um espaço amplo e bem delimitado. Pacientes com mamas pendulares podem se beneficiar dela porque a separação diminui e a homogeneidade do tecido no planejamento melhora, algo que pode reduzir toxicidade aguda. O texto ainda aponta duas consequências dosimétricas: menos radiação no pulmão e possibilidade de evitar melhor o coração. Só que os autores fazem a ressalva que interessa à prática: se o leito tumoral encosta na parede torácica, o coração pode paradoxalmente se aproximar do campo de tratamento. O capítulo não vende a prona como solução automática; ele a apresenta como ferramenta útil, desde que o caso seja lido com cuidado.
Há também disciplina mecânica no setup prono. A paciente deve ser colocada em uma prancha dedicada para mama, e o conforto precisa ser garantido porque a reprodutibilidade depende disso. O texto fecha esse bloco lembrando que lesões ortopédicas no dorso ou no pescoço podem tornar a prona uma má escolha. É um ponto simples, mas clínico. O melhor arranjo geométrico perde valor se a paciente não consegue reproduzi-lo ao longo do tratamento.
Essa comparação entre supino e prono conversa diretamente com o planejamento das figuras. O exemplo em prono usa tangentes com field-in-field, a mesma prescrição de 42,4 Gy em 2,65 Gy por fração e boost com mini-tangentes fotônicos até 10 Gy em 2,5 Gy por fração. A legenda ainda acrescenta um detalhe anatômico que serve de guia: a borda posterior do campo deve incluir parte do músculo peitoral. Para quem quiser avançar do raciocínio da mama inicial para cobertura regional, vale continuar a leitura no nosso artigo sobre irradiação nodal regional no câncer de mama.
Boost do leito tumoral e uso seletivo de APBI
O capítulo é claro ao resumir o papel do boost. Irradiar o leito tumoral após a mama inteira reduz ainda mais o risco de recorrência local, mas esse reforço pode ser omitido em pacientes de baixo risco. O texto não transforma essa decisão em fórmula rígida. Ele só define o ponto de partida: boost tem valor reconhecido, porém existe um grupo em que a omissão pode ser aceitável.
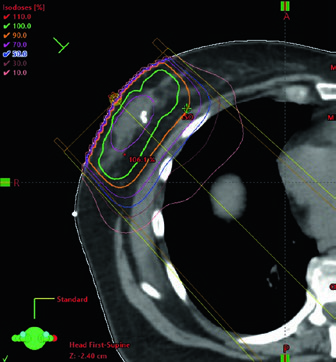
Quando o boost é indicado, o planejamento mais comum descrito pelos autores usa elétrons em incidência en face. A seleção da energia deve obedecer à profundidade do leito tumoral somada a uma margem, sem ultrapassar a superfície anterior dos músculos peitorais. A figura do boost em posição supina torna isso quase didático ao mostrar a escolha de 12 MeV para garantir cobertura da isodose de 90% até a superfície anterior do peitoral. Se o leito é profundo, o texto admite uma alternativa prática: considerar mini-tangentes.
A APBI aparece em seguida, com formulação cuidadosa. Ainda não é apresentada como padrão de tratamento, mas já é considerada alternativa aceitável para pacientes selecionadas de baixo risco e com doença unifocal. O capítulo não vai além disso, e essa contenção ajuda. Em vez de prometer uma mudança de paradigma, ele delimita um território específico em que a irradiação parcial acelerada pode ser usada de forma responsável.
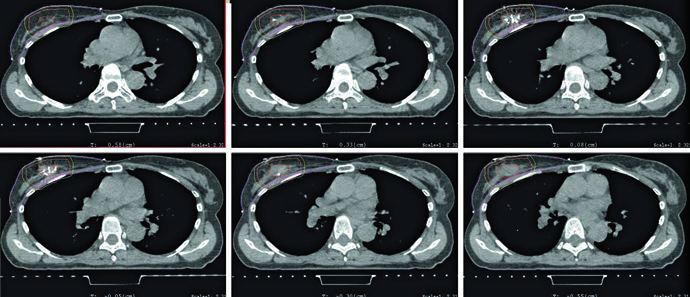
As figuras e a tabela explicam como esse volume é construído. A cavidade de lumpectomia deve incorporar seroma, clipes e alterações marcantes do tecido glandular. A tabela recomenda expansão de 1,0 a 1,5 cm para o CTV e de 0,5 a 1,0 cm para o PTV, conforme incerteza de setup e movimento previsto. Já a legenda da figura de APBI mostra um exemplo típico: CTV de 1,5 cm ao redor da cavidade, excluindo músculo peitoral, costela e parede torácica, sem ultrapassar o tecido mamário contornado e sem chegar à pele, ficando restrito a 5 mm da superfície. Em seguida, o PTV é formado por expansão de aproximadamente 5 mm em torno do CTV, dependendo da incerteza institucional.
Essa combinação entre tabela e figura afasta dois erros comuns. O primeiro é expandir o volume de forma automática, sem checar onde o tecido mamário realmente termina. O segundo é transformar o PTV em um volume anatomicamente limpo demais, esquecendo que o próprio capítulo permite que ele ultrapasse a superfície e avance para peitoral ou parede torácica quando isso decorre da margem de setup. Em APBI, o texto pede duas coisas ao mesmo tempo: disciplina anatômica no CTV e honestidade geométrica no PTV.
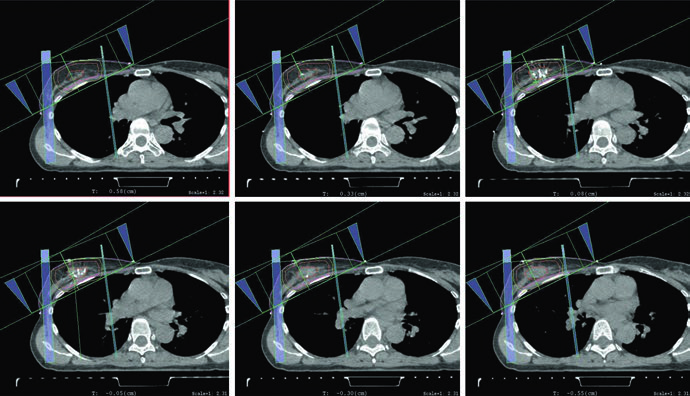
A figura do plano de APBI fecha esse bloco de forma coerente com o restante do capítulo. O arranjo usa mini-tangentes fotônicos combinados com um campo de elétrons en face. Não há nenhuma tentativa de tratar APBI como algo descolado do raciocínio da mama inteira. O que muda é o volume abordado, mas o capítulo continua exigindo o mesmo cuidado com orientação dos campos, profundidade útil do boost e correspondência entre anatomia operada e distribuição de dose.
Delineamento do volume alvo da mama e da cavidade cirúrgica
O capítulo define o volume da mama com base em referência clínica obrigatória. A mama pode ser marcada com fio ou com bordas colocadas clinicamente na tomografia, e o contorno deve abranger todo o tecido glandular. A descrição anatômica é precisa: o limite cranial fica abaixo da cabeça da clavícula e na inserção da segunda costela; o caudal aparece quando o tecido mamário desaparece; o medial segue a borda do esterno sem cruzar a linha média; o lateral acompanha a linha axilar média, respeitando o quanto a ptose altera a posição do tecido; o limite anterior coincide com a pele ou com poucos milímetros abaixo dela quando o interesse é relatar dose; e o posterior alcança músculos peitorais e parede torácica, sem incluir músculos nem costelas.
Volumes-alvo sugeridos para planejamento 3D na mama inicial
A Tabela 11.1 concentra o núcleo do delineamento descrito no capítulo. Ela define o que entra em cada volume, onde os limites anatômicos devem parar e em que ponto a expansão deixa de ser aceitável.
| Volume-alvo | Definição e descrição |
|---|---|
| Mama | É necessária referência clínica para delinear o tecido mamário. A mama pode ser marcada com fio ou com bordas colocadas clinicamente no momento da tomografia. O contorno deve incluir todo o tecido glandular mamário. O limite cranial fica abaixo da cabeça da clavícula e na inserção da segunda costela. O limite caudal é definido pela perda do tecido mamário. O limite medial fica na borda do esterno e não deve cruzar a linha média. O limite lateral segue a linha axilar média, mas depende da ptose mamária. O limite anterior é a pele ou poucos milímetros abaixo da superfície cutânea quando o objetivo é relatar dose. O limite posterior corresponde aos músculos peitorais e aos músculos da parede torácica. O volume não deve incluir esses músculos nem as costelas. Em casos muito mediais ou laterais, os limites podem ultrapassar discretamente essas definições para assegurar margem adequada ao redor da cavidade de lumpectomia. |
| Cavidade da lumpectomia | Devem ser incluídos o seroma, os clipes cirúrgicos e diferenças marcantes no tecido glandular da mama. A comparação com a mama contralateral pode ajudar, sobretudo quando não há líquido nem clipes. Todos os exames de imagem disponíveis devem ser revisados antes do planejamento para ajudar a definir esse volume. Ele não deve se estender para fora do tecido mamário. |
| CTV da lumpectomiaa | Corresponde à cavidade de lumpectomia com expansão de 1,0 a 1,5 cm. Esse volume não deve sair do corpo nem entrar nos músculos peitorais ou nos músculos da parede torácica. |
| PTV da lumpectomiaa | É o CTV da lumpectomia com margem baseada na incerteza de setup e no movimento previsto da paciente, em geral entre 0,5 e 1,0 cm. Esse volume pode ultrapassar a superfície do paciente e invadir os músculos peitorais ou da parede torácica. Ajustes podem ser necessários quando o objetivo é relatar dose. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 11.1)
a Apenas para APBI; na irradiação de mama inteira, a cavidade da lumpectomia isoladamente é o alvo do boost.
Esse detalhamento mostra por que os autores exigem referência clínica. A mama não é um volume que se resolve apenas com janela de partes moles. A distribuição do tecido glandular, a queda lateral e inferior causada pela ptose e a relação com o esterno ou com a linha axilar média pedem interpretação clínica já no momento da tomografia. O capítulo ainda admite pequena extrapolação desses limites em casos extremamente mediais ou laterais para garantir margem adequada sobre a cavidade da lumpectomia. Ou seja, a regra anatômica existe, mas não deve sabotar a cobertura do leito operado.
A cavidade da lumpectomia recebe outra lógica. Seroma, clipes e diferenças nítidas no tecido glandular entram no volume. Se esses marcadores forem discretos ou ausentes, o capítulo recomenda recorrer à comparação com a mama contralateral e à revisão das imagens prévias. O que ele proíbe de forma implícita é desenhar a cavidade como uma estimativa vaga, baseada em memória cirúrgica ou em densidades pouco convincentes. O alvo do boost, e em APBI também a base do CTV e do PTV, precisa ser demonstrável.
Há ainda uma diferença importante entre mama inteira e APBI. Na irradiação de mama inteira, a cavidade isoladamente é o alvo do boost. Já em APBI, o processo de expansão vira parte estrutural do tratamento, com CTV e PTV dedicados. O capítulo deixa esse ponto em nota, mas a implicação prática é grande: não convém misturar regras do boost após mama inteira com regras da irradiação parcial acelerada. Cada indicação carrega seu próprio mapa geométrico.
Coração, pulmões e os detalhes do contorno cardíaco
Em todos os casos, os órgãos de risco devem incluir coração e pulmões. O capítulo especifica que o coração deve ser contornado superiormente até a bifurcação da artéria pulmonar, incluindo o pericárdio e a gordura epicárdica situada entre o músculo cardíaco e o pericárdio. A gordura pericárdica que fica fora do pericárdio não precisa ser incluída. A figura correspondente mostra exatamente essa diferença e evita uma fonte frequente de inconsistência entre planejadores.
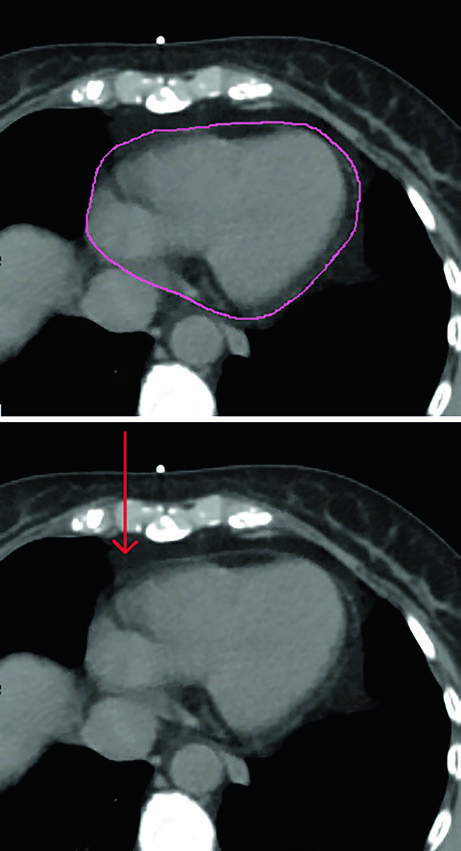
Os autores também organizam a hierarquia do que medir. A melhor evidência para proteção cardíaca continua sendo a redução da dose média no coração. Ao mesmo tempo, eles registram que estão surgindo dados que sugerem relevância para a dose recebida pela artéria descendente anterior esquerda e pelo ventrículo esquerdo. Por isso, essas estruturas podem ser contornadas com base nos atlas publicados por Feng et al. e Duane et al., exatamente como indicado nas referências do capítulo.
Essa combinação entre um desfecho consolidado, que é a dose média cardíaca, e uma avaliação mais refinada de LAD e ventrículo esquerdo ajuda a ler o texto sem exageros. O capítulo não troca um parâmetro robusto por outro ainda emergente. Ele propõe que a equipe some precisão quando isso fizer sentido, sem abandonar o indicador com melhor suporte de evidência. Em prática diária, esse equilíbrio combina bem com a recomendação de considerar DIBH nos casos à esquerda e com o uso de pequenos bloqueios por MLC quando o plano supino exigir proteção cardíaca adicional.
O que as figuras acrescentam à rotina
As figuras do capítulo não servem apenas para ilustrar o texto; elas refinam a tomada de decisão. As imagens axiais em supino e prono mostram como a relação entre mama, pulmão e coração muda com o setup, e isso explica por que o capítulo não trata a posição da paciente como questão de preferência pessoal. A figura de APBI, por sua vez, aproxima a regra abstrata da expansão do que realmente se vê na tomografia, deixando claro onde o CTV deve parar e onde o PTV pode ultrapassar a superfície.
Quando todas essas peças são lidas em conjunto, o recado do capítulo fica bem definido. O caso de mama inicial deve ser planejado com técnica padronizada, revisão minuciosa da cirurgia e da imagem, simulação reproduzível, respeito aos limites anatômicos do tecido mamário e atenção contínua ao coração e aos pulmões. O texto não precisa de adornos para convencer. Ele funciona porque cada escolha descrita, do corte tomográfico de 1,5 a 2 mm na APBI até a borda posterior incluindo parte do peitoral no plano prono, está amarrada a um detalhe concreto do tratamento.