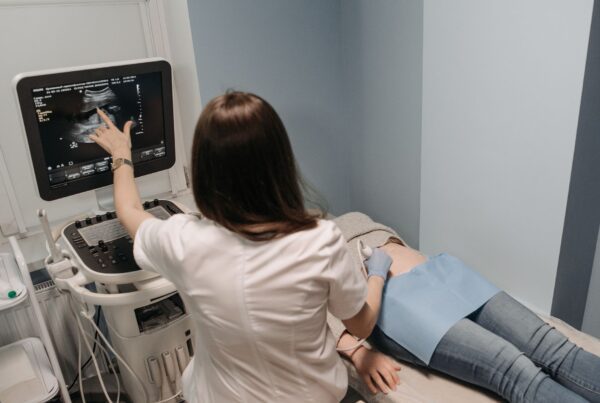
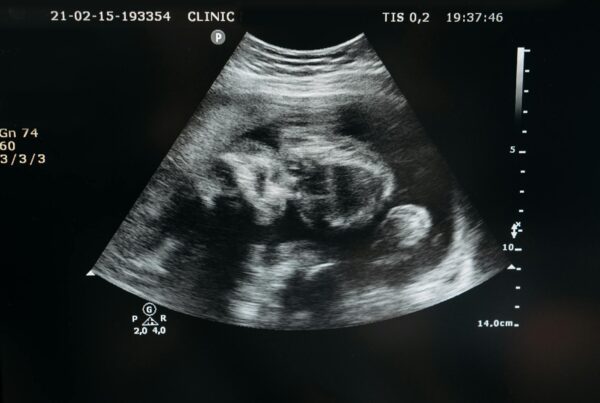
Um modelo preditivo baseado em radiômica de ressonância magnética e aprendizado de máquina é capaz de estimar a expressão de PD-L1 em pacientes com câncer de mama antes do início da imunoterapia. A informação foi apresentada na reunião da International Society for Magnetic Resonance in Medicine (ISMRM) de 2026 e dá continuidade a uma linha de pesquisa que vem maturando há cinco anos: usar a RM já realizada na rotina diagnóstica para extrair um biomarcador de imunoterapia, sem precisar de nova biópsia.
Por que a expressão de PD-L1 importa
PD-L1 é o ligante do receptor PD-1 nos linfócitos T. Quando o tumor superexpressa essa molécula, ele “esfria” a resposta imune local — e, ao mesmo tempo, vira um candidato ideal para inibidores de checkpoint imunológico como pembrolizumabe e atezolizumabe. No câncer de mama triplo-negativo (TNBC), essa decisão terapêutica é central: o ensaio KEYNOTE-522 estabeleceu o pembrolizumabe combinado à quimioterapia como padrão neoadjuvante para boa parte dessas pacientes, e o status de PD-L1 ajuda a refinar quem mais se beneficia. O problema clínico é prático: a leitura imuno-histoquímica do PD-L1 depende de fragmento adequado de tecido, varia entre patologistas e pode mudar entre pré e pós-tratamento.
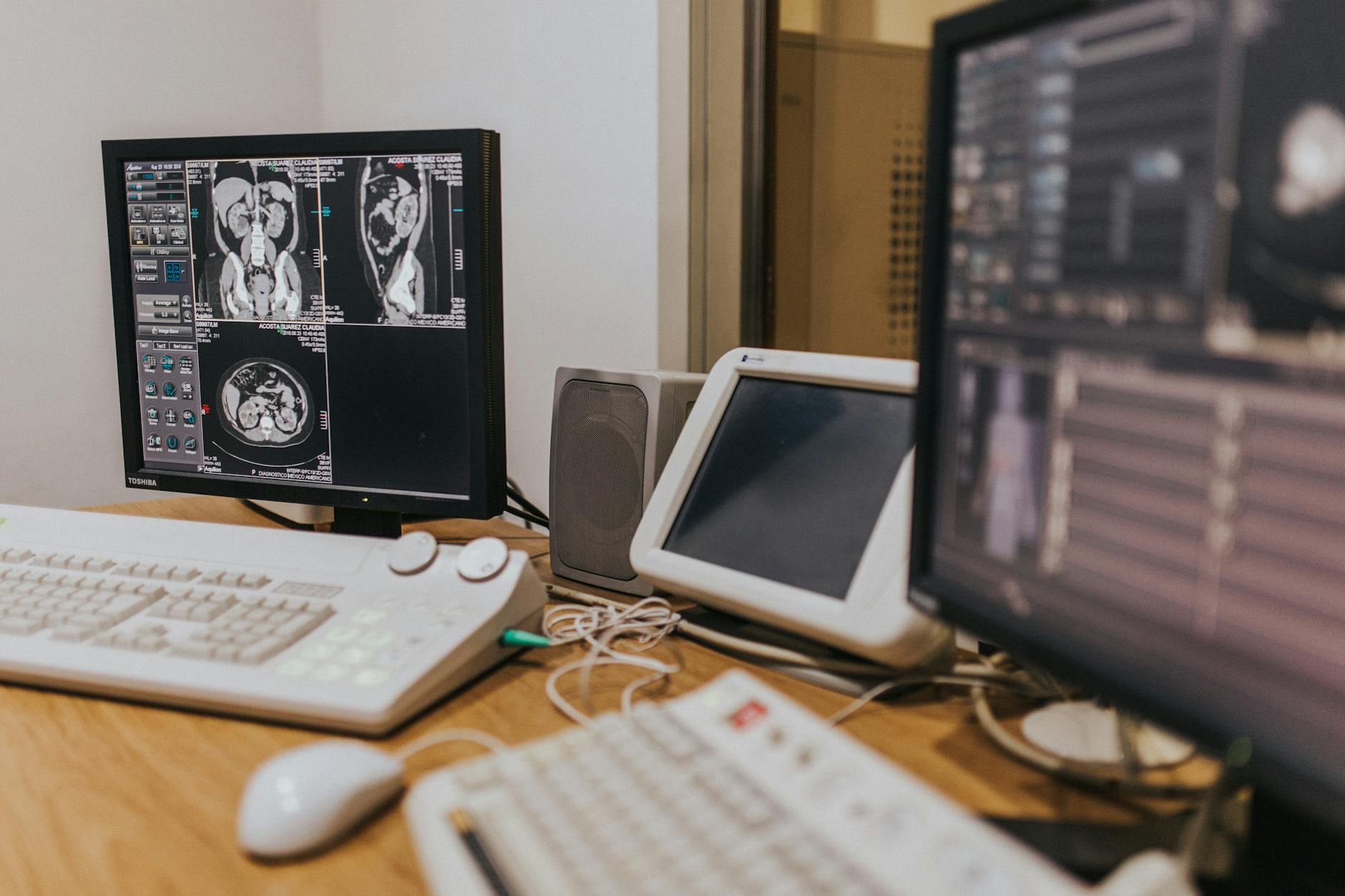
Como funciona a radiômica aplicada à mama
O pipeline apresentado na ISMRM segue a arquitetura clássica desse tipo de estudo. Primeiro, a lesão é segmentada na RM dinâmica com contraste (DCE-MRI), normalmente em 3D, abrangendo todas as fases pós-contraste. A partir dessa máscara, software dedicado extrai centenas de descritores: variância de primeira ordem, métricas de textura derivadas da matriz de co-ocorrência (GLCM) e da matriz de comprimentos de execução (GLRLM), além de descritores baseados em zonas de cinza (GLSZM). Esses números compõem um perfil quantitativo da heterogeneidade interna do tumor — algo que o olho humano não consegue medir com confiabilidade.
Em seguida, algoritmos de aprendizado de máquina (random forest, SVM, árvores de decisão, redes neurais leves) selecionam o subconjunto de descritores que melhor separa pacientes PD-L1 positivos dos negativos. A validação interna costuma utilizar cinco partições cruzadas, e os modelos mais maduros já são testados em coortes externas.
O que a literatura recente mostra
O resultado apresentado na ISMRM ecoa achados independentes. Um estudo do Memorial Sloan Kettering Cancer Center, publicado em Cancers em 2021, avaliou 62 mulheres com TNBC e construiu um modelo com apenas três descritores (variância de primeira ordem, variância de run length e ênfase de baixa intensidade em zonas grandes). O desempenho foi superior à leitura qualitativa do radiologista: 90,7% de sensibilidade, 85,1% de especificidade e 88,2% de acurácia diagnóstica. Importante: a avaliação BI-RADS clássica não mostrou associação significativa com o status de PD-L1, reforçando que a informação útil está em medidas que escapam à inspeção visual.
Em 2024, grupo da Universidade Sul da China levou a abordagem para o terreno multicêntrico. Cinco coortes foram analisadas, e os autores integraram RNA-seq de 1.089 pacientes do TCGA com 94 RMs do TCIA para construir uma assinatura radiômica capaz de estimar fenótipos do microambiente tumoral — incluindo subtipos imuno-inflamados versus imuno-desérticos. A análise validou o conceito em coorte independente e reforçou que o sinal radiômico não é artefato de um único centro.
Implicações para a prática clínica
O atrativo desse tipo de modelo é claro: estimar PD-L1 sem nova biópsia, em todo tumor primário, sem viés de amostra. Isso ajuda especialmente em três cenários — pacientes com tumores pequenos onde a biópsia retira a maior parte da lesão, casos com PD-L1 limítrofe (CPS 1-10) onde a discordância entre laboratórios é maior, e pacientes em monitoramento neoadjuvante, em que repetir biópsia para acompanhar a resposta imune é inviável. Vale lembrar que algoritmos de imagem já vêm superando radiologistas em outras tarefas oncológicas, e a tendência é integrar essas leituras ao laudo estruturado.
No Brasil e na América Latina, onde o acesso à imuno-histoquímica de PD-L1 ainda é heterogêneo, um biomarcador derivado de RM rotineira pode atuar como triagem antes do exame anatomopatológico mais oneroso — desde que validado em coortes locais. Plataformas comerciais de IA aplicada à mamografia já mostraram ganho de especificidade em rastreamento, e o desafio agora é replicar esse rigor de validação em pipelines de radiômica.
Limitações e próximos passos
O entusiasmo precisa ser temperado por questões metodológicas. Coortes ainda são pequenas, há variabilidade na intensidade do campo magnético e nos protocolos de aquisição, e modelos treinados em um scanner podem não funcionar em outro sem harmonização (ComBat, normalização de assinatura). Reproduzibilidade entre vendedores — Siemens, GE, Philips — segue como desafio aberto. Iniciativas que combinam RM em larga escala com IA têm pressionado a comunidade a publicar pipelines reproduzíveis e abrir códigos.
Outro ponto sensível é regulatório. Para virar prática clínica, um classificador de PD-L1 baseado em RM precisaria de validação prospectiva multicêntrica, comparação direta contra a imuno-histoquímica padrão e, eventualmente, autorização da Anvisa ou de agências internacionais. A apresentação da ISMRM 2026 marca, portanto, um passo importante — mas não o último — em direção a um biomarcador imageológico que poderia mudar o fluxo decisório em câncer de mama.
Fonte: AuntMinnie — ISMRM: Predictive model evaluates PD-L1 status in breast cancer (10/05/2026)