Las especificaciones técnicas de equipos de radioterapia en EBRT no son un detalle administrativo: determinan si la dosis calculada realmente se entrega con exactitud clínica. Un LINAC moderno, por sí solo, no garantiza seguridad. Lo que marca la diferencia es la integración entre dosimetría de referencia, dosimetría relativa y control de calidad durante todo el ciclo operativo.
Este artículo técnico convierte las Tablas 7 a 11 en una guía de implementación para físicos médicos, radioncólogos, ingenieros clínicos y responsables de servicio. El objetivo es operativo: pasar de “lista de equipos” a criterios verificables de compra, aceptación, calibración y uso sostenido.
En Este Artículo
Especificaciones técnicas de equipos de radioterapia en EBRT
Respuesta directa: la precisión en EBRT depende de una cadena metrológica completa, no de equipos aislados. Las Tablas 7-11 muestran que cámaras, electrómetros, fantomas, detectores y software deben funcionar como un sistema único con trazabilidad y reglas de QA explícitas.
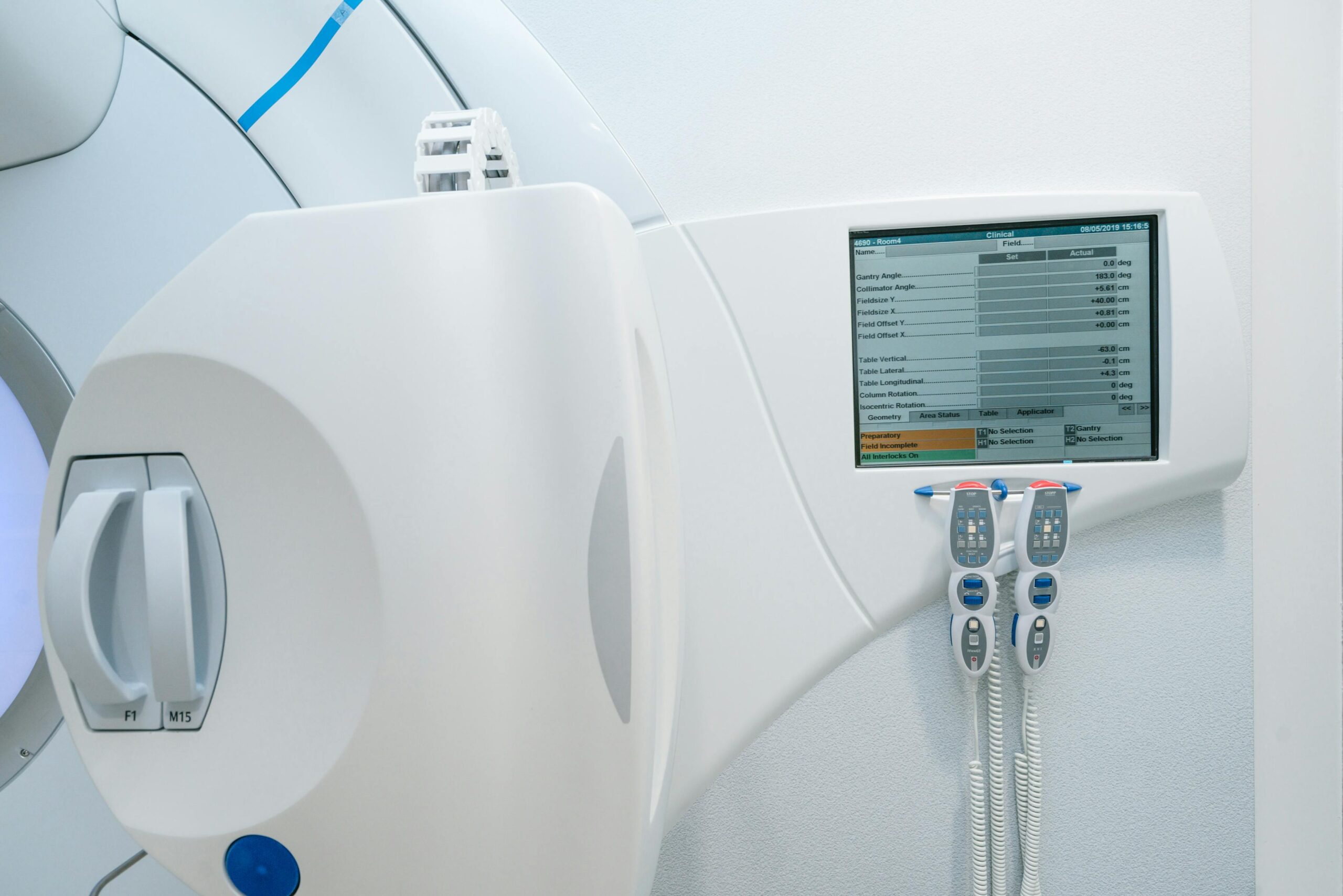
Normativamente, IEC 60731 e IEC 61674 establecen la base para dosímetros y detectores con calidad clínica. En la práctica, esto implica que la compra debe incluir desde el inicio: periodicidad de calibración, compatibilidad de conectores, exportación de datos al TPS y plan de mantenimiento preventivo con criterios documentados.
Una estructura útil para organizar decisiones técnicas es:
- Capa de referencia absoluta: anclaje de dosis absorbida con trazabilidad SSDL/PSDL.
- Capa de caracterización de haz: adquisición de PDD/perfiles para modelado del TPS.
- Capa de verificación clínica: controles in vivo y validaciones previas al tratamiento.
- Capa geométrica y de imagen: coherencia entre posicionamiento, imagen y entrega de dosis.
Para una visión integral del tema, revisa nuestro artículo principal sobre especificaciones de equipos de radioterapia.
Dosimetría de referencia (Tabla 7): base de toda decisión clínica
Sin referencia dosimétrica sólida, cualquier comparación posterior pierde valor. La Tabla 7 prioriza cámara tipo Farmer, cámara plano-paralela cuando hay electrones, electrómetros de clase adecuada, cables triaxiales confiables y correcciones ambientales con instrumentos calibrados.
La cámara Farmer (~0,6 cm3) sigue siendo estándar para referencia en fotones. En electrones, la plano-paralela (~0,4 cm3) mejora el desempeño en zonas superficiales y gradientes pronunciados. La recalibración cada dos años en SSDL/PSDL debe verse como mínimo regulatorio; ante incidentes de manipulación o lecturas atípicas, la verificación extraordinaria es obligatoria.
Una formulación útil de dosis absorbida en agua es:
$$D_{w,Q} = M_Q \cdot N_{D,w,Q_0} \cdot k_{Q,Q_0}$$
- $D_{w,Q}$: dosis absorbida en agua para calidad de haz $Q$ (Gy)
- $M_Q$: lectura corregida cámara-electrómetro
- $N_{D,w,Q_0}$: factor de calibración en calidad de referencia
- $k_{Q,Q_0}$: corrección por calidad de haz
La corrección de temperatura y presión debe aplicarse de forma sistemática:
$$k_{TP}=\frac{273{,}15 + T}{293{,}15}\cdot\frac{101{,}325}{P}$$
donde $T$ está en $^\circ$C y $P$ en kPa. Con $T=24^\circ$C y $P=98{,}0$ kPa, se obtiene $k_{TP}\approx1{,}047$; omitir esta corrección introduce sesgo clínicamente relevante.
Dos detalles operativos con impacto real:
- Los cables triaxiales fallan por uso repetido; contar con repuesto validado evita interrupciones.
- El desecante del electrómetro requiere recambio periódico; la humedad afecta estabilidad de lectura.
Dosimetría relativa y comisionamiento (Tabla 8)
En comisionamiento, la calidad de datos importa más que la velocidad de adquisición. La Tabla 8 exige tanque 3D con precisión de posicionamiento, control electrométrico sensible y software capaz de transferir datos al TPS sin pérdida de integridad.
Dimensiones de barrido hasta 480 x 480 x 400 mm3, exactitud/repetibilidad de ±0,1 mm, polarización de 50-400 V y fuga <250 fA son criterios coherentes con modelado de IMRT/VMAT. También es crítico definir por contrato qué formatos exporta el software y cómo se conserva la trazabilidad entre adquisición, análisis e importación al TPS.
Para electrones y regiones de alto gradiente, una cámara plano-paralela de pequeño volumen (~0,05 cm3) y conjuntos de diodos entregan información complementaria. El film radiocrómico aporta alta resolución espacial en verificaciones complejas, aunque exige flujo de calibración y análisis más riguroso.
Un enfoque práctico combina:
- Tanque 3D como fuente primaria de datos de haz.
- Cámara thimble para consistencia global de curvas y perfiles.
- Diodos para campos pequeños y gradientes fuertes.
- Film para confirmación espacial fina en casos seleccionados.
Equipamiento de control de calidad (Tabla 9): sostener rendimiento en el tiempo
La Tabla 9 conecta física médica con operación diaria. Incluye medidor de constancia, fantomas de alineación del LINAC y láseres, fantoma de densidad electrónica para CT y fantomas de calidad de imagen para EPID, kV planar y kV volumétrico.
El medidor diario debe almacenar tendencias, permitir límites de tolerancia y disparar alertas fuera de rango. Si solo entrega lectura instantánea, el servicio pierde capacidad de anticipar deriva y termina respondiendo tarde.
Una métrica sencilla para seguimiento es:
$$\Delta(\%) = \frac{X_{\text{hoy}}-X_{\text{baseline}}}{X_{\text{baseline}}}\times 100$$
donde $X$ puede ser salida, simetría u otro parámetro crítico. El valor práctico está en asociar esta métrica a umbrales de acción y responsables claramente definidos.
Este nivel de disciplina reduce paradas no planificadas, reprocesos y tensión operativa en agendas de tratamiento exigentes.
Dosimetría in vivo y dosimetría de soporte en radiología (Tablas 10 y 11)
La dosimetría in vivo agrega verificación independiente de seguridad clínica. En EBRT, los diodos para entrada en fotones (6-15 MV), electrones (6-18 MeV), superficie y fuera de campo son útiles cuando se calibran considerando dependencia de energía, tasa de dosis y temperatura.
La Tabla 11 amplía el alcance con instrumentación para rayos X diagnósticos y CT (cámara en kV, medidor de kVp, cámara lápiz y fantoma CTDI). Esto es clave porque la calidad de imagen impacta directamente en posicionamiento, verificación y planificación.
Si te interesa reforzar redundancia de verificación en radioterapia, también puede ayudarte nuestro artículo sobre especificaciones de LINAC para EBRT.
Comparación técnica: precisión, productividad y costo operativo
No existe una sola tecnología óptima para todos los escenarios. La selección debe responder al contexto clínico y al presupuesto de incertidumbre permitido.
| Tecnología | Fortaleza principal | Limitación clave | Uso típico en EBRT |
|---|---|---|---|
| Cámara Farmer | Robustez metrológica y trazabilidad | Resolución espacial limitada en gradientes altos | Referencia absoluta y línea base |
| Cámara plano-paralela | Buen desempeño en electrones | Requiere estrategia de calibración rigurosa | Referencia/relativa en electrones |
| Diodos | Lectura rápida y buena resolución local | Dependencia de energía y tasa de dosis | Campos pequeños e in vivo |
| Film radiocrómico | Alta resolución 2D | Mayor carga de calibración y análisis | Validación de campos complejos |
| Array 2D | Alta productividad para IMRT/VMAT | Resolución limitada por separación de detectores | QA pretratamiento y tendencias |
Microcaso: comisionamiento de un LINAC de 10 MV
Un centro inicia comisionamiento de fotones 6 MV y 10 MV. Define línea base de salida absoluta con cámara de referencia y electrómetro, y adquiere PDD/perfiles en tanque 3D para modelado del TPS. En la segunda semana, la constancia diaria muestra +1,6% respecto al baseline.
Tras revisar tendencia y recalcular $k_{TP}$, se identifica efecto combinado de presión atmosférica y condición ambiental de sala. Al repetir mediciones bajo control metrológico, la desviación baja a +0,3%, dentro del umbral de acción del servicio.
Para un campo modulado con gradiente acentuado, el equipo compara array 2D y film. El array acelera la liberación rutinaria; el film confirma zonas críticas cercanas a límites de órgano en riesgo. Con esto, se adopta un flujo híbrido basado en riesgo clínico.
Errores frecuentes, limitaciones y cuándo no simplificar
Los fallos más comunes no provienen de “falta de equipos”, sino de procesos inconsistentes. Tres errores recurrentes:
- Error 1: medir bien y documentar mal. Sin trazabilidad, no hay auditoría ni aprendizaje de tendencia.
- Error 2: gestión deficiente de cables y conectores. Intercambios no controlados alteran lecturas.
- Error 3: usar un solo detector para todos los escenarios. Aumenta puntos ciegos.
Limitaciones prácticas que conviene explicitar:
- No basar decisiones complejas solo en un array cuando hay gradientes extremos.
- No usar cámaras de mayor volumen en campos pequeños donde el promediado volumétrico distorsiona resultados.
- No corregir clínicamente tras una única lectura fuera de rango sin revisar estado ambiental e instrumental.
¿Cuándo no conviene una estrategia simplificada? En planes de alta complejidad, campos pequeños, restricciones estrictas de OAR o situaciones donde la acumulación de incertidumbre puede afectar la confianza clínica.
Checklist de implementación para compra y operación
- Definir por contrato alcance y periodicidad de calibración SSDL/PSDL.
- Exigir compatibilidad documentada de exportación al TPS.
- Establecer matriz de tolerancias y acciones con responsables.
- Estandarizar identificación/manipulación de cables y accesorios.
- Mantener plan de contingencia ante falla de detector o electrómetro.
- Integrar QA de imagen dentro de la gobernanza de QA de dosis.
Qué auditar en los primeros 90 días
Tras la implementación, el control más útil no es revisar inventario, sino verificar desempeño clínico real. En los primeros 90 días conviene auditar si los datos diarios permiten tomar decisiones con confianza: tendencias estables, trazabilidad completa y respuesta documentada ante desvíos.
Una auditoría breve pero rigurosa debe confirmar: estabilidad de constancia diaria, repetibilidad de la cadena de referencia tras manipulación rutinaria y coherencia entre el modelo del TPS y las mediciones de verificación. Cuando aparece discordancia, con frecuencia el problema está en el proceso (etiquetado, flujo de datos o responsabilidades), no solo en el hardware.
- Validar que baseline, tolerancias y niveles de acción estén versionados y aprobados.
- Cuantificar variabilidad intraoperador e interoperator mediante repeticiones planificadas.
- Confirmar cierre documental de eventos fuera de tolerancia con acciones correctivas.
- Comprobar acceso inmediato a certificados de calibración y mapeo de detectores.
Para seguir profundizando en la serie técnica, revisa el artículo de estructura general, luego la definición de paquetes de equipamiento y también las especificaciones del simulador CT en EBRT.
Conclusión: la precisión clínica en EBRT es el resultado de ingeniería de sistema, disciplina metrológica y decisiones técnicas bien documentadas. Usa este artículo como referencia operativa y vuelve al artículo principal de especificaciones técnicas para una visión completa.

