Câncer de tireoide e radioterapia externa — o delineamento de volumes-alvo é um dos pilares do planejamento radioterápico para tumores tireoidianos que exigem irradiação. Carcinomas anaplásicos irressecáveis, recorrências locais pós-cirúrgicas com margens comprometidas e doença pouco diferenciada refratária ao iodo radioativo representam os cenários mais frequentes em que a radioterapia conformacional com modulação de intensidade (IMRT) assume papel central. Este artigo detalha os princípios de planejamento, os volumes prescritos e cinco casos clínicos reais extraídos do livro de referência. Para uma visão mais ampla de todos os sítios anatômicos, confira nosso guia completo sobre delineamento de volume alvo e configuração de campos.
Princípios de Planejamento e Avaliação por Imagem
O primeiro passo antes de qualquer delineamento é garantir um estadiamento por imagem adequado. Exame físico minucioso, ultrassonografia cervical e ressonância magnética ajudam a detectar linfadenopatias e extensão extratireoidiana que a tomografia isolada pode subestimar. Um ponto operacionalmente crítico: o uso de contraste iodado na TC de simulação deve ser evitado quando o paciente ainda poderá receber iodo radioativo, pois a sobrecarga de iodo estável pode interferir na captação por até 6 meses. Quando o contraste for clinicamente indispensável, a decisão precisa estar formalmente justificada antes da administração.
Carcinomas pouco diferenciados ou anaplásicos fogem do padrão dos tumores tireoidianos bem diferenciados: eles podem ser ávidos por FDG no PET-CT, oferecendo informação complementar relevante para definir o GTV. Já papilares e foliculares bem diferenciados raramente captam FDG de forma significativa. Essa distinção tem implicação prática direta: se o subtipo histológico sugere avidez por FDG, o PET-CT agrega informação real ao planejamento; caso contrário, seu valor é limitado.
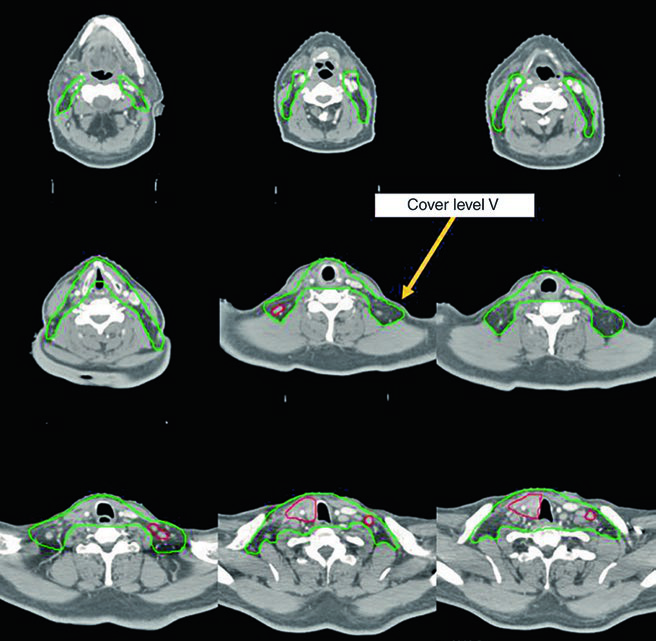
A imobilização deve incluir máscara termoplástica cobrindo cabeça, pescoço e ombros — não apenas cabeça e pescoço. A cabeça deve ficar levemente estendida para afastar a cavidade oral do campo e reduzir dose à mucosa oral. Esse detalhe aparentemente simples muda significativamente a distribuição de dose no palato e na língua, e muitas vezes é a diferença entre uma mucosite grau 2 e uma grau 3 no final do tratamento.
A prescrição de dose segue dois patamares principais: 66–70 Gy para doença macroscópica ou leito tumoral com margens positivas, e 54–63 Gy para regiões subclínicas de risco. O tratamento pode ser entregue em 30–35 frações, com dose por fração de 1,8 a 2 Gy por CTV, usando plano IMRT com dose-painting simultâneo ou, alternativamente, um curso inicial seguido de boost sequencial. A escolha entre dose-painting e boost sequencial depende da experiência da equipe e das restrições de dose nos órgãos de risco adjacentes.
Volumes-Alvo para Doença Macroscópica (66–70 Gy)
A definição de GTV e CTV para doença macroscópica segue critérios bem estabelecidos. O GTV inclui toda doença identificável ao exame físico e por imagem: massa primária residual ou recorrente e linfonodos cervicais com diâmetro ≥ 1 cm ou com centro necrótico. A tabela a seguir resume as definições recomendadas pelo livro de referência.
Volumes-alvo sugeridos para doença macroscópica
| Volume | Definição e Descrição |
|---|---|
| GTV66–70 | Primário: toda doença macroscópica ao exame físico e imagem. Linfonodos cervicais: todos os nódulos ≥ 1 cm ou com centro necrótico. |
| CTV66–70 | Geralmente idêntico ao GTV66–70. Se necessário margem por incerteza na extensão da doença macroscópica, adicionar 3–5 mm (GTV + 3–5 mm = CTV). Quando adjacente à medula espinhal: margem de 1 mm é aceitável, pois a proteção medular é prioritária. Para linfonodos suspeitos pequenos (< 1 cm): considerar dose de 66 Gy (CTV66). |
| PTV66–70 | CTV66–70 + 3–5 mm conforme variabilidade do posicionamento diário. Quando adjacente à medula espinhal: margem de 1 mm é aceitável. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 9.1). Dose sugerida para doença macroscópica: 70 Gy. Quando houver risco de toxicidade ao plexo braquial, laringe, medula espinhal, pulmão ou esôfago, 66 Gy pode ser considerado. No cenário pós-operatório com ressecção macroscópica mas margem(ns) positiva(s) significativa(s), o leito tumoral ou região de preocupação pode receber 66 Gy.
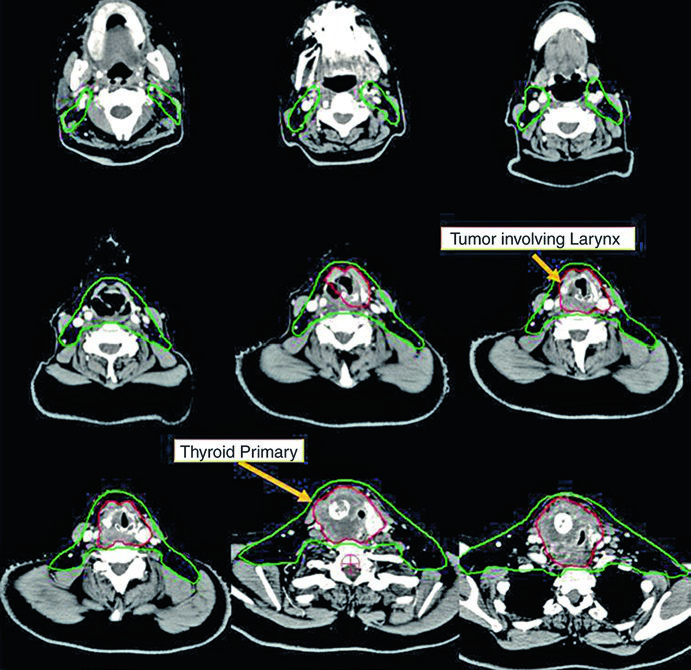
Na prática, a decisão entre 70 Gy e 66 Gy depende da proximidade com estruturas críticas e do balanço risco-benefício para cada paciente individual. Um tumor volumoso aderido à traqueia anterior pode receber 70 Gy sem maiores riscos, mas quando o GTV encosta na medula espinhal a apenas alguns milímetros, reduzir para 66 Gy e aceitar margem de CTV de 1 mm passa a ser a opção mais prudente. A proteção medular não é negociável — uma mielopatia actínica é irreversível e devastadora.
Linfonodos suspeitos com diâmetro inferior a 1 cm representam um dilema clínico frequente. Nesses casos, uma dose intermediária de 66 Gy pode ser suficiente: alta o bastante para esterilizar doença microscópica, mas com menor risco de toxicidade ao tecido adjacente. A seleção dessas lesões menores exige correlação cuidadosa entre exame físico, ultrassonografia e achados na TC de simulação.
Volumes-Alvo para Região Subclínica de Risco (54–63 Gy)
O CTV subclínico abrange as regiões com risco de doença microscópica, mesmo sem evidência macroscópica. A definição varia conforme o cenário clínico — definitivo ou pós-operatório — e exige atenção a detalhes anatômicos específicos da tireoide.
Volumes-alvo sugeridos para região subclínica
| Volume | Definição e Descrição |
|---|---|
| CTV54–63 (Primário) | Deve incluir o sulco traqueoesofágico e margem > 5 mm ao redor de qualquer CTV66–70. No cenário pós-operatório: englobar leito tumoral e sulco traqueoesofágico do(s) lado(s) envolvido(s). Se traqueostomia realizada: incluir o estoma até a superfície cutânea. Idealmente, excluir laringe alta (pregas vocais/aritenoides e acima) e esôfago posterior, quando não adjacentes ao tumor ou ao leito tumoral. |
| CTV54–63 (Pescoço lateral) | Incluir níveis cervicais bilaterais II–VII. A cobertura do pescoço lateral pode ser omitida quando se irradia o compartimento central e o mediastino superior até o nível da carina. Níveis I e retrofaríngeos são geralmente omitidos, a menos que estejam em risco. |
| PTV54–63 | CTV54–63 + 3–5 mm. Quando adjacente à medula espinhal: 1 mm aceitável. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 9.2). Dose subclínica sugerida: 60–63 Gy. Regiões nodais não envolvidas podem ser classificadas como baixo risco subclínico e tratadas com 54 Gy, a critério do médico.
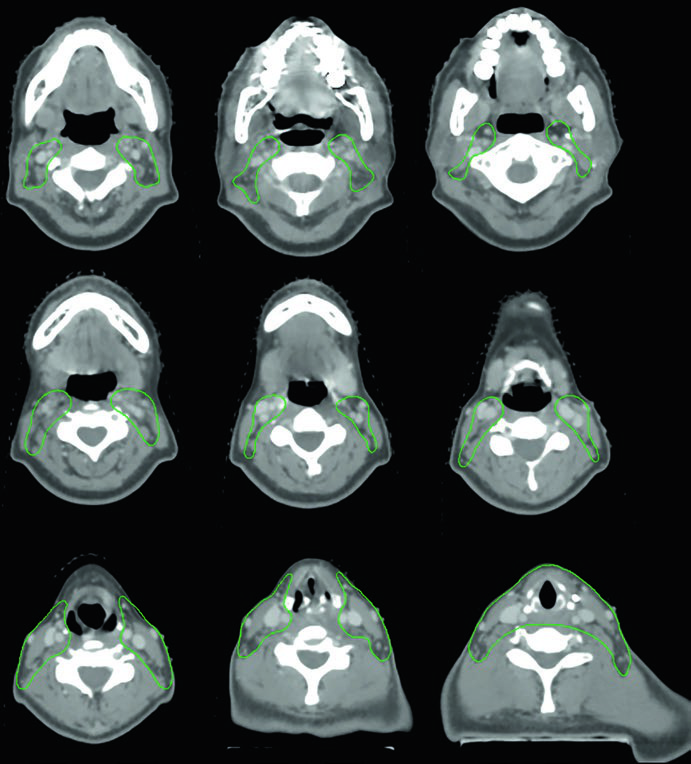
O sulco traqueoesofágico merece atenção especial: essa região é o sítio mais frequente de recorrência local no câncer de tireoide, e seu delineamento inadequado compromete todo o tratamento. No cenário pós-operatório, é fundamental verificar se houve traqueostomia — quando presente, o estoma precisa ser incluído até a superfície da pele, pois representa via de disseminação potencial para implantes cutâneos.
A exclusão da laringe alta e do esôfago posterior, quando possível, reduz significativamente a toxicidade de deglutição e preserva a voz. Porém, se o tumor primário ou o leito cirúrgico for adjacente a essas estruturas, a exclusão não se aplica e a cobertura completa é obrigatória. A tentativa de poupar essas estruturas às custas da cobertura oncológica não é aceitável.
O nível I e os linfonodos retrofaríngeos são geralmente omitidos no câncer de tireoide. Essa é uma diferença importante em relação a outros tumores de cabeça e pescoço, como o carcinoma de nasofaringe, onde a cobertura retrofaríngea é mandatória. No câncer tireoidiano, o padrão de disseminação linfática favorece os níveis centrais (VI–VII) e laterais (II–V), tornando a inclusão de nível I e retrofaríngeos desnecessária na maioria dos casos.
Cenários Clínicos: Doença Irressecável e Quimiorradioterapia Definitiva
Dois dos cinco casos ilustrativos do livro de referência demonstram o manejo de doença irressecável tratada com quimiorradioterapia definitiva. Ambos receberam plano IMRT com dose-painting simultâneo.
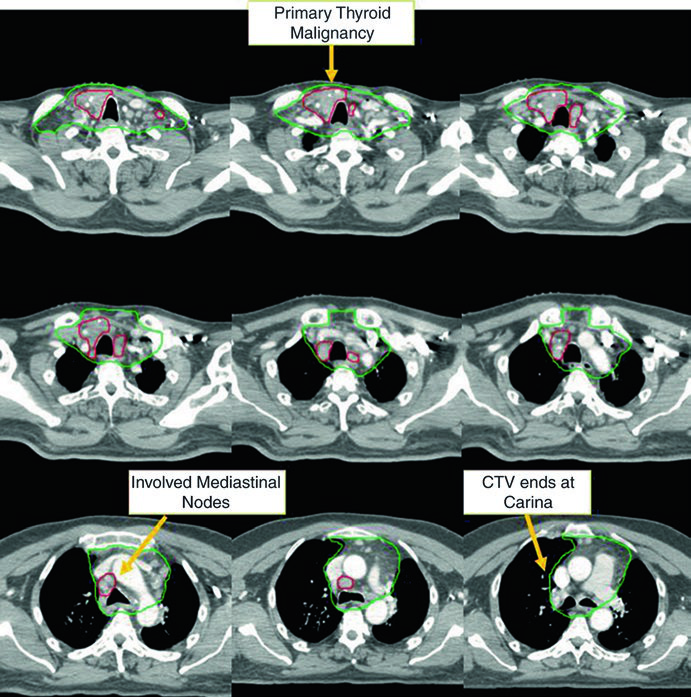
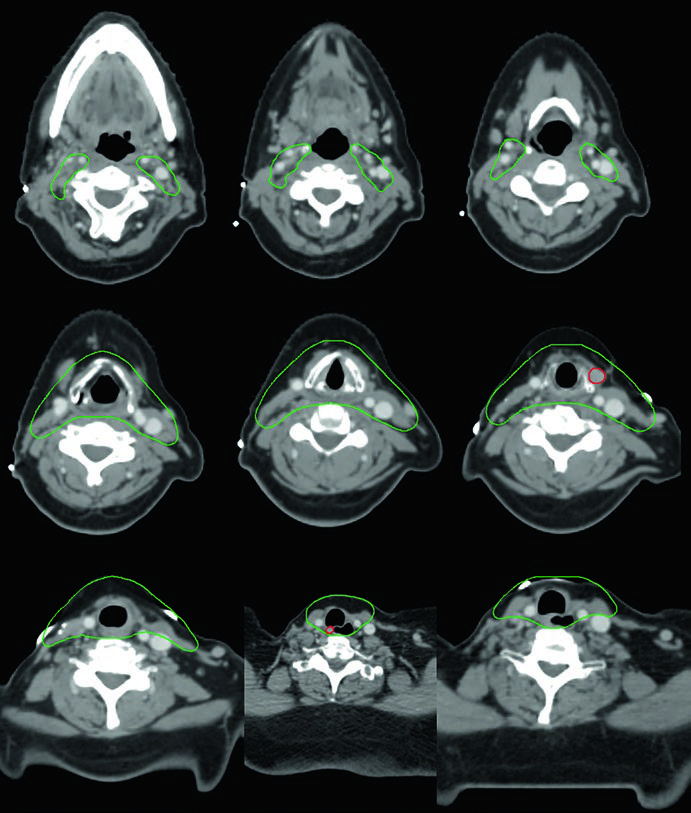
Caso 1 — Carcinoma papilar metastático (Fig. 9.1): Homem de 58 anos com carcinoma papilar metastático de tireoide, submetido a múltiplas ressecções prévias, que se apresentou com recorrência local irressecável e múltiplos linfonodos mediastinais. Recebeu quimiorradioterapia definitiva para prevenir progressão local. O CTV70 Gy (vermelho) abrange a recorrência local e linfonodos mediastinais envolvidos, enquanto o CTV60 Gy (verde) cobre as regiões subclínicas de risco. Este caso exemplifica o cenário de doença recorrente que esgotou as opções cirúrgicas — a radioterapia com dose definitiva é a melhor alternativa para controle local.
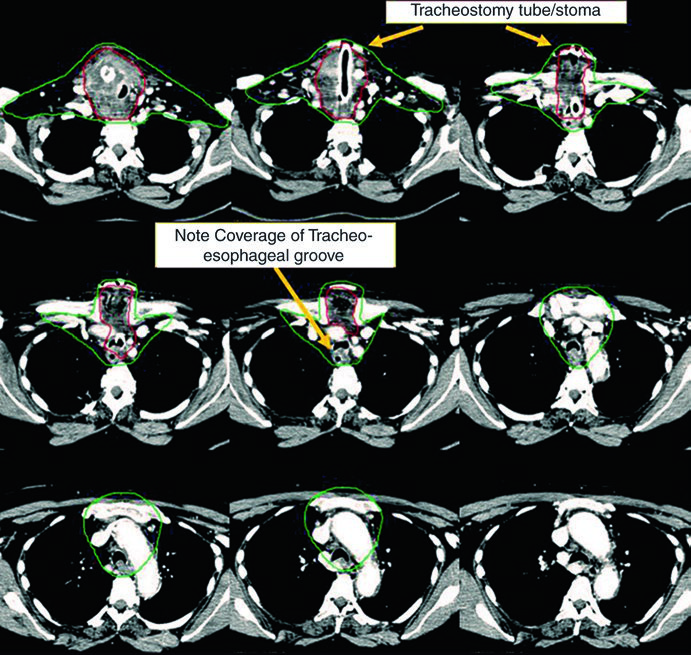
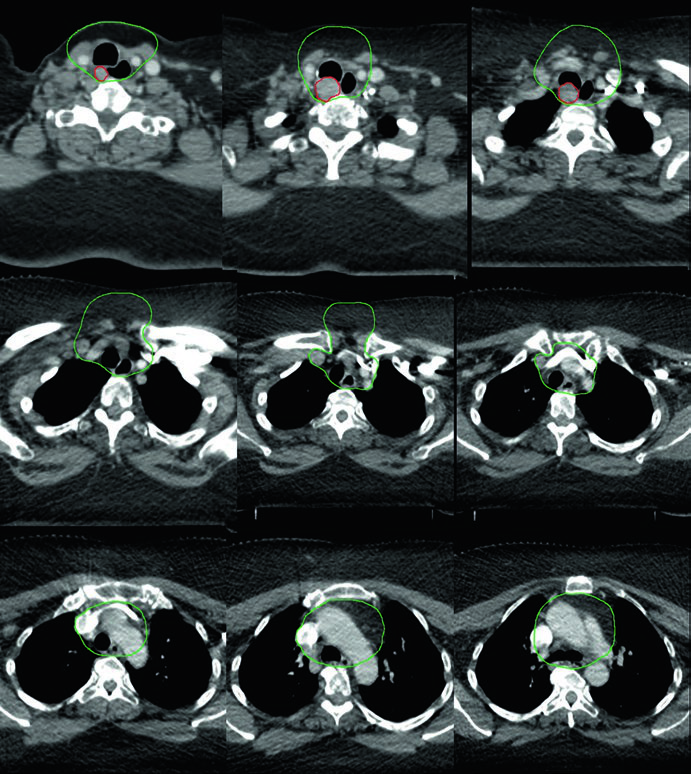
Caso 2 — Carcinoma anaplásico irressecável (Fig. 9.2): Mulher de 73 anos com carcinoma anaplásico de tireoide invadindo laringe, traqueia e esôfago. Recebeu quimiorradioterapia definitiva com doxorrubicina concomitante. O CTV70 Gy (vermelho) engloba toda a doença volumosa, e o CTV60 Gy (verde) abrange o risco subclínico. Detalhe importante: o manúbrio, que normalmente não é incluído no volume de risco, foi englobado neste caso específico por conta da doença volumosa anterior agressiva no pescoço. Essa decisão é atípica e deve ser individualizada — não se trata de protocolo, mas de resposta a uma apresentação clínica particular.
Esses dois casos ilustram a versatilidade da IMRT com dose-painting: o plano entrega simultaneamente 70 Gy ao volume de alto risco e 60 Gy ao volume subclínico, sem necessidade de boost sequencial. A escolha de doxorrubicina como quimioterápico concomitante no anaplásico reflete a agressividade dessa histologia e a necessidade de sensibilização ao tratamento, embora as opções sistêmicas tenham evoluído significativamente nos últimos anos.
Radioterapia Pós-Operatória e Margens Comprometidas
O cenário pós-operatório no câncer de tireoide exige atenção redobrada ao leito cirúrgico, especialmente quando há extensão extratireoidiana ou margens positivas. Clips cirúrgicos orientam o delineamento do leito e devem ser sistematicamente identificados em cada corte da TC.
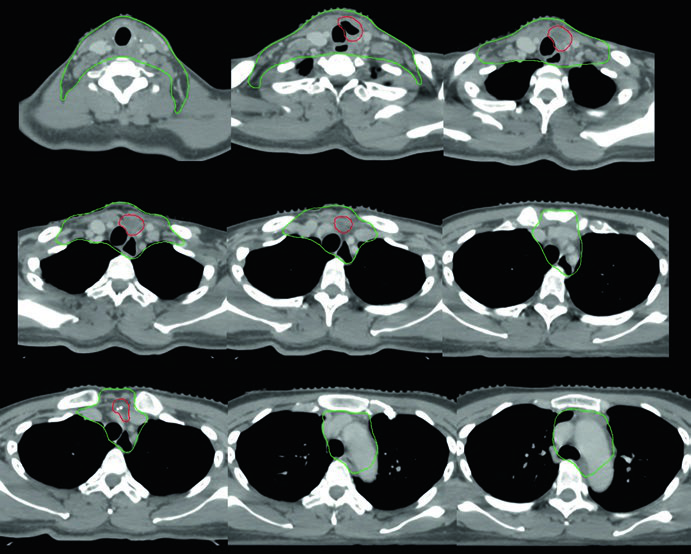
Caso 3 — Anaplásico pós-operatório (Fig. 9.3): Mulher de 50 anos com carcinoma anaplásico submetida a ressecção com extensão extratireoidiana e margens positivas, sem linfonodos envolvidos. Recebeu quimiorradiação pós-operatória. O CTV70 Gy (vermelho) inclui o leito tumoral e os clips cirúrgicos, enquanto o CTV60 Gy (verde) cobre o risco subclínico do compartimento central. A ausência de linfonodos positivos não elimina a necessidade de irradiação subclínica nesse subtipo histológico agressivo — o anaplásico tem taxa de recorrência local e a distância significativamente maior que os diferenciados.
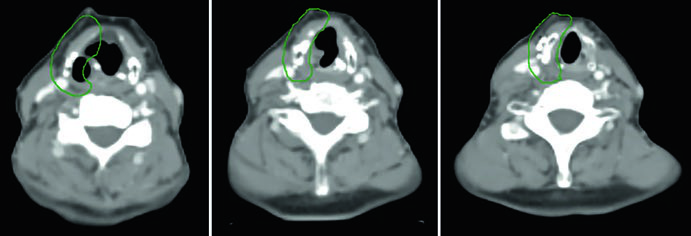
Caso 4 — Recorrência multifocal de variante de células altas (Fig. 9.4): Mulher de 61 anos com variante de células altas do carcinoma papilar, submetida a três cirurgias prévias, que se apresentou com recorrência multifocal. Foi tratada com quimiorradioterapia definitiva. O GTV70 Gy (vermelho) demarca cada foco de recorrência, e o CTV60 Gy (verde) cobre o pescoço subclínico em risco. A variante de células altas é reconhecidamente mais agressiva que a variante papilar clássica, com maior propensão a recorrência e comportamento biologicamente mais adverso.
Quando há recorrência multifocal após múltiplas cirurgias, o campo cirúrgico se torna hostil — fibrose extensa, distorção anatômica e risco aumentado de lesão nervosa tornam nova ressecção proibitivamente arriscada. A quimiorradioterapia definitiva com IMRT permite entregar 70 Gy a cada foco individualmente, com gradiente de dose favorável para os tecidos adjacentes. Cada foco de recorrência exige seu próprio GTV delineado, e o plano precisa acomodar múltiplos alvos de alta dose simultaneamente.
Doença Pouco Diferenciada e Omissão do Pescoço Lateral
Nem todos os casos exigem irradiação bilateral do pescoço lateral. O último caso do capítulo demonstra um cenário em que a omissão do pescoço lateral foi deliberada e clinicamente justificada, ilustrando o princípio de individualização baseada no padrão de recorrência do paciente.
Caso 5 — Câncer pouco diferenciado, fenótipo folicular (Fig. 9.5): Mulher de 69 anos com câncer de tireoide pouco diferenciado de fenótipo folicular, aderido a traqueia e esôfago, submetida a ressecção e iodo radioativo, que recorreu com massa paratraqueal direita invadindo a traqueia. Após nova ressecção e esvaziamento cervical, recebeu quimiorradiação adjuvante. O CTV60 Gy (verde) cobre o compartimento central e o mediastino superior. O tratamento do pescoço lateral foi omitido, dada a alta probabilidade de recorrência no compartimento central — a dose e o risco foram priorizados onde o benefício clínico era máximo.
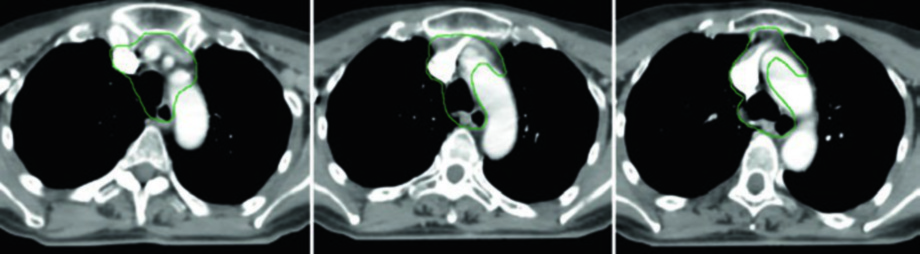
A decisão de omitir o pescoço lateral não é trivial. Ela pressupõe que o risco de recorrência lateral é suficientemente baixo para que a redução de toxicidade justifique a ausência de cobertura. No cenário deste caso — doença central recorrente com esvaziamento cervical recente e sem linfonodos laterais comprometidos — a omissão é razoável e alinhada com o princípio de individualização do tratamento. Omitir o pescoço lateral reduz significativamente o volume irradiado, com benefício direto na preservação da função de deglutição e redução de xerostomia.
Considerações Práticas de Planejamento
O planejamento IMRT para câncer de tireoide exige delineamento slice a slice de todos os volumes — GTV e CTV — em cada corte da TC de planejamento. A seleção acurada do CTV para doença macroscópica (CTV66–70) e para a região subclínica (CTV54–63) é crítica para o resultado terapêutico. O tratamento pode ser entregue como plano all-in-one com dose-painting simultâneo em 30–35 frações ou como curso inicial seguido de boost.
Quando a dose de 70 Gy gera preocupação com toxicidade ao plexo braquial, laringe, medula espinhal, pulmão ou esôfago, a redução para 66 Gy é justificável. No cenário pós-operatório com ressecção macroscópica mas margem positiva significativa, o leito tumoral ou a região de preocupação pode receber 66 Gy em vez de 70 Gy, equilibrando controle local e preservação funcional. Essa flexibilidade entre 66 e 70 Gy não é fraqueza do protocolo — é reconhecimento de que a dose ótima varia conforme a relação espacial entre o alvo e os órgãos de risco em cada caso.
As regiões nodais não envolvidas classificadas como baixo risco subclínico podem ser tratadas com 54 Gy, a critério do médico responsável. Essa flexibilidade permite poupar tecido normal adjacente sem comprometer a cobertura oncológica quando a probabilidade de doença oculta naquela região específica é limitada. Na prática, a decisão de tratar com 54 Gy versus 60 Gy depende da carga de doença original, da extensão do esvaziamento cervical e da agressividade histológica do tumor.
Para um panorama completo dos princípios de delineamento em todos os sítios anatômicos da oncologia radioterápica, confira nosso guia completo sobre delineamento de volume alvo e configuração de campos.