Delineamento de volumes-alvo em tumores cerebrais pediátricos
A radioterapia pediátrica do sistema nervoso central exige precisão milimétrica e compreensão profunda das particularidades anatômicas e biológicas de cada tumor. Meduloblastoma, ependimoma e germinoma puro representam as três entidades mais frequentes nesse contexto, e cada uma demanda estratégias de delineamento distintas. O planejamento volumétrico baseado em tomografia computadorizada é obrigatório independentemente da técnica — seja radioterapia conformacional 3D, IMRT, VMAT ou prótons.
Para uma visão abrangente de todos os sítios anatômicos, consulte nosso guia completo sobre delineamento de volume alvo na radioterapia.
Meduloblastoma: estadiamento e simulação
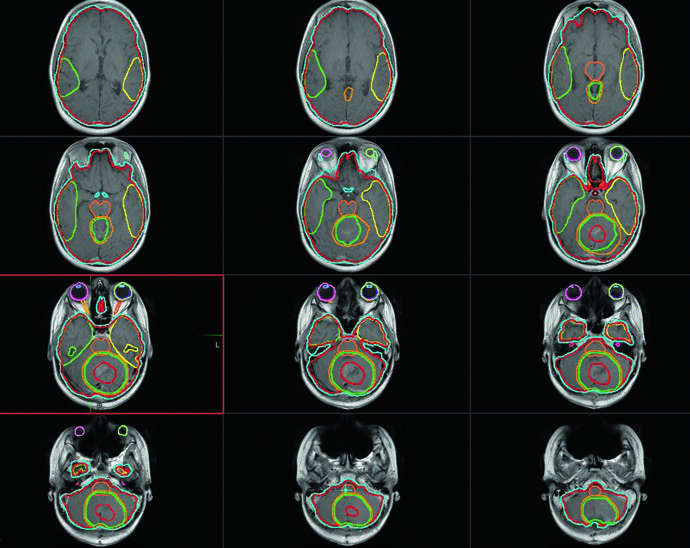
O estadiamento completo é o ponto de partida para definir dose e volume. Todo paciente precisa de RM encefálica com contraste em cortes finos de 1 a 3 mm — tanto no pré quanto no pós-operatório — além de RM de coluna com contraste e análise de líquor cefalorraquidiano. Pacientes com citologia positiva, metástase macroscópica ou resíduo tumoral igual ou superior a 1,5 cm² na RM pós-operatória são classificados como alto risco. Aqueles com doença M0 e resíduo inferior a 1,5 cm² entram no grupo de risco padrão.
A simulação por TC deve ser realizada de forma reprodutível, com ou sem anestesia. A imobilização consiste tipicamente em VacLok ou alpha cradle de corpo inteiro combinado com máscara craniana. Marcações múltiplas servem tanto para triangulação quanto para alinhamento longitudinal espinal. O scan deve capturar desde o topo do crânio até as gônadas.
Um ponto que merece atenção: a conversa entre o radio-oncologista e o anestesista sobre o tipo de via aérea é fundamental. Se a criança começa intubada mas vai migrar para máscara laríngea ou cânula nasal, inserir uma cânula oral durante a confecção da máscara garante posição reprodutível do queixo e evita necessidade de re-simulação.
Volumes-alvo para irradiação cranioespinal no meduloblastoma
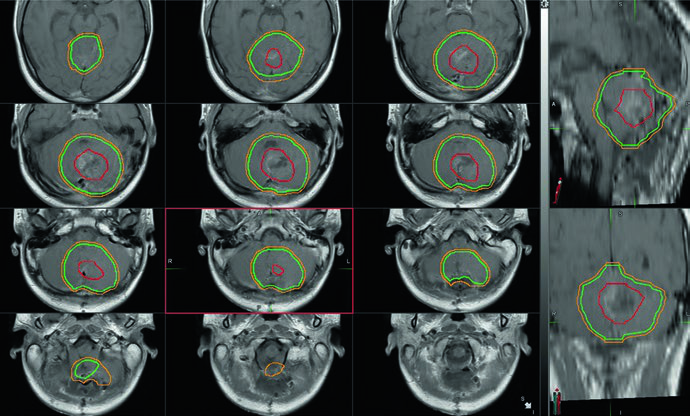
O delineamento precisa acontecer fatia por fatia na TC de planejamento. A tabela abaixo resume as definições recomendadas para o eixo cranioespinal.
Volumes recomendados para irradiação cranioespinal (CSI)
| Volume | Definição |
|---|---|
| GTV | Leito tumoral incluindo toda doença residual macroscópica e paredes da cavidade de ressecção na RM, além de áreas de preocupação indicadas pelo neurocirurgião. Defeitos cirúrgicos causados pelo trajeto de acesso não integram o GTV. |
| CTVCSI | Todo o volume contido pela dura-máter em contato com o líquor, incluindo pseudomeningocele pós-operatória. Em criança em crescimento, inclui o corpo vertebral inteiro e o canal; em indivíduo adulto, apenas o canal. |
| PTVCSI | CTVCSI + 3 a 10 mm conforme confiança no posicionamento diário e experiência institucional. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.1)
Volumes recomendados para o boost do leito tumoral
| Volume | Definição |
|---|---|
| GTV | Leito tumoral com doença residual macroscópica e paredes da cavidade na RM, mais áreas sinalizadas pelo neurocirurgião. |
| CTVboost | GTV + 1 a 1,5 cm de margem anatômica confinada. Excluir barreiras de disseminação como o tentório. Limitar margem no tronco cerebral a 2–3 mm nas áreas de contato tumoral. |
| PTVboost | CTVboost + 3 a 5 mm conforme imagem diária e experiência institucional. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.2)
Doses e estratificação por risco no meduloblastoma
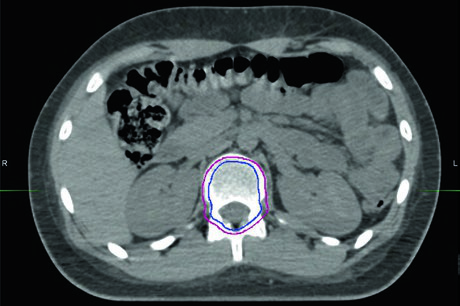
O braço de 18 Gy do estudo ACNS0331 do Children’s Oncology Group apresentou aumento de falhas, e 23,4 Gy para o eixo cranioespinal permanece como padrão para risco padrão. O mesmo estudo demonstrou equivalência do boost de campo envolvido em relação à irradiação de toda a fossa posterior nesses pacientes. A recomendação é portanto 23,4 Gy cranioespinal seguido de boost de campo envolvido até 54 Gy.
Para doença de alto risco ou pacientes sem condição para quimioterapia (como alguns adultos), a dose cranioespinal sobe para 36 Gy com boost até 54 Gy. Séries retrospectivas sustentam o boost de leito tumoral nesses casos sem excesso de falhas fora do leito, embora não haja ensaios randomizados.
Na terapia com prótons em criança em crescimento, há recomendação de tratar o corpo vertebral inteiro até 30 Gy quando a CSI é de 36 Gy, para evitar assimetria no crescimento. Muitos radio-oncologistas incluem o osso no PTV sem expansão adicional para poupar esôfago e pulmões. Dados iniciais sugerem que cobrir todo o corpo vertebral pode não ser estritamente necessário, e o tema é objeto de ensaio clínico ativo (NCT03281889).
Pacientes com doença M2 podem receber boost até 54 Gy em áreas de doença metastática supratentorial ou na fossa posterior. Doença M3 é subdividida em difusa e focal: doença espinal difusa recebe 39,6 Gy, doença focal acima da medula 45 Gy, e focal abaixo da medula 50,4 Gy, conforme o protocolo ACNS 0332.
Volumes para boost de fossa posterior inteira
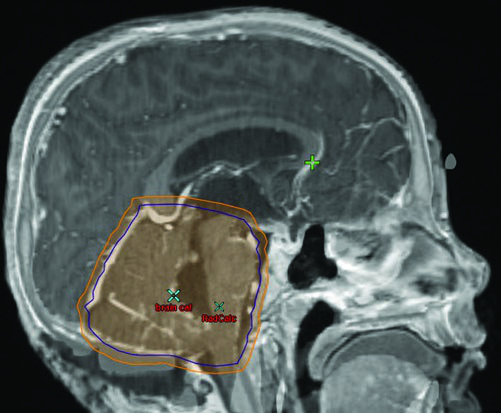
| Volume | Definição |
|---|---|
| GTV | Leito tumoral com doença residual, paredes da cavidade e áreas indicadas pelo neurocirurgião. |
| CTVFP | Toda a fossa posterior incluindo tronco cerebral inteiro. Limites: base do crânio anteriormente, tentório superiormente, forame magno inferiormente. Osso do crânio restringe posterior e lateralmente. |
| PTVFP | CTVFP + 3 a 5 mm conforme frequência de imagem e experiência institucional. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.3)
A identificação do fundo de saco tecal é essencial — geralmente ao nível de S2, mas não sempre. Tratar mais inferiormente que o necessário aumenta a dose de saída nas gônadas quando se usa campo fotônico posterior único, o que não ocorre com prótons.
Ependimoma: delineamento e margens de CTV
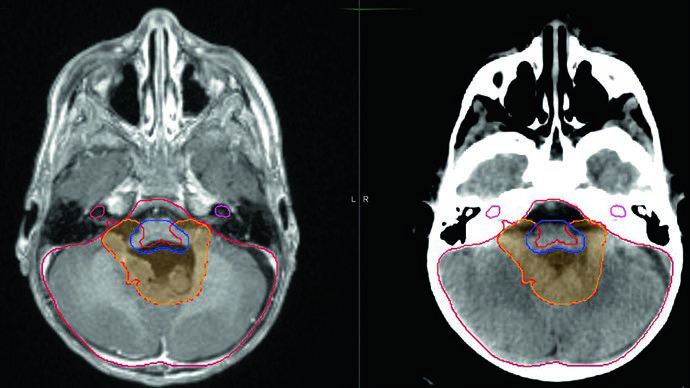
Assim como no meduloblastoma, o delineamento volumétrico por TC é obrigatório. Todos os pacientes precisam de RM pré e pós-operatória de alta qualidade com cortes de 1–3 mm do encéfalo e da coluna total. A disseminação pelo líquor é menos frequente que no meduloblastoma — inferior a 10% ao diagnóstico — mas deve ser descartada com RM espinal e citologia liquórica.
A extensão da ressecção é o fator prognóstico mais importante. Se a RM pós-operatória revelar doença residual, re-ressecção deve ser considerada quando a morbidade antecipada for aceitável.
O GTV consiste na cavidade de ressecção pós-operatória com atenção especial aos forames de Luschka e Magendie, frequentemente envolvidos. A conversa com o neurocirurgião é valiosa para identificar achados intraoperatórios não evidentes na imagem.
As margens de GTV para CTV diminuíram ao longo da última década. O protocolo ACNS 0831 do COG tratou com CTV = GTV + 0,5 cm até dose total de 54 Gy em 30 frações. Para minimizar toxicidade no tronco cerebral, a expansão do CTV no tronco foi limitada a 3 mm. Um conedown adicional até 59,4 Gy (para crianças acima de 18 meses) exclui completamente tronco cerebral, quiasma óptico e medula cervical do volume de boost.
Volumes recomendados para ependimoma infratentorial
| Volume | Definição |
|---|---|
| GTV | Leito tumoral com doença residual e paredes da cavidade na RM. Atenção especial aos forames de Magendie e Luschka. |
| CTV54 | GTV + 5 a 10 mm, limitado por osso e tentório. Não avança no tronco cerebral mais que 3 mm. |
| CTV59,4 | GTV + 5 mm excluindo totalmente tronco cerebral, quiasma óptico e medula cervical. |
| PTV | CTV + 3 a 5 mm. Aceita-se subdosagem do PTV em regiões onde seria necessário violar tolerância de medula cervical e quiasma óptico. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.4)
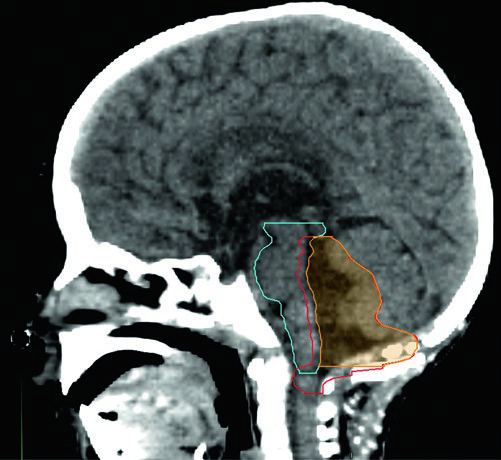
Muitos radio-oncologistas pediátricos ainda preferem margens maiores (CTV = GTV + 1 cm) com dose total de 54 Gy fora de protocolo, e essa abordagem é considerada aceitável. O protocolo ACNS 0831 estabeleceu como meta D10% da medula cervical ≤ 57 Gy, e durante o tratamento do PTV59,4, o volume total da medula espinal não deve receber mais que 70% ou 126 cGy por fração nas últimas três sessões.
Quando se trata até 59,4 Gy, uma abordagem em duas fases é recomendada: o conedown em 54 Gy permite poupar tronco cerebral, quiasma óptico e medula cervical. Independentemente da extensão inferior do tumor, o PTV54 não deve estender-se abaixo do forame magno.
Germinoma puro: irradiação ventricular e boost
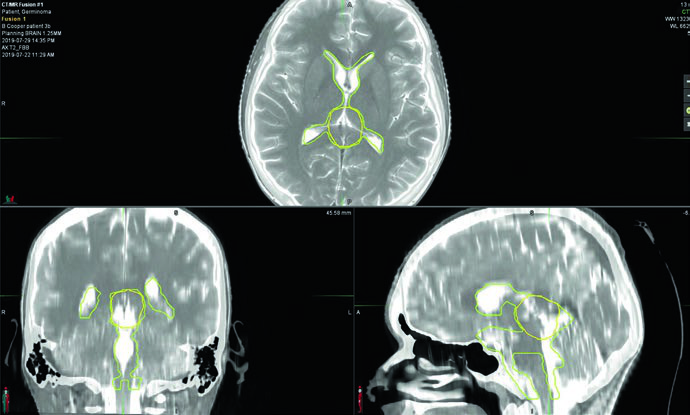
O planejamento exige RM pré e pós-operatória de 1–3 mm de espessura de corte, cobrindo encéfalo e coluna. Marcadores séricos e liquóricos de beta-hCG e alfa-fetoproteína são fundamentais para excluir componente não germinomatoso: qualquer elevação de AFP reclassifica o tumor como NGGCT. No protocolo ACNS 1123, pacientes com beta-hCG sérico ou liquórico acima de 100 mIU/mL foram tratados como NGGCT.
Germinomas bifocais — envolvimento simultâneo suprasselar e pineal — são tratados como doença localizada com irradiação ventricular total seguida de boost de campo envolvido. O volume-alvo inclui o tumor pré-quimioterapia, qualquer doença residual e todo o sistema ventricular. É crítico delinear a doença pré-quimioterapia já no planejamento inicial, porque o volume de boost frequentemente se estende além dos limites ventriculares normais.
O boost CTV é definido como GTV pré-quimioterapia + 1 a 1,5 cm. A inclusão da cisterna pré-pontina é opcional, mas deve ser considerada em pacientes submetidos a ventriculostomia ou com tumores suprasselares volumosos.
Esquemas de dose para germinoma puro
Quando a radioterapia é modalidade única, o volume ventricular recebe 21 a 24 Gy com boost até 45 Gy no volume pré-quimioterapia. Uma fração de 1,5 Gy é preferida por muitos centros dado o bom prognóstico e o desejo de minimizar toxicidade neurocognitiva, embora 1,8 Gy por fração não seja contraindicado.
Com quimioterapia neoadjuvante e resposta completa do primário, a dose ventricular cai para 21 Gy com boost de 9 a 15 Gy, totalizando 30 a 36 Gy no tumor primário. O estudo ACNS 1123 testou redução da dose ventricular para 18 Gy: não houve falhas ventriculares nos 74 pacientes avaliáveis, mas o estudo não conseguiu demonstrar não-inferioridade frente ao limiar de 95% de sobrevida livre de progressão em 3 anos. Pacientes com resposta parcial ou progressão precisam de boost até 36 a 45 Gy no tumor primário.
O artigo sobre tumores malignos do SNC complementa este conteúdo com o delineamento de gliomas de alto grau em adultos. Já o artigo sobre tumores benignos do SNC aborda meningiomas e schwannomas.


![Imagem fundida PET/TC com captação de [89Zr]girentuximab em massa renal posterior](https://rtmedical.com.br/wp-content/uploads/2026/05/article10_pet-600x403.jpg)