Delineamento do câncer de pâncreas na radioterapia
O adenocarcinoma pancreático desafia o planejamento radioterápico como poucos tumores abdominais. A proximidade com estruturas luminais radiosensíveis — estômago, duodeno e intestino delgado — torna o equilíbrio entre cobertura tumoral e proteção de órgãos de risco (OARs) uma tarefa que exige técnica refinada, controle rigoroso de movimento e conhecimento detalhado da anatomia vascular peripancreática. A IMRT tornou-se a técnica padrão para tratar o câncer de pâncreas em cenários neoadjuvante, adjuvante e definitivo, enquanto abordagens ablativas requerem SBRT ou técnicas guiadas por imagem.
Para uma visão abrangente de todos os sítios anatômicos abordados neste livro, confira nosso guia completo sobre delineamento de volume alvo e campos na radioterapia.
Simulação e controle de movimento respiratório
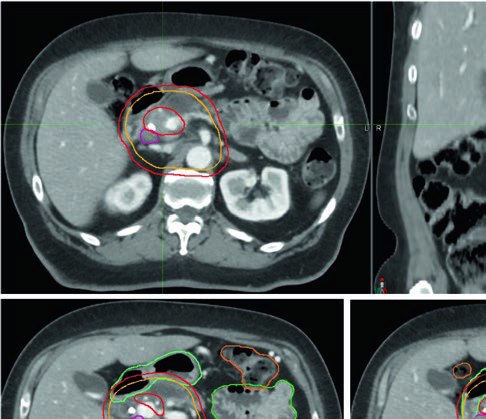
A TC de simulação com contraste IV em protocolo pancreático é indispensável para o delineamento preciso do alvo e dos OARs. O protocolo típico utiliza 150 cc de contraste iodado a 5 cc/s, com aquisição em duas fases: arterial tardia (35 s) e portal venosa (90 s). Essa abordagem dupla permite delimitar tanto o tumor primário — geralmente hipointenso — quanto a extensão vascular, que é crítica no planejamento de doses acima de 50 Gy em EQD2.
O manejo do movimento respiratório reduz as doses nos OARs e maximiza a cobertura do alvo. Para qualquer abordagem ablativa, o controle de movimento é obrigatório. O gating — seja em inspiração profunda sustentada (DIBH) ou gating expiratório — é preferível, mas exige fiduciais metálicos ou stent metálico como referência. Quando o gating não é viável, a alternativa é o volume-alvo interno (ITV), delineando o GTV em todas as fases do 4D-CT. O paciente é imobilizado em alpha-cradle customizado, com braços elevados acima da cabeça sempre que tolerável.
Volumes-alvo no cenário neoadjuvante (ressecável borderline)
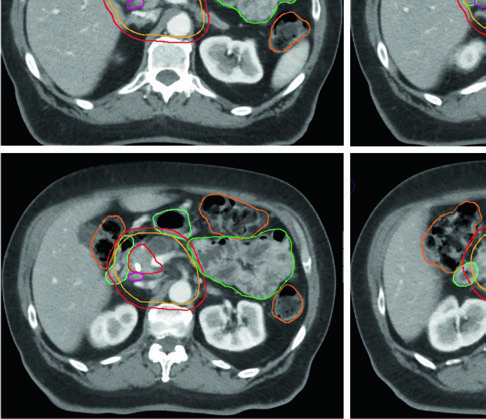
O tratamento pré-operatório de doença borderline ressecável ou ressecável de alto risco requer doses mais baixas e, consequentemente, tecnologia menos complexa. No entanto, as margens devem ser generosas o suficiente para cobrir toda a doença microscópica e a extensão radiograficamente oculta ao longo da vasculatura.
Definição dos volumes neoadjuvantes
| Volume | Definição e descrição |
|---|---|
| GTV | Toda doença macroscópica na imagem, incluindo o tumor primário (tipicamente hipointenso), com atenção especial à extensão ao longo dos vasos, e todos os linfonodos suspeitos |
| ITV (opcional) | Se utilizada abordagem ITV, delinear o GTV em todas as fases do 4D-CT |
| CTV | Expansão uniforme de pelo menos 1 cm sobre toda doença macroscópica + cobertura das cadeias do tronco celíaco (CA) e artéria mesentérica superior (AMS) + margem adicional ao longo dos vasos em caso de incerteza + cobertura do hilo esplênico (lesões de corpo/cauda) + cobertura opcional da porta hepatis (lesões de cabeça) |
| PTV | Margem baseada na técnica de controle de movimento, mínimo 0,5 cm. Sem ITV e em respiração livre, expansão de 1–1,5 cm na direção craniocaudal |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.1)
Os esquemas de fracionamento apropriados incluem 25 Gy em 5 frações, 30 Gy em 10 frações, 36 Gy em 12 frações e 50,4 Gy em 28 frações. A escolha depende da intenção terapêutica, da anatomia do paciente e da tecnologia disponível.
Tratamento definitivo de doença irressecável: doses ablativas
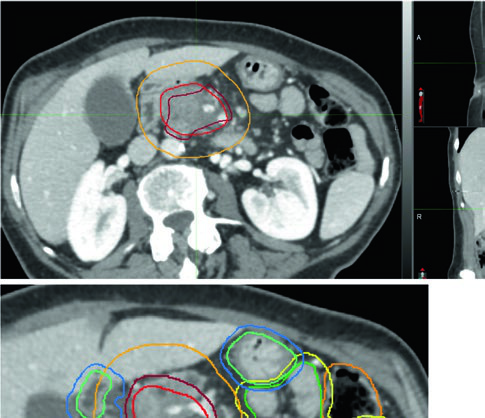
Tumores irressecáveis devem receber doses ablativas ($\text{BED}_{10} \geq 100\ \text{Gy}$) sempre que técnicas de controle de movimento e guia por imagem estiverem disponíveis. A tendência de reduzir o número de frações, impulsionada pela natureza intensiva do planejamento estereotático, precisa ser equilibrada por considerações radiobiológicas e dosimétricas que garantam dose realmente ablativa.
A proximidade dos OARs luminais radiosensíveis frequentemente exige esquemas hipofracionados com mais de cinco frações. A recomendação prática é: 75 Gy em 25 frações para tumores a menos de 1 cm dos OARs, e 67,5 Gy em 15 frações para tumores a mais de 1 cm. O esquema de 50 Gy em 5 frações pode ser usado seletivamente quando o tumor está a mais de 2 cm dos OARs. Quando o contato extenso entre tumor e OARs impede cobertura adequada com dose ablativa, alternativas não ablativas como 50,4–56 Gy em 28 frações ou 33 Gy em 5 frações são aceitáveis.
Volumes-alvo no cenário definitivo
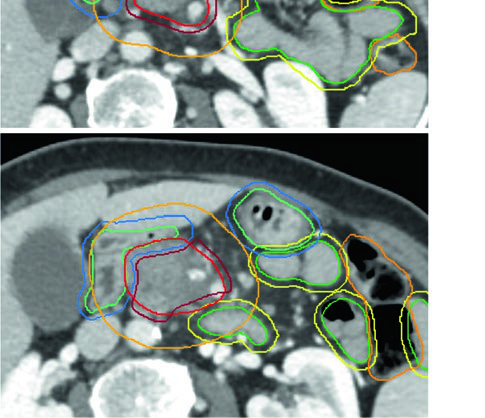
| Volume | Definição e descrição |
|---|---|
| GTV | Toda doença macroscópica na imagem, incluindo o tumor primário e extensão vascular |
| ITV (opcional) | Se utilizada abordagem ITV, delinear o GTV em todas as fases do 4D-CT |
| CTV alta dose | Corresponde ao GTV (ou ITV se utilizado) sem margem adicional |
| CTV dose microscópica | Expansão uniforme ≥ 1 cm sobre toda doença macroscópica + cadeias CA e AMS + hilo esplênico (corpo/cauda) + margem vascular adicional + porta hepatis opcional (cabeça) |
| PTV alta dose | Expansão 0–0,5 cm, subtraindo OARs críticos sobrepostos com margem de segurança: • 56 Gy/28 fx ou 33 Gy/5 fx: subtrair estômago e intestino delgado sem margem adicional • 50 Gy/10 fx, 67,5 Gy/15 fx ou 75 Gy/25 fx: subtrair com expansão de 0,5 cm (0,7 cm para interface longa) |
| PTV microscópico | Mínimo 0,5 cm; sem ITV em respiração livre, 1–1,5 cm craniocaudal |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.2)
Um detalhe frequentemente subestimado: dada a natureza infiltrativa do PDAC, o over-contouring do GTV para incluir o parênquima pancreático circundante pode ser razoável, especialmente quando suportado por imagem diagnóstica adicional. Nas regiões de contato direto entre GTV e OAR crítico, o PTV deve excluir o OAR com margem de segurança que exceda a expansão do PRV.
PRVs para doses ablativas
| Estrutura | Definição do PRV |
|---|---|
| Estômago/duodeno proximal PRV | Estômago e segmentos 1–2 do duodeno + 0,3 cm (0,5 cm para interface longa com o alvo) |
| Intestino delgado PRV | Restante do intestino delgado + 0,3 cm (0,5 cm para interface longa) |
Aplicável para doses ≥ 60 Gy em 25 frações ou equivalente em BED. Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.2)
Planejamento adjuvante pós-pancreatectomia
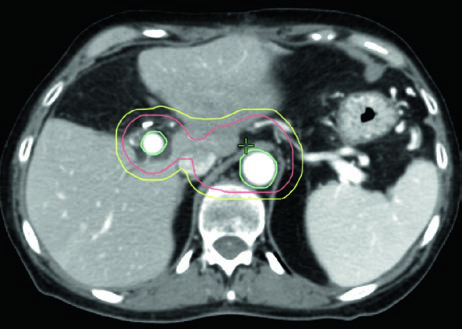
O cenário adjuvante segue a abordagem escalonada do atlas de delineamento do RTOG 0848, baseado em regiões de interesse (ROIs) que foram escolhidas pela facilidade de identificação e reprodutibilidade nas imagens. Campos menores focados no leito cirúrgico, CA e AMS também podem ser apropriados quando OARs limitantes de dose estão presentes.
Volumes-alvo adjuvantes (atlas RTOG 0848)
| Volume | Definição e descrição |
|---|---|
| GTV | Não aplicável |
| CTV | Leito cirúrgico e pancreaticojejunostomia (PJ) + cadeias nodais peripancreáticas, CA, AMS, paraaórticas, veia porta (tumores de cabeça) e esplênicas (corpo/cauda). ROIs do RTOG 0848: • CA (1–1,5 cm proximal) • AMS (2,5–3 cm proximal) • Veia porta (VP: início na confluência VMS/veia esplênica) • PJ • Aorta (superiormente ao mais cefálico entre CA, VP ou PJ; inferiormente a L2, ou L3 para cobrir GTV pré-operatório) • Leito tumoral (baseado em imagem pré-op, laudo patológico, clipes cirúrgicos) |
| Expansões | VP, PJ, CA, AMS: 1,0 cm. Aorta: 2,5–3,0 cm à direita, 1,0 cm à esquerda, 2–2,5 cm anterior, 0,2 cm posterior. CTV = união das expansões, confirmando cobertura do leito tumoral |
| PTV | Mínimo 0,5 cm; sem ITV em respiração livre, 1–1,5 cm craniocaudal |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.3)
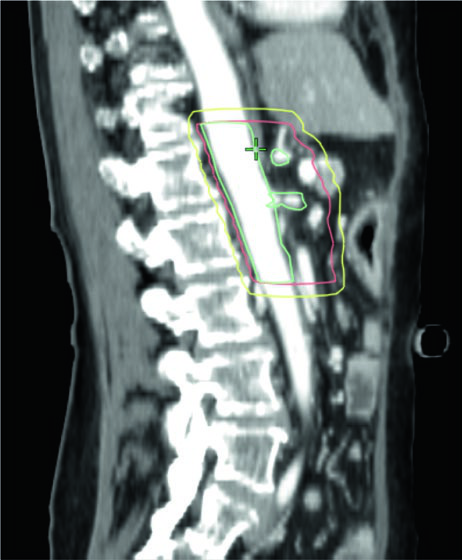
Restrições de dose aos órgãos de risco
As restrições de dose variam conforme o esquema de fracionamento. A tabela abaixo sintetiza os limites mais relevantes para os principais OARs no planejamento pancreático, organizados por número de frações. A distinção entre Limite (L — nunca ultrapassar) e Guideline (G — restrição sugerida quando a cobertura não é comprometida) é fundamental para otimizar o plano.
| OAR | 5 frações | 10 frações | 15–25 frações |
|---|---|---|---|
| Estômago/duodeno | Dmax ≤ 23 Gy (G); D2cc ≤ 23 Gy (G) | Dmax ≤ 28 Gy (G); D2cc ≤ 28 Gy (G) | Dmax ≤ 40 Gy (G); D2cc ≤ 40 Gy (G) |
| Intestino delgado | Dmax ≤ 23 Gy (G); D5cc ≤ 21 Gy (L) | Dmax ≤ 28 Gy (G); D5cc ≤ 25 Gy (L) | Dmax ≤ 40 Gy (G); D5cc ≤ 25 Gy (L) |
| Intestino grosso | Dmax ≤ 25 Gy (G); D5cc ≤ 25 Gy (L) | Dmax ≤ 30 Gy (G); D5cc ≤ 30 Gy (L) | Dmax ≤ 45 Gy (L) |
| Fígado* | Dmean < 15 Gy; V15 < 700 cc (L) | Dmean < 16 Gy; V16 < 700 cc (L) | Dmean < 20 Gy; V20 < 700 cc (L) |
| Rins (cada) | V10 < 50%; D < 10 cc (L) | V10 < 50%; D < 10 cc (L) | V20 < 50%; Dmean (L) |
| Rim único | D5cc < 16 Gy (L) | D5cc < 16 Gy (L) | D5cc < 20 Gy (L) |
| Medula | Dmax < 18 Gy (L) | Dmax < 18 Gy (L) | Dmax < 35–45 Gy (L) |
| Ductos hepáticos/biliares | Dmax ≤ 40 Gy (G) | Dmax ≤ 55 Gy (G) | Dmax ≤ 70–80 Gy (G) |
| Esôfago | Dmax ≤ 25 Gy (G) | Dmax ≤ 30 Gy (G) | Dmax ≤ 45–65 Gy (G) |
L = Limite (nunca ultrapassar); G = Guideline (restrição sugerida). *Fígado: se sem cirrose, usar restrições inferiores. Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.4)
Uma nuance importante: quando o PTV se sobrepõe a um OAR crítico, a restrição com sufixo “se overlap” entra em vigor. Para o estômago, por exemplo, o D5cc com sobreposição pode ser limitado a 30 Gy em 5 frações ou 33 Gy em 10 frações. Esse nível de detalhe faz diferença entre um plano que entrega dose ablativa e um que fica aquém.
Integração prática: do diagnóstico ao plano final
A escolha do fracionamento no câncer pancreático nunca é puramente acadêmica. Três fatores determinam o esquema ideal: a intenção de tratamento (pré-operatório, adjuvante ou definitivo), a tecnologia disponível (gating, CBCT, fiduciais) e a anatomia específica do paciente — em particular, a extensão da interface tumor-OAR.
Na prática, o fluxo de trabalho começa pela avaliação da ressecabilidade. Tumores borderline recebem esquemas de dose mais baixa (25–50,4 Gy), com margens CTV generosas de pelo menos 1 cm e cobertura das cadeias vasculares. Tumores irressecáveis são candidatos a dose ablativa (BED₁₀ ≥ 100 Gy), mas a viabilidade depende diretamente da capacidade de excluir OARs do PTV de alta dose com margens de segurança adequadas. Já o cenário adjuvante, sem GTV a ser delineado, segue o atlas padronizado do RTOG 0848 com suas expansões específicas por ROI.
Para quem está planejando um caso de câncer gástrico ou hepatocarcinoma, muitas das restrições de OARs e princípios de controle de movimento são compartilhados e vale a consulta cruzada.
Referências
- Reyngold M, Parikh P, Crane CH. Ablative radiation therapy for locally advanced pancreatic cancer: techniques and results. Radiat Oncol. 2019;14(1):95.
- Goodman KA, Regine WF, Dawson LA, et al. Radiation Therapy Oncology Group consensus panel guidelines for the delineation of the clinical target volume in the postoperative treatment of pancreatic head cancer. Int J Radiat Oncol Biol Phys. 2012;83(3):901–8.


![Imagem fundida PET/TC com captação de [89Zr]girentuximab em massa renal posterior](https://rtmedical.com.br/wp-content/uploads/2026/05/article10_pet-600x403.jpg)