Princípios do Planejamento Radioterápico nos Tumores Malignos do SNC
O tratamento radioterápico dos tumores malignos primários do sistema nervoso central exige uma abordagem que integra avaliação clínica detalhada, imagem multimodal e técnicas modernas de entrega de dose. Na prática, antes de iniciar qualquer planejamento, o radioterapeuta precisa de um histórico completo, exame neurológico focado, avaliação hormonal basal, hemograma (especialmente para pacientes que receberão quimioterapia concomitante), campo visual, audiometria e função neurocognitiva de base. Tudo isso informa o plano de forma direta.
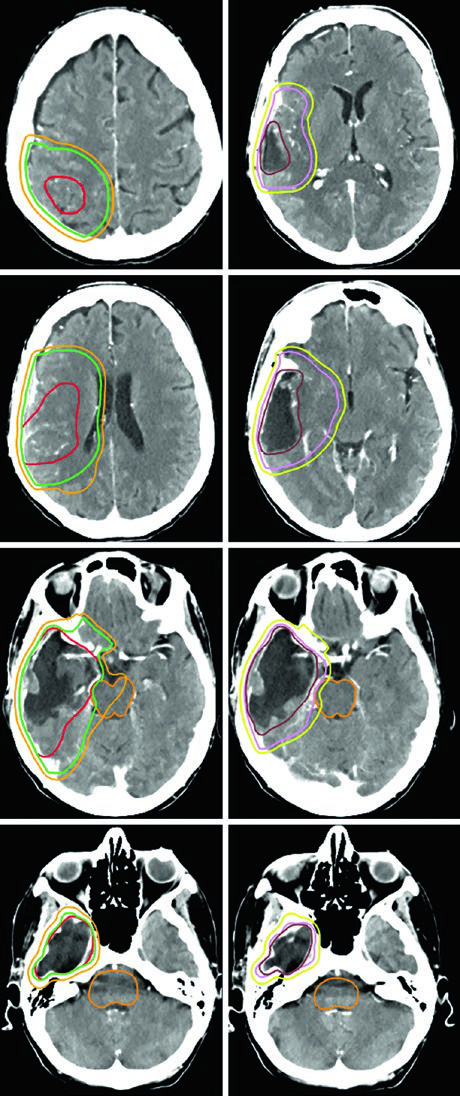
A ressecção cirúrgica máxima e segura continua como padrão-ouro para pacientes com tumores operáveis. O objetivo é a ressecção macroscópica total sempre que possível. Para os inoperáveis, a radioterapia definitiva se aplica — geralmente após biópsia para diagnóstico e caracterização molecular. A radioterapia adjuvante, por sua vez, entra para a maioria dos pacientes após a ressecção.
Diversas técnicas são empregadas: radioterapia conformacional 3D (3D-CRT), radiocirurgia estereotáxica fracionada (FSRT), radioterapia de intensidade modulada (IMRT), arco volumétrico modulado (VMAT), radiocirurgia estereotáxica (SRS) e até próton-terapia (PBT). A escolha depende do tamanho, localização e proximidade com estruturas críticas.
O ponto central é este: a delineação precisa tanto dos volumes-alvo quanto dos órgãos de risco determina qual técnica será mais vantajosa para cada paciente. E para isso, a corregistração de RM diagnóstica no CT de planejamento não é opcional — é fortemente recomendada. As sequências T1 pós-contraste e FLAIR permitem visualizar tanto o tumor residual quanto o edema perilesional, enquanto sequências T1 simples e 3D-T2/CISS ajudam a delinear estruturas como hipocampo e nervos cranianos. Para mais contexto sobre os princípios gerais de delineamento, confira nosso guia completo sobre delineamento de volume alvo na radioterapia.
Posicionamento, Imobilização e Simulação
Pacientes com tumores malignos primários do cérebro são tipicamente simulados em decúbito dorsal, braços estendidos junto ao corpo e ombros em posição natural. Para simulação por CT, uma máscara termoplástica indexada de 3 pontos é o padrão para imobilização. Tumores de base de crânio ou próximos ao aparato óptico podem exigir uma máscara de 5 pontos — a extensão ao pescoço reforça o posicionamento cervical.
Na simulação por RM, usa-se uma máscara tipo clamshell. Cabeça e queixo ficam em posição neutra, salvo quando instruções específicas de posicionamento para base de crânio se aplicam.
A espessura dos cortes axiais na simulação por CT é de 1 mm para SRS, FSRT ou PBT, e 2 mm para 3D-CRT, IMRT ou VMAT. As imagens devem cobrir toda a cabeça até o nível dos ombros. A corregistração com RM diagnóstica é altamente recomendada, e o contraste IV pode auxiliar na fusão com imagens pré-operatórias e na visualização de cavidades de ressecção.
Estruturas Normais e Órgãos de Risco
Os órgãos de risco (OARs) são delineados no CT de planejamento com apoio da RM. Volumes de risco de planejamento (PRVs) podem ser criados para tumores que tangenciam estruturas críticas, auxiliando tanto no planejamento dosimétrico quanto na avaliação final do plano.
Lista de OARs para tumores cerebrais primários
| Estrutura | Observação |
|---|---|
| Encéfalo | Volume total |
| Encéfalo não envolvido | Encéfalo minus GTV ou CTV, conforme cenário clínico |
| Tronco encefálico | Core e superfície separados |
| Medula espinhal | — |
| Cócleas (D/E) | Bilateral |
| Globos oculares (D/E) | Bilateral |
| Cristalinos (D/E) | Bilateral |
| Nervos ópticos (D/E) | Bilateral |
| Quiasma óptico | — |
| Retinas (D/E) | Bilateral |
| Glândulas lacrimais (D/E) | Bilateral |
| Lobos temporais (D/E) | Bilateral |
| Hipocampos (D/E) | Delineados preferencialmente na T1 pós-contraste |
| Hipotálamo | — |
| Hipófise | — |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 30.1)
Glioma de Alto Grau: Volumes-Alvo e Fracionamento
Pacientes com astrocitoma de alto grau e oligodendroglioma passam por ressecção cirúrgica máxima para diagnóstico, caracterização molecular e citorredução. O tratamento padrão combina radioterapia conformacional fracionada com quimioterapia — seja concomitante, adjuvante ou ambas.
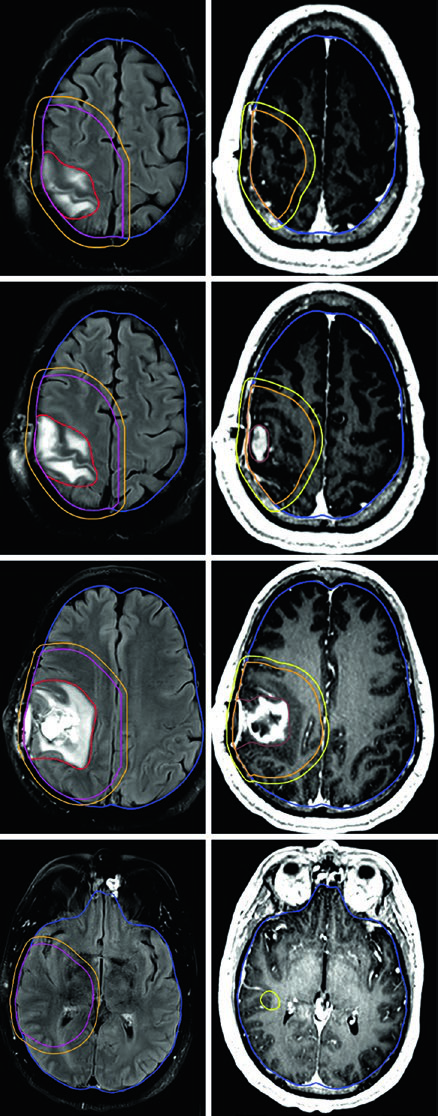
A dose padrão para gliomas de alto grau é de 59,4–60 Gy com fracionamento convencional. Para pacientes idosos, frágeis ou com performance status limitado, esquemas hipofracionados são uma alternativa validada: 40,05 Gy em 15 frações ou até 25 Gy em 5 frações, com margens reduzidas (0,5–1 cm). A tabela a seguir resume os volumes recomendados por tipo tumoral.
Volumes-alvo recomendados para glioma de alto grau
| Tipo tumoral | Dose/Fracionamento | Definição do GTV | Expansão CTV | Expansão PTV |
|---|---|---|---|---|
| Glioma anaplásico (captante) | Cone-down sequencial: PTV1 50,4 Gy (1,8 Gy/fx), PTV2 59,4 Gy (1,8 Gy/fx); ou SIB: PTV1 54,45 Gy (1,65 Gy/fx), PTV2 59,4 Gy (1,8 Gy/fx) | GTV1: volume T2/FLAIR; GTV2: cavidade pós-operatória + tumor residual na T1 pós-contraste | CTV1: 1,5 cm restrito anatomicamente; CTV2: 1,0 cm restrito | 0,3–0,5 cm |
| Glioma anaplásico (não captante) / Astrocitoma difuso IDH-wild type | PTV1: 59,4 Gy (1,8 Gy/fx) | GTV: cavidade pós-operatória + tumor residual em T2/FLAIR | CTV: 1,5 cm restrito anatomicamente | 0,3–0,5 cm |
| Glioblastoma | Cone-down: PTV1 46 Gy (2 Gy/fx), PTV2 60 Gy (2 Gy/fx); ou SIB: PTV1 50–51 Gy (1,67–1,7 Gy/fx), PTV2 60 Gy (2 Gy/fx) | GTV1: volume T2/FLAIR; GTV2: cavidade + tumor residual na T1 pós-contraste | CTV1: 2 cm restrito anatomicamente; CTV2: 2 cm restrito | 0,3–0,5 cm |
| Gliossarcoma | Cone-down: PTV1 46 Gy (2 Gy/fx), PTV2 60 Gy (2 Gy/fx); ou SIB: PTV1 50–51 Gy (1,67–1,7 Gy/fx), PTV2 60 Gy (2 Gy/fx) | GTV1: volume T2/FLAIR; GTV2: cavidade + tumor residual na T1 pós-contraste | CTV1: 1,5–2 cm restrito; CTV2: 1,5–2 cm restrito | 0,3–0,5 cm |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 30.2)
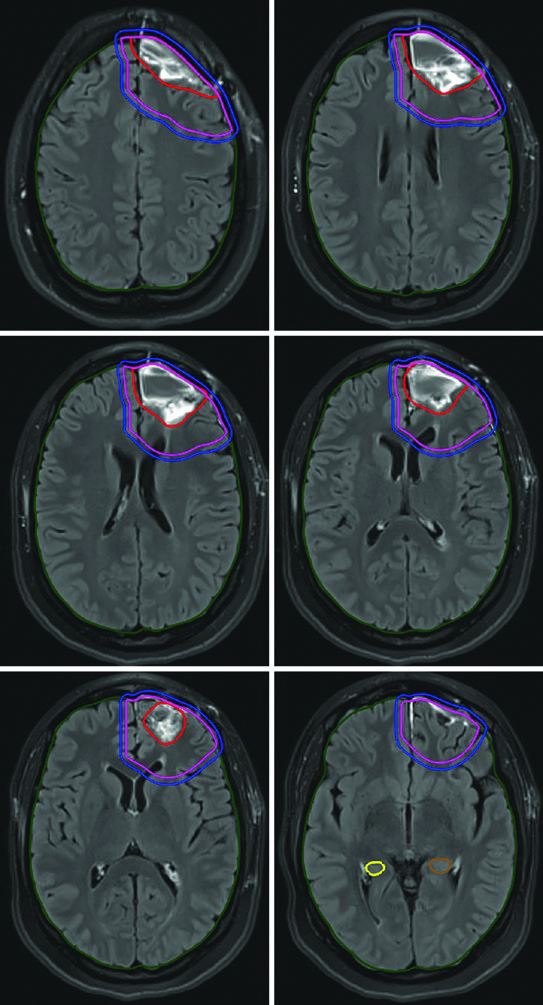
Um ponto prático fundamental: as expansões anatomicamente restritas significam que o CTV não cruza a linha média, não invade a cisterna pré-pontina, não se estende pelo crânio e não ultrapassa o tentório para a fossa posterior. No entanto, tratos em risco para disseminação tumoral contralateral — como o joelho do corpo caloso — devem ser incluídos. Essa nuance aparece claramente nos casos de glioblastoma frontal em que o tumor se aproxima do corpo caloso.
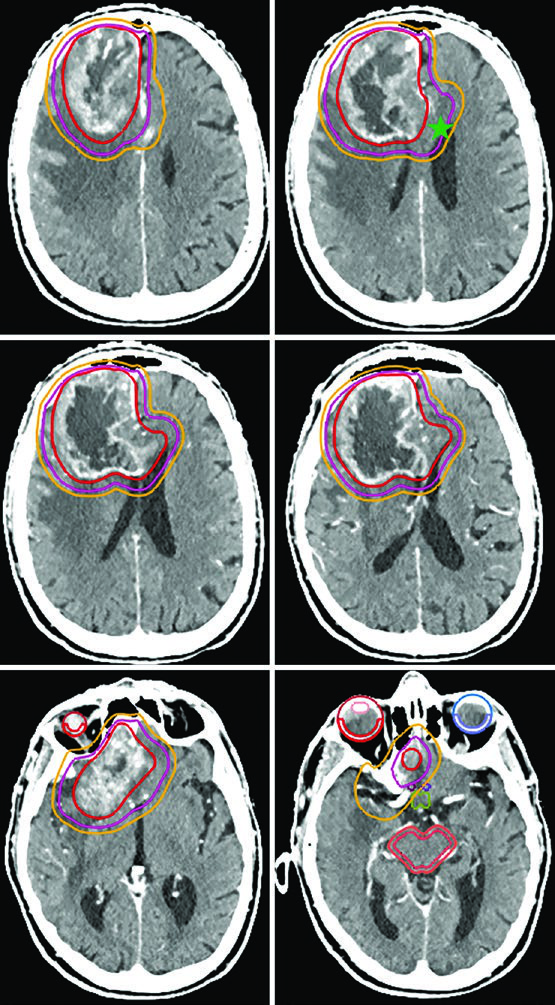
Cenários Especiais: Hipofracionamento em Pacientes de Alto Risco
Pacientes idosos ou com performance status comprometido representam um desafio particular. O esquema de 40 Gy em 15 frações funciona bem quando há pouco volume FLAIR fora do tumor captante — o GTV inclui cavidade de ressecção, tumor residual e nódulos satélites na T1 pós-contraste, com expansão de CTV de apenas 1,0 cm e restrição anatômica ao tentório.
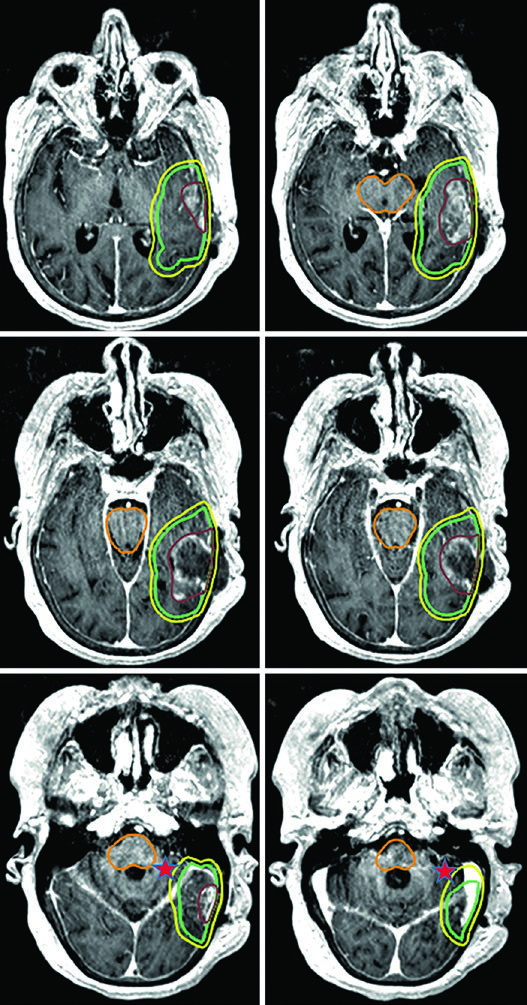
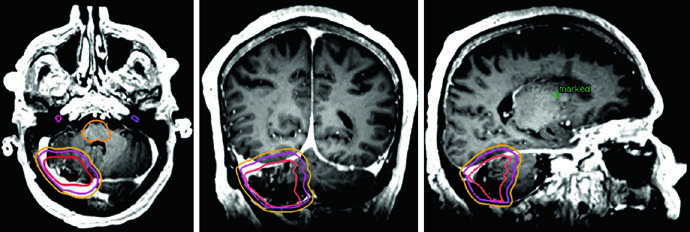
Para situações ainda mais agressivas em termos de prognóstico, o regime ultra-hipofracionado de 25 Gy em 5 frações é uma opção, com margens de 0,5 cm do GTV para o CTV. Um exemplo típico é o glioblastoma cerebelar — a cóclea e o tronco encefálico ficam visíveis e servem como referência direta na dosimetria.
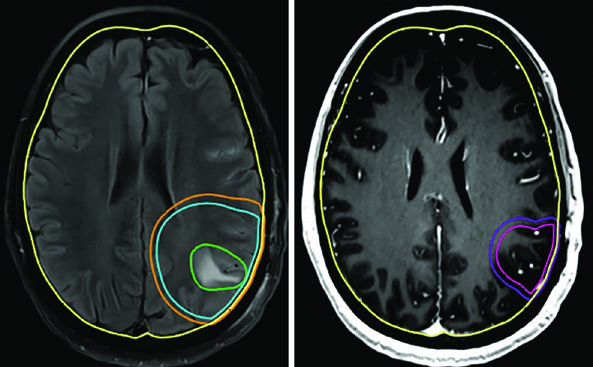
Já o gliossarcoma segue paradigma semelhante ao do glioblastoma. Dois volumes sequenciais costumam ser empregados — o primeiro baseado no FLAIR (46 Gy) e o segundo na T1 pós-contraste (60 Gy), com expansões de CTV de 1,5 cm anatomicamente restritas.
Meningioma Atípico e Maligno: Graus II e III da OMS
Os meningiomas são os tumores intracranianos primários mais comuns em adultos. Menos de 30% são classificados como atípicos (OMS grau II) ou malignos (OMS grau III). O manejo radioterápico desses subtipos difere substancialmente do meningioma benigno.
Para meningioma grau II, a radioterapia adjuvante pode ser considerada após ressecção macroscópica total e é recomendada após ressecção subtotal. Para grau III, a radioterapia é recomendada para todos os pacientes independentemente da extensão da ressecção. Para conhecer o manejo dos tumores benignos do SNC, confira nosso artigo dedicado sobre tumores benignos do SNC.
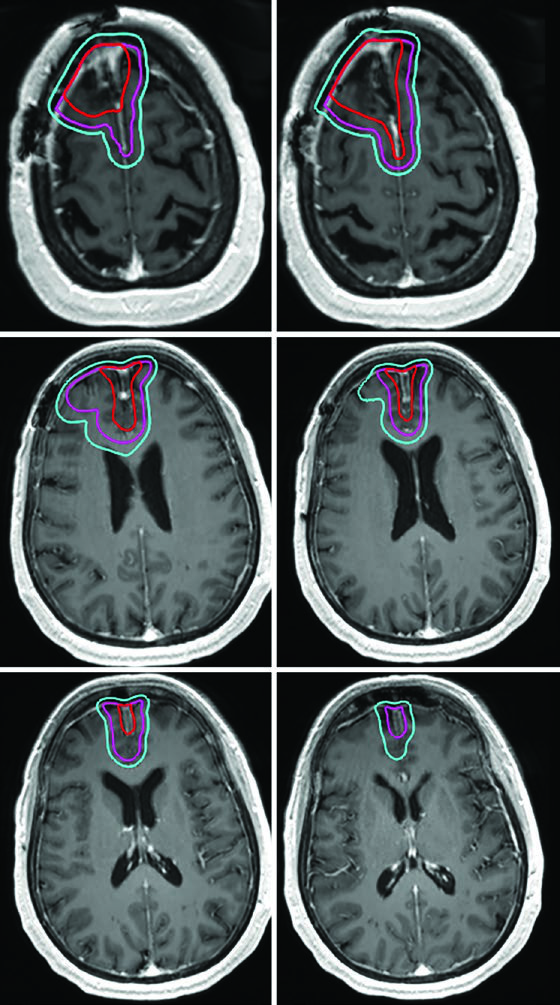
Um detalhe crítico que diferencia os meningiomas de grau II e III: como esses tumores podem invadir osso e parênquima cerebral, crânio e encéfalo normal não funcionam necessariamente como barreiras naturais à disseminação. Se os achados operatórios ou anatomopatológicos indicam invasão cerebral, as margens devem incluir o parênquima em risco. E para tumores recorrentes de grau II, é essencial avaliar a inserção dural original no diagnóstico inicial — ela pode ter sido sede de doença microscópica.
Volumes-alvo para meningioma grau II/III e hemangiopericitoma
| Tipo tumoral | Dose/Fracionamento | Definição do GTV | Expansão CTV | Expansão PTV |
|---|---|---|---|---|
| Meningioma grau II (upfront) | 54–59,4 Gy (1,8 Gy/fx) | Cavidade pós-operatória, tumor residual incluindo envolvimento dural/ósseo suspeito na T1 pós-contraste | 0,5 cm restrito anatomicamente | 0,3–0,5 cm |
| Meningioma grau II (recorrente) | 54–59,4 Gy (1,8 Gy/fx) | Idem + avaliação da inserção dural prévia no diagnóstico inicial | 0,5–1,0 cm restrito | 0,3–0,5 cm |
| Meningioma grau III (upfront ou recorrente) | 59,4–60 Gy (1,8–2 Gy/fx) | Idem + inserção dural prévia | 1,0–1,5 cm restrito | 0,3–0,5 cm |
| Hemangiopericitoma | 59,4–60 Gy (1,8–2 Gy/fx) | Cavidade pós-op, tumor residual, envolvimento dural/ósseo na T1 pós-contraste | 1,5 cm restrito, mas incluir totalidade do osso envolvido | 0,3–0,5 cm |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 30.3)
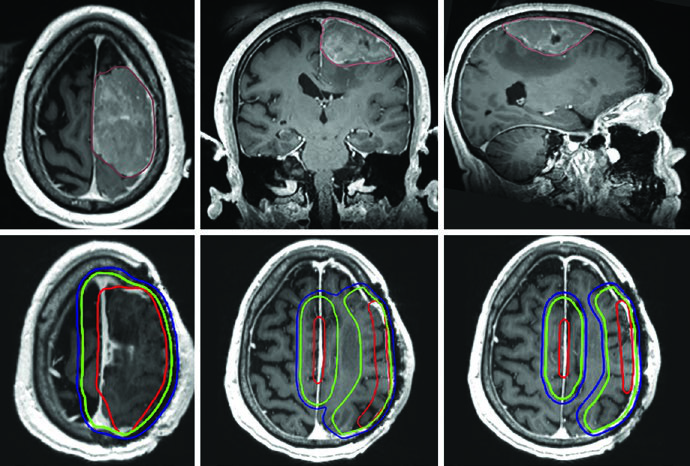
O hemangiopericitoma merece menção especial. A expansão de CTV de 1,5 cm segue o padrão, mas diferentemente dos meningiomas, todo o osso envolvido deve ser incluído no volume sem redução em barreiras ósseas — a natureza infiltrativa desse tumor justifica essa conduta mais agressiva.
Considerações Práticas e Armadilhas Frequentes
Alguns erros recorrentes no planejamento de tumores malignos do SNC merecem destaque. O mais comum é aplicar expansões isotrópicas sem respeitar as barreiras anatômicas. O CTV de um glioblastoma frontal não deve cruzar a linha média — a menos que o joelho do corpo caloso esteja em risco, caso em que essa estrutura deve ser explicitamente incluída. Outro erro é ignorar a diferença entre as sequências de RM: o GTV1 deve ser baseado no FLAIR (edema perilesional), enquanto o GTV2 usa a T1 pós-contraste (doença captante residual).
Para pacientes tratados com SRS ou FSRT, a espessura de corte de 1 mm é mandatória — cortes mais espessos comprometem a precisão geométrica. E para o IGRT diário, a expansão PTV de 0,3 cm pode ser suficiente; sem verificação de imagem frequente, 0,5 cm é mais prudente.
Artigos relacionados desta série podem fornecer contexto adicional: veja nosso artigo sobre metástases cerebrais e WBRT/SRS, que aborda princípios de radiocirurgia complementares ao manejo de tumores primários, e o artigo sobre tumores cerebrais pediátricos, que traz peculiaridades do planejamento na população mais jovem.