O Que Torna a SBRT uma Opção para Tumores de Cabeça e Pescoço?
A radioterapia estereotáxica corporal (SBRT) para cânceres de cabeça e pescoço representa um avanço significativo no arsenal terapêutico do radio-oncologista. Pacientes idosos, frágeis ou com comorbidades graves frequentemente não toleram ciclos longos de radioterapia convencional com quimioterapia concomitante. Para esses pacientes, a SBRT oferece controle local durável com curso de tratamento encurtado e perfil de efeitos colaterais aceitável.
Originalmente, a SBRT de cabeça e pescoço era empregada quase exclusivamente em cenários de re-irradiação. Entretanto, seu maior valor pode estar justamente no cenário não irradiado, onde o tempo prolongado de tratamento e recuperação de uma abordagem radical é indesejável ou irrealista para determinados pacientes. Centros de alto volume demonstram que a SBRT pode alcançar controle local durável, conforme descrito na literatura com doses de 35 a 50 Gy em 3 a 8 frações.
A decisão contra um curso prolongado de radioterapia geralmente envolve múltiplos fatores: preferência do paciente, fatores tumorais (morbidade esperada da progressão versus risco do tratamento e probabilidade de sucesso), expectativa de vida (influência de idade e comorbidades), tolerância ao tratamento agressivo baseada no performance status, e fatores não relacionados ao paciente como distância do hospital e disponibilidade de suporte social, financeiro e psicológico.
Equipe Multidisciplinar e Requisitos Técnicos
A SBRT de cabeça e pescoço exige uma equipe multidisciplinar altamente experiente, incluindo físicos médicos, dosimetristas e técnicos de radioterapia. Não se trata de simplesmente adaptar um protocolo de SBRT de pulmão para a região cervicofacial — a proximidade de estruturas neurológicas críticas e a complexidade anatômica impõem desafios específicos.
O delineamento preciso do GTV é absolutamente crítico para SBRT segura. Fotos intraorais que documentem achados do exame clínico podem ser valiosas. A revisão por neurorradiologista pode esclarecer a extensão tumoral e localizar órgãos em risco radiossensíveis com maior precisão.
Simulação e Imagem: CT com Contraste e Fusão com RM
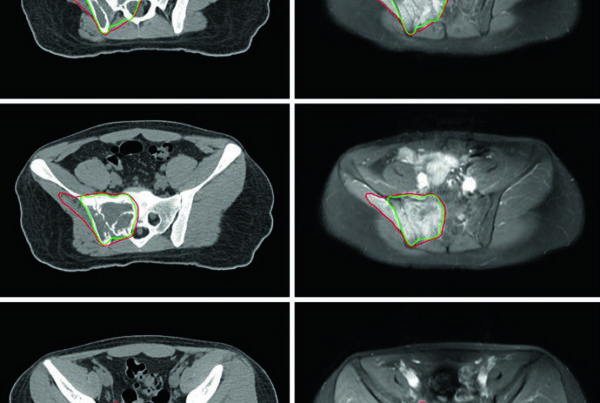
A simulação com tomografia computadorizada contrastada é obrigatória para definição volumétrica precisa. A fusão com ressonância magnética de simulação melhora substancialmente a visualização da doença macroscópica. Na prática, a fusão com RM é fortemente recomendada sempre que disponível — a diferença na qualidade do delineamento é notável.
Quando a RM não está disponível, a simulação com duplo contraste pode ser uma alternativa viável. Um caso ilustrativo documenta uma paciente de 79 anos com carcinoma de células escamosas T1N1 da base da língua: a CT com contraste simples (80 mL) não visualizou adequadamente o GTV, enquanto a simulação com duplo contraste (160 mL) permitiu definição excelente do tumor.
Obturações dentárias metálicas que causem artefatos e prejudiquem a visualização devem ser removidas antes da SBRT. Em um caso descrito, um paciente frágil de 87 anos com marca-passo incompatível com RM teve artefatos severos causados por obturações metálicas. O delineamento do GTV só foi possível após extração dos dentes afetados. Alternativamente, restaurações metálicas podem ser substituídas por materiais não metálicos.
Imobilização, Margens de PTV e Protocolo de Dose
A máscara termoplástica de cinco pontos combinada com cone beam CT (CBCT) diário permite imobilização reprodutível e redução das margens de PTV para 3 mm. A toxicidade é adicionalmente minimizada pela eliminação dos volumes microscópicos abrangentes tradicionais.
A faixa de dose padrão para o GTV situa-se entre 40 e 50 Gy, com duas frações por semana, sendo 45 Gy a prescrição mais comum. Um ponto crucial: não se utiliza expansão de CTV de alta ou baixa dose a partir do GTV. Um CTV microscópico nodal pode ser criado para linfonodos imediatamente adjacentes em risco. O PTV com redução de dose é criado com expansão de 3 mm do GTV/CTV de alta dose.
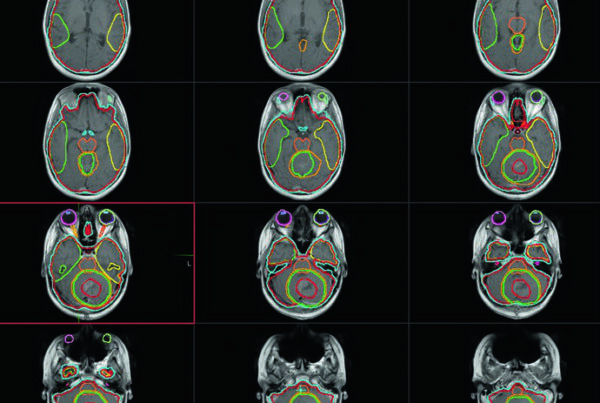
Os hot spots devem estar posicionados dentro do GTV e distantes dos órgãos em risco. Um índice de conformidade de 1,1 do GTV e PTV é desejável. A cobertura do alvo deve ser comprometida quando em proximidade com estruturas neurológicas críticas — plexo braquial, vias ópticas, cérebro e tronco cerebral. A dose na artéria carótida, entretanto, não deve comprometer a cobertura do alvo, exceto em situações de re-irradiação.
Volumes-Alvo: Definições e Expansões
A tabela abaixo resume as definições de volumes-alvo utilizadas no protocolo de SBRT de cabeça e pescoço, demonstrando a abordagem escalonada com diferentes níveis de dose.
| Volume | Definição e Descrição |
|---|---|
| GTV40-50 | Primário: toda doença macroscópica no exame físico e imagem, incluindo sequências RM T1-gadolínio, T1 com saturação de gordura e T2. Fusão de CT de simulação contrastada com RM. Se fatores do paciente impedem RM, a visualização do GTV na CT de simulação pode ser melhorada com duplo contraste. Linfonodos cervicais: com centro necrótico ou PET-ávidos. |
| CTV40-50 | Com delineamento preciso do GTV, este volume é igual ao GTV40-50. |
| PTV35-40 | CTV40-50 (equivalente ao GTV40-50) + 3 mm, com CBCT diário. |
| CTV35-40 | Linfonodos suspeitos (arredondados, com realce). |
| PTV30-35 | CTV35-40 + 3 mm se este volume estiver próximo de outros volumes de alta dose e bom match no cone beam for esperado. Se não viável, CTV35-40 + 5 mm. |
| CTV25 | Inclui bacias linfonodais de alto risco imediatamente adjacentes aos volumes de tratamento, onde re-irradiação para recidiva regional seria difícil. |
| PTV25 | CTV25 + 3-5 mm. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 3.1)
Garantia de Qualidade e Verificação de Imagem
Um programa robusto de garantia de qualidade (QA) é indispensável. O protocolo descrito emprega um teste de alinhamento de isocentro Winston-Lutz modificado para garantir tolerância dentro de 2,5 mm. O CBCT diário para matching com osso e tecido mole é imperativo.
Um detalhe que merece atenção: como o número total de CBCTs é mínimo (geralmente 5 frações), tentativas de reduzir a dose do CBCT são de pouco valor e não devem impedir a obtenção de imagens de alta qualidade. Priorize sempre a qualidade da imagem de verificação sobre a economia de dose nesse contexto.
Casos Clínicos: Versatilidade da SBRT em Cabeça e Pescoço
A literatura documenta casos que demonstram a amplitude de aplicação da SBRT de cabeça e pescoço. Uma paciente de 73 anos com carcinoma de células escamosas T1N3 do seio piriforme irressecável, comprimindo a veia jugular interna, optou contra curso prolongado de radiação. Recebeu 50 Gy em cinco frações no GTV nodal e 40 Gy em cinco frações no GTV primário, com duas frações por semana. A cobertura do alvo não foi comprometida para poupar a artéria carótida. Sem evidência de doença em 2 anos.
Outro caso marcante: uma paciente de 65 anos com carcinoma extenso de cavidade oral medindo 6,9 por 4,0 cm, estendendo-se da base do crânio pela fossa infratemporal até o espaço mastigador e mandíbula direita, causando fratura patológica e trismo com abertura bucal de 1,5 cm. Recebeu 45 Gy em cinco frações. Quatro anos depois, conseguia abrir a boca 4 cm e permanecia livre de doença.
A abordagem funciona inclusive em pacientes muito idosos. Uma paciente de 100 anos com recidiva de carcinoma espinocelular de pele na parótida e linfonodos cervicais foi tratada com SBRT. O CTV nodal englobou a bacia nodal de alto risco recebendo 25 Gy, enquanto o GTV recebeu 45 Gy. Permaneceu bem por 6 meses, com recidiva regional posterior tanto dentro quanto fora do campo de baixa dose — o que demonstra a limitação da SBRT quando não se trata a doença microscópica regional.
A SBRT também se aplica a pacientes com neoplasias concomitantes. Um paciente de 66 anos com obstrução da veia cava superior por massa pulmonar de células não pequenas e carcinoma T2N1 da base da língua cruzando a linha média recebeu 45 Gy em cinco frações, duas por semana. O GTV primário foi delineado em vermelho, o GTV nodal maior em laranja (45 Gy) e o menor em verde (40 Gy). Após a SBRT cervical, iniciou terapia sistêmica de segunda linha para o tumor pulmonar. Sem evidência de doença cervical em 18 meses, tolerando todas as texturas de alimento sem dor.
Tumores primários de parótida constituem outra indicação relevante. Um paciente de 91 anos com paralisia do nervo facial por carcinoma pouco diferenciado da parótida esquerda e dois linfonodos retrofaríngeos recebeu 50 Gy em cinco frações. Alcançou resposta clínica completa com retorno da função do nervo facial. Um ectrópio paralítico menor do olho seria tratado com cantotomia e cantopexia. Sem evidência de doença em 6 meses.
A doença oligometastática adjacente a estruturas neurológicas críticas também pode ser abordada. Uma paciente de 55 anos com metástase solitária irressecável de câncer colorretal na fossa supraclavicular — uma massa de 6 cm — teve a RM de simulação utilizada para diferenciar o GTV do plexo braquial, permitindo tratamento seguro com 45 Gy em cinco frações, duas por semana. A massa recidivou 3 anos depois no pescoço esquerdo.
Avaliação Pós-Tratamento e Resposta Tardia
A taxa de regressão após SBRT é variável, e a resposta máxima frequentemente é alcançada além dos cronogramas tradicionais — tipicamente após 3 meses. Avaliações de resposta precoces podem ser enganosas e gerar ansiedade desnecessária.
Um caso de imagem discordante pós-tratamento ilustra bem este ponto: paciente de 83 anos tratada cirurgicamente há 3 anos por carcinoma espinocelular da língua direita apresentou massa nodal dolorosa no nível II direito, profunda à parótida e estendendo-se para o espaço parafaríngeo e bainha carotídea. Recebeu 45 Gy em cinco frações, com delineamento do GTV auxiliado por fusão com RM. Apesar de melhora da dor, a RM em 4 meses mostrou possível progressão em T1 mas resposta em T2. Aos 9 meses, a RM demonstrou estabilidade da doença com paciente sem dor. Esse caso reforça a necessidade de paciência e correlação clínica nas avaliações pós-SBRT.
Para uma visão completa sobre delineamento de volumes-alvo em diversas topografias oncológicas, confira nosso guia completo sobre delineamento de volume alvo e planejamento de campos. Veja também nosso artigo sobre radioterapia vertical Marie da Leo Cancer Care, outra abordagem inovadora no campo da radioterapia moderna.