WBRT versus Radiocirurgia nas Metástases Cerebrais
A decisão entre irradiação total do encéfalo (WBRT) e radiocirurgia estereotáxica (SRS) depende de fatores como número e volume das metástases, status de performance e perfil molecular. Ferramentas prognósticas como o Graded Prognostic Assessment (GPA) molecular auxiliam nessa tomada de decisão. Na prática clínica, a SRS preserva melhor a função neurocognitiva e a qualidade de vida do paciente, enquanto a WBRT melhora as taxas de controle intracraniano distante e global.
Essa distinção importa muito na hora de discutir com o paciente e a equipe multidisciplinar — cada abordagem carrega trade-offs reais que afetam desfechos funcionais a longo prazo. O GPA molecular incorpora fatores como histologia do tumor primário, número de metástases, presença de mutações acionáveis e status de performance Karnofsky, oferecendo estratificação prognóstica mais refinada do que escalas antigas baseadas apenas em RPA.
Para uma visão completa das técnicas de delineamento em radioterapia, confira nosso guia completo sobre delineamento de volume alvo.
WBRT: Princípios de Planejamento e Delineamento
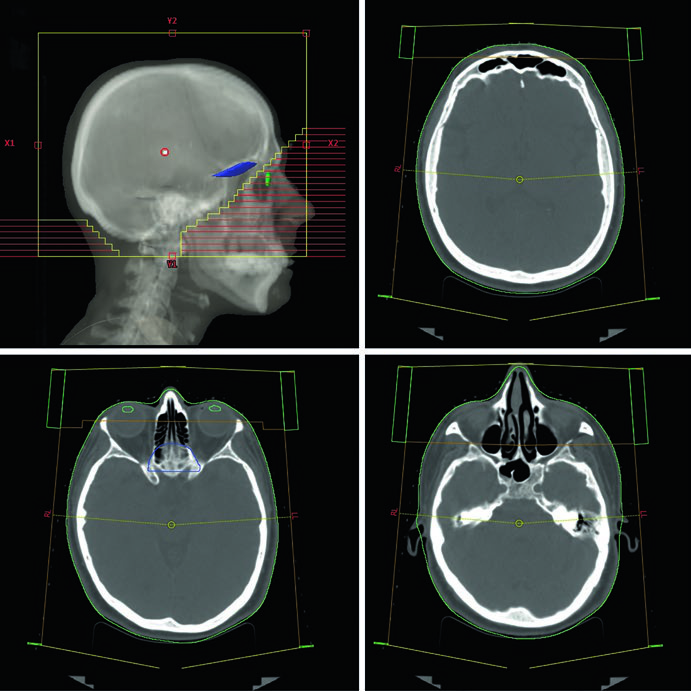
O planejamento da WBRT convencional utiliza 3D-CRT com feixes laterais opostos de fótons de 6 MV. Os feixes são levemente rotacionados em oblíquo anterior direito e esquerdo (RAO/LAO) para evitar divergência nos cristalinos. O colimador multi-lâminas (MLC) bloqueia os cristalinos enquanto cobre adequadamente a placa cribiforme e os lobos temporais. Um detalhe técnico que faz diferença no dia a dia: o isocentro pode ser posicionado na linha média ao nível do canto do olho, eliminando a divergência do feixe para os olhos e cristalinos — uma alternativa prática à rotação dos feixes.
A TC de planejamento sem contraste vai do vértice até a coluna cervical superior, com espessura de corte axial ≤2,5 mm. O paciente fica em decúbito dorsal, cabeça em posição neutra, imobilizado com máscara termoplástica e campo de visão de 600 mm. A verificação de setup usa filmes ortogonais com imagem MV semanalmente na WBRT convencional. O kV diário fica reservado para WBRT baseada em IMRT, onde a precisão de entrega exige verificação mais frequente.
As bordas de campo na WBRT convencional seguem um padrão bem definido: superiormente, 2 cm de flash acima do vértice; posteriormente, 2 cm de flash com possível extensão cervical posterior; inferiormente, base de C1; e anteriormente, o MLC bloqueia desde o flash de 2 cm até a face anterior de C1, protegendo as parótidas e os cristalinos. A cobertura dos lobos temporais e da placa cribiforme é obrigatória em todos os cenários.
Cenários Clínicos e Campos Sugeridos para WBRT
O planejamento muda conforme o cenário clínico. Metástases difusas (numerosas ou “incontáveis”) e PCI para SCLC recebem campos convencionais. Doença leptomeníngea exige cobertura adicional dos nervos ópticos, região retroorbital e lâmina cribosa, com margens expandidas de 8–10 mm para penumbra e setup diário nos lobos temporais e placa cribiforme. A leucemia e o linfoma de SNC demandam inclusão da retina e, se houver envolvimento ocular confirmado por exame de lâmpada de fenda, cobertura dos globos oculares inteiros.
| Cenário | Campos | Volumes Alvo | Bordas de Campo |
|---|---|---|---|
| WBRT Convencional | 3D-CRT lateral oposta (RAO/LAO) | Conteúdo craniano inteiro | Sup: 2 cm flash; Post: 2 cm flash; Inf: base de C1; Ant: MLC bloqueia parótida e cristalinos |
| Doença Leptomeníngea | 3D-CRT lateral oposta | Conteúdo craniano + nervos ópticos + região retroorbital + lâmina cribosa | Lobos temporais e placa cribiforme com margem adicional de 8–10 mm para penumbra e setup |
| Linfoma/Leucemia de SNC | 3D-CRT lateral oposta | Conteúdo craniano + nervos ópticos + região retroorbital + retina ± globos inteiros | Posterior 1/3 dos globos se sem envolvimento ocular; globos inteiros se envolvimento confirmado |
| Scalp-Sparing | 3D-CRT lateral oposta | Conteúdo craniano inteiro | Borda do MLC posicionada na tábua externa da calvária |
| HA-WBRT | IMRT/VMAT | CTV: parênquima cerebral até o forame magno; PTV: CTV menos (hipocampos + 5 mm) | Sem margem de setup adicional |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.1)
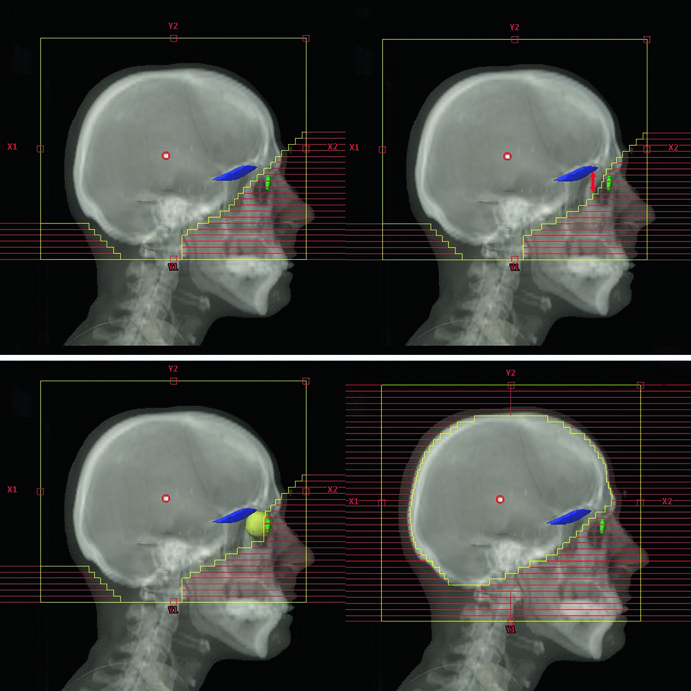
A técnica de scalp-sparing merece menção especial: o resultado cosmético é prioridade aqui, mas o método pode produzir um efeito de “Mohawk invertido” na alopécia — algo que vale discutir com o paciente antes do tratamento para alinhar expectativas. Nesta técnica, a borda do MLC é posicionada na tábua externa da calvária em vez do flash convencional de 2 cm, reduzindo a dose no couro cabeludo mas mantendo cobertura adequada do parênquima cerebral.
Dose e Fracionamento na WBRT
O fracionamento varia conforme a indicação clínica e o prognóstico do paciente. O esquema mais comum para metástases cerebrais e doença leptomeníngea é 30 Gy em 10 frações. A reirradiação com WBRT é possível com 20–25 Gy em 10 frações, mas exige intervalo mínimo de 4–6 meses entre os cursos para permitir recuperação do tecido neural.
| Cenário Clínico | Dose e Fracionamento |
|---|---|
| WBRT / Doença leptomeníngea | 30 Gy / 10 fx (mais comum), 37,5 Gy / 15 fx (RTOG), 30 Gy / 12 fx, 20 Gy / 5 fx (prognóstico ruim) |
| WBRT reirradiação | 20–25 Gy / 10 fx (intervalo mínimo de 4–6 meses) |
| PCI para SCLC | 25 Gy / 10 fx (mais comum) |
| Profilaxia SNC para LLA | 12 Gy / 8 fx |
| Leucemia SNC (alto risco) | ≥18 Gy / 9–10 fx (dose baseada na intensidade da terapia sistêmica) |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.2)
Preservação Hipocampal na WBRT (HA-WBRT)
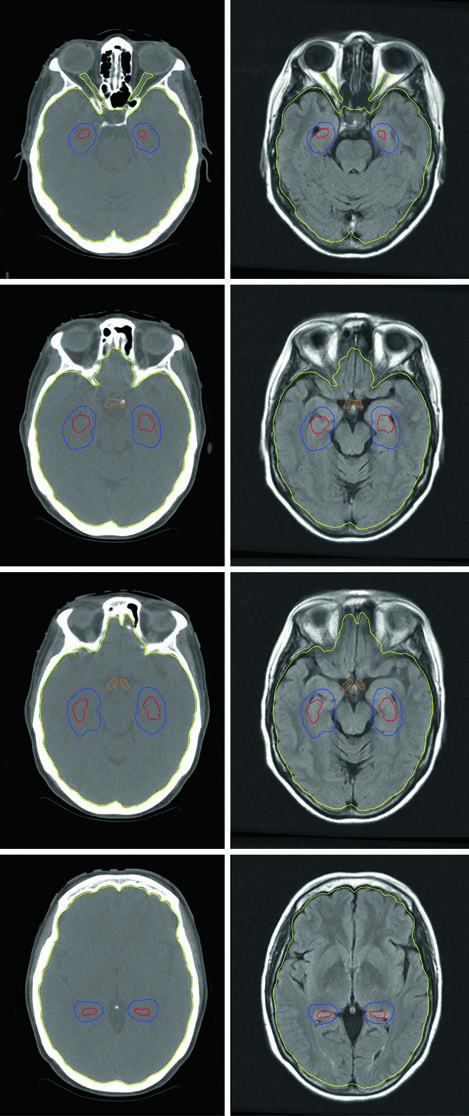
Estratégias para preservar a função neurocognitiva incluem a adição de memantina e/ou a técnica de HA-WBRT. A preservação hipocampal é particularmente relevante porque a neurogênese adulta ocorre na zona subgranular (SGZ) do hipocampo — a irradiação dessa região contribui significativamente para o declínio cognitivo pós-WBRT, especialmente memória e aprendizado verbal.
O planejamento da HA-WBRT requer IMRT com planejamento inverso, usando TC de planejamento fusionada com RM contrastada com gadolínio. A sequência utilizada é spoiled gradient tridimensional com espessura de corte axial de 1,25–1,5 mm para definir a região de exclusão hipocampal com precisão adequada. Segundo as diretrizes de contorno do RTOG 0933, apenas a porção SGZ dos hipocampos é contornada (não a estrutura inteira), e uma expansão volumétrica de 5 mm é aplicada para criar a zona de exclusão. O PTV consiste no tecido cerebral inteiro (parênquima até o forame magno) menos os hipocampos expandidos, sem margem de setup adicional.
As restrições de dose são rigorosas e variam conforme a indicação. Para metástases cerebrais: hipocampos D100% ≤9 Gy, Dmax ≤16 Gy; nervos ópticos e quiasma Dmax ≤30 Gy. Para PCI de SCLC com preservação hipocampal, os limites ficam ainda mais apertados: hipocampos D100% ≤7,5 Gy, Dmax ≤13,5 Gy; nervos ópticos e quiasma Dmax ≤25 Gy. Uma limitação importante que precisa ser avaliada na seleção do paciente: lesões localizadas a menos de 5 mm do hipocampo excluem o paciente da HA-WBRT.
SRS: Princípios de Planejamento e Delineamento do Alvo
A radiocirurgia estereotáxica abrange cenários de fração única e SRS fracionada (2–5 frações) tanto para metástases intactas quanto para cavidades pós-ressecção. Os instrumentos disponíveis incluem sistemas baseados em frame ou frameless com Gamma Knife (cobalto-60) e sistemas baseados em LINAC. Cada plataforma tem suas particularidades: no Gamma Knife, PTV = CTV sem expansão adicional; em sistemas LINAC, uma pequena margem de PTV pode ser necessária dependendo da precisão mecânica do sistema e do protocolo de verificação de imagem.
O delineamento do volume alvo e o planejamento utilizam RM volumétrica contrastada ponderada em T1 com cortes de 1–2 mm preferencialmente. Quando o paciente não tolera RM ou possui dispositivo implantado incompatível, TC contrastada é a alternativa. Para SRS baseada em LINAC, uma TC de corte fino é adquirida e corregistrada com a RM para cálculo dosimétrico preciso. Imagem diária é obrigatória em sistemas LINAC.
Delineamento do Volume Alvo na SRS
O delineamento varia significativamente entre metástases intactas e cavidades pós-cirúrgicas. Para lesões intactas, o processo é direto: o GTV é a lesão captante de contraste na sequência T1 da RM, e o CTV é GTV + 0 mm — sem margem adicional. Já para cavidades pós-ressecção, existem dois métodos bem estabelecidos na literatura, cada um com filosofia distinta de margem.
| Alvo | GTV | CTV |
|---|---|---|
| Metástases não ressecadas | Lesão captante de contraste na RM T1 | GTV + 0 mm |
| Cavidade pós-ressecção (Método 1 — Soltys et al.) | n/a | Margem de expansão de 2 mm uniforme ao redor das bordas da cavidade de ressecção visualizadas na RM pós-contraste |
| Cavidade pós-ressecção (Método 2 — Soliman et al.) | n/a | Toda região captante + cavidade + trajeto cirúrgico na RM pós-operatória; 5–10 mm ao longo do retalho ósseo se contato dural prévio; 1–5 mm se sem contato dural; 1–5 mm ao longo do seio venoso se contato prévio |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.3)
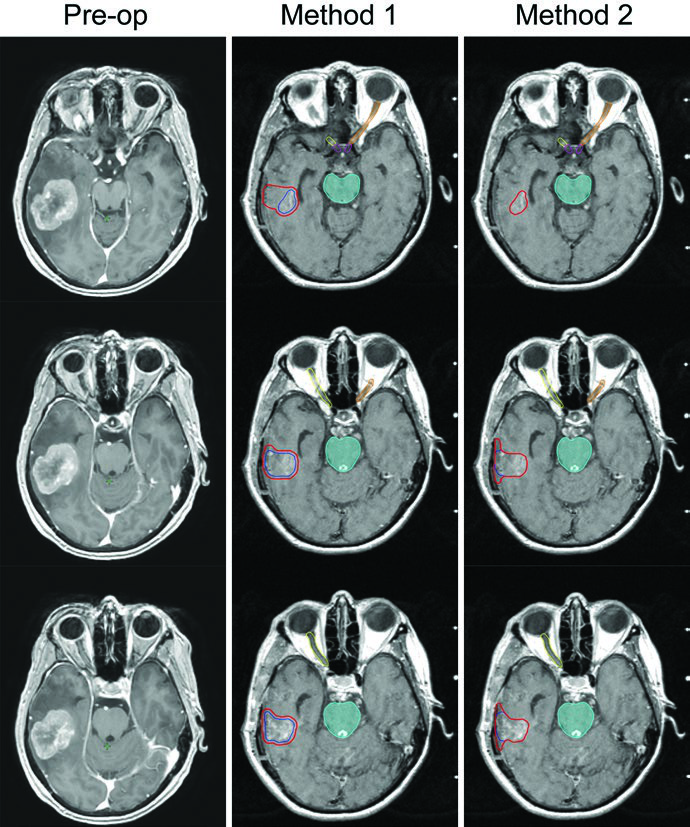
O Método 2 de Soliman et al. é mais conservador e tende a gerar volumes de CTV maiores. No exemplo da figura, uma cavidade de 24 mm no lobo temporal esquerdo — após ressecção total de metástase de 33 mm de câncer retal primário com contato dural pré-operatório mas sem contato com seio venoso — receberia margem de 10 mm ao longo do retalho ósseo. A fração única foi escolhida pelo tamanho pequeno da cavidade (<3 cm) e distância suficiente de estruturas cerebrais delicadas. No Gamma Knife, PTV = CTV sem expansão adicional. O Método 1 (Soltys) aplica simplesmente 2 mm uniformes ao redor da cavidade visualizada na RM T1 pós-gadolínio, resultando em volume menor e potencialmente menos toxicidade.
Dose e Restrições de Órgãos em Risco na SRS
A dose na SRS depende do tamanho ou volume da lesão e da distância de estruturas críticas. Os esquemas de fracionamento abaixo baseiam-se no protocolo Alliance A071801, que oferece orientação para cavidades pós-operatórias e metástases intactas em 1, 3 ou 5 frações.
| Parâmetro | 1 Fração | 3 Frações | 5 Frações |
|---|---|---|---|
| Dose PTV — cavidade pós-op | 20 Gy (<4,2 cm³), 18 Gy (4,2–8,0 cm³), 17 Gy (8,0–14,4 cm³), 15 Gy (14,4–20 cm³), 14 Gy (20–30 cm³), 12 Gy (≥30 cm³ a <5 cm) | 27 Gy (<30 cm³) | 30 Gy (≥30 cm³ a <5 cm) |
| Dose PTV — metástases intactas | 24 Gy (<1 cm), 22 Gy (1,0–2,0 cm), 18 Gy (2,0–3,0 cm), 15 Gy (3,0–4,0 cm) | 27 Gy | 30 Gy |
| Tronco cerebral | V12 Gy < 1 cm³ | 23,1 Gy máx; V18 Gy < 0,5 cm³ | 28 Gy máx; V23 Gy < 0,5 cm³ |
| Aparato óptico | 9 Gy máx | 17,4 Gy máx; V13,8 Gy < 0,2 cm³ | 23 Gy máx; V20 Gy < 0,2 cm³ |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.4 — baseado no protocolo Alliance A071801)
A escolha entre fração única e fracionada depende fundamentalmente do tamanho da lesão e da proximidade de estruturas nobres. Lesões pequenas (<3 cm) com distância suficiente de estruturas delicadas recebem fração única com doses mais altas. Cavidades maiores (≥30 cm³) e lesões próximas ao tronco cerebral ou aparato óptico beneficiam-se do fracionamento em 3–5 frações, que permite entrega de dose total efetiva elevada enquanto respeita os limites de tolerância dos órgãos em risco através da reparação celular entre frações.
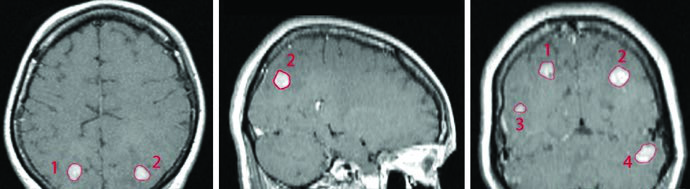
A SRS de múltiplos isocentros permite tratar simultaneamente lesões em diferentes localizações — como nos lobos parietais, temporal e cerebelo — em uma única sessão de tratamento. No exemplo do livro, quatro metástases de câncer de mama (volumes de 0,07 a 1,92 cm³, diâmetros de 6 a 20 mm) foram tratadas com fração única em paciente que já recebera WBRT prévia de 30 Gy em 10 frações. O GTV de cada lesão foi definido pela captação de contraste na RM T1 pós-gadolínio, e com Gamma Knife, PTV e CTV utilizaram expansão de 0 mm a partir do GTV.
Para se aprofundar em outros temas de delineamento cerebral, confira os artigos sobre tumores benignos do SNC e tumores malignos do SNC da mesma série.