O carcinoma hepatocelular exige delineamento em radioterapia antes mesmo do primeiro contorno. O capitulo deixa isso claro logo na abertura: a qualidade do plano depende de TC trifasica com contraste, avaliacao clinica completa, leitura disciplinada da invasao vascular, imobilizacao confiavel e uma estrategia respiratoria que consiga reproduzir a posicao do figado ao longo de todo o tratamento. Para encaixar este capitulo no panorama maior da especialidade, vale consultar tambem nosso guia completo sobre delineamento de volume alvo e campos na radioterapia.
Esse ponto merece atencao porque o figado nao se comporta como um alvo estatico. A fase arterial mostra melhor o tumor viavel, a fase portal ajuda a reconhecer os limites anatomicos guiados pelos vasos intra-hepaticos, a fase tardia mostra melhor a extensao para a veia cava inferior e o movimento respiratorio desloca tudo isso durante simulacao e tratamento. O capitulo de hepatocarcinoma trabalha justamente nessa intersecao entre imagem, movimento e risco microscopico. O resultado e um raciocinio de planejamento muito mais util do que uma lista solta de margens.
Carcinoma hepatocelular: principios do delineamento
A resposta direta do capitulo e simples: em carcinoma hepatocelular, a tecnica deve proteger figado normal sem perder a coerencia anatomica do alvo. Por isso step-and-shoot IMRT e volumetric modulated arc therapy continuam como tecnicas padrao quando o numero de angulos, ou a extensao do arco, e limitado para reduzir a disseminacao de baixa dose sobre o parenquima nao acometido.
O texto tambem define quando SBRT ganha preferencia. O esquema com ate 5 ou 6 fracoes e favorecido quando ha poupanca intestinal segura, disponibilidade de alta taxa de dose, imobilizacao adequada e image guidance confiavel. Nao e uma recomendacao abstrata. O capitulo condiciona SBRT a um cenario em que o time consiga verificar o posicionamento e manter a proximidade com o trato gastrointestinal sob controle. Quando o tumor se aproxima de tecidos gastrointestinais luminais, o tratamento hipofracionado pode ser escolhido exatamente por causa dessa relacao anatomica.
Na pratica, essa abertura organiza todo o restante do capitulo. A escolha tecnica nao vem depois do contorno; ela ja nasce da combinacao entre volume, orgaos de risco e reproducibilidade. Isso explica por que o texto insiste tanto em respiracao, posicao de simulacao e fusao de imagens. Sem essas pecas, a margem deixa de refletir o caso real e passa a ser apenas um numero defensivo.
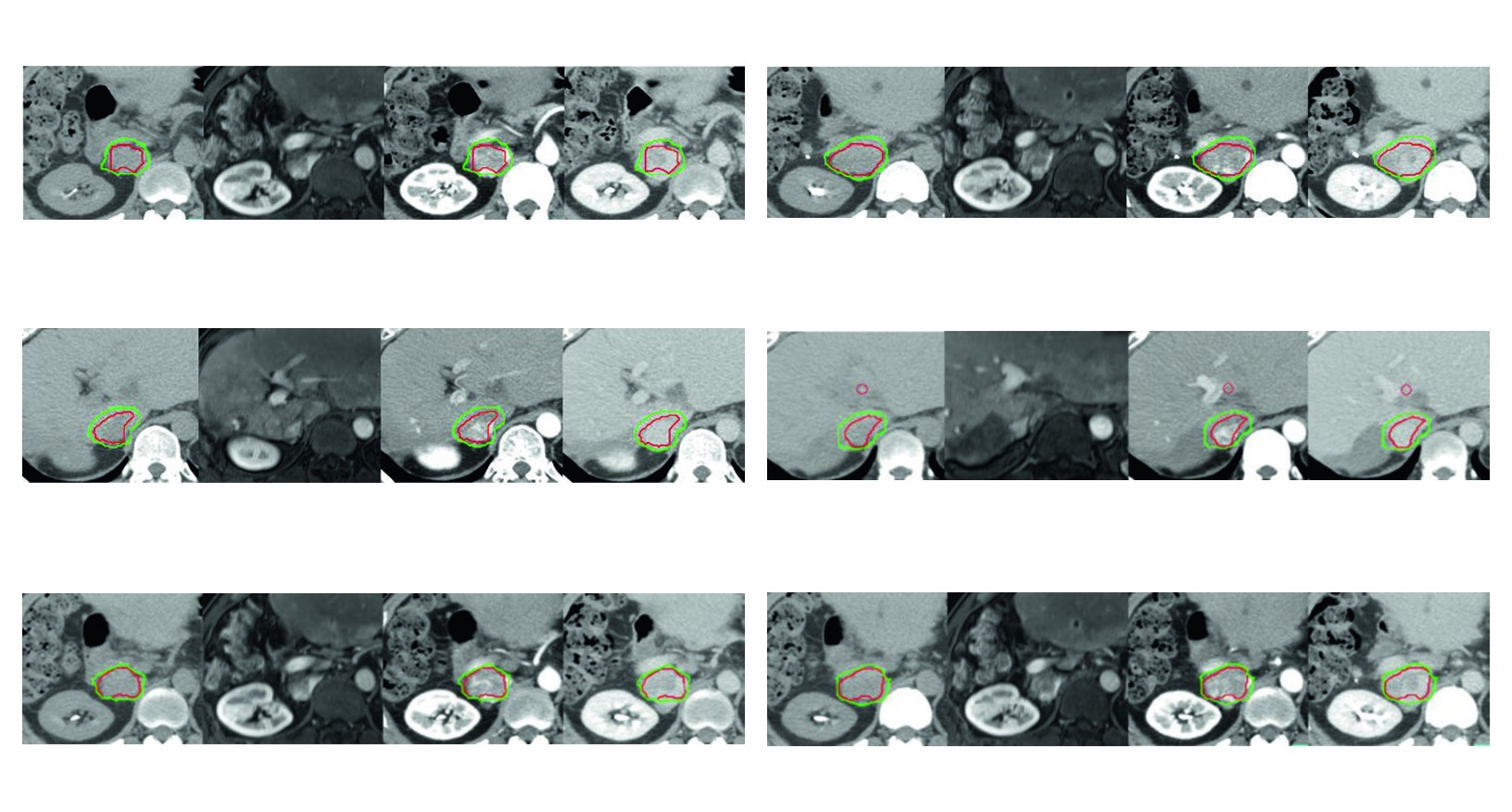
A Figura 17.1 ajuda a enxergar esse raciocinio desde cedo. O caso de tumor residual apos quimioembolizacao arterial transcateter e radiofrequencia mostra que o GTV pode incluir nao apenas o tumor contrastado, mas tambem trombose invadida da veia cava inferior. O CTV, nesse exemplo, recebe margem de 5 mm dentro do limite hepatico e 3 mm ao redor do componente intravascular. O livro nao apresenta a expansao como automatica. Ele mostra uma margem que conversa com a anatomia da recidiva tratada.
Imagem trifasica e estadiamento para planejar com seguranca
O capitulo pede uma base clinica completa antes da simulacao. Historia, exame fisico, exames laboratoriais, avaliacao da funcao hepatica e estudos de imagem entram na mesma etapa porque todos influenciam diagnostico, estadiamento e planejamento. Em hepatocarcinoma, separar essas decisoes costuma gerar erro. O volume a ser tratado depende da biologia do caso e do quanto o figado restante consegue tolerar.
O exame central e uma TC contrastada do figado, de preferencia trifasica, com fases arterial, portal-venosa e tardia, obtida com espessura de corte de 3 a 5 mm. Esse detalhe numerico importa. Cortes nessa faixa permitem leitura adequada do realce tumoral e das relacoes vasculares sem abrir mao de resolucao suficiente para a fusao com a simulacao. O livro nao trata a TC trifasica como opcao elegante. Ela e o eixo da definicao do alvo.
A ressonancia magnetica dinamica multifasica entra como complemento quando o paciente consegue manter a apneia necessaria para aquisicao, ou quando o contraste da TC e contraindicado. Com fusao de imagens, a RM pode ser complementar a TC no delineamento. Esse verbo, complementar, e importante. O capitulo nao substitui um exame pelo outro; ele usa cada modalidade para responder perguntas diferentes dentro do mesmo caso.
O PET aparece de forma mais seletiva. Imagens com 18F-FDG e com outros tracadores, como 11C-acetato e 11C-colina, podem ajudar a localizar tumor viavel em casos individuais, sobretudo quando ha doenca residual ou recorrente em areas de retencao previa de lipiodol e ou em zonas tratadas por radiofrequencia. Essa observacao e clinicamente util porque impede o uso indiscriminado do PET. O livro o reserva para situacoes em que a duvida principal e onde ainda existe tumor viavel.
Se voce quiser comparar essa logica com outro sitio abdominal da mesma serie, vale ler tambem nosso artigo sobre cancer de pancreas e delineamento na radioterapia. A vantagem dessa comparacao e perceber que, no abdome superior, a decisao de imagem e de controle respiratorio pesa tanto quanto a geometria do campo.
Outro merito do capitulo e mostrar que cada fase de contraste tem uma funcao propria. Em vez de pedir uma unica imagem que resolva tudo, o texto distribui tarefas entre as fases. Isso torna o planejamento mais coerente e ajuda a evitar uma falha comum: desenhar margem em cima de uma leitura incompleta do comportamento tumoral.
Imobilizacao e controle do movimento hepatica
O capitulo nao trata manejo do movimento como refinamento opcional. Ele diz de forma objetiva que e necessaria imobilizacao de meio corpo ou de corpo inteiro com controle respiratorio para melhorar a reprodutibilidade. Dispositivos como vacuum bag ou chest board podem ser usados, idealmente com os bracos elevados, tanto na simulacao quanto durante todo o tratamento.
Existem duas razoes para essa recomendacao. A primeira e geometrica: manter a mesma configuracao ao longo das fracoes. A segunda e mecanica: preservar liberdade espacial para os feixes. O livro ainda acrescenta um criterio que costuma passar despercebido em textos mais resumidos. O sistema de imobilizacao nao deve atenuar a dose de radiacao nem interferir nas posicoes de gantry necessarias para feixes coplanares ou nao coplanares.
Na sequencia, o capitulo entra no ponto mais delicado do tratamento do figado: o movimento respiratorio. A apneia ativa ajuda a reduzir o volume tratado e e preferivel para pacientes que conseguem sustentar mais de 30 segundos de apneia. Esse numero nao aparece por acaso. Ele funciona como um limiar pratico para saber se a estrategia vai gerar imagens uteis e um tratamento reprodutivel.
Quando a apneia nao e tolerada, a compressao abdominal pode ser usada. O texto, porem, nao romantiza essa escolha. Ele ressalta que a compressao pode deformar o abdome ou alterar a forma dos orgaos. Em outras palavras, nao basta reduzir amplitude de movimento; e preciso aceitar que a forma do alvo pode mudar no processo. Isso explica por que o delineamento costuma ser feito em imagens multifasicas e multimodais obtidas em apneia, reproduzindo o mais fielmente possivel a forma diagnostica do HCC.
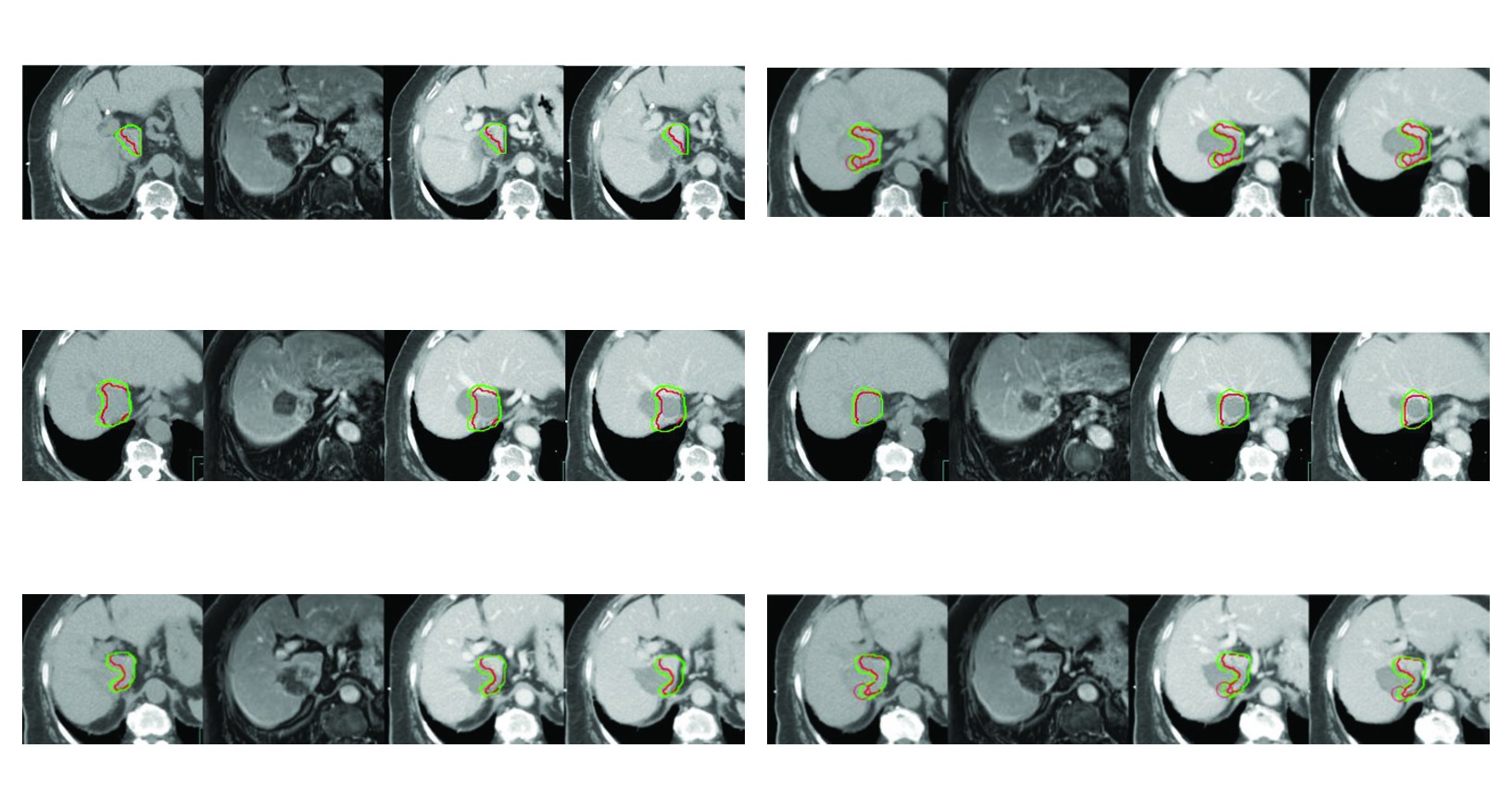
Image-guided radiation therapy e tratada como obrigatoria para compensar mudancas intra e interfaccionais na posicao do figado. Para pacientes que nao toleram controle respiratorio voluntario, o uso de compressao abdominal passiva associado a 4DCT fornece informacao sobre movimento interno e pode compensar mudancas de posicao hepatico. O tratamento com gating tambem pode ser util nesses doentes, embora prolongue a duracao da sessao porque trabalha dentro de uma janela inspiratoria ou expirataria selecionada.
A Figura 17.2 reforca por que esse cuidado e central. O caso de recorrencia com trombose parcial da veia cava inferior apos radiofrequencia repetida so se torna bem delimitado porque a simulacao trifasica foi obtida com coordenacao de apneia para imobilizacao hepatica. O CTV inclui o tumor contrastado, o trombo tumoral visto como GTV e ainda uma margem de 5 mm ao redor do GTV dentro do limite do figado e da zona previamente ablada quando isso e clinicamente necessario. E um excelente exemplo de movimento e historia de tratamento alterando o volume final.
TC de simulacao e leitura especifica de cada fase
A simulacao precisa ser feita com contraste intravenoso e aquisicao multifasica, sempre com o paciente em posicao de tratamento e com coordenacao respiratoria. O livro insiste nisso porque o alvo nao deve nascer de uma anatomia generica. Ele precisa ser contornado na mesma condicao geometrica em que sera tratado. Esse alinhamento entre imagem diagnostica, posicao de simulacao e estrategia respiratoria e um dos pilares práticos do capitulo.
A fusao entre as diferentes fases da simulacao e, quando necessario, com imagens diagnosticas auxilia a definicao do GTV. O HCC viavel costuma ser melhor visualizado, e mais brilhante, na fase arterial. Nas fases venosa e tardia ele mostra menor realce em relacao ao figado. Essa sequencia de realce seguido de washout nao serve apenas para diagnostico. No planejamento, ela ajuda a separar o tumor viavel das alteracoes adjacentes tratadas previamente.
A fase portal tem outro papel. O capitulo explica que ela deve ser usada com a distribuicao dos vasos intra-hepaticos para reconhecer os limites anatomicos do tumor tratado, especialmente quando a forma do figado esta deformada pela imobilizacao e pelo controle respiratorio. Quando a pergunta clinica e invasao de estruturas vasculares, a fase portal-venosa e a mais util. Se a preocupacao e a extensao do comprometimento para a veia cava inferior, a fase tardia mostra melhor esse alcance.
Essa distribuicao de funcoes entre as fases e uma das melhores lições do texto. O capitulo nao tenta fazer a fase arterial resolver tudo nem transforma a fase portal em mera confirmacao. Cada fase responde a uma parte do problema: uma mostra melhor o tumor viavel, outra define barreiras anatomicas e a outra esclarece a extensao venosa maior. Em planejamento de carcinoma hepatocelular, essa disciplina na leitura costuma ser mais valiosa do que acrescentar margem sem criterio.
GTV, CTV e PTV no carcinoma hepatocelular
O capitulo reconhece que, em circunstancias especificas de SBRT, apenas o tumor visivel pode ser tratado como GTV. Essa e a excecao descrita no texto. O comportamento mais comum e ampliar o GTV para constituir o CTV de acordo com o risco clinico de disseminacao microscopica dentro do parenquima hepatico, incluindo areas ao redor de uma zona previa de radiofrequencia ou de embolizacao.
Ao mesmo tempo, o livro avisa que o CTV nao e um objeto fixo. Ele pode variar de tamanho e de posicao por causa do movimento respiratorio e da dinamica dos orgaos. Essa observacao muda a forma de ler qualquer tabela de margens. O valor numérico so faz sentido quando esta amarrado ao controle respiratorio realmente obtido e ao comportamento geometrico do figado naquele paciente.
Tabela 17.1. Volumes sugeridos nas regioes de GTV e CTV
Essa tabela concentra a parte operacional do capitulo. Ela separa doenca macroscopica visivel, extensao contigua tratada como macroscópica, risco microscopico opcional e a expansao final de planejamento. Lida com calma, ela mostra que o livro nao mistura doenca evidente com cobertura eletiva por habito.
| Volume alvo | Definicao e descricao |
|---|---|
| GTVa | Tumor hepatico: tumor intra-hepatico com realce na TC contrastada em fase arterial e washout na TC venosa ou tardia. Lipiodol retido: lipiodol branco contiguo ao tumor que realca. Tumor refratario apos ablacao: tumor com realce arterial adjacente a zona ablada hipodensa. Trombo tumoral vascular: trombo com realce arterial e washout na fase venosa. |
| CTVmacroscopica | Tumor hepatico: o tumor intra-hepatico com realce na fase arterial. Zona embolizada contigua ao tumor que realca incluida no GTV. Tumor com realce arterial adjacente a zona ablada hipodensa. Trombo tumoral vascular com realce arterial. |
| CTVmicroscopic eletivob | Margem de 3 a 5 mm ao redor do GTV intra-hepatico. Margem opcional de 2 a 3 mm ao redor do GTV de trombo tumoral dentro do vaso, de acordo com indicacao clinica ou protocolo. Trombo bland adjacente ao GTV de trombo tumoral. Zona de radiofrequencia adjacente ao GTV. Zona embolizada nao diretamente adjacente ao GTV. O CTV nao deve cruzar barreiras naturais, como a superficie ou o limite do figado. |
| PTV | CTV, ou GTV/CTVmacroscopic, acrescido de 5 a 20 mm, podendo ser assimetrico, conforme a imobilizacao e o controle respiratorio. O movimento interno de orgaos e o erro de setup formam a base do PTV. O 4DCT adquirido em todas as fases respiratorias pode ajudar a definir o PTV e cobrir a extensao do movimento interno. |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 17.1)
Notas da tabela: a GTV e CTV macroscópico podem ser tratados, por exemplo, com 45 a 54 Gy em 3 a 6 fracoes, lembrando que a dose segura pode precisar ser reduzida se os tecidos normais limitarem o plano. b O CTV eletivo ou microscópico pode ser tratado, por exemplo, com 24 a 30 Gy em 3 a 6 fracoes; o proprio texto acrescenta que a autora L.A.D. nao recomenda rotineiramente um CTV microscópico ao redor do GTV. c A margem adicional ao redor do GTV intra-hepatico pode receber dose macroscópica, ou mais alta, se isso for seguro.
Esse comentario final e valioso porque evita transformar a tabela em protocolo cego. O livro oferece um quadro de referencia, mas admite que o CTV microscópico e opcional e pode nao ser rotina. Tambem lembra que dose e margem precisam respeitar a tolerancia dos tecidos normais. Em hepatocarcinoma, esse equilibrio pesa tanto quanto a vontade de cobrir extensao subclinica.
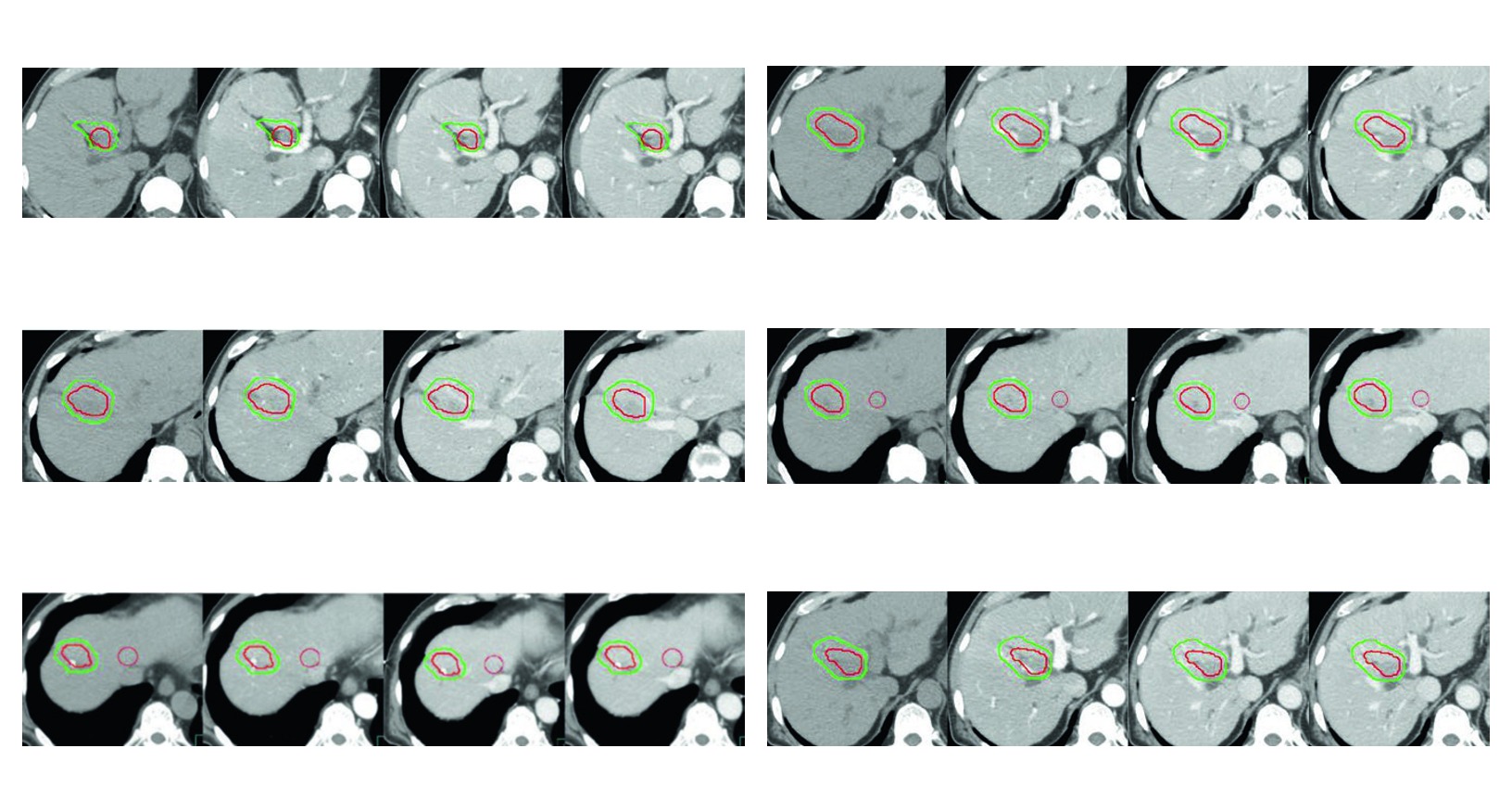
A Figura 17.3 traduz bem essa filosofia. O caso de recorrencia apos cirurgia e radiofrequencia, com alto risco de lesao de ducto biliar pela ablacao, usa simulacao com fases sem contraste, arterial, portal e venosa tardia, sempre em apneia. O CTV em verde inclui o tumor contrastado mostrado como GTV em vermelho, uma margem de 5 mm no parenquima hepatico e uma margem intravascular de 3 mm ao redor do GTV. Nao ha expansao gratuita. Ha resposta a um contexto clinico especifico.
O que as quatro figuras ensinam ao planejamento
As quatro figuras do capitulo funcionam como exemplos aplicados da mesma logica. Todas usam simulacao multiphasica com coordenacao de apneia para imobilizacao do figado. Todas mostram GTV em vermelho e CTV em verde. E todas deixam claro que a margem muda quando entram em cena trombo tumoral, zona previamente ablada, area embolizada ou risco de extensao ao longo do vaso.
Figura 17.1
No primeiro caso, o alvo residual apos quimioembolizacao e radiofrequencia inclui tambem trombose invadida da veia cava inferior. Isso ensina que, quando a doenca ultrapassa o parenquima e entra no compartimento vascular, o planejamento precisa incorporar essa geometria e nao apenas o nodulo hepatico.
Figura 17.2
No segundo, a recidiva apos radiofrequencia repetida mostra como o volume pode incluir o leito previamente tratado quando ha necessidade clinica. A margem de 5 mm ao redor do GTV dentro do figado e da area ablada nao representa excesso. Ela reflete risco contiguo dentro de um contexto de tratamento anterior.
Figura 17.3
No terceiro, o risco biliar apos cirurgia e radiofrequencia reforca que delineamento e planejamento nao podem ser separados. O contorno ja nasce condicionado por uma historia local que influencia seguranca, distribuicao de dose e escolha de margem.
Figura 17.4
No quarto caso, o HCC refratario ao sorafenibe com progressao de tromboses em veia porta e veia hepatica media resume bem o capitulo. O CTV inclui o tumor contrastado, o GTV em vermelho e uma margem tridimensional de 5 mm dentro do limite hepatico. Aqui o livro mostra que, mesmo diante de invasao vascular importante, a expansao ainda precisa respeitar a fronteira anatomica do figado.
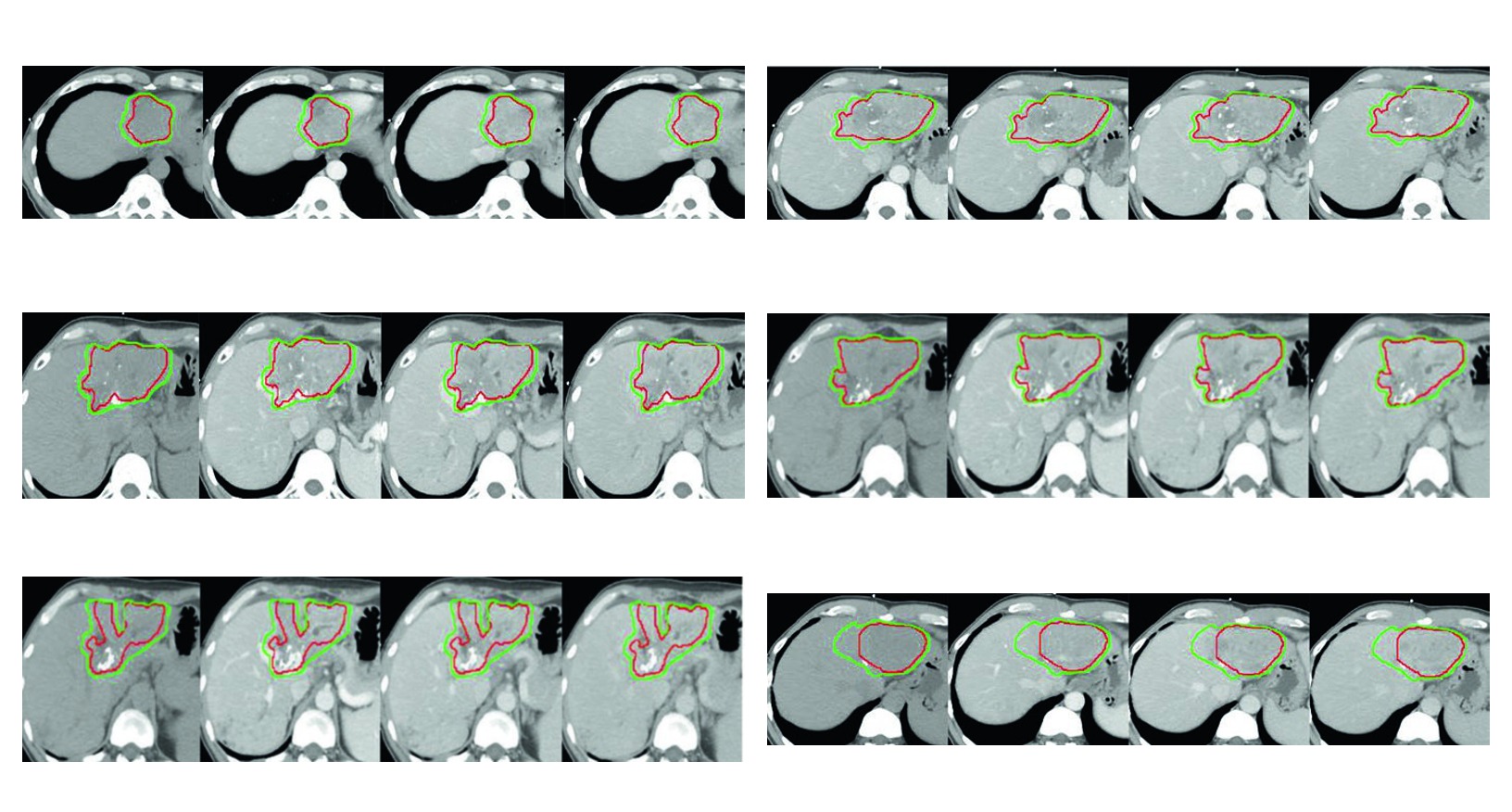
Lidas em conjunto, as figuras defendem uma mensagem muito consistente. A margem intraparenquimatosa cobre risco adjacente dentro do figado. A margem intravascular aparece quando o trombo tumoral faz parte real do problema geometrico. A zona ablada ou embolizada entra no volume quando o caso exige, nao por automatismo. Esse e provavelmente o trecho mais didatico do capitulo para quem precisa justificar o desenho final do volume em reuniao clinica ou revisao de caso.
Leituras citadas pelo capitulo e conclusao pratica
O fechamento do capitulo nao traz novos contornos, mas deixa claro de onde vem esse raciocinio. As referencias incluem radioterapia local com ou sem quimioembolizacao transarterial em doenca irressecavel, variabilidade interobservador e consensos para definicao de alvo com e sem trombo portal, atlas de orgaos de risco do abdome superior, comparacao entre protonterapia e radiofrequencia em recidiva, consensos APPLE sobre radioterapia e SBRT, estudos de SBRT individualizada, fatores associados a microinvasao e um ensaio randomizado que comparou quimioembolizacao transarterial mais radioterapia externa com sorafenibe em invasao vascular macroscopica.
O leitor sai do capitulo com uma regra de ouro bastante clara. Em carcinoma hepatocelular, delinear bem significa casar o realce correto com a fase correta, controlar o movimento respiratorio de modo reproduzivel e escolher margens que possam ser defendidas tanto pela anatomia quanto pela historia de tratamento. Quando essas tres camadas andam juntas, GTV, CTV e PTV deixam de ser siglas abstratas e passam a expressar a doenca real do paciente. Para retomar a visao global da serie, volte ao artigo principal sobre delineamento de volume alvo e campos na radioterapia.




