Neste Artigo
Indicações da IMRT Pós-Operatória em Câncer Ginecológico
A radioterapia pós-operatória com IMRT para câncer ginecológico reduz toxicidade gastrointestinal e geniturinária aguda em comparação à técnica 3D conformacional, conforme demonstrado em ensaio clínico randomizado de fase III (NRG Oncology-RTOG 1203). A qualidade de vida também melhora significativamente com IMRT, e o volume de medula óssea irradiada diminui de forma clinicamente relevante em pacientes com câncer de colo uterino e endométrio submetidas a radioterapia pélvica adjuvante.
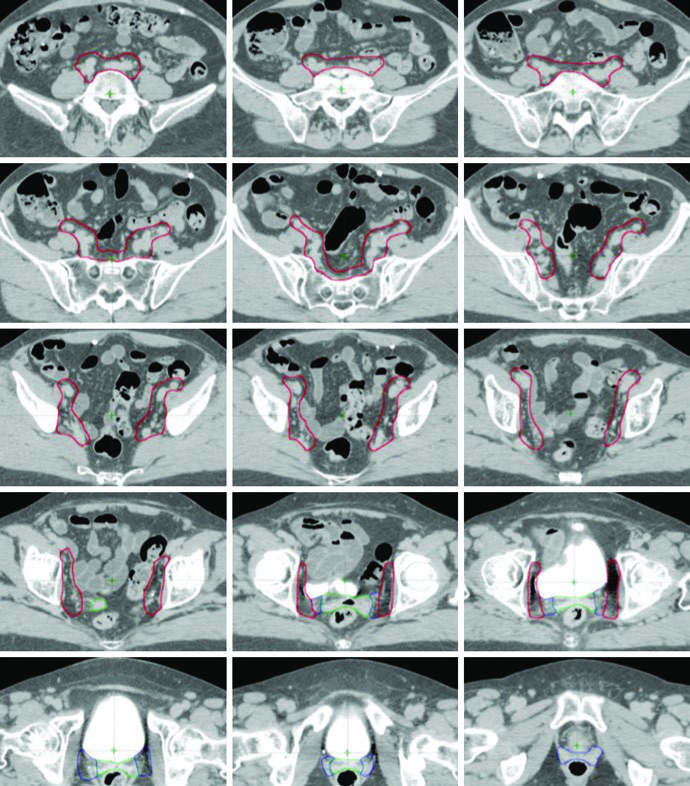
O paradigma de tratamento varia conforme o sítio da doença. No câncer cervical, a cirurgia é preferida para doença em estádio inicial, mas a radioterapia adjuvante é indicada em pacientes com fatores de alto risco: tamanho tumoral ≥4 cm, invasão do espaço linfovascular (LVSI), invasão estromal cervical profunda, margens positivas, envolvimento parametrial ou linfonodal. Já no câncer de endométrio, o tratamento padrão começa com histerectomia total abdominal ou laparoscópica com salpingo-ooforectomia bilateral (TAH ou TLH-BSO), seguida de radioterapia quando há fatores patológicos adversos — doença de alto grau, invasão miometrial profunda, extensão estromal cervical ou envolvimento linfonodal regional.
Para pacientes com câncer endometrial de alto risco de recorrência nodal — estádio I-II com histologia não endometrioide ou adenocarcinoma endometrioide grau 3 com invasão miometrial profunda — a radioterapia pélvica total é recomendada. Nos estádios III-IV, a irradiação pélvica total reduz o risco de recorrência pélvica e para-aórtica. Um ensaio de fase III comparando braquiterapia de cúpula vaginal com quimioterapia versus radioterapia pélvica isolada em pacientes de alto risco intermediário e alto risco não demonstrou superioridade com a adição de quimioterapia à braquiterapia, e a toxicidade aguda foi maior no braço com quimioterapia. Assim, a radioterapia pélvica total permanece eficaz e bem tolerada como tratamento adjuvante. Para uma visão geral de todos os sítios anatômicos, confira nosso guia completo sobre delineamento de volumes-alvo.
Pacientes de baixo risco em estádio inicial, adequadamente estadiadas cirurgicamente e com linfonodos negativos, podem receber apenas braquiterapia vaginal isolada.
Investigação Diagnóstica Relevante para Delineamento
Toda paciente com câncer ginecológico deve passar por anamnese completa e exame físico, incluindo exame pélvico e avaliação dos linfonodos inguinais e supraclaviculares como parte do diagnóstico e estadiamento iniciais. A investigação radiológica padrão inclui tomografia computadorizada (TC) para avaliar a extensão do envolvimento local e sítios de disseminação extrauterina.
Durante o exame pélvico, atenção especial deve ser dada à avaliação da cúpula vaginal, septo retovaginal, paramétrios bilaterais e paredes laterais da pelve. Se o desconforto da paciente impedir um exame completo, está indicado o exame sob anestesia. Pacientes com suspeita de envolvimento vesical ou retal devem ser submetidas a cistoscopia ou retossigmoidoscopia.
A PET/TC e a ressonância magnética (RM) da pelve são úteis em pacientes selecionadas para delinear volume tumoral bruto residual ou linfonodos envolvidos. A PET/TC é particularmente valiosa na investigação do câncer cervical para avaliar disseminação nodal para-aórtica e metástases a distância.
Simulação e Localização Diária
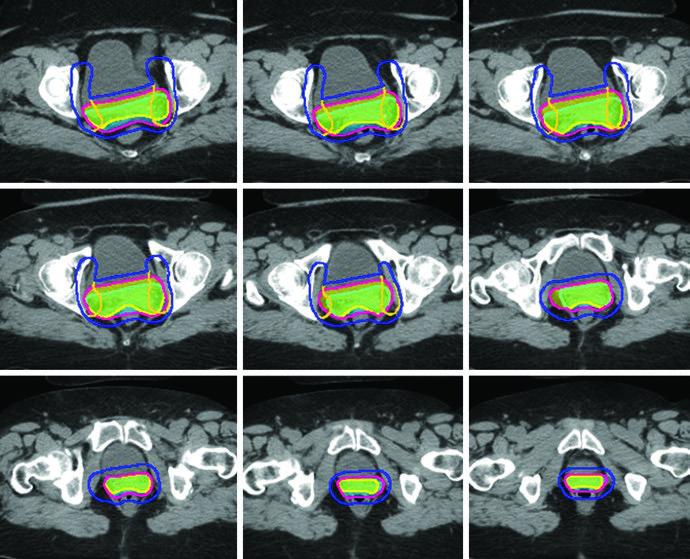
A simulação é realizada em decúbito dorsal. A imobilização da região inferior do corpo — e da região superior quando se utiliza campo estendido — com dispositivos tipo cradle ou Vac-Lok é recomendada. A TC de simulação deve ter espessura de corte ≤3 mm e é realizada com bexiga confortavelmente cheia e com bexiga vazia, permitindo a fusão dessas imagens para gerar um volume-alvo interno (ITV).
O contraste intravenoso é recomendado para identificar a vasculatura da paciente como substituto para os linfonodos, exceto quando contraindicado. Contraste oral para opacificar o intestino delgado como órgão de risco crítico também deve ser considerado. As pacientes devem esvaziar o reto na manhã da simulação e de cada fração de tratamento. Enema retal pode ser considerado.
Marcadores internos são essenciais: um marcador vaginal para identificar o ápice da vagina e um marcador no introito são padrão. A simulação com bexiga cheia e vazia permite gerar o ITV, que acomoda as variações de posição do alvo causadas pelo enchimento e esvaziamento vesical. As pacientes devem ser tratadas consistentemente com bexiga cheia ou vazia para minimizar o impacto do enchimento vesical sobre o movimento do alvo.
Para a localização diária, recomenda-se imagem ortogonal planar diária (MV ou kV). Imagem com cone beam CT (CBCT) semanal deve ser feita no mínimo para verificar o setup do tratamento; CBCT diário para monitorar variações no enchimento vesical e intestinal também pode ser realizado.
Delineamento de Volumes-Alvo e Planejamento do Tratamento
O delineamento pós-operatório de câncer cervical e endometrial utiliza múltiplos CTVs — CTV1, CTV2 e CTV3 — para permitir expansões anisotrópicas de CTV para PTV. Cada componente tem função anatômica e margem distintas, conforme definido no ensaio clínico randomizado TIME-C.
Definição dos Volumes-Alvo: CTV1, CTV2 e CTV3
| Volume | Definição | Expansão para PTV |
|---|---|---|
| CTV1 | Cúpula vaginal, incluindo tecido adiposo e partes moles anterior e posterior à cúpula entre a bexiga e o reto | 15 mm |
| CTV2 | Tecidos paravaginais/parametriais, vagina proximal (excluindo a cúpula) | 10 mm |
| CTV3 | Regiões nodais ilíaca comum, ilíaca externa e ilíaca interna — vasos pélvicos + expansão de 7 mm (excluindo osso, músculo e intestino), tecidos entre vasos ilíacos internos e externos, linfonodos pré-sacrais (tecidos moles anteriores ao S1-S2, mínimo 1,0 cm). Limite superior: 7 mm inferior ao interespaço L4-L5. Limite inferior: aspecto superior da cabeça femoral | 7 mm |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 20.1)
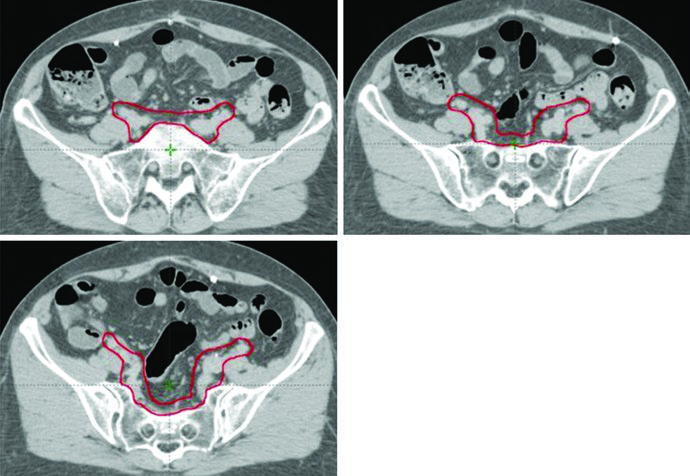
Em relação ao CTV1, a porção anterior do ligamento uterossacral é removida durante a histerectomia radical. Por isso, a fáscia mesorretal serve como estrutura substituta para a borda posterior da cúpula vaginal e do paramétrio no CTV. Boost vaginal pode ser considerado em pacientes de maior risco de recorrência por fatores como invasão estromal cervical, histerectomia supracervical, LVSI extenso ou envolvimento vaginal extenso.
No câncer de endométrio, o CTV3 é modificado para incluir a região pré-sacral quando há invasão estromal cervical. Nos casos com envolvimento patológico de linfonodos para-aórticos ou ilíacos comuns altos, utilizam-se campos estendidos pélvico-para-aórticos, com o limite superior do CTV estendendo-se ao interespaço T12-L1 ou L1-L2, ou à vasculatura renal.
Quando há envolvimento do terço distal da vagina, os linfonodos inguinais devem ser contornados continuamente desde os linfonodos ilíacos externos até 2 cm caudal à junção safeno-femoral.
Composição do PTV Final
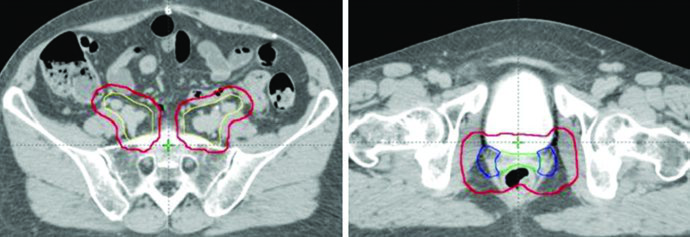
Os PTVs são criados para cada CTV com margens diferentes — 15 mm para CTV1, 10 mm para CTV2 e 7 mm para CTV3 — refletindo o grau de movimento interno e incerteza de setup de cada componente. O PTV final usado para planejamento é gerado pela união de PTV1, PTV2 e PTV3: PTV = PTV1 ∪ PTV2 ∪ PTV3.
Quando se utiliza a abordagem de ITV, o CTV1 e CTV2 devem ser contornados nas TC com bexiga cheia e vazia e fusionados para gerar o ITV. Uma expansão de 7 mm no ITV gera o PTV, que é combinado com o PTV3 para o PTV final. Essa estratégia é particularmente relevante porque a cúpula vaginal e os tecidos paravaginais sofrem deslocamento significativo com as variações de enchimento vesical.
Campos Estendidos e Boost com SIB
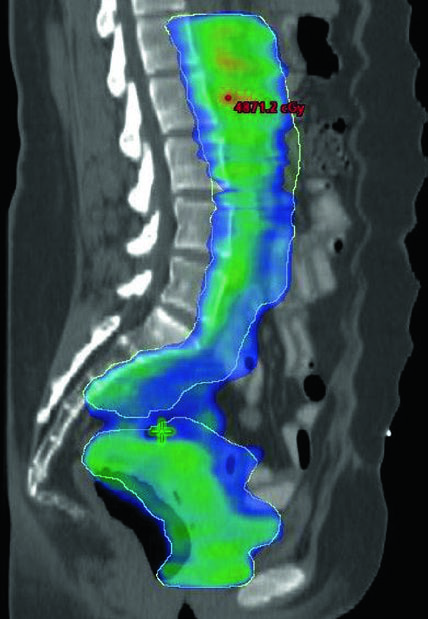
A radioterapia de campo estendido é frequentemente indicada quando há envolvimento patológico de linfonodos para-aórticos ou ilíacos comuns altos. Nesses casos, o limite superior do CTV3 pode se estender ao interespaço T12-L1 ou L1-L2, ou à vasculatura renal. Campos estendidos modificados com limites superiores entre L4-L5 e L1-L2 podem ser utilizados em pacientes com envolvimento nodal pélvico extenso ou de ilíacas comuns altas.
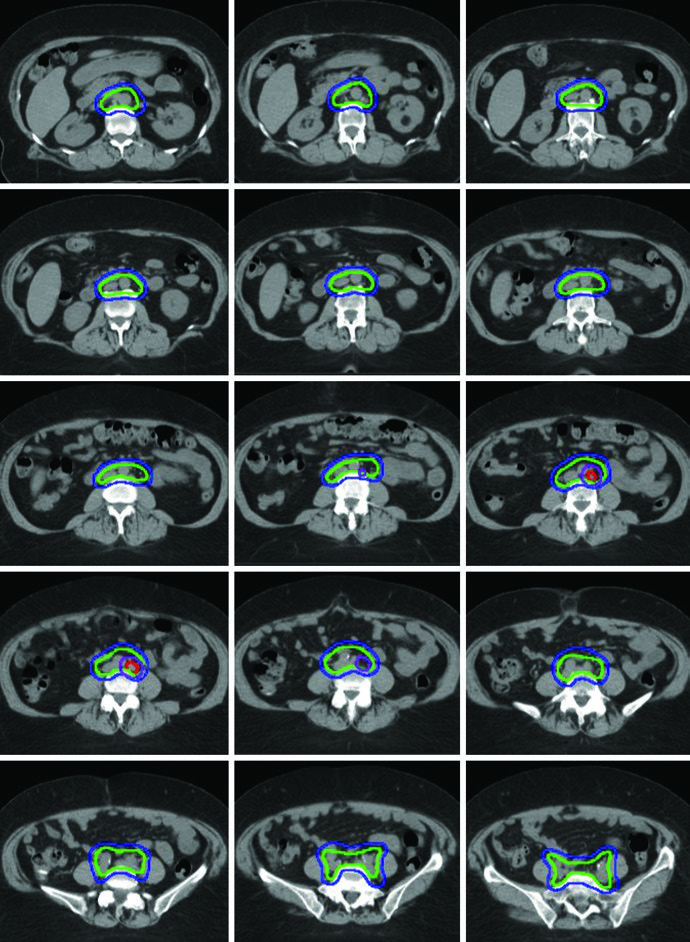
Um boost de 5 a 15 Gy pode ser adicionado para doença nodal bruta ou envolvimento parametrial. Esse boost pode ser administrado de forma sequencial ou como boost integrado simultâneo (SIB). O livro ilustra um caso de adenocarcinoma endometrioide estádio IB, pós-histerectomia laparoscópica assistida por robô, em que um linfonodo para-aórtico aumentado foi encontrado na simulação. A paciente foi tratada com IMRT de campo estendido usando técnica ITV. O limite superior do CTV3 foi modificado para incluir o hilo renal, o GTV da doença nodal bruta foi contornado e recebeu SIB de 5940 cGy com 4760 cGy em 28 frações para os demais linfonodos.
Essa abordagem de SIB permite tratar o volume nodal macroscópico com dose escalada sem adicionar frações extras ao curso do tratamento. Na prática clínica, a escolha entre SIB e boost sequencial depende da geometria do caso e das restrições de dose nos órgãos de risco adjacentes. Para estratégias complementares na radioterapia ginecológica definitiva com IMRT, confira o artigo dedicado.
Avaliação do Plano e Restrições de Dose para OAR
A avaliação do plano exige que pelo menos 95% do PTV receba 100% da dose de prescrição e que ≥99% do PTV receba ≥90% da dose prescrita. O máximo de dose deve ocorrer dentro do PTV, e áreas com >100% da dose de prescrição fora do PTV devem ser minimizadas.
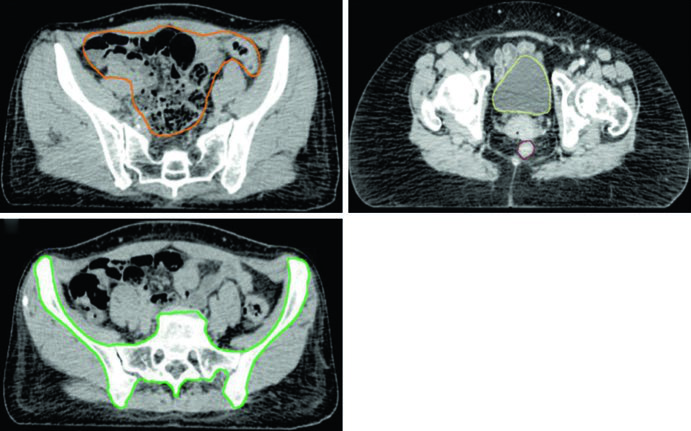
Os órgãos de risco (OAR) no planejamento incluem intestino, bexiga, reto e cabeças femorais. Em pacientes recebendo quimioterapia adjuvante concomitante, a medula óssea pélvica deve ser incluída como OAR — essa técnica demonstrou reduzir o risco de toxicidade hematológica.
Restrições de Dose para Órgãos de Risco
| Órgão | Definição | Restrições de Dose |
|---|---|---|
| Intestino (bowel) | Alças intestinais mais externas do nível L4-L5 até a flexura sigmoide, incluindo cólon sigmoide e ascendente/descendente na pelve | V35 Gy < 35%; V45 Gy < 200 cc |
| Reto | Parede retal externa da flexura sigmoide ao ânus | V45 Gy < 50% |
| Bexiga | Parede vesical externa | V45 Gy < 35% |
| Medula óssea | Ossos pélvicos (os coxae, corpo vertebral L5, sacro inteiro, acetábulos e fêmures proximais). Superior: borda superior de L5 ou crista ilíaca. Inferior: tuberosidades isquiáticas | V10 Gy < 90%; V20 Gy < 75%; V40 Gy < 37% |
| Cabeças femorais | Cabeça femoral inteira excluindo colo femoral | V30 Gy < 15%; V50 Gy < 5% |
| Rins | Contorno externo sólido contínuo, direito e esquerdo | V18 Gy < 50% |
| Medula espinhal | De T10/T11 ao interespaço L1/L2 | Dmáx < 45 Gy |
| Duodeno | Contorno sólido contínuo do estômago distal ao jejuno | V40 Gy < 50%; V55 Gy < 5 cc |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition (Table 20.2) — Diretrizes UCSD e protocolo TIME-C
O contorno do intestino merece atenção especial: deve incluir todo o espaço peritoneal englobando o intestino, com limites superoinferior estendendo-se 1,5 cm superior ao aspecto caudal do PTV e inferiormente até a junção retossigmoide. Na direção anteroposterior, vai da parede abdominal anterior até a extensão posterior máxima do intestino. As bordas laterais do intestino servem como limites direito-esquerdo.
Na prática, a inclusão da medula óssea como OAR ganhou importância crescente porque a IMRT permite reduzir a dose na medula pélvica sem comprometer a cobertura do alvo. Isso é particularmente relevante quando a paciente receberá quimioterapia concomitante com cisplatina, onde a mielossupressão pode ser dose-limitante. Para técnicas avançadas de entrega como VMAT e SBRT nesse contexto, veja nosso artigo sobre tecnologias avançadas na radioterapia ginecológica.
Em resumo, o planejamento pós-operatório de IMRT para câncer cervical e endometrial exige delineamento preciso de três CTVs com expansões anisotrópicas, uso criterioso de ITV para compensar movimento vesical, e respeito rigoroso às restrições de dose de OAR. Estratégias como boost por SIB e campos estendidos personalizam o tratamento conforme o risco e extensão da doença. A abordagem para câncer de vulva compartilha princípios semelhantes de cobertura nodal pélvica e inguinal.