El seminoma testicular sigue siendo uno de los escenarios más ordenados de la radioterapia, pero el capítulo deja claro que la planificación no empieza en los bordes del campo. Empieza con la orquiectomía inguinal radical, la confirmación de seminoma puro, una estadificación adecuada y una decisión cuidadosa entre vigilancia, radioterapia adyuvante y quimioterapia.
Esa forma de abrir el tema importa porque los autores recuerdan que la radioterapia posoperatoria suele considerarse solo para seminomas puros, el subtipo más frecuente de los tumores de células germinales testiculares y además una enfermedad muy radiosensible. En los tumores no seminomatosos, menos frecuentes y menos radiosensibles, la misma estrategia aparece como rara. La histología no actúa aquí como detalle secundario. Funciona como el primer filtro de indicación.
Si este capítulo se reduce a “PA strip en estadio I” y “dogleg en estadio II”, se pierde lo esencial. El texto está realmente organizado alrededor de la topografía nodal, la lateralidad, la cirugía previa y la diferencia entre un campo electivo, un campo inicial y un refuerzo sobre enfermedad nodal macroscópica. Para una visión más amplia del tema, consulta nuestro guía completo sobre delineación de volumen blanco y campos en radioterapia. Si quieres comparar este flujo con otro capítulo genitourinario de la misma serie, revisa también nuestro artículo sobre adenocarcinoma de próstata: delineación e IMRT.
En Este Artículo
Planificación inicial y estadificación
La respuesta directa es sencilla: la planificación empieza antes del contorneo. En casi todos los casos, el manejo inicial del cáncer testicular incluye una orquiectomía inguinal radical, y la conducta posoperatoria depende del subtipo histológico y de la extensión de la enfermedad. El capítulo abre así porque evita un error frecuente: discutir dosis y campos antes de confirmar con precisión qué enfermedad se va a tratar y hasta dónde llega.
Antes de cualquier tratamiento, el estudio debe ser suficiente para asegurar que se trata de un seminoma puro. El capítulo enumera historia clínica detallada, exploración física, marcadores séricos AFP, β-hCG y LDH, perfil bioquímico, ecografía testicular y radiografía de tórax. Tras la orquiectomía inguinal radical, los marcadores deben repetirse, y la estadificación debe completarse con tomografía de tórax, abdomen y pelvis, con resonancia cerebral cuando esté indicada. Los autores añaden además una recomendación práctica que conviene no relegar a una nota marginal: todos los pacientes candidatos a tratamiento del cáncer testicular deben recibir oferta de evaluación de fertilidad y criopreservación de semen.
En la práctica, esta apertura ordena toda la decisión posterior. Separa a los pacientes que pertenecen al grupo de vigilancia de aquellos que pasan a una discusión adyuvante, identifica si existe enfermedad nodal macroscópica y por tanto si un boost es relevante, y deja claro que el diseño anatómico del campo solo tiene sentido cuando la estadificación ya está cerrada. El capítulo trata la evaluación previa al tratamiento como la base de la seguridad técnica.
Topografía nodal, lateralidad y cirugía previa
La lateralidad del seminoma y la cirugía previa modifican el patrón de diseminación. Ese es uno de los mensajes más útiles del capítulo porque evita la simetría automática. El seminoma derecho tiende a drenar hacia cadenas paracava, precava y aortocava. El seminoma izquierdo, en cambio, tiende a drenar hacia cadenas lateroaórtica y preaórtica. Cuando el texto separa esas rutas, en realidad está diciendo que la anatomía vascular no solo sirve para identificar vasos. Sirve para construir el volumen.
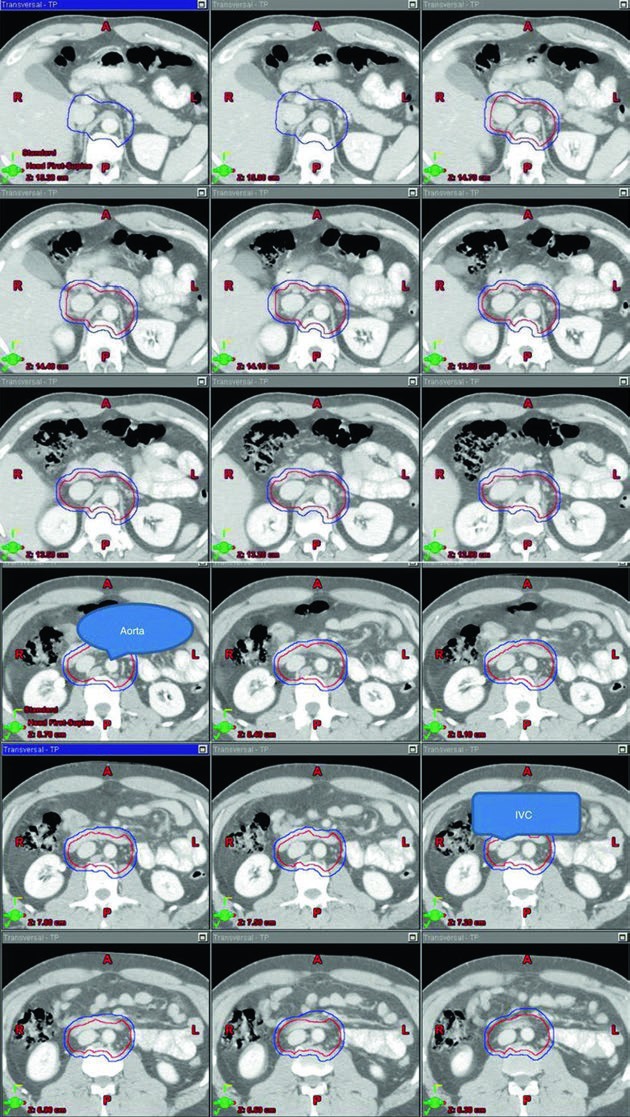
El capítulo también señala que los ganglios pélvicos, ilíacos externos o inguinales pueden estar en riesgo en pacientes con cirugía escrotal o inguinal previa. La frase es breve, pero su impacto sobre el campo es grande. Sin violación previa, la discusión puede mantenerse centrada en el retroperitoneo. Con violación previa, el campo debe incorporar de forma deliberada regiones que no entrarían de rutina. La biología del tumor no cambia, pero sí cambia la ruta anatómica que debe contemplarse.
Las imágenes del estadio I ayudan mucho porque muestran el volumen apoyado sobre la anatomía vascular, no como un dibujo aislado. A lo largo de los cortes de superior a inferior, se aprecia cómo la aorta y la vena cava inferior funcionan como eje geométrico del contorno. Esa lógica visual coincide muy bien con el lenguaje de la tabla y facilita reproducir el volumen con consistencia.
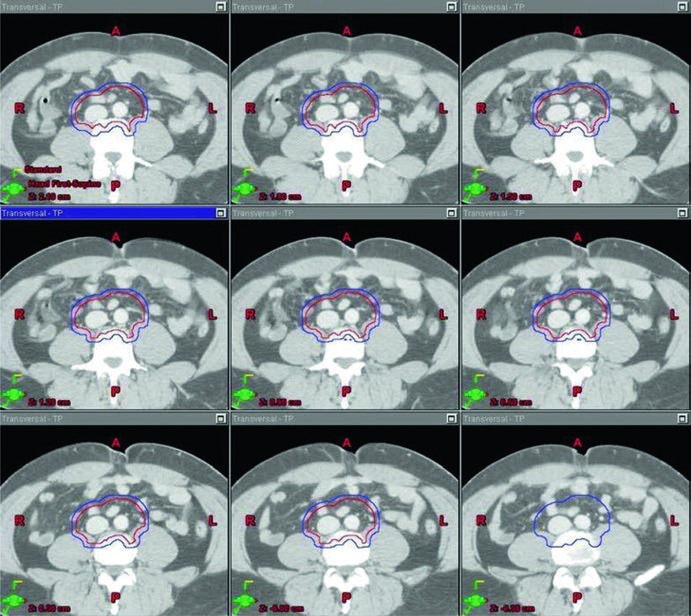
Para el trabajo diario, la conclusión es sencilla y rigurosa a la vez: los campos del seminoma no deben tratarse como plantillas heredadas. Siguen dependiendo del patrón de drenaje, del lado de origen y de la historia quirúrgica. La topografía nodal sigue mandando.
Seminoma testicular en estadio I
En el estadio I, el capítulo responde de forma muy directa: la vigilancia posorquiectomía es, en general, la estrategia fuertemente preferida. La radioterapia adyuvante queda para pacientes con seminoma estadio I que rechazan la vigilancia, apoyándose en los ensayos MRC TE10 y TE18 citados por los autores. Otra opción adyuvante considerada no inferior es carboplatino en 1 o 2 ciclos. La radioterapia aparece, por tanto, como una alternativa válida, pero no como destino automático.
Cuando se utiliza radioterapia en ese contexto, el objetivo recomendado es solo la región ganglionar paraaórtica, el clásico PA strip, salvo que exista violación inguinal o escrotal previa. El capítulo indica una dosis total de 20 a 25,5 Gy para el PTV, administrada en fracciones de 1,5 a 2,0 Gy. Ese rango de dosis no se presenta aislado. Va unido a una definición vascular del CTV y a referencias anatómicas concretas.
El CTV del estadio I empieza con el contorneo de la vena cava inferior y la aorta desde 2 cm por debajo del polo superior del riñón, en sentido superior, hasta la bifurcación de los vasos ilíacos, en sentido inferior. La cava se expande 1,2 cm y la aorta 1,9 cm. Ambos volúmenes se combinan y luego se restan hueso, músculo e intestino. Ese detalle importa porque el capítulo no solo explica qué cubrir. También muestra dónde detener el contorno. Después, el CTV final se expande 0,5 cm más 0,7 cm hasta el borde del bloque para generar el PTV.
La descripción con referencias anatómicas completa el esquema. El borde superior queda en la parte superior de T11, aunque el capítulo aclara que algunas fuentes prefieren la parte superior de T12. El borde inferior se sitúa en la parte inferior de L5. Lateralmente, el campo llega hasta el borde de las apófisis transversas, con una anchura típica cercana a 10 cm. Para seminoma izquierdo, los estudios de mapeo nodal citados sugieren que la cobertura del hilio renal izquierdo es opcional. Esa frase mantiene criterio clínico sin forzar uniformidad artificial.
Tabla 27.1. Volúmenes sugeridos para seminoma testicular en estadio I
La tabla siguiente resume cómo el capítulo combina anatomía vascular, referencias óseas y dosis en el escenario adyuvante del estadio I. Es el puente práctico entre el texto y la figura del PA strip.
| Volumen blanco | Definición basada en TC y anatomía vascular | Definición basada en referencias anatómicas |
|---|---|---|
| CTV | Contornear la vena cava inferior y la aorta desde 2 cm por debajo del polo superior del riñón en sentido superior hasta la bifurcación de los vasos ilíacos en sentido inferior. Expandir la vena cava 1,2 cm y la aorta 1,9 cm. Combinar ambos volúmenes y sustraer hueso, músculo e intestino. |
Borde superior: parte superior de T11, con algunas fuentes recomendando T12 [6]. Borde inferior: parte inferior de L5. Bordes laterales: borde de las apófisis transversas, típicamente alrededor de 10 cm de anchura. |
| PTV 20–25,5 Gy en 1,5–2,0 Gy por fracción |
Expandir el CTV final 0,5 cm + 0,7 cm hasta el borde del bloque. | En seminoma izquierdo, los estudios de mapeo nodal sugieren que cubrir el hilio renal izquierdo es opcional [7]. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 27.1).
Esta tabla deja muy claro el escenario del estadio I. No se trata de irradiar “el retroperitoneo” de forma vaga. Se trata de un volumen paraaórtico cuidadosamente delimitado, seleccionado para un contexto clínico concreto, con dosis adyuvante moderada y con modificaciones cuando la violación inguinal o escrotal previa cambia la lógica del campo.
Seminoma testicular en estadio II
En el estadio II, la escala cambia. Aquí, los pacientes con seminoma puro pueden tratarse con un campo dogleg hasta 30 Gy en estadio IIA o 36 Gy en estadio IIB. Como alternativa, el capítulo menciona quimioterapia primaria, habitualmente etopósido y cisplatino con o sin bleomicina durante 3 a 4 ciclos. De nuevo, la radioterapia se presenta como opción sólida, pero no como única posibilidad.
El punto técnico más útil es que el campo dogleg no se improvisa. Parte del mismo contorneo de vena cava inferior y aorta utilizado en estadio I. Después incorpora vasos ilíacos comunes, porciones proximales de los ilíacos internos hasta el origen de la glútea superior y vasos ilíacos externos hasta el borde superior del acetábulo, con expansión de 1,2 cm respetando límites anatómicos. La enfermedad nodal macroscópica se contornea como GTV y se expande 0,8 cm respetando la anatomía para crear un CTV nodal. El CTV vascular y el CTV nodal se unen para formar el CTV inicial.
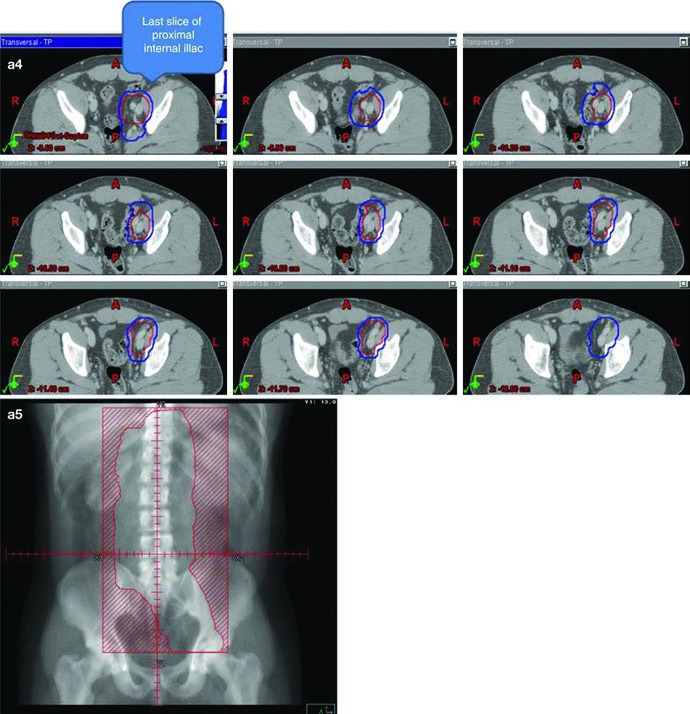
Ese campo inicial recibe la misma expansión de 0,5 cm más 0,7 cm hasta el borde del bloque para generar el PTV inicial, todavía dentro del rango de 20 a 25,5 Gy con fracciones de 1,5 a 2,0 Gy. El boost en conedown sigue la misma lógica geométrica aplicada sobre el CTV nodal y eleva la dosis total a 30–36 Gy en fracciones de 2 Gy. El capítulo añade una regla práctica para la enfermedad visible: asegurar un margen de 2 cm alrededor de toda adenopatía macroscópica visible.
Las referencias anatómicas mantienen el campo anclado. Superiormente, el límite sigue en la parte superior de T11, con la misma nota de que algunas fuentes usan T12. Inferiormente, el capítulo lo sitúa en la parte superior del acetábulo, aunque otras fuentes prefieren la zona media o inferior del foramen obturador. Lateralmente, el campo alcanza las puntas de las apófisis transversas lumbares, habitualmente alrededor de L3 teniendo en cuenta la posición renal, y se prolonga para cubrir el borde lateral del acetábulo en el extremo inferior. En seminoma izquierdo, la cobertura del hilio renal izquierdo vuelve a describirse como opcional.
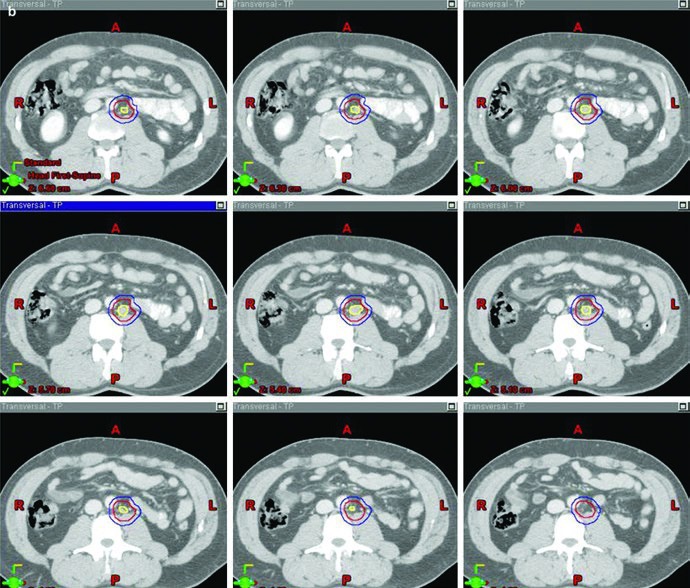
La figura del boost cierra muy bien esa lógica. En el ejemplo de estadio IIA, separa visualmente GTV en amarillo, CTV en rojo y PTV en azul. Eso importa porque el capítulo no usa la palabra “boost” de forma vaga. Describe un volumen de enfermedad macroscópica, una expansión que respeta la anatomía y un volumen de planificación final construido con intención precisa.
Tabla 27.2. Volúmenes sugeridos para seminoma testicular en estadio II
En el estadio II, la tabla del capítulo expone la construcción del dogleg paso a paso. Es breve, pero concentra la mayor parte de la lógica dosimétrica y geométrica.
| Volumen blanco y dosis | Definición basada en TC y anatomía vascular | Definición basada en referencias anatómicas |
|---|---|---|
| CTV inicial | Utilizar los mismos contornos y expansiones de vena cava inferior y aorta descritos en la Table 27.1. Después, contornear los vasos ilíacos comunes, las porciones proximales de los ilíacos internos hasta el origen de la glútea superior y los vasos ilíacos externos hasta el borde superior del acetábulo, con expansión de 1,2 cm respetando límites anatómicos. Contornear la enfermedad nodal macroscópica (GTV) y expandir 0,8 cm respetando límites anatómicos. Combinar el CTV vascular y el CTV nodal para formar el CTV inicial. |
Borde superior: parte superior de T11, con algunas fuentes recomendando T12 [6]. Borde inferior: parte superior del acetábulo, con algunas fuentes recomendando la parte media o inferior del foramen obturador [6]. Borde lateral: puntas de las apófisis transversas lumbares, habitualmente alrededor de L3 teniendo en cuenta la localización renal, extendiéndose para cubrir el borde lateral del acetábulo en el extremo inferior. |
| PTV inicial 20–25,5 Gy en 1,5–2,0 Gy por fracción |
Expandir el CTV inicial 0,5 cm + 0,7 cm hasta el borde del bloque. | En seminoma izquierdo, los estudios de mapeo nodal sugieren que cubrir el hilio renal izquierdo es opcional [7]. |
| PTV de boost en conedown Total de 30–36 Gy en 2 Gy por fracción |
Expandir el CTV nodal 0,5 cm + 0,7 cm hasta el borde del bloque. | Asegurar un margen de 2 cm alrededor de toda adenopatía macroscópica visible. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 27.2).
Ahí es donde el capítulo gana más valor práctico. En lugar de oponer “campos clásicos” a “planificación moderna”, muestra cómo construir el dogleg a partir de vasos, referencias anatómicas y enfermedad visible. En estadio IIA, la dosis total es 30 Gy. En estadio IIB, la misma lógica continúa hasta 36 Gy. El resultado es mucho menos automático de lo que sugieren los resúmenes rápidos.
Simulación, inmovilización y entrega del tratamiento
Las instrucciones finales de simulación deben leerse como parte del delineamiento, no como un apéndice técnico separado. En la institución de los autores, los parámetros estándar incluyen tomografía con grosor de corte de 2 mm, paciente en decúbito supino y brazos elevados. La inmovilización se realiza con alpha cradle. En pacientes estadio II, se usa contraste intravenoso con frecuencia para ayudar al delineamiento de enfermedad nodal macroscópica. Si existe un PET de estadificación, también puede fusionarse con la tomografía de simulación.
El capítulo también especifica que el testículo contralateral íntegro debe protegerse con un clamshell. Ese detalle encaja con el tono general del texto. Incluso en una enfermedad muy radiosensible, la planificación no es informal. La técnica estándar indicada es 3D-CRT con campos AP/PA definidos por referencias óseas o por anatomía vascular. El objetivo del capítulo no es sonar sofisticado. Es sonar reproducible.
La cirugía inguinal o escrotal previa vuelve a modificar el campo. En ese contexto, deben incluirse las regiones inguinal e ilíaca ipsilaterales. Si hubo penetración escrotal, los autores recomiendan considerar un boost con electrones sobre escroto y cicatriz. Esa observación final une todas las partes del capítulo. Diseminación linfática, historia quirúrgica, simulación y técnica de tratamiento aparecen como elementos de un mismo flujo de planificación.
Si hay una idea central que merece quedarse con el lector, es esta: en el seminoma testicular, la radioterapia funciona mejor cuando la decisión de irradiar, el mapeo nodal y la simulación se manejan como una sola conversación clínica. El estadio I exige selectividad y respeto por la vigilancia como preferencia general. El estadio II devuelve al centro del plan el campo dogleg, el boost y la enfermedad visible. En ambos casos, la anatomía vascular sigue siendo el idioma del volumen blanco.
Referencias del capítulo
Las recomendaciones resumidas arriba se apoyan en las referencias listadas por los autores al final del capítulo.
- Gilligan T, Lin DW, Aggarwal R, et al. Guía NCCN para cáncer testicular, versión 2.2020.
- Paly JJ, Efstathiou JA, Hedgire SS, et al. Mapeo de los patrones de metástasis nodales en seminoma.
- McMahon CJ, Rofsky NM, Pedrosa I. Clasificación anatómica, caracterización y estadificación de metástasis linfáticas de tumores pélvicos.
- Fosså SD, Horwich A, Russell JM, et al. Ensayo aleatorizado del Medical Research Council sobre volumen blanco en seminoma testicular estadio I.
- Jones WG, Fossa SD, Mead GM, et al. Ensayo aleatorizado que comparó 30 Gy frente a 20 Gy en el tratamiento adyuvante del seminoma testicular estadio I.
- Wilder RB, Buyyounouski MK, Efstathiou JA, et al. Planificación radioterápica para seminoma testicular.
- Dinniwell R, Chan P, Czarnota G, et al. Topografía ganglionar pélvica para planificación radioterápica basada en resonancia magnética con contraste.
- Mead GM, Fossa SD, Oliver RTD, et al. Ensayos aleatorizados en 2466 pacientes con seminoma estadio I, incluidos patrones de recaída y seguimiento.