Principios de las Técnicas Avanzadas en Ginecología
Los resultados del tratamiento de tumores ginecológicos locorregionalmente avanzados continúan siendo subóptimos. Las toxicidades hematológicas y gastrointestinales comprometen la entrega completa del esquema terapéutico en una proporción significativa de pacientes. Dos frentes de desarrollo se imponen simultáneamente: intensificar el tratamiento cuando sea posible y reducir la toxicidad de manera consistente.
La radioterapia de intensidad modulada (IMRT) se ha consolidado como modalidad estándar tanto en el tratamiento definitivo como en el posoperatorio del cáncer cervical y endometrial. Persiste cierta controversia sobre la implementación rutinaria dado el volumen limitado de datos prospectivos y aleatorizados, pero la práctica clínica ya ha incorporado la técnica ampliamente. La IMRT con guía de imagen diaria (IG-IMRT) mejora la localización de los blancos y de los órganos en riesgo (OARs), posibilitando planes más conformales sin comprometer las dosis tumoricidas.
Este progreso técnico no se limita a la conformación del haz. La replanificación adaptativa corrige cambios en la anatomía tumoral y de la paciente a lo largo del curso de tratamiento. La IMRT con preservación de médula ósea (BM-IMRT) reduce la toxicidad hematológica — un problema clínico real cuando se administra quimioterapia concurrente basada en cisplatino. La SBRT ofrece una alternativa de boost para pacientes inelegibles o que rechazan la braquiterapia, además de posibilitar la reirradiación de áreas previamente tratadas. La terapia con protones puede disminuir la toxicidad gracias a la caída de dosis distal rápida, aunque los datos comparativos de alta calidad siguen siendo escasos.
Para una visión integral del delineamiento de volumen blanco en diversas localizaciones anatómicas, consulte nuestra guía completa sobre delineación de volumen blanco y campos en radioterapia.
Guía de Imagen en Radioterapia Ginecológica
La IMRT permite planificaciones sofisticadas y conformales que reducen el volumen irradiado. Sin embargo, esta ventaja exige delineación precisa de las estructuras blanco y de los OARs, además de manejo adecuado del movimiento orgánico y de la incertidumbre de posicionamiento. Los órganos pélvicos se mueven tanto entre fracciones como durante la entrega de cada fracción individual.
La IG-IMRT se ha asociado con mejora tanto en la toxicidad hematológica como gastrointestinal en comparación con la IMRT aislada. Tres enfoques de guía de imagen merecen atención en la práctica clínica:
- kV ortogonal diario: las imágenes kV en el momento del tratamiento alinean la anatomía ósea con el posicionamiento inicial de la simulación CT. Método accesible, pero no captura variaciones de tejido blando.
- Cone-beam CT (CBCT) diario: permite identificar el estado de llenado rectal y vesical en comparación con la simulación. Con expansión de PTV basada en modelo de forma y guía diaria por CBCT, la cobertura del blanco dentro de la isodosis del 95% es excelente.
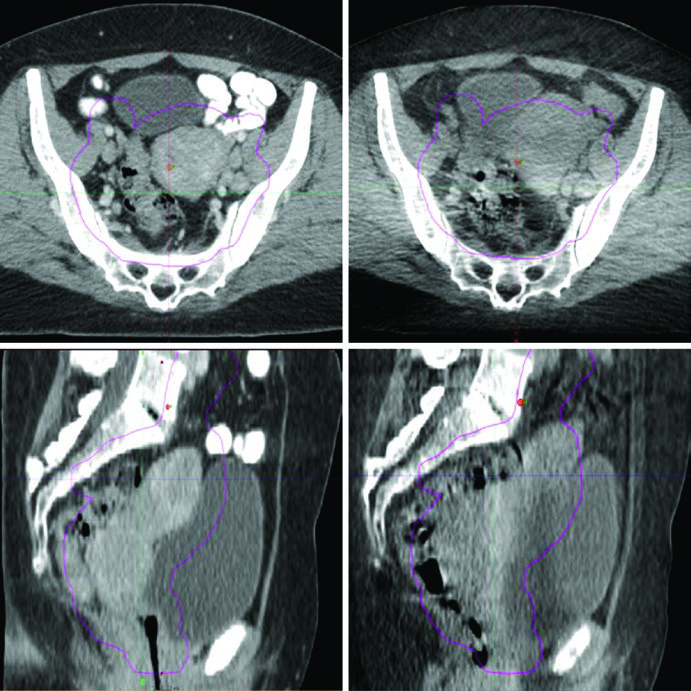
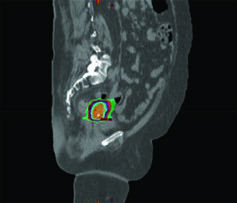
- Monitoreo de variación: la Figura 24.1 ilustra un caso real donde cambios en el llenado vesical y rectal desplazaron el fondo uterino fuera del PTV — exactamente el tipo de evento que el CBCT pretratamiento detecta y permite corregir.
En la práctica diaria, el CBCT ofrece el mejor equilibrio entre información anatómica y viabilidad logística. La dosis adicional de imagen es clínicamente aceptable cuando se compara con el riesgo de subdosificación tumoral por desplazamiento no detectado.
IMRT con Preservación de Médula Ósea
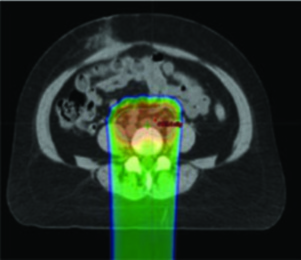
La IMRT puede emplearse específicamente para preservar médula ósea en pacientes sometidas a RT pélvica, y esta estrategia ha demostrado reducir la toxicidad hematológica de forma significativa. Quien trabaja con quimiorradiación concurrente sabe que las citopenias prolongadas retrasan ciclos, comprometen la intensidad de dosis y ocasionalmente conducen a hospitalización. Preservar médula activa es una respuesta concreta a este problema.
Diversas estrategias han sido implementadas y validadas clínicamente:
IG-IMRT basada en PET/CT implica contornear los huesos pélvicos y definir médula activa como regiones con SUV superior al SUV medio intraóseo, aplicando restricciones de dosis a la médula. Las restricciones publicadas, basadas en modelado NTCP, siguen la siguiente jerarquía:
| Estructura | Tipo de Restricción | Dosis Media | V10 (%) | V20 (%) |
|---|---|---|---|---|
| Médula ósea pélvica | Soft constraint | ≤27 Gy | ≤85,5% | ≤66% |
| Médula ósea pélvica | Hard constraint | ≤29 Gy | ≤90% | ≤75% |
| Médula ósea activa | Soft constraint | ≤28,5 Gy | ≤90% | ≤70% |
| Médula ósea activa | Hard constraint | ≤30 Gy | ≤90% | ≤75% |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition — restricciones basadas en modelado NTCP (Rose et al.)
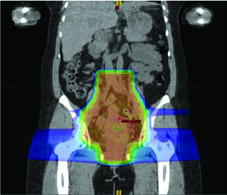
Cuando el PET/CT no está disponible, dos alternativas funcionan bien. Un enfoque basado en atlas es factible y reproducible entre centros. La otra opción delimita la médula ósea como las regiones de baja densidad dentro de los huesos en el CT de simulación, aplicando las mismas restricciones de dosis. Ambas reducen la toxicidad hematológica de forma mensurable, incluso sin la información funcional del PET.
Esta estrategia resulta particularmente relevante en el cáncer cervical tratado con quimiorradiación concurrente. La reducción de citopenias permite mantener la intensidad de dosis del cisplatino semanal, lo que tiene impacto directo en el control tumoral. Detalles sobre el delineamiento de los volúmenes pélvicos pueden encontrarse en los artículos sobre radioterapia definitiva en ginecología y tratamiento posoperatorio ginecológico.
Replanificación Adaptativa en la Pelvis
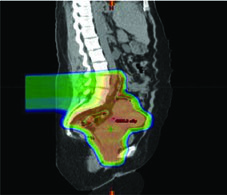
La replanificación adaptativa se subdivide en tres categorías principales: offline (entre fracciones), online (inmediatamente antes de una fracción) y en tiempo real (durante la entrega del tratamiento). Cada una responde a escenarios clínicos diferentes, y la elección depende de la infraestructura disponible y del grado de variación anatómica esperado.
Técnica plan-del-día (plan-of-the-day): genera una biblioteca de planes específicos de la paciente correspondientes a diferentes volúmenes blanco y configuraciones de movimiento orgánico. El CBCT pretratamiento selecciona el plan de la biblioteca más similar a la configuración del día. Esta estrategia es elegante porque no requiere replanificación en tiempo real, pero demanda inversión inicial en la creación de la biblioteca.
Replanificación programada: puede realizarse con RM semanal. El registro deformable de imagen modela la dosis acumulada en blancos y OARs. En la práctica, funciona bien para pacientes que pierden peso progresivamente o cuyos tumores regresan significativamente durante el tratamiento.
La radioterapia adaptativa offline (ART) debe considerarse para pacientes con pérdida de peso significativa o cambio sustancial en el tamaño tumoral. Una nueva simulación puede ser necesaria si la replanificación no puede realizarse con las imágenes adquiridas en la sala de tratamiento. Los sistemas avanzados de planificación permiten monitoreo automatizado de dosis y métricas dosis-volumen que pueden revisarse offline para orientar la decisión de replanificar.
En la radioterapia adaptativa online, la variación en el llenado del recto y la vejiga desplaza tanto los blancos como los OARs de formas que la simulación CT inicial no captura. Las tecnologías emergentes integran CBCT iterativo para cálculo de dosis y replanificación diaria, o utilizan RM para replanificación online. La plataforma MR-Linac representa el ejemplo más avanzado de esta categoría, combinando imagen en tiempo real con adaptación del plan en la misma sesión.
Terapia con Protones en Tumores Ginecológicos
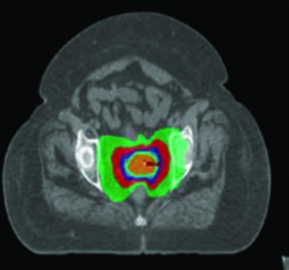
La terapia con protones aprovecha un build-up de dosis relativamente gradual y una caída de dosis abrupta distal al blanco en comparación con fotones. Esta propiedad física fundamental permite reducir la dosis en los OARs — especialmente distales a los campos de tratamiento incidentes — y disminuir la dosis integral, preservando cobertura adecuada de los blancos.
Los escenarios donde los protones pueden ofrecer ventaja sobre la IMRT incluyen el tratamiento de ganglios paraaórticos y la reirradiación. Los estudios dosimétricos y clínicos iniciales muestran mejora en la dosis a estructuras normales adyacentes, incluyendo intestino, vejiga y médula ósea. Los protones también permiten mejor preservación ovárica en mujeres premenopáusicas — por ejemplo, respetando un ovario con dosis media inferior a 15 Gy.
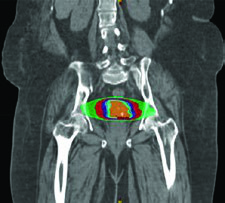
Para el manejo definitivo, la dosimetría al blanco debe ser idéntica a la utilizada con fotones, corregida por la efectividad biológica relativa (RBE) asumida de 1,1 para protones. El delineamiento de GTV y CTV sigue los mismos principios del capítulo de EBRT definitiva. Los PTVs son específicos por haz, basados en la incertidumbre de alcance. Una consideración fundamental: evitar arreglos de haz que coloquen estructuras críticas en el campo distal al blanco.
La terapia con protones puede considerarse como alternativa de boost para pacientes que no pueden recibir braquiterapia. Los protones presentan ventajas dosimétricas en vejiga, intestino, cabezas femorales y recto en comparación con VMAT. El CTV de boost puede determinarse mediante RM obtenida después de 3 semanas de quimiorradiación, administrando entonces 30 Gy/Gy equivalente en 5 fracciones en sustitución de la braquiterapia. Sin embargo, la evidencia prospectiva de alta calidad es insuficiente, y la relación entre dosimetría mejorada y reducción clínicamente significativa de la toxicidad permanece sin comprobación definitiva.
SBRT para Cáncer Cervical
En el cáncer cervical locorregionalmente avanzado, el estándar de tratamiento combina EBRT fraccionada diaria con cisplatino concurrente seguido de boost con braquiterapia, alcanzando dosis EQD2 final de 80 a 95 Gy en el blanco. La SBRT surge como modalidad especializada que entrega dosis altas en 1 a 5 fracciones, exigiendo visualización precisa del blanco, delineación exacta de tumor y OARs, y posicionamiento de alta fidelidad con guía de imagen.
Los ganglios linfáticos pueden recibir boost con SBRT. La técnica también se aplica al escenario de reirradiación para enfermedad recurrente o tratamiento de sitios limitados de metástasis. Algunas pacientes no son candidatas a braquiterapia por comorbilidades severas, y otras rechazan el procedimiento — incluyendo pacientes en riesgo de trastorno de estrés postraumático.
La SBRT permite entrega conformal de boost en alta dosis, pero los resultados recientes exigen cautela. Un ensayo fase II investigando SBRT (28 Gy en 4 fracciones) como sustituto de la braquiterapia se cerró prematuramente por toxicidad mayor a la esperada y tasas de control local, supervivencia libre de progresión y supervivencia global inferiores a lo previsto a 2 años. La braquiterapia sigue siendo el estándar de tratamiento para pacientes elegibles.
Para pacientes que definitivamente no recibirán braquiterapia, un esquema de 5 fracciones (por ejemplo, 27,5 Gy en 5 fracciones) tras 45 Gy en la pelvis puede considerarse, resultando en EQD2 de 80 Gy (α/β = 10). La determinación de dosis y fraccionamiento debe considerar el tamaño del blanco, RT previa en el área y tolerancia de los OARs adyacentes. Para régimen de 5 fracciones, la dosis por fracción se sitúa típicamente en el rango de 4 a 8 Gy, aunque fracciones de 8 a 15 Gy también han sido reportadas. La EQD2 total debe calcularse para el área tratada. Para una perspectiva más amplia sobre aplicaciones de SBRT, consulte nuestro artículo dedicado sobre SBRT en cabeza y cuello.
SBRT en Cáncer de Endometrio
La SBRT también se ha considerado como modalidad alternativa para entrega de boost en el escenario posoperatorio del cáncer endometrial. Los ganglios linfáticos también pueden recibir boost con SBRT. La reirradiación o SBRT dirigida a metástasis representan indicaciones adicionales en pacientes cuidadosamente seleccionadas.
Una serie retrospectiva evaluó pacientes con focos recurrentes, persistentes u oligometastásicos tratados con dosis mediana de 24 Gy (rango de 10 a 50 Gy) en mediana de 4 fracciones (rango de 1 a 6). Los resultados mostraron tasas de control local de 80% a 1 año y 68% a 3 años, con control más favorable en tumores menores. El perfil de seguridad fue aceptable: tasa de toxicidad grado ≥2 de 4,3%, con solo un evento grado 3 y ninguna toxicidad grado 4 o 5.
Estos datos justifican la SBRT como opción razonable en pacientes seleccionadas, pero las series retrospectivas tienen limitaciones inherentes. La decisión clínica debe ponderar tamaño tumoral, localización en relación con estructuras previamente irradiadas y dosis acumulativa. Para más información sobre la braquiterapia ginecológica, consulte nuestro artículo sobre braquiterapia guiada por imagen.
Consideraciones Prácticas e Integración Clínica
La elección entre estas tecnologías avanzadas no sigue una receta única. El escenario clínico determina el mejor enfoque: IG-IMRT con preservación de médula ósea es prácticamente obligatoria cuando se administra quimiorradiación concurrente; la replanificación adaptativa se justifica en tratamientos prolongados con anatomía variable; los protones pueden considerarse cuando estructuras críticas están en posición desfavorable o en escenarios de reirradiación; la SBRT cubre la brecha cuando la braquiterapia no es viable.
Lo que une todas estas estrategias es la necesidad de infraestructura de imagen robusta y equipo entrenado en delineamiento preciso. Sin CBCT o RM de calidad, las ventajas de la IMRT conformal se pierden. Sin restricciones de dosis bien definidas para médula ósea, la toxicidad hematológica persiste. Sin guía de imagen rigurosa, la SBRT se vuelve peligrosa.
La radioterapia ginecológica avanzada exige integración entre física médica, dosimetría y oncología clínica en cada decisión de tratamiento. Los datos actuales sustentan beneficios dosimétricos claros para estas técnicas, pero la traducción en resultados clínicos superiores depende de la ejecución cuidadosa en cada etapa del proceso. Para comprender el contexto completo del delineamiento ginecológico, explore la guía completa sobre delineación de volumen blanco y campos en radioterapia, además de los artículos sobre cáncer de vulva e IMRT.