La planificación del cáncer de mama inicial en este capítulo se apoya en tres exigencias técnicas: tangentes bien construidas, dosis homogénea dentro de la mama y definición rigurosa del lecho quirúrgico cuando hay indicación de boost o de APBI. Los autores recorren todo el flujo, desde la revisión de mamografía, ecografía y patología hasta la simulación, el posicionamiento, el contorneo de volúmenes y la valoración de corazón y pulmones. Para una visión más amplia del tema, consulte nuestra guía completa sobre delineación de volumen blanco y campos en radioterapia.
Cáncer de mama inicial: principios generales de planificación
El capítulo identifica a la radioterapia conformada tridimensional con compensación adecuada como la técnica estándar en el escenario adyuvante. Esa compensación puede lograrse con la técnica field-in-field y, cuando hace falta, con haces de energía mixta, siempre con un objetivo práctico: mantener dosis homogénea en el tejido mamario. En el mismo apartado se afirma que el mayor nivel de evidencia respalda la irradiación de mama completa en esquema hipofraccionado, de modo que la uniformidad de dosis queda planteada como un requisito central y no como un refinamiento secundario.
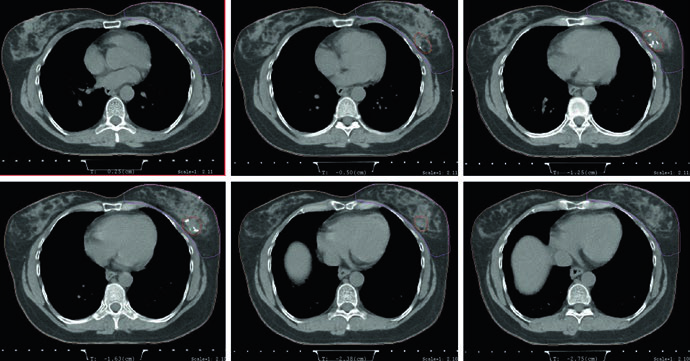
Esa apertura del capítulo es deliberadamente directa. El texto no separa contorneo y planificación porque la cobertura homogénea de la mama depende tanto de cómo se dibuja el volumen como de cómo se compensan los tangentes. Cuando menciona 3D CRT e IMRT como técnicas posibles, no está defendiendo una plataforma frente a otra. Está diciendo que la técnica elegida debe preservar el mismo resultado operativo: cubrir la mama de forma uniforme sin perder el control de la dosis que reciben corazón y pulmones.
Las figuras de planificación vuelven concreto ese argumento. El ejemplo en supino utiliza tangentes con técnica field-in-field para homogeneidad y un pequeño bloqueo con MLC para proteger el corazón. La misma leyenda aporta la prescripción: 42,4 Gy con fracciones de 2,65 Gy, seguidos de boost con electrones sobre la cavidad de tumorectomía hasta 10 Gy con fracciones de 2,5 Gy. La compensación, por tanto, no aparece como un ajuste tardío. Forma parte de la técnica estándar desde el inicio.
También es notable la disciplina del alcance. El capítulo se mantiene en el escenario de mama inicial y no se dispersa hacia situaciones regionales o localmente avanzadas. Esa contención ayuda porque obliga a concentrarse en la mama, la cavidad quirúrgica y los detalles de setup que hacen reproducible el tratamiento diario.
Imagen, cirugía y patología antes de la simulación
Antes de planificar, el capítulo exige revisar con detalle la exploración física, las imágenes preoperatorias y la anatomía patológica. Todas las pacientes deben tener mamografía en el diagnóstico, y la ecografía suele añadirse con frecuencia. La resonancia magnética tiene indicaciones limitadas en enfermedad temprana, pero si está disponible debe revisarse antes de planificar para apoyar tanto los márgenes de mama completa como la localización precisa del boost y de la APBI.
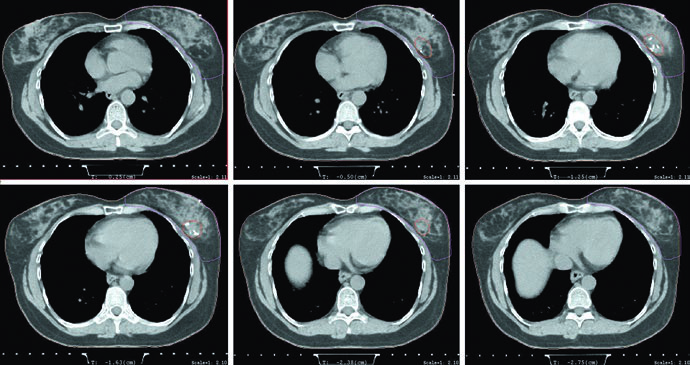
La secuencia quirúrgica y patológica está igual de ordenada. La biopsia guiada por imagen suele confirmar el diagnóstico. Para carcinoma ductal in situ, la opción quirúrgica citada es tumorectomía o escisión segmentaria aislada. Para enfermedad invasiva temprana, el capítulo recomienda tumorectomía asociada a biopsia de ganglio centinela. Después, la revisión de patología se vuelve decisiva porque el texto fija criterios muy concretos de margen: ausencia de tumor en tinta para enfermedad invasiva y 2 mm para DCIS puro, según el consenso SSO-ASTRO de 2016 mencionado por los autores.
Los clips quirúrgicos reciben una observación especialmente práctica. El capítulo prefiere, aunque no exige, que el cirujano los coloque en el acto quirúrgico para ayudar a delinear el lecho tumoral y facilitar la localización radiográfica antes de administrar la dosis. Su utilidad crece todavía más cuando se contempla APBI. Si no hay clips, el planificador depende mucho más del seroma, de las diferencias en el tejido glandular y de la comparación con la mama contralateral.
Por eso el texto insiste tanto en revisar toda la imagen disponible antes de abrir la planificación. El lecho de tumorectomía no debe inferirse solo desde la tomografía de simulación. El material original remite de forma explícita a mamografía, ecografía y resonancia cuando estén disponibles. La delineación correcta empieza antes de la primera línea de contorno.
Tomografía de simulación, posición supina, prona y DIBH
Para la irradiación de mama completa, el capítulo recomienda tomografía con espesor de corte menor o igual a 3 mm, en posición supina o prona. Para APBI, la exigencia se vuelve más fina: cortes de 1,5 a 2 mm a través de la cavidad de tumorectomía pueden mejorar su delineación. No es un detalle administrativo. Es la diferencia entre una cavidad apenas sugerida y un volumen visible que luego sostendrá las expansiones de CTV y PTV.
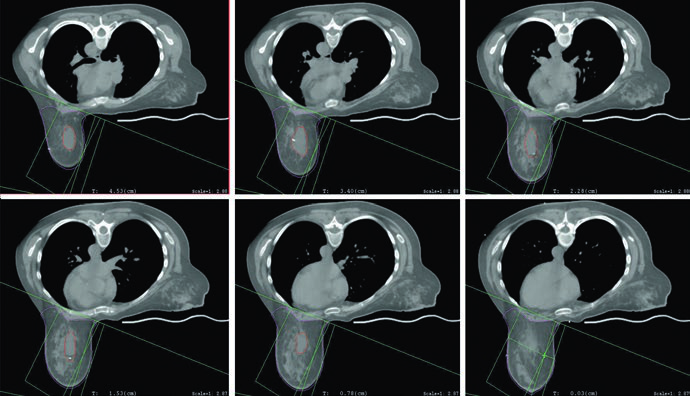
En la posición supina, la paciente debe colocarse en una tabla mamaria con los brazos por encima de la cabeza. En los tumores izquierdos, el capítulo aconseja considerar la inspiración profunda mantenida, DIBH, para reducir la dosis al corazón. El verbo importa. DIBH no se presenta como obligación universal para todo caso izquierdo, pero sí como recurso que debe entrar en la decisión cuando puede ofrecer protección cardíaca reproducible.
La posición prona se presenta con el mismo tono práctico. Las pacientes con mamas péndulas pueden beneficiarse porque disminuye la separación y mejora la homogeneidad tisular del plan, lo que puede reducir toxicidad aguda. El texto añade dos consecuencias dosimétricas: menos irradiación pulmonar y posible evitación cardíaca. Luego introduce la advertencia que vuelve útil la recomendación: si el lecho tumoral contacta la pared torácica, el corazón puede acercarse paradójicamente al campo. La prona es una herramienta valiosa, no una mejora automática.
El componente mecánico del setup prono también está descrito. La paciente debe colocarse en una tabla prona dedicada para mama, y la comodidad importa porque de ella depende la reproducibilidad. Las lesiones ortopédicas de espalda o cuello pueden convertir la prona en una mala opción. Esa observación breve mantiene el texto conectado con la realidad diaria del tratamiento.
Las figuras de planificación refuerzan el mismo mensaje. El ejemplo en prono utiliza tangentes con field-in-field, la misma prescripción de 42,4 Gy en 2,65 Gy por fracción y boost con mini-tangentes fotónicos hasta 10 Gy en 2,5 Gy por fracción. La leyenda agrega un detalle geométrico muy útil: el borde posterior del campo debe incluir parte del músculo pectoral. Si desea ampliar ese razonamiento hacia cadenas ganglionares, continúe con nuestro artículo sobre irradiación nodal regional en cáncer de mama.
Boost del lecho tumoral y uso selectivo de APBI
El capítulo resume el papel del boost con una frase de mucha consecuencia clínica. Irradiar el lecho tumoral después de la mama completa reduce aún más el riesgo de recurrencia local, pero puede omitirse en pacientes de bajo riesgo. El objetivo no es convertir la decisión en una fórmula rígida. El punto es establecer el terreno de trabajo: el boost tiene valor reconocido, aunque su omisión puede ser razonable en un grupo seleccionado.
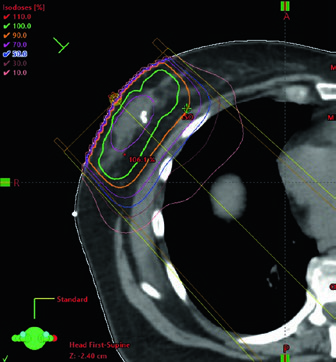
Cuando el boost está indicado, la planificación descrita con mayor frecuencia utiliza electrones en incidencia en face. La energía debe elegirse según la profundidad del lecho tumoral más un margen, sin sobrepasar la superficie anterior de los músculos pectorales. La figura del boost en supino vuelve visible esa regla al mostrar el uso de 12 MeV para cubrir la línea de isodosis del 90% hasta la superficie anterior del pectoral. Si el lecho es profundo, el texto acepta una alternativa práctica: mini-tangentes.
La APBI aparece después con una formulación prudente. Todavía no se la define como estándar de cuidado, pero sí como alternativa aceptable para pacientes seleccionadas de bajo riesgo con enfermedad unifocal. El capítulo no va más allá, y esa sobriedad es parte de su fortaleza. En lugar de sobredimensionar la APBI, delimita el contexto exacto en el que puede justificarse.
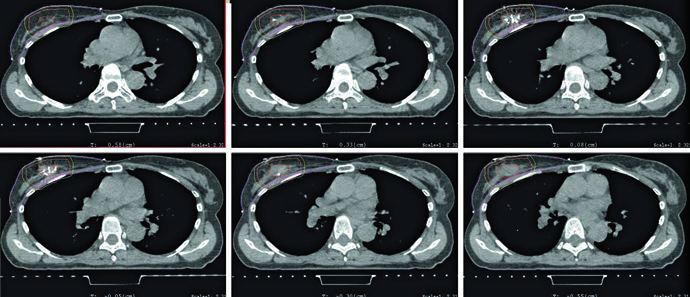
La figura y la tabla explican cómo se construye ese volumen. La cavidad de tumorectomía debe incluir seroma, clips y diferencias relevantes en el tejido glandular. La Tabla 11.1 recomienda expansión de 1,0 a 1,5 cm para el CTV y de 0,5 a 1,0 cm para el PTV según la incertidumbre de setup y el movimiento previsto. La leyenda de APBI añade un ejemplo típico: CTV de 1,5 cm alrededor de la cavidad, excluyendo músculo pectoral, costilla y pared torácica, sin extenderse fuera del tejido mamario contorneado y sin llegar a la piel, quedando a 5 mm de la superficie. Después, el PTV se genera con una expansión aproximada de 5 mm alrededor del CTV, según la incertidumbre institucional.
Esa combinación de tabla y figura evita dos errores frecuentes. El primero es expandir de manera automática sin comprobar dónde termina realmente el tejido mamario. El segundo es dibujar un PTV excesivamente prolijo y olvidar que el propio capítulo permite que se extienda fuera de la superficie del paciente y hacia músculos pectorales o de la pared torácica cuando eso refleja el margen de setup. En APBI, el texto exige disciplina anatómica para el CTV y honestidad geométrica para el PTV.
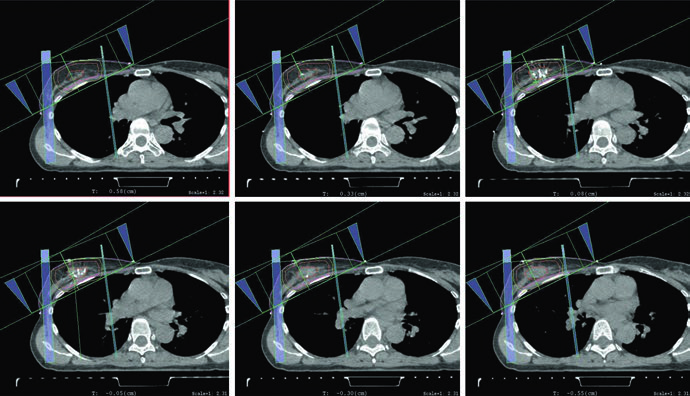
La figura del plan de APBI cierra el apartado con coherencia. Utiliza mini-tangentes fotónicos combinados con un campo de electrones en face. Nada en el capítulo presenta la APBI como algo desligado de la lógica de mama completa. Cambia el volumen tratado, pero se mantienen las mismas exigencias de orientación de campos, profundidad útil y concordancia con la anatomía operada.
Delineación del volumen blanco de mama y de la cavidad quirúrgica
El volumen de la mama se define a partir de referencia clínica obligatoria. La mama puede marcarse con alambre o con bordes colocados clínicamente en la tomografía, y el contorno debe incluir todo el tejido glandular mamario. La descripción anatómica es precisa: límite craneal por debajo de la cabeza de la clavícula y en la inserción de la segunda costilla; límite caudal donde desaparece el tejido mamario; límite medial en el borde del esternón sin cruzar la línea media; límite lateral en la línea axilar media, reconociendo que la ptosis modifica la percepción de ese borde; límite anterior en la piel o pocos milímetros por debajo cuando el interés es reportar dosis; y límite posterior en músculos pectorales y pared torácica, sin incluir músculos ni costillas.
Volúmenes blanco sugeridos para la planificación 3D en mama inicial
La Tabla 11.1 concentra la parte más operativa del capítulo. Define qué debe entrar en cada volumen, dónde deben terminar los límites anatómicos y en qué punto una expansión deja de ser aceptable.
| Volumen blanco | Definición y descripción |
|---|---|
| Mama | Se requiere referencia clínica para delinear el tejido mamario. La mama puede marcarse con alambre o con bordes colocados clínicamente al momento de la tomografía. El contorno debe incluir todo el tejido glandular mamario. El límite craneal debe quedar por debajo de la cabeza de la clavícula y en la inserción de la segunda costilla. El límite caudal se define por la pérdida del tejido mamario. El límite medial se ubica en el borde del esternón y no debe cruzar la línea media. El límite lateral corresponde a la línea axilar media, aunque la ptosis puede modificar esa apreciación. El límite anterior es la piel o unos pocos milímetros por debajo de la superficie cutánea cuando el objetivo es reportar dosis. El límite posterior son los músculos pectorales y los músculos de la pared torácica. El volumen no debe incluir esos músculos ni las costillas. En casos muy mediales o muy laterales, los límites pueden extenderse ligeramente más allá de estas definiciones para asegurar margen adecuado alrededor de la cavidad de tumorectomía. |
| Cavidad de tumorectomía | Debe incluir seroma, clips quirúrgicos y diferencias llamativas en el tejido glandular de la mama. La comparación con la mama contralateral puede ayudar, sobre todo cuando no hay líquido ni clips. Todos los estudios de imagen disponibles deben revisarse antes de planificar para ayudar a definir este volumen. Este volumen no debe extenderse fuera del tejido mamario. |
| CTV de tumorectomíaa | Corresponde a la cavidad de tumorectomía con expansión de 1,0 a 1,5 cm. No debe extenderse fuera del cuerpo ni entrar en los músculos pectorales o de la pared torácica. |
| PTV de tumorectomíaa | Es el CTV de tumorectomía con un margen basado en la incertidumbre del setup y el movimiento previsto de la paciente, en general entre 0,5 y 1,0 cm. Este volumen puede extenderse más allá de la superficie del paciente e introducirse en los músculos pectorales o de la pared torácica. Pueden requerirse ajustes para fines de reporte de dosis. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 11.1)
a Solo para APBI; en la irradiación de mama completa, la cavidad de tumorectomía por sí sola es el blanco del boost.
Ese nivel de detalle explica por qué los autores exigen referencia clínica. La mama no es un volumen que deba resolverse solo con la ventana de partes blandas. La distribución glandular, la caída inferior y lateral por la ptosis y la relación con esternón y línea axilar media exigen lectura clínica ya en la simulación. El texto incluso permite una discreta extensión más allá de esas reglas en casos muy mediales o muy laterales para asegurar margen adecuado sobre la cavidad de tumorectomía. La norma anatómica existe, pero no debe comprometer la cobertura del lecho operado.
La cavidad de tumorectomía sigue otra lógica. Entran seroma, clips y diferencias evidentes del tejido glandular. Si esos signos son sutiles o están ausentes, el capítulo recomienda comparar con la mama contralateral y revisar las imágenes previas. Lo que desaconseja de forma implícita es un contorno vago basado en memoria o en indicios pobres sobre la tomografía. El blanco del boost, y en APBI la base de CTV y PTV, debe ser defendible.
Además, el capítulo marca una diferencia nítida entre mama completa y APBI. En la irradiación de mama completa, la cavidad sola es el blanco del boost. En APBI, la expansión pasa a formar parte estructural del tratamiento con CTV y PTV propios. Ese cambio parece pequeño, pero modifica toda la geometría del plan.
Corazón, pulmones y los detalles del contorneo cardíaco
En todos los casos, los órganos de riesgo deben incluir corazón y pulmones. El corazón debe contornearse superiormente hasta la bifurcación de la arteria pulmonar, incluyendo el pericardio y la grasa epicárdica situada entre el músculo cardíaco y el pericardio. La grasa pericárdica por fuera del pericardio no necesita incluirse. La figura correspondiente muestra exactamente esa diferencia y elimina una fuente frecuente de variabilidad entre planificadores.
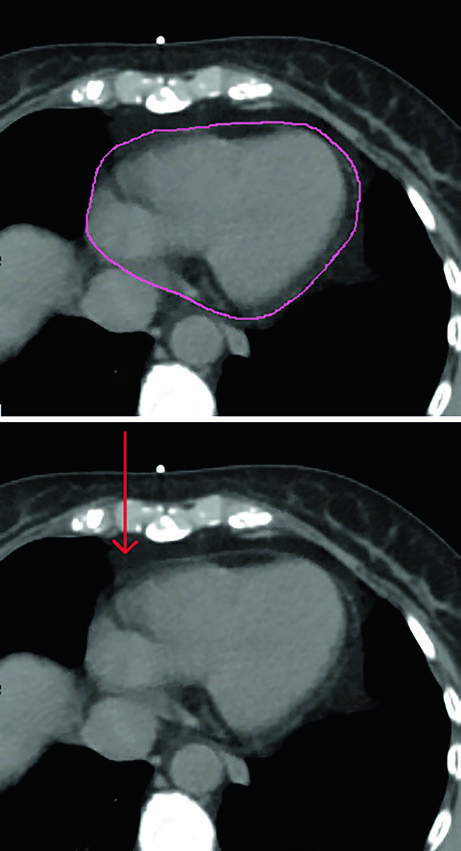
El capítulo también ordena la jerarquía de evaluación. La mejor evidencia para evitar toxicidad cardíaca sigue apoyándose en la reducción de la dosis media al corazón. Al mismo tiempo, los autores señalan que están emergiendo datos sobre la importancia potencial de la dosis a la arteria descendente anterior izquierda y al ventrículo izquierdo. Por eso, esas estructuras pueden contornearse con ayuda de los atlas publicados por Feng et al. y Duane et al., tal como figura en las referencias del capítulo.
Esa convivencia entre un parámetro consolidado y una evaluación más fina de subestructuras es una de las virtudes del texto. No reemplaza de manera prematura un criterio robusto por otro aún emergente. Permite sumar precisión cuando sea útil, sin abandonar la dosis media cardíaca como eje de decisión. Esa lectura encaja bien con la recomendación de considerar DIBH en tumores izquierdos y con el uso de pequeños bloqueos MLC cuando el plan supino necesite protección adicional.
Lo que aportan las figuras a la práctica diaria
Las figuras del capítulo hacen más que ilustrar. Las imágenes axiales en supino y prono muestran cómo cambia la relación entre mama, pulmón y corazón según el setup, y por eso la posición de la paciente aparece como decisión de planificación y no como costumbre. La figura de APBI convierte una regla abstracta de expansión en un ejercicio anatómico visible. Las figuras de boost y del plan APBI terminan de mostrar que la elección del haz debe seguir la profundidad y la geometría del blanco, no la inercia.
Leído en conjunto, el capítulo deja un mensaje muy estable. La radioterapia de mama inicial debe planificarse con técnica estandarizada, revisión minuciosa de cirugía e imagen, simulación reproducible, respeto estricto de los límites anatómicos de la mama y vigilancia continua sobre corazón y pulmones. El texto convence porque cada recomendación, desde los cortes de 1,5 a 2 mm en APBI hasta la inclusión de parte del pectoral en el borde posterior del campo prono, está ligada a una consecuencia concreta del tratamiento.




