Radioterapia en Linfoma: De la EFRT a la ISRT Moderna
La delineación de campo en radioterapia para linfoma de Hodgkin (LH) y linfoma no Hodgkin (LNH) ha experimentado una transformación profunda en las últimas dos décadas. La antigua radioterapia de campo extendido (EFRT), utilizada como tratamiento definitivo sin quimioterapia, fue reemplazada por la radioterapia de campo involucrado (IFRT) con la adopción de terapia combinada. Hoy, la radioterapia de sitio involucrado (ISRT) es el estándar recomendado por las directrices internacionales del ILROG.
La ISRT reduce aún más los volúmenes tratados en comparación con la IFRT, centrándose en la extensión original de la enfermedad con márgenes que compensan las limitaciones de imagen. El objetivo es claro: minimizar los efectos tardíos del tratamiento y mejorar la calidad de vida de los supervivientes, especialmente considerando que muchos pacientes con linfoma son adultos jóvenes con larga expectativa de vida.
Cuando el oncólogo radioterapeuta evalúa al paciente antes de la imagen diagnóstica, se puede emplear la técnica de radioterapia de ganglio involucrado (INRT). Los principios de delineación para INRT e ISRT son similares, pero los márgenes de ISRT deben ser mayores debido a las incertidumbres en el registro de imagen. En Europa, donde el PET-CT prequimioterapia en posición de tratamiento es rutina, prevalece la INRT. En Norteamérica, la ISRT sigue siendo el estándar. Para una visión completa de las estrategias de delineación, consulte nuestra guía completa sobre delineación de volúmenes blanco.
Principios de Delineación: GTV, CTV, ITV y PTV
La simulación para ISRT requiere planificación tridimensional — CT simulador, PET/CT o RM. El contraste intravenoso debe utilizarse siempre que las condiciones del paciente lo permitan para identificar los vasos con precisión. Cuando la RT consolida la respuesta tras quimioterapia, el PET-CT pre y posquimioterapia debe fusionarse con el CT de simulación en el sistema de planificación.
La delineación sigue la nomenclatura del ICRU Report 83:
- GTV prequimioterapia — toda la enfermedad macroscópica visible en la imagen inicial.
- GTV posquimioterapia — enfermedad residual en la simulación.
- CTV — volumen que engloba la extensión superior e inferior del GTV prequimioterapia, con límites radiales que respetan las estructuras normales no involucradas (pulmones, riñones, músculos). Típicamente, el CTV se extiende 1–2 cm más allá del GTV prequimio en dirección craneocaudal. Los volúmenes ganglionares separados por más de 5 cm pueden tratarse como campos independientes.
- ITV — CTV más margen para movimiento respiratorio según ICRU Report 83. Una simulación 4D-CT es ideal; sin ella, márgenes de 1,5 a 2 cm pueden ser necesarios en tórax y abdomen superior.
- PTV — margen institucional para incertidumbres de posicionamiento e inmovilización.
El CTV para ISRT tiende a ser mayor que el de INRT por la falta de imagen pretratamiento óptima. Cuando la RT se utiliza como modalidad única en LNH indolente estadio inicial o LH nodular de predominio linfocítico, el CTV debe ser más generoso ante la mayor preocupación por enfermedad subclínica sin quimioterapia previa.
Casos Clínicos: Delineación por Subtipo y Estadio
LH Estadio Inicial Favorable
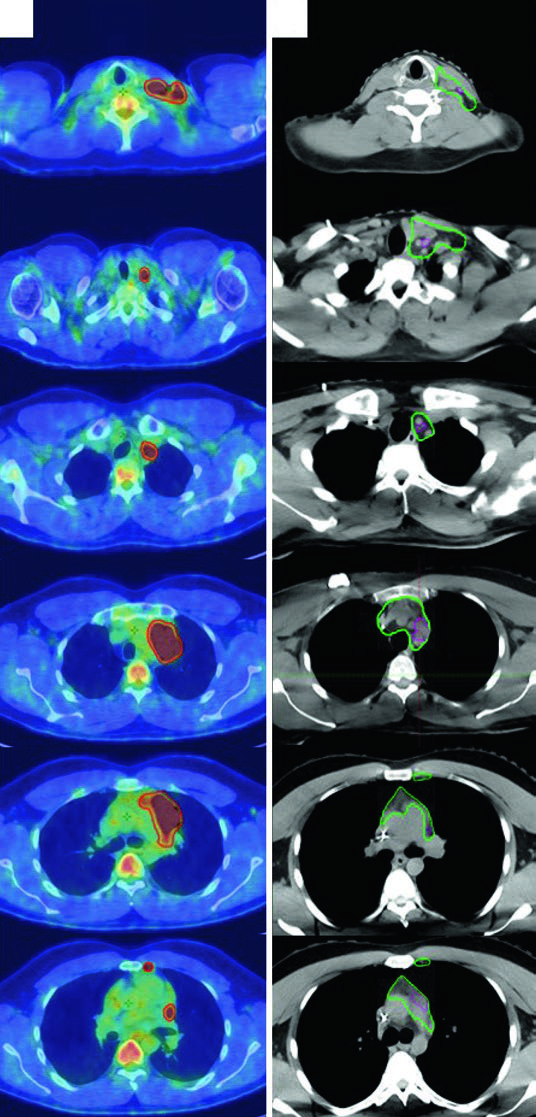
El caso clásico es un hombre de 27 años con LH esclerosis nodular estadio IIA, no voluminoso, riesgo favorable, que involucra las regiones supraclavicular izquierda y mediastínica. Tras 2 ciclos de ABVD, el PET posquimioterapia mostró respuesta metabólica completa (Deauville 2). Siguiendo los criterios del H10 (German Hodgkin Study Group), recibió 20 Gy de RT.
El PET/CT prequimioterapia se registró con el CT de simulación. Los cambios en la posición de los brazos, el cuello hiperextendido y la máscara de 5 puntos retrayendo los hombros generan diferencias anatómicas entre los estudios — precisamente esas incertidumbres que el abordaje ISRT resuelve. Este paciente usó técnica de breath-hold, por lo que no hay expansión de CTV a ITV.
LH Avanzado con Enfermedad Voluminosa
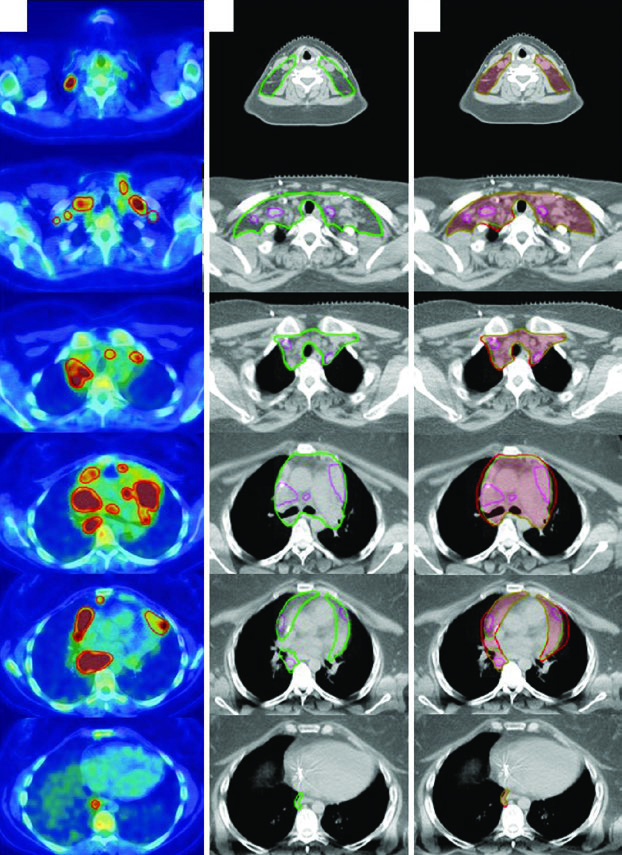
Una mujer de 31 años con LH esclerosis nodular estadio IIB voluminoso que involucra ganglios cervicales, supraclaviculares, mediastínicos e hiliares bilaterales recibió 2 ciclos de ABVD (respuesta completa en PET interino, Deauville 2), seguidos de 4 ciclos de AVD (Bleomicina suspendida por toxicidad pulmonar). La RT consolidativa fue indicada por la enfermedad voluminosa inicial.
El ITV final se obtuvo por 4D-CT en la simulación, capturando las variaciones anatómicas respiratorias. La prescripción se realizó al ITV más el margen de PTV institucional. Este caso demuestra cómo la ISRT se adapta a la anatomía posquimioterapia: el CTV respeta la extensión craneocaudal del GTV prequimio mientras limita la exposición radial de las estructuras normales adyacentes.
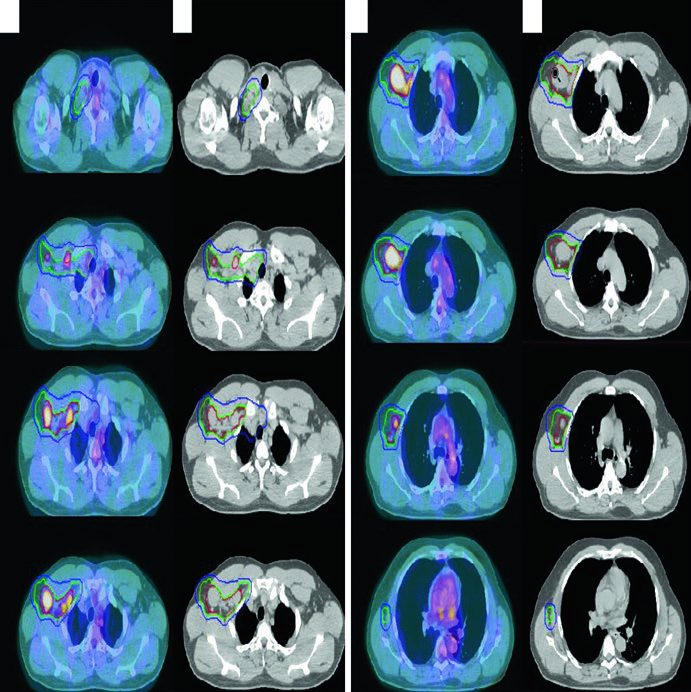
LH Nodular de Predominio Linfocítico (NLPHL)
Un hombre de 61 años con NLPHL estadio IIA que involucra ganglios supraclavicular derecho, subpectoral y axilar fue tratado con RT definitiva aislada. Simulado con brazos elevados en wingboard. El PET diagnóstico se fusionó al CT de simulación. Como la RT fue modalidad única (sin quimioterapia), márgenes de CTV más generosos fueron necesarios para cubrir la potencial enfermedad subclínica.
DLBCL de Cabeza y Cuello
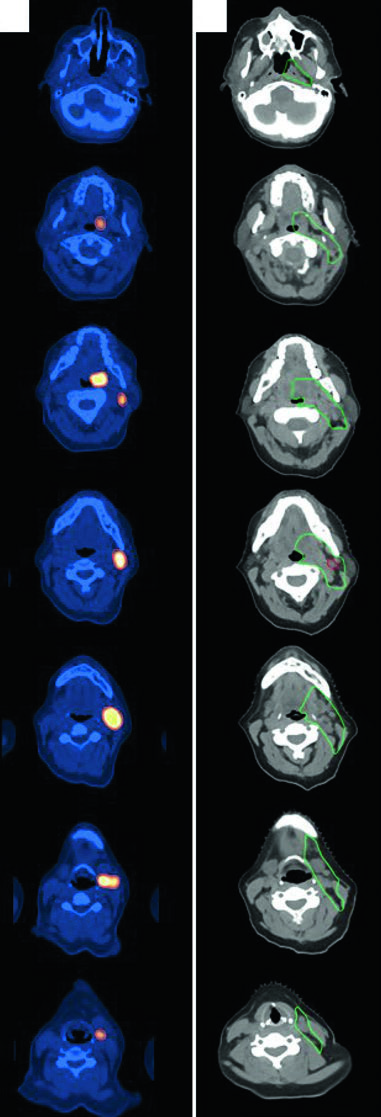
Una mujer de 47 años con DLBCL estadio IIA de amígdala izquierda y cuello izquierdo (nivel 2, 5,6 cm) recibió 3 ciclos de R-CHOP seguidos de RT consolidativa. Simulada con cuello en extensión, inmovilizada con máscara aquaplast de 5 puntos. El CTV ISRT cubre toda la amígdala izquierda y el nivel ganglionar involucrado, incluyendo 1–2 cm superior e inferior a la extensión prequimioterapia. Los casos de linfoma de cabeza y cuello exigen atención meticulosa al registro entre PET diagnóstico y CT de simulación.
Linfoma Folicular Inguinal
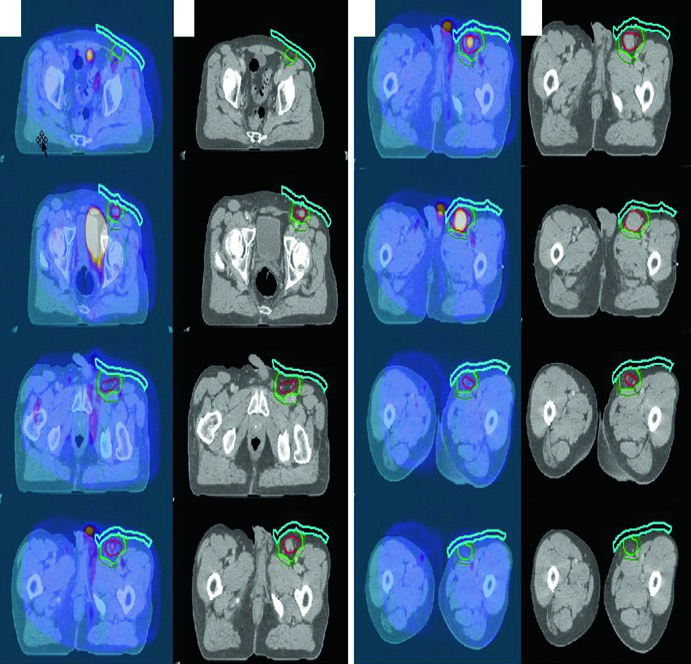
Un hombre de 70 años con linfoma folicular grado I/II estadio IA de la región inguinal/femoral izquierda fue tratado con RT definitiva aislada. El PET diagnóstico se fusionó al CT de simulación. Se utilizó bolus para aumentar la dosis superficial y mejorar la cobertura dosimétrica — un detalle frecuentemente olvidado en lesiones subcutáneas inguinales.
Sitios Extranodales: Inguinal, Gástrico y Orbital
Linfoma Inguinal y Pélvico
La simulación debe realizarse en posición de «patas de rana» para separar el muslo de los genitales externos y aplanar los pliegues cutáneos inguinales, minimizando las reacciones de piel. En hombres, blindar los testículos con clamshell y recomendar criopreservación de esperma. En mujeres en edad reproductiva, considerar la posición de los ovarios. Técnicas modernas como 3DCRT e IMRT son recomendadas, con adición de bolus cuando sea necesario.
Linfoma Gástrico
Los pacientes deben ayunar 3–4 horas antes de la simulación y de cada fracción para disminuir la motilidad gástrica. El contraste oral es obligatorio en todos los casos y el IV se recomienda cuando hay ganglios involucrados. La simulación usa posición con brazos elevados y molde personalizado. El movimiento respiratorio debe evaluarse por 4D-CT, y el tratamiento con DIBH (respiración profunda sostenida) debe considerarse.
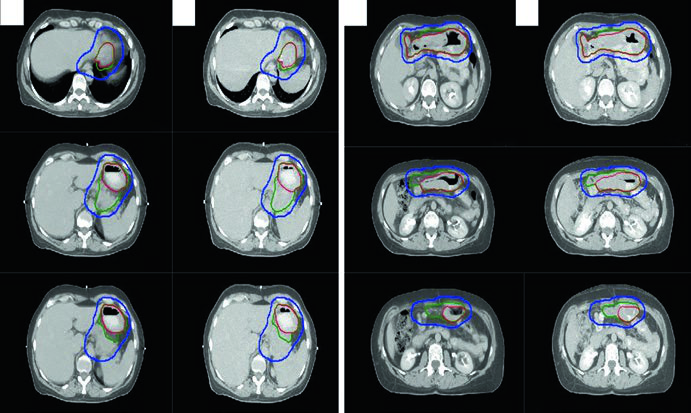
Las técnicas conformacionales 3DCRT e IMRT son recomendadas para proteger riñón e hígado. Los volúmenes blanco sugeridos para linfoma extranodal se detallan en la siguiente tabla.
Volúmenes Blanco Sugeridos para Sitios Extranodales
| Sitio | Definición de Volúmenes |
|---|---|
| Gástrico | GTV = enfermedad macroscópica; CTV = GTV + estómago desde la unión gastroesofágica a la gastroduodenal; PTV = CTV + 2 cm (evaluar 4D-CT) |
| Orbital | GTV = enfermedad macroscópica; CTV = GTV + órbita completa; PTV = CTV + 5 mm |
| Sinonasal | CTV = GTV prequimio + seno(s) involucrado(s) completo(s); PTV = CTV + 4–5 mm (según técnica de posicionamiento) |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 31.1)
En la práctica, el margen de 2 cm del PTV gástrico puede no ser suficiente en algunos pacientes — el grado de motilidad del estómago varía considerablemente, y la evaluación por 4D-CT es decisiva para definir la expansión adecuada.
Linfoma Orbital y Sinonasal
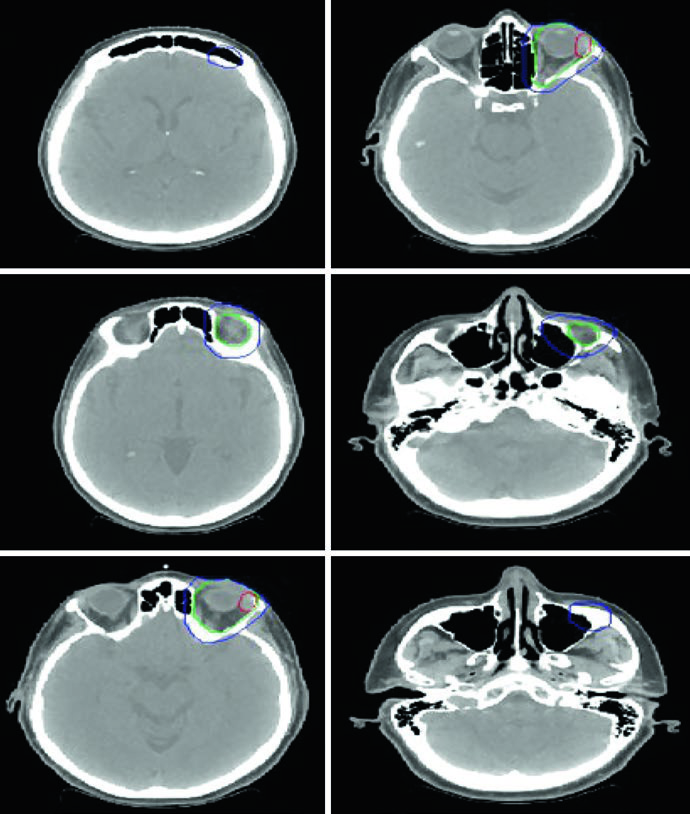
La simulación se realiza en decúbito supino, brazos al lado del cuerpo e inmovilización con máscara termoplástica. Para linfoma orbital, las opciones técnicas incluyen par de cuñas superior-inferior, 3DCRT o IMRT. El bolus puede aumentar la dosis superficial en enfermedad localizada de tejidos blandos. Cuando la dosis prescrita alcanza 30 Gy o más, considerar el blindaje de la glándula lagrimal.
En enfermedad indolente limitada de la conjuntiva, el tratamiento con haz de electrones anterior o energía mixta electrones/fotones es una alternativa, con blindaje del cristalino si el tumor está en la periferia. Para linfomas sinonasales, la 3DCRT o IMRT es recomendada por las dosis más altas necesarias y la proximidad de estructuras críticas.
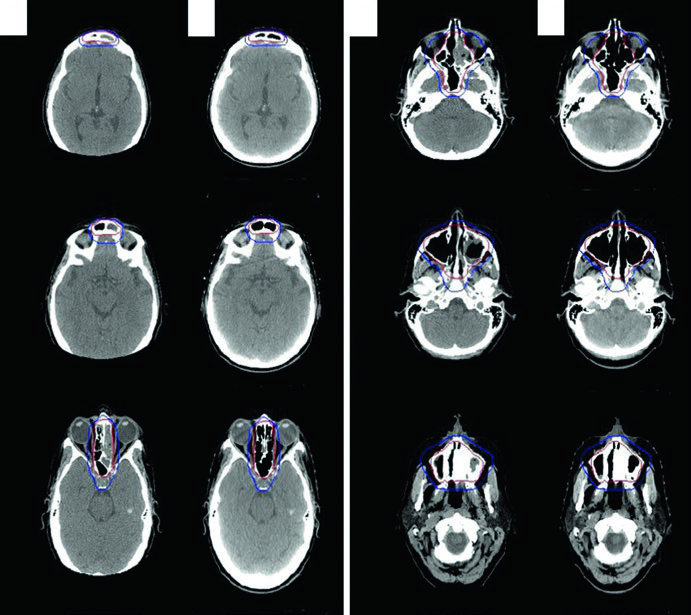
El caso ilustrativo es una mujer de 56 años con DLBCL de seno etmoides/esfenoides izquierdo, con extensión hacia la cavidad nasal derecha cruzando el tabique, erosión de la placa cribiforme superiormente, erosión de la pared orbitaria medial izquierda lateralmente y extensión al seno maxilar izquierdo inferiormente. El seno frontal izquierdo estaba completamente opacificado. Tras resección casi total y 3 ciclos de R-CHOP, la RT consolidativa fue administrada con CTV ISRT cubriendo la totalidad de los senos involucrados. El abordaje de delineación de tumores de la cavidad nasal y senos paranasales sigue principios similares.
Consideraciones Prácticas y Recomendaciones
La calidad del registro entre imagen prequimioterapia y CT de simulación es el factor crítico que define si los márgenes de ISRT pueden minimizarse o deben permanecer generosos. Cuando el PET-CT prequimioterapia se adquiere en la misma posición del tratamiento — como es rutina en centros europeos especializados — la transición a INRT es natural y permite campos aún más pequeños.
El uso consistente de 4D-CT para lesiones mediastínicas y del abdomen superior es altamente recomendable, ya que márgenes de 1,5–2 cm pueden ser necesarios sin esta información. Para la planificación detallada de sitios como cáncer gástrico y metástasis cerebrales, otros artículos de esta serie profundizan aspectos específicos de cada topografía. La delineación en linfoma exige una integración cuidadosa de imágenes multimodales — PET, CT y RM — para equilibrar la cobertura tumoral y la protección de tejidos normales.




