La cáncer de pulmón delineación de volumen blanco exige dominar simultáneamente el movimiento respiratorio, la anatomía linfonodal mediastínica y los principios biofísicos del fracionamiento ablativo. Desde el SBRT de un tumor periférico de 1,5 cm hasta la irradiación de una cadena N3 con quimiorradioterapia concurrente, cada escenario tiene su propia lógica de márgenes. Este artículo sigue el capítulo de Wijetunga, Liao y Gomez en Target Volume Delineation and Field Setup, 2nd Edition y traduce esos principios en criterios clínicos accionables.
Este artículo detallado forma parte de la guía completa de delineación de volumen blanco, que cubre pulmón, mama, esófago y otros sitios torácicos de forma sistemática. Para comparar con la cobertura nodal en mama, el artículo sobre irradiación nodal regional de mama aborda territorios anatómicos adyacentes en las regiones supraclavicular y mamaria interna.
¿Qué técnica de planificación corresponde a cada escenario pulmonar?
El estadio define la técnica: SBRT para enfermedad localizada estadio I, IMRT o 3D-CRT con quimioterapia para enfermedad localmente avanzada, campos limitados en el escenario posoperatorio. En todos los casos, el manejo del movimiento respiratorio determina si los márgenes son racionales o arbitrarios — no es un paso opcional.
La TC con contraste es la base del plan. La TC 4D captura el movimiento tumoral a lo largo del ciclo respiratorio y genera el GTV interno (iGTV) o el volumen interno de tumor (ITV), según la estrategia de márgenes elegida. La PET-TC añade información metabólica fundamental para distinguir tumor viable del colapso postobstructivo — problema frecuente en pulmón. La mediastinoscopía y el EBUS completan la estadificación ganglionar cuando la imagen resulta equívoca.
La delimitación de OAR incluye ambos pulmones, corazón, médula espinal, esófago, pared torácica, grandes vasos, árbol bronquial proximal (PBT) y plexo braquial en los tumores de sulco superior. Las restricciones de dosis siguen la publicación QUANTEC (Marks et al., 2010).
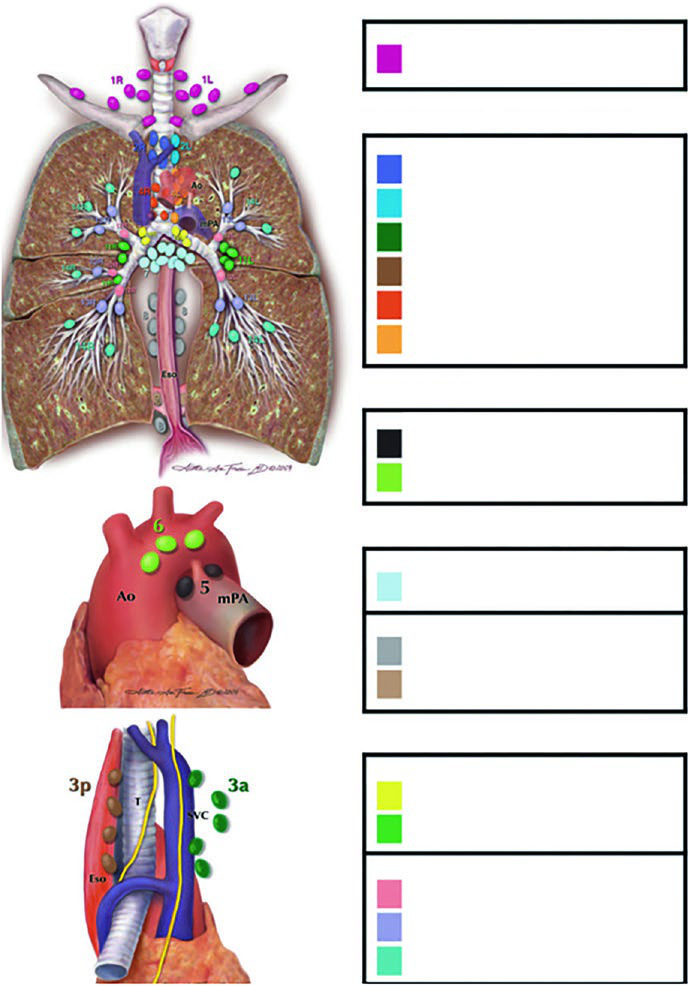
Estaciones linfonodales: el atlas de Michigan como referencia
Todo planificador torácico necesita tener el atlas linfonodal de Michigan incorporado a su razonamiento espacial. Sin ese mapa, las decisiones sobre campo involucrado versus electivo se vuelven arbitrarias.
Las estaciones se agrupan por zonas anatómicas:
- Supraclavicular: Estación 1
- Mediastino superior: 2R, 2L, 3a, 3p, 4R, 4L
- Aórtica: 5, 6
- Mediastino inferior: 7, 8, 9
- N1 (intrapulmonares): 10, 11, 12, 13, 14
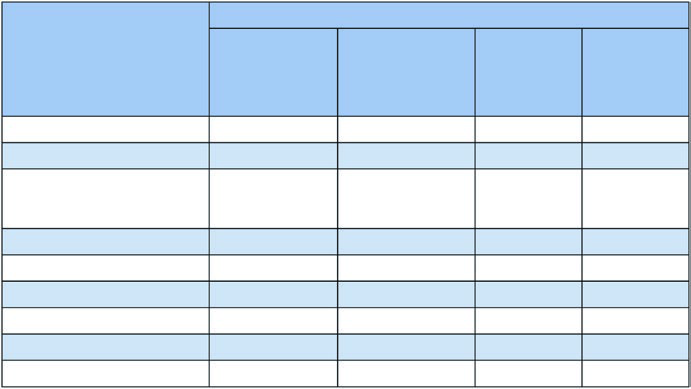
La tabla a continuación, basada en los datos de la Figura 13.1b del capítulo, muestra el riesgo de compromiso por estación según la localización del tumor primario. Estos porcentajes orientan la decisión de incluir o excluir regiones electivas del campo.
Riesgo de compromiso linfonodal por lóbulo tumoral
| Estación | LSD (%) | LMD (%) | LID (%) | LSI (%) | LII (%) |
|---|---|---|---|---|---|
| 1 (Supraclavicular) | 11 | 4 | 3 | 17 | 3 |
| 2R | 31 | 26 | 12 | 5 | 3 |
| 2L | 3 | 0 | 2 | 21 | 7 |
| 3a | 4 | 7 | 5 | 3 | 3 |
| 4R | 64 | 59 | 26 | 8 | 4 |
| 4L | 6 | 4 | 5 | 56 | 18 |
| 5 | 4 | 0 | 2 | 71 | 22 |
| 6 | 2 | 0 | 2 | 32 | 8 |
| 7 (Subcarinal) | 20 | 48 | 35 | 19 | 33 |
| 8 | 2 | 11 | 15 | 5 | 50 |
| 9 | 2 | 4 | 5 | 2 | 17 |
| 10 (Hilar ipsilateral) | 59 | 63 | 49 | 56 | 46 |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition. LSD=lóbulo superior derecho, LMD=lóbulo medio derecho, LID=lóbulo inferior derecho, LSI=lóbulo superior izquierdo, LII=lóbulo inferior izquierdo.
Enfoque de campo involucrado: por qué no irradiar de forma electiva
La irradiación nodal electiva de rutina fue abandonada porque los estudios mostraron tasa baja de fallo ganglionar electivo y toxicidad esofágica y pulmonar inaceptable cuando los campos grandes cubrían todo el mediastino. El ensayo aleatorizado que comparó campo involucrado versus electivo demostró mejores resultados con el campo involucrado — coherente con la biología: irradiar ganglios clínicamente negativos agrega dosis sin beneficio demostrado.
La lógica es directa: tratar lo que se ve en la imagen. El GTV incluye el tumor primario y los ganglios PET-positivos o con criterio de tamaño por TC. Las regiones electivas quedan fuera salvo indicación específica, como CPCP de estadio limitado con enfermedad hilar.
Expansiones GTV → PTV: dos estrategias prácticas
El capítulo describe dos enfoques para incorporar el movimiento respiratorio en las expansiones del volumen blanco:
Enfoque 1 — basado en iGTV: GTV → iGTV (envolvente de movimiento de TC 4D) → iCTV (expansión isotrópica sobre el iGTV) → PTV (margen de setup). Este enfoque es el preferido en SBRT, donde la definición precisa del iGTV es crítica para respetar la zona de no irradiación (ZNI) peribronquial.
Enfoque 2 — CTV convencional con ITV: GTV → CTV (expansión microscópica) → ITV (CTV desplazado por el envolvente de la TC 4D) → PTV. Preferido en casos posoperatorios sin volumen tumoral macroscópico y en CPCNP localmente avanzado con IGRT sistemático.
Simulación: posicionamiento y adquisición antes de la delineación
El posicionamiento reproducible es la precondición para márgenes racionales. Brazos por encima de la cabeza reduce la dosis en el plexo braquial para los tumores superiores y retira los brazos de los haces. Un dispositivo de inmovilización — molde personalizado o tabla con soportes para los brazos — debe usarse de forma consistente a lo largo de todo el tratamiento.
La TC 4D requiere un entrenamiento adecuado para lograr una respiración regular. La respiración irregular durante la TC 4D genera artefactos en la reconstrucción de fase que se traducen directamente en una definición imprecisa del iGTV. Si el entrenamiento no está disponible, la TC lenta (tiempo de rotación prolongado que captura el movimiento medio) es una alternativa razonable para casos no-SBRT.
La TC con contraste en la sesión de simulación es preferible para la delineación mediastínica: aclara los límites vasculares en las estaciones 4R, 4L, 5 y 6, donde distinguir ganglios de estructuras vasculares adyacentes puede ser genuinamente difícil en la imagen sin contraste. La fusión con PET afina aún más la definición del GTV cuando existe atelectasia: el pulmón colapsado debe excluirse del GTV salvo que el PET muestre actividad metabólica dentro del colapso.
SBRT en CPCNP estadio inicial: máxima precisión, máxima BED
El SBRT es el tratamiento de elección para el CPCNP estadio I en pacientes médicamente inoperables y crece como alternativa en operables de alto riesgo. El objetivo es BED > 100 Gy en el tumor con la mínima dosis posible en el tejido normal circundante.
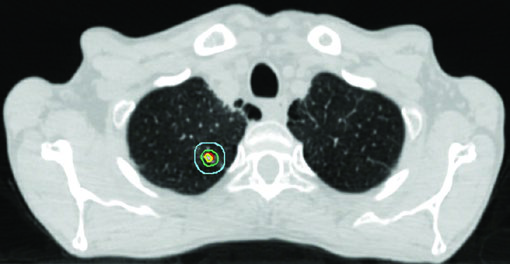
La expansión iGTV → iCTV en estadio inicial es pequeña: 0 a 0,2 cm. Para un tumor pequeño y periférico, la extensión microscópica es mínima y el margen de setup domina la expansión final. El margen PTV adicional depende de la tecnología de IGRT disponible.
El árbol bronquial proximal (PBT) — definido como los 2 cm distales de la tráquea, carina, bronquios principales, bronquios lobares y los primeros segmentos de los bronquios segmentarios — es la estructura más crítica en la planificación SBRT. Se define una zona de no irradiación (ZNI) de 2 cm más allá del PBT. Los tumores dentro o adyacentes a la ZNI se clasifican como centrales y requieren fraccionamiento menos ablativo.
Los esquemas de dosis varían según la localización:
- Periférico: 54 Gy/3fx (18 Gy/fx), 48 Gy/4fx (12 Gy/fx), 50 Gy/4fx o 50 Gy/5fx
- Central: 50 Gy/5fx, 70 Gy/10fx o 60 Gy/8fx
La dosis máxima en punto del PBT se restringe a 55 Gy en cualquier esquema. La Figura 13.2 del texto ilustra tres casos de estadio inicial: tumor periférico clásico tratado con 54 Gy/3fx, tumor próximo al PBT con 48 Gy/4fx y tumor central con 50 Gy/5fx.
CPCNP localmente avanzado (estadios II–III): control nodal con quimiorradioterapia
En la enfermedad localmente avanzada, la expansión iGTV → iCTV aumenta a 0,5–0,8 cm, reflejando los datos histológicos que muestran extensión microscópica significativa en CPCNP. El margen PTV depende del nivel de control de movimiento e IGRT implementado:
- 1,0–1,5 cm sin control de movimiento ni IGRT
- 0,5–1,0 cm con TC 4D o CBCT, pero no ambos
- 0,3–0,5 cm con TC 4D + kV/CBCT (enfoque preferido)
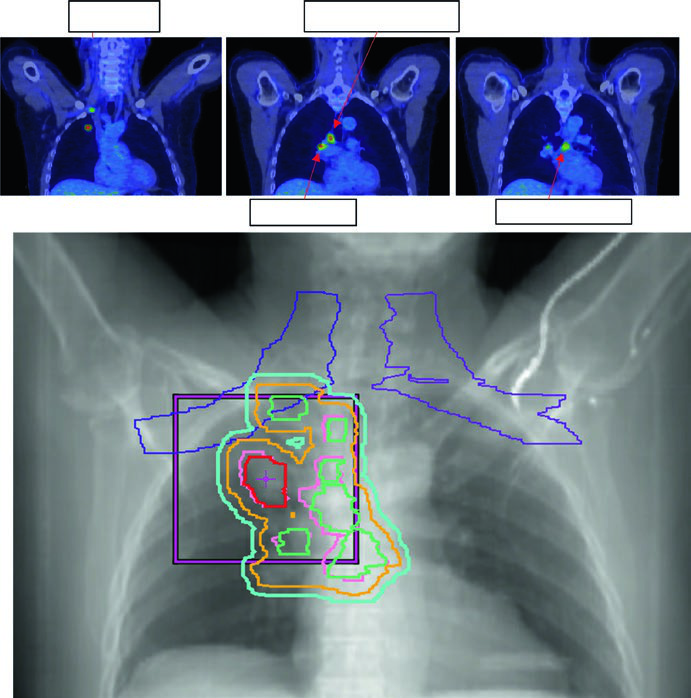
La dosis estándar para CPCNP estadio II–III con quimioterapia concurrente es 60 Gy en 30 fracciones (2 Gy/fx). La escalada de dosis por encima de 60 Gy no demostró beneficio en ensayos aleatorizados y aumenta la toxicidad. El GTV incluye tumor primario y ganglios comprometidos visibles en TC o PET.
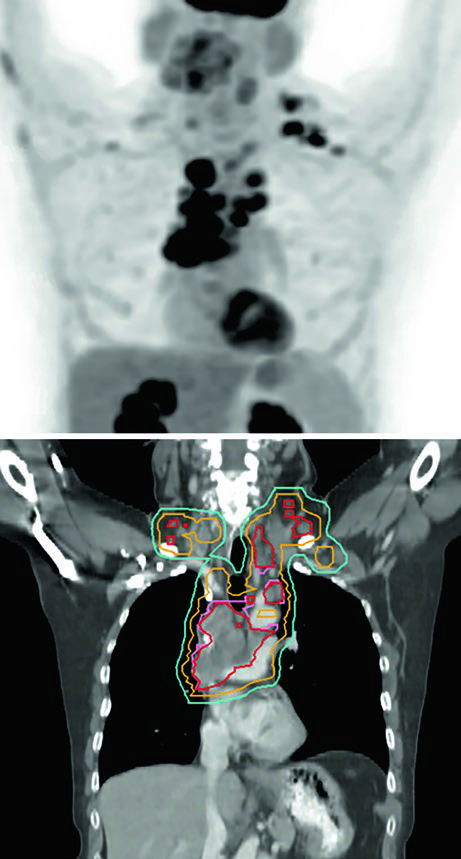
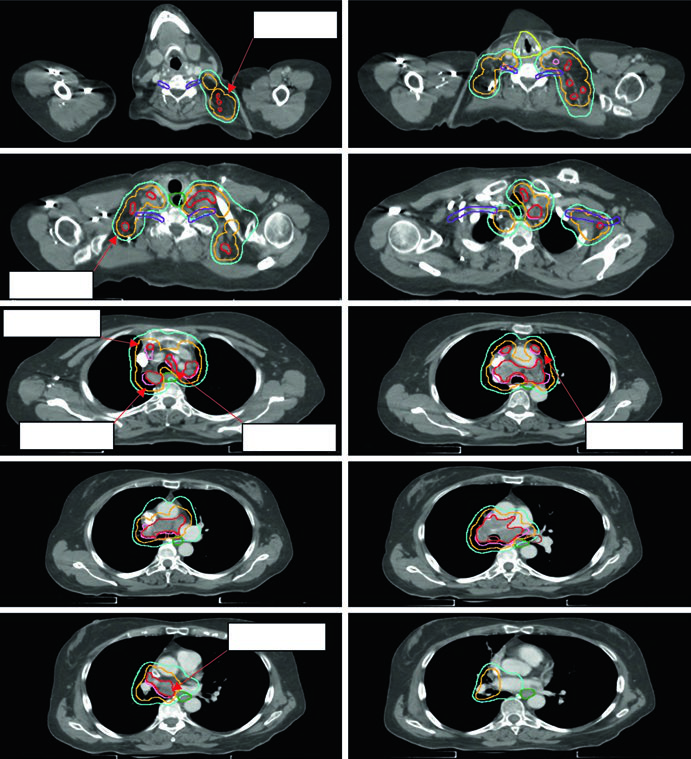
La Figura 13.3 muestra un caso cT1cN3M0 estadio IIIB: tumor en LSD con compromiso hilar derecho, subcarinal, paratraqueal y SCV derecha. El plan de 60 Gy/30fx cubre todos los sitios PET-positivos con exclusión de las cadenas electivas contralaterales. La Figura 13.4 muestra un caso cT4N3M0 estadio IIIC con SCV bilateral comprometida y síndrome de vena cava superior, requiriendo un campo que incluye el mediastino superior bilateral.
CPCNP posoperatorio: el campo limitado como nuevo estándar
La radioterapia posoperatoria en CPCNP ha evolucionado rápidamente. El enfoque histórico irradiaba campos extensos — lecho tumoral, ganglios comprometidos, mediastino bilateral, muñón ipsilateral y fosa supraclavicular — con toxicidad pulmonar y cardíaca relevante. El ensayo Lung ART reformuló ese paradigma.
El enfoque actual es limitado: regiones ganglionares patológicamente comprometidas más el muñón bronquial ipsilateral, con opción de extender un nivel por encima y por debajo de los niveles positivos. No hay GTV — la delineación comienza en el CTV. La secuencia estándar es CTV → ITV (movimiento respiratorio) → PTV (~0,5 cm de margen de setup).
Las dosis se estratifican por el estado del margen quirúrgico:
- R0 (márgenes libres): 50–54 Gy a 1,8–2,0 Gy/fx
- R1 (margen microscópicamente positivo): 54–60 Gy a 1,8–2,0 Gy/fx
- R2 (enfermedad macroscópica residual): 60 Gy con quimioterapia concurrente
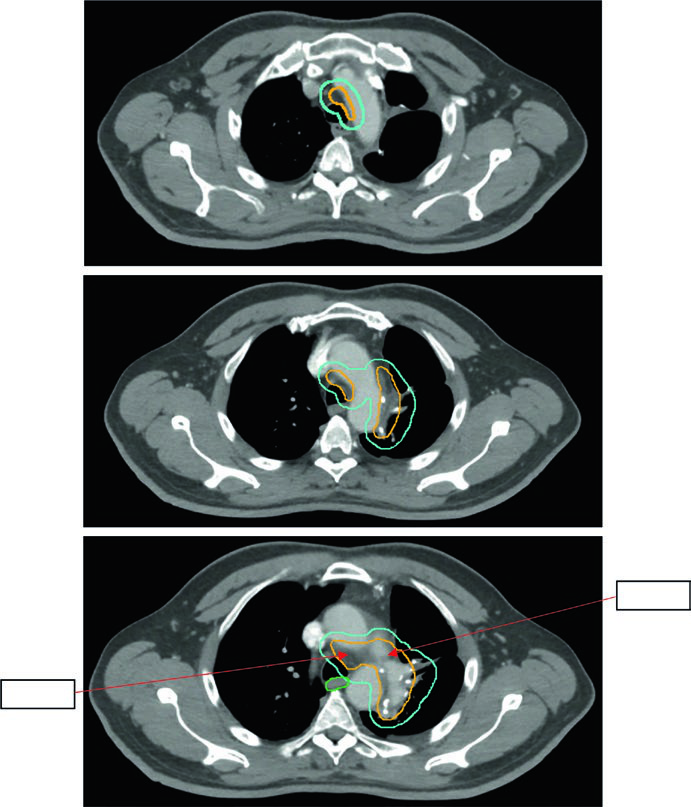
La Figura 13.5 muestra un tumor de 5,8 cm en LSI con positividad en los niveles 5 y 10L. Se utiliza el campo limitado según Lung ART, con 54 Gy/30fx.
CPCP: campo involucrado en enfermedad limitada y extensiva
El carcinoma de células pequeñas crece rápidamente y es relativamente radiorresistente como modalidad única, pero responde bien a la quimiorradioterapia combinada. El enfoque de campo involucrado es aceptado en ambos estadios.
La expansión GTV → CTV en CPCP es de 0,5 a 1,0 cm, incluyendo frecuentemente el hilio ipsilateral incluso sin evidencia PET, dados los patrones de drenaje linfático. Los márgenes CTV → PTV siguen las mismas directrices del CPCNP, calibradas según el IGRT disponible.
Los esquemas de dosis difieren por estadio:
- Estadio limitado: 45 Gy a 1,5 Gy dos veces al día (30 fracciones) — el esquema clásico de Turrisi — o 66–70 Gy a 2,0 Gy diario como alternativa de mayor dosis
- Estadio extensivo (consolidación): 30–45 Gy a 3,0 Gy/fx en sitios de enfermedad voluminosa
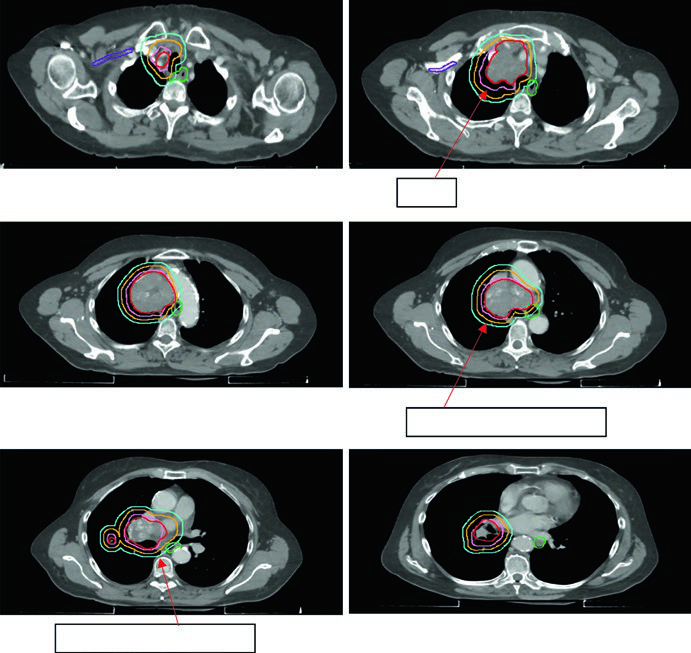
La Figura 13.6 muestra un caso cT2N2 de estadio limitado con el campo involucrado cubriendo el tumor primario y los ganglios mediastínicos comprometidos, pero excluyendo las cadenas electivas. El esquema utilizado fue 45 Gy/30fx BID.
Replanificación adaptativa: cuando la anatomía cambia durante el tratamiento
Los tumores obstructivos que causan atelectasia pueden resolverse parcialmente durante el tratamiento a medida que la radioterapia reduce el volumen tumoral y el pulmón se reaereas. Este fenómeno, visible en la CBCT de verificación, puede exponer tejido pulmonar previamente colapsado a dosis previstas para el tumor, alterando dramáticamente la distribución de dosis.
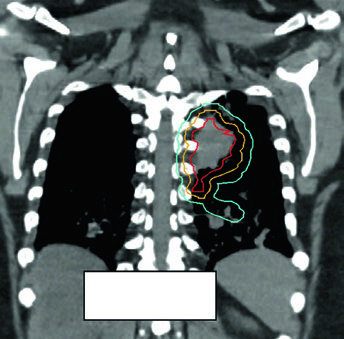
La replanificación adaptativa debe considerarse cuando la CBCT muestra cambio anatómico significativo — expansión pulmonar ipsilateral, resolución de derrame o reversión del colapso. El caso de la Figura 13.7 ilustra una lesión metastásica tratada con 45 Gy/15fx: la reaireación pulmonar durante el tratamiento exigió replanificación para proteger el pulmón recién ventilado.
No existe un protocolo universal para el desencadenante de la replanificación adaptativa. La revisión semanal de la CBCT por el dosimetrista y el oncólogo radioterapeuta es el mínimo razonable. Cualquier cambio visual significativo en el contorno pulmonar o mediastínico justifica recalcular los DVH antes de continuar.
Edición del iCTV y cobertura de dosis
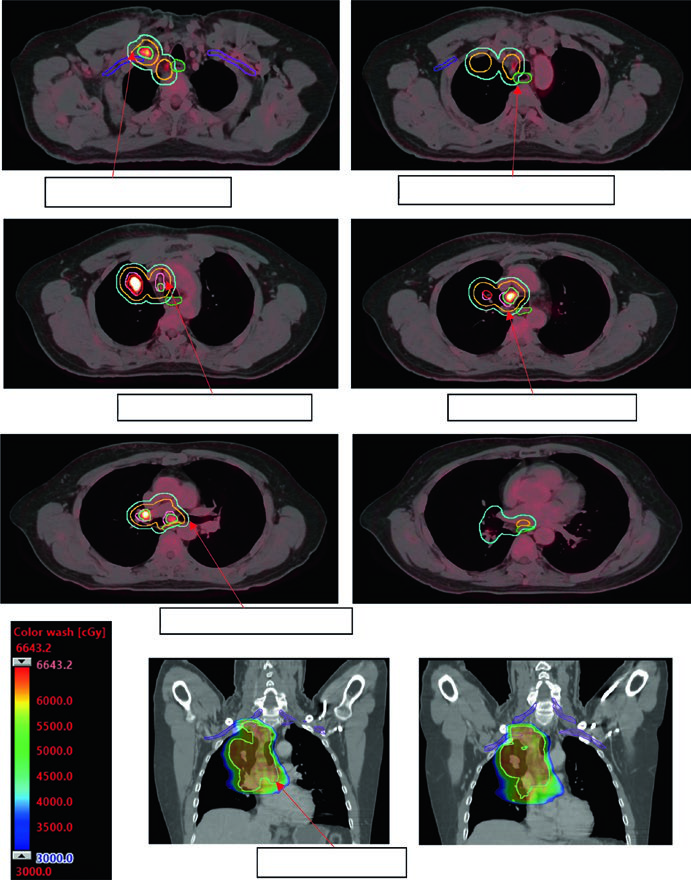
El iCTV se edita a partir del iGTV con atención a las barreras anatómicas: pleura, pared torácica, mediastino y grandes vasos limitan la extensión microscópica y permiten retraer el margen en esas direcciones. Esta edición reduce el volumen irradiado sin comprometer el control tumoral — siempre que la reconstrucción de fase media de la TC 4D se realice con rigor.
La cobertura de dosis adecuada se verifica mediante los DVH: V95 ≥ 95% del PTV, Dmin ≥ 90% de la dosis prescrita. En SBRT, la conformidad se evalúa por el índice PITV (relación volumen de isodosis prescrita / volumen PTV) y el índice de gradiente de dosis (GI). Una curva de isodosis ajustada al PTV con caída rápida hacia los tejidos normales circundantes es el objetivo.
Resumen de regímenes de dosis
| Escenario | Dosis Total | Fraccionamiento | Observaciones |
|---|---|---|---|
| CPCNP estadio I SBRT periférico | 54 Gy / 48 Gy / 50 Gy / 50 Gy | 3 fx / 4 fx / 4 fx / 5 fx | BED >100 Gy; máx PBT 55 Gy |
| CPCNP estadio I SBRT central | 50 Gy / 70 Gy / 60 Gy | 5 fx / 10 fx / 8 fx | Dentro o adyacente a la ZNI |
| CPCNP estadio II–III | 60 Gy | 30 fx (2 Gy/fx) | Con quimioterapia concurrente |
| Posoperatorio R0 | 50–54 Gy | 1,8–2,0 Gy/fx | Márgenes quirúrgicos libres |
| Posoperatorio R1 | 54–60 Gy | 1,8–2,0 Gy/fx | Margen microscópicamente positivo |
| Posoperatorio R2 | 60 Gy | 2,0 Gy/fx | Con quimioterapia concurrente |
| CPCP estadio limitado | 45 Gy o 66–70 Gy | 1,5 Gy BID (30 fx) o 2,0 Gy diario | Campo involucrado |
| CPCP extensivo consolidación | 30–45 Gy | 3,0 Gy/fx | Enfermedad voluminosa residual |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition — Capítulo 13 (Wijetunga, Liao, Gomez).
Restricciones de OAR y evaluación del plan de tratamiento
Las restricciones de dosis en los OAR pulmonares no son valores de referencia opcionales — superarlos produce eventos clínicos documentados. Corazón, pulmones, esófago y médula espinal son las cuatro estructuras que con mayor frecuencia limitan la calidad del plan.
Para los pulmones, los parámetros más utilizados son la dosis media pulmonar (DMP) y el V20 (volumen que recibe 20 Gy o más). DMP por debajo de 20 Gy y V20 por debajo del 35% son los umbrales convencionales para el tratamiento con fraccionamiento convencional. En SBRT, el V20 pierde relevancia; el V12,5 Gy y la dosis media del pulmón contralateral se convierten en los parámetros clave. El pulmón ipsilateral recibe dosis elevada por diseño en el SBRT lobar — el trabajo de restricción se centra en el pulmón contralateral y en el pulmón global menos el volumen del GTV.
La toxicidad esofágica es el OAR más limitante en el CPCNP localmente avanzado con quimioterapia concurrente. QUANTEC recomienda dosis media esofágica por debajo de 34 Gy, con V50 < 40% y V60 < 30%. En la práctica, la cobertura de ganglios mediastínicos frecuentemente supera estos límites; cuando eso ocurre, es necesaria una discusión explícita sobre el riesgo de toxicidad frente al beneficio de control local.
Las restricciones cardíacas incluyen V30 pericárdico y dosis media cardíaca. Los tumores voluminosos del lóbulo inferior izquierdo irradiados con quimioterapia concurrente producen frecuentemente dosis medias cardíacas superiores a 20 Gy; existe evidencia creciente que asocia esto con eventos cardíacos tardíos. La optimización de arcos IMRT para proteger la base cardíaca es recomendable cuando es técnicamente factible.
Integración clínica y práctica diaria
El pulmón concentra prácticamente todos los desafíos de la planificación en radioterapia: heterogeneidad tisular, movimiento, múltiples cadenas nodales, proximidad a estructuras críticas y escenarios que van del ablativo al paliativo. El clínico que domina estos principios puede adaptar el protocolo al paciente real — no al caso ideal del ensayo clínico.
Para quienes trabajan en oncología torácica de forma amplia, el artículo sobre cáncer de esófago: delineación y campos aporta principios complementarios para el mediastino inferior y la unión gastroesofágica. La guía completa de delineación ofrece el contexto sistemático para todos los sitios. Para mama con compromiso nodal, el artículo sobre irradiación nodal regional de mama es el complemento natural para entender las estaciones supraclaviculares y mamarias internas que se superponen anatómicamente al mediastino superior.




