La delineación en cáncer de pulmón depende de tres decisiones que el capítulo mantiene unidas de principio a fin: manejo del movimiento respiratorio, lectura correcta de las estaciones ganglionares torácicas y márgenes consistentes entre GTV, iGTV, iCTV, ITV y PTV. En NSCLC y SCLC, la planificación basada en CT con técnicas conformadas sigue siendo el estándar de cuidado, pero solo ayuda cuando la enfermedad macroscópica, la porción móvil y los órganos de riesgo vecinos están definidos con precisión.
3D-CRT, IMRT y SBRT emplean múltiples ángulos de haz y distintos niveles de conformidad, pero ninguna técnica compensa un mal contorneo. Si el objetivo está mal dibujado, el DVH solo describe el error con más detalle. Por eso el capítulo apoya el plan en examen físico, CT con contraste, PET y evaluación del mediastino mediante mediastinoscopia o EBUS antes de fijar el diseño final. Para ampliar el marco general, revise nuestra guía completa sobre delineación de volumen blanco y campos. Si desea comparar cómo la misma disciplina de márgenes y órganos críticos cambia en otro sitio, vea también el artículo dedicado al cáncer de laringe.
En este artículo
- Principios de planificación en cáncer de pulmón
- Estaciones nodales mediastínicas y patrón de riesgo
- Cómo definir GTV, iGTV, iCTV, ITV y PTV
- NSCLC inicial: SBRT, PBT y no-fly zone
- NSCLC estadio II-III: márgenes y dosis
- NSCLC posoperatorio
- SCLC y radioterapia torácica de consolidación
- Dosis aceptadas por escenario clínico
- Cuándo el CBCT obliga a replantear
- Referencias
Principios de planificación en cáncer de pulmón
En cáncer de pulmón, la planificación basada en CT y el manejo del movimiento respiratorio son el estándar tanto para NSCLC como para SCLC. El capítulo no presenta la simulación, la posición y la inmovilización como detalles menores. De ellas depende cuántas geometrías de haz son realmente utilizables y hasta dónde pueden reducirse los márgenes con seguridad.
El paciente debería simularse idealmente con los brazos por encima de la cabeza para maximizar las posibilidades geométricas del plan. Además, se recomienda una simulación en 4D para evaluar el movimiento interno. En radioterapia torácica esa decisión pesa mucho porque condiciona si el flujo de trabajo se apoya primero en iGTV o si el movimiento se incorpora después mediante un ITV.
El capítulo también es preciso respecto a las estructuras normales que deben contornearse cuando quedan próximas al campo: corazón, pulmones, médula espinal, esófago, pared torácica, grandes vasos, árbol bronquial proximal y plexo braquial en tumores superiores o con afectación paratraqueal alta o supraclavicular. El hígado debe incluirse en tumores del lóbulo inferior derecho cercanos al diafragma, y el bazo puede recibir dosis relevante en tumores muy bajos del pulmón izquierdo o en tumores pleurales izquierdos.
La filosofía de campos queda delimitada por una preferencia clara por la irradiación de campo involucrado. En NSCLC y SCLC con enfermedad macroscópica, el capítulo se apoya en series con baja tasa de fallo ganglionar electivo y en un ensayo aleatorizado que mostró mejores resultados con campo involucrado frente a irradiación nodal electiva. La conclusión práctica es directa: no deben cubrirse de rutina regiones nodales electivas si el médico entiende bien dónde está la enfermedad activa.
Estaciones nodales mediastínicas y patrón de riesgo
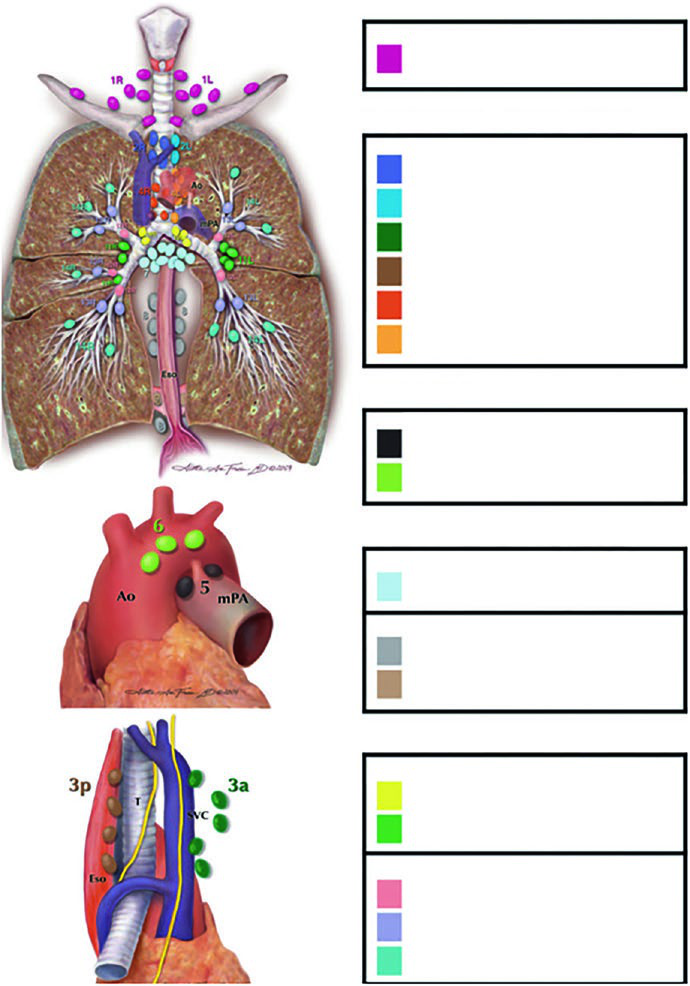
La irradiación de campo involucrado solo es segura cuando el mapa mediastínico se domina de memoria. El capítulo remite a atlas de consenso y organiza las estaciones de forma muy práctica: estación 1 en la zona supraclavicular; 2R, 2L, 3a, 3p, 4R y 4L en el mediastino superior; 5 y 6 en la región aórtica; 7, 8 y 9 en el mediastino inferior; y estaciones N1, de la 10 a la 14, a lo largo del hilio, interlóbulo, lóbulo, segmento y subsegmento.
Ese mapa no sirve solo para etiquetar ganglios. Ordena la lectura del PET/CT, orienta el muestreo con EBUS y da base anatómica a la omisión de regiones no afectadas. La Figura 13.1(b) es especialmente útil porque muestra que el riesgo nodal cambia con el lóbulo primario. Los tumores del lóbulo superior derecho favorecen estaciones paratraqueales y estación 3; los del lóbulo superior izquierdo desplazan el riesgo hacia 5 y 6; y los del lóbulo inferior izquierdo cargan más en 8 y 7 que en el mediastino superior.
Riesgo de afectación nodal según la localización del tumor primario
La tabla siguiente reproduce los porcentajes de la Figura 13.1(b). Resulta muy útil porque recuerda que un campo limitado solo es seguro cuando la anatomía de drenaje se conoce de verdad.
| Estación afectada | Lóbulo superior derecho (n=45) | Lóbulo medio/inferior derecho (n=36) | Lóbulo superior izquierdo (n=35) | Lóbulo inferior izquierdo (n=8) |
|---|---|---|---|---|
| Mediastino superior (1) | 9% | 3% | 0% | 0% |
| Paratraqueal (2) | 40% | 31% | 3% | 0% |
| Prevascular, retrotraqueal, pretraqueal (3) | 73% | 47% | 29% | 0% |
| Paratraqueal inferior (4) | 36% | 28% | 17% | 13% |
| Subaórtica (5) | – | – | 71% | 13% |
| Paraaórtica (6) | – | – | 43% | 25% |
| Subcarinal (7) | 36% | 69% | 20% | 38% |
| Paraesofágica (8) | 9% | 11% | 3% | 50% |
| Ligamento pulmonar (9) | 2% | 6% | 6% | 13% |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Fig. 13.1b)
Cómo definir GTV, iGTV, iCTV, ITV y PTV
El capítulo acepta dos rutas coherentes para construir el volumen blanco. En la primera, el médico delinea el GTV, evalúa el movimiento interno y genera el iGTV; a partir de allí se crean iCTV y luego PTV. En la segunda, el GTV se expande a CTV, el CTV se expande a ITV para incorporar el movimiento interno y, por último, el ITV se expande a PTV. Esa segunda secuencia también se usa en el escenario posoperatorio, donde no existe un GTV macroscópico.
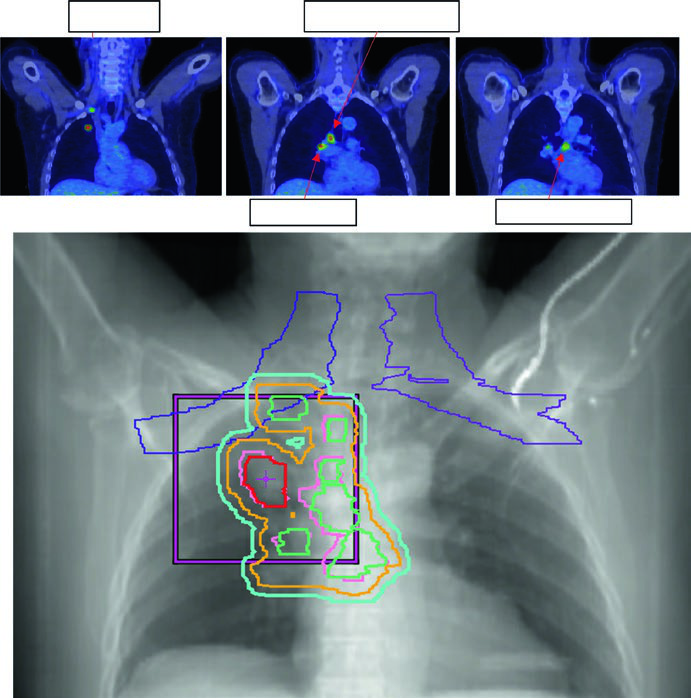
El ejemplo de NSCLC localmente avanzado del capítulo muestra por qué estas definiciones importan. El paciente tenía un tumor de 2,3 cm en el lóbulo superior derecho y adenopatías hiliares derechas, subcarinales, precarinales, paratraqueales y supraclaviculares derechas. El tumor primario y la región hiliar se delinearon en ventanas pulmonares de la CT, mientras que las estaciones nodales se definieron integrando PET/CT, CT con contraste y EBUS. Ese orden evita tanto subcontornear el primario como llenar el mediastino por inercia.
La figura de continuación añade un detalle de planificación muy valioso. El iCTV se editó para excluir hueso y esófago, y el iGTV ya incorporaba el movimiento de los ganglios. La expansión de iGTV a iCTV fue de 0,7 cm, seguida por 0,5 cm de iCTV a PTV. El mensaje de fondo es claro: el volumen clínico sigue siendo un volumen clínico, no una simple corona geométrica alrededor del tumor visible.
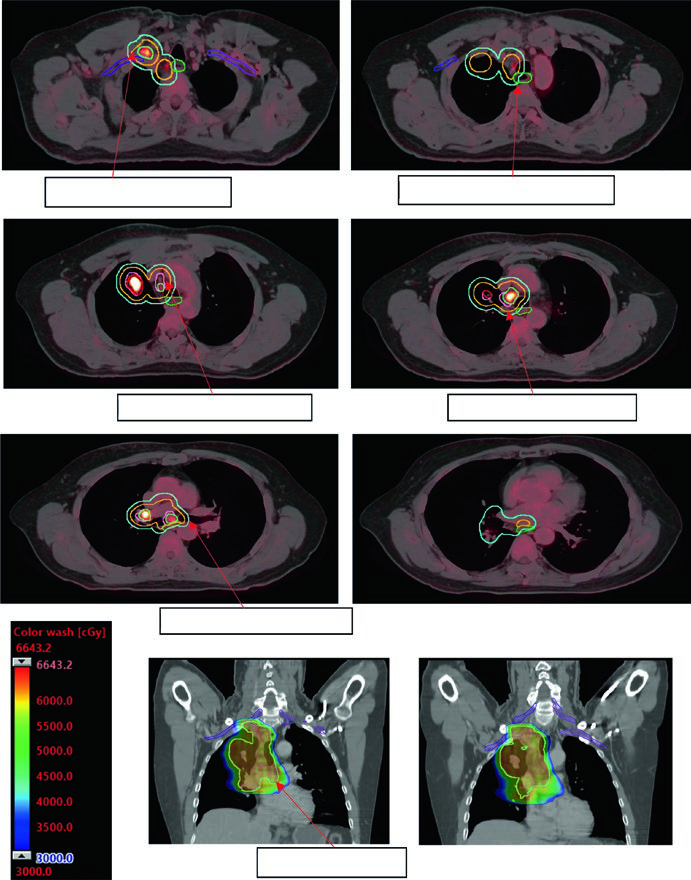
En tórax, ese matiz importa mucho. Cada milímetro innecesario puede aumentar dosis en pulmón, esófago o vía aérea central. El capítulo no propone márgenes mínimos por principio; propone márgenes que realmente correspondan a la información anatómica y al estudio de movimiento disponible.
NSCLC inicial: SBRT, PBT y no-fly zone
En el NSCLC inicial, los márgenes son pequeños porque el objetivo es mantener un tratamiento ablativo muy conformado. El capítulo indica una expansión estándar de 0 a 0,2 cm desde iGTV hasta iCTV. Eso encaja con la lógica de SBRT siempre que el movimiento haya sido evaluado de forma adecuada y la anatomía central se respete con rigor.
El árbol bronquial proximal debe contornearse de forma consistente. Incluye los 2 cm distales de la tráquea, la carina, los bronquios principales derecho e izquierdo y los bronquios lobares. Los autores definen una zona radial de 2 cm más allá del PBT, llamada no-fly zone. En la práctica, esa definición ayuda a distinguir lesiones periféricas, lesiones cercanas al árbol pulmonar y lesiones claramente centrales.
Las figuras del capítulo muestran tres escenarios muy útiles. Un tumor periférico se trató con 54 Gy en tres fracciones de 18 Gy. Una lesión próxima al árbol pulmonar en un paciente médicamente inoperable recibió 48 Gy en cuatro fracciones de 12 Gy. Una lesión central que rozaba los bronquios recibió 50 Gy en cinco fracciones, y los autores señalan que suelen limitar la dosis puntual máxima en el PBT a 55 Gy. El criterio biológico común para los esquemas de SBRT es alcanzar un BED superior a 100 Gy.
Esa flexibilidad es una de las fortalezas prácticas del capítulo. En vez de imponer el mismo fraccionamiento a todas las lesiones de estadio I, la selección de dosis sigue la localización y la extensión. En planificación real, eso suele ser más fiable que tratar igual una lesión periférica y otra que contacta la vía aérea proximal.
NSCLC estadio II-III: márgenes y dosis
En NSCLC estadio II-III, la expansión de iGTV a iCTV suele situarse entre 0,5 y 0,8 cm, apoyada en análisis histológicos previos de extensión microscópica. El capítulo aporta un detalle muy práctico al definir cuándo el PTV puede reducirse: 1,0 a 1,5 cm si no existe evaluación del movimiento ni IGRT diaria; 0,5 a 1,0 cm si hay 4D CT o CBCT, pero no ambos; y 0,3 a 0,5 cm desde CTV, o desde iGTV, hasta PTV cuando la planificación usa 4D CT junto con kV/CBCT, que es la combinación preferida.
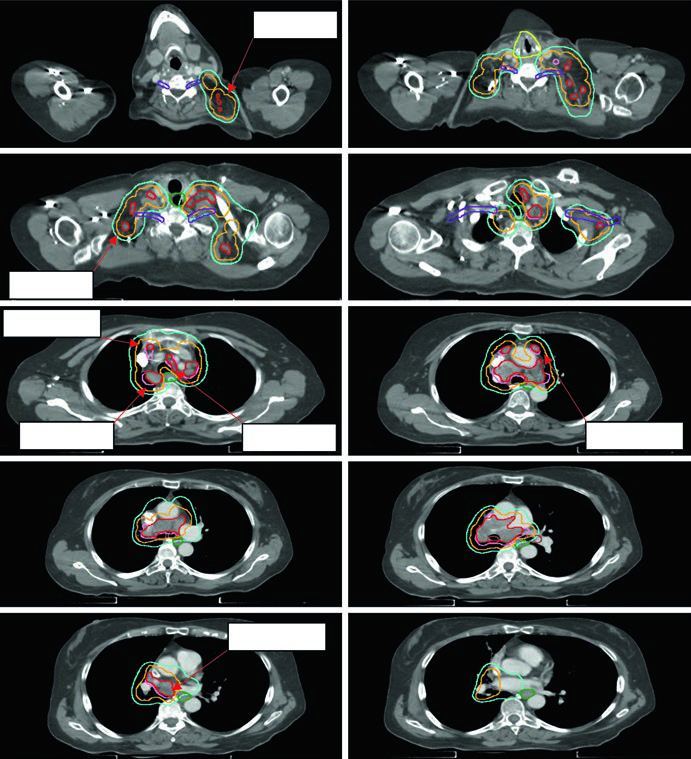
Los ejemplos clínicos ayudan a entender esa estratificación. En el caso IIIB, el paciente recibió 60 Gy en 30 fracciones con contornos separados para tumor primario, ganglios, iGTV, iCTV, PTV, plexo braquial y esófago. En otro caso, un adenocarcinoma cT4N3M0 se presentó con síndrome de vena cava superior, gran masa hiliar-suprahiliar derecha y adenopatía mediastínica extensa con metástasis supraclaviculares bilaterales. En ese contexto, el plexo braquial, el esófago y la laringe pasan a ser estructuras activamente limitantes del plan.
La dosis estándar en el escenario de quimiorradioterapia sigue siendo 60 Gy en 30 fracciones. Lo valioso del capítulo es que vincula esa dosis con la calidad de la imagen diaria. Reducir PTV sin 4D CT y sin IGRT diaria es una apuesta débil; mantener PTV amplio después de una buena evaluación de movimiento y CBCT diario también lo es cuando pulmón y esófago absorben la diferencia.
NSCLC posoperatorio
En el escenario posoperatorio, el capítulo se aleja de los campos históricos amplios que incluían lecho tumoral, niveles ganglionares afectados, mediastino bilateral, muñón bronquial ipsilateral y, en tumores superiores, ganglios supraclaviculares. Con la planificación por CT y la disección mediastínica más completa, ese enfoque ha dejado de ser habitual.
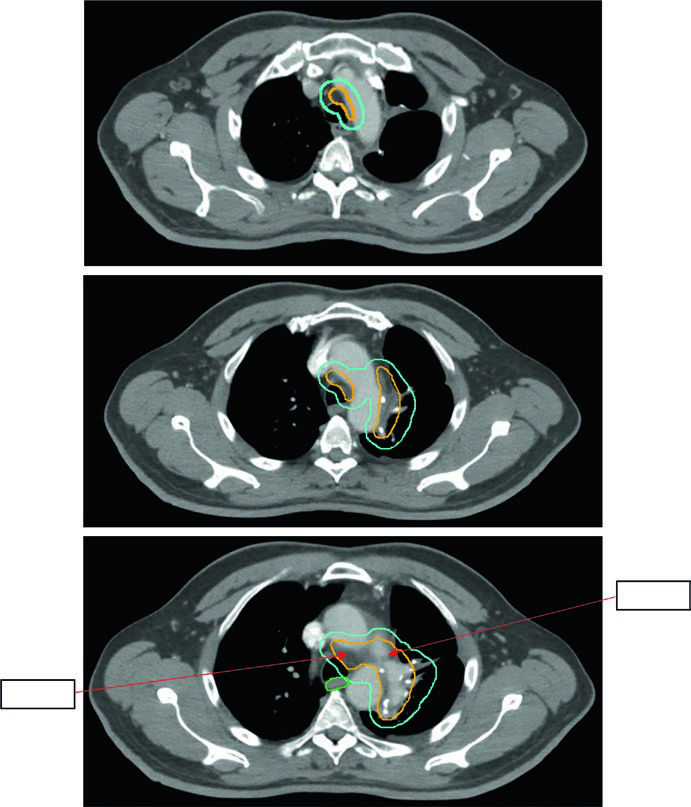
Muchas instituciones, incluida la de los autores, emplean ahora un campo mediastínico limitado que cubre las regiones nodales afectadas y el muñón bronquial ipsilateral, con consideración de un nivel por encima y uno por debajo de la región comprometida. El capítulo señala que esta filosofía se parece a la usada en el estudio Lung ART. Como no hay GTV, la secuencia pasa por CTV, ITV y un PTV con expansión aproximada de 0,5 cm desde ITV, ajustada según la IGRT disponible.
El caso mostrado es muy concreto. Se trata de un tumor de 5,8 cm en lóbulo superior izquierdo con afectación de 4L demostrada por EBUS antes de la cirugía. Tras quimioterapia neoadyuvante y resección, los márgenes fueron negativos, pero los niveles 5 y 10L resultaron positivos. El plan posoperatorio cubrió lecho tumoral, niveles 4L, 5 y 7, además del muñón bronquial ipsilateral, con una prescripción de 54 Gy en 30 fracciones de 1,8 Gy.
Ese diseño resulta más defendible que el campo amplio antiguo porque sigue la evidencia quirúrgica y patológica real. Tras la resección, la pregunta deja de ser dónde está el tumor visible y pasa a ser qué superficies y cadenas ganglionares tienen un riesgo residual suficientemente plausible como para justificar dosis terapéutica.
SCLC y radioterapia torácica de consolidación
En SCLC, la definición de volúmenes cambia menos de lo que muchas veces se supone. El capítulo dice que no existe un margen estándar único de GTV a CTV, pero acepta 0,5 a 1,0 cm y con frecuencia incluye el hilio ipsilateral. El margen de CTV a PTV sigue la misma lógica aplicada en NSCLC, con reducción solo cuando el manejo del movimiento y la imagen diaria lo respaldan.
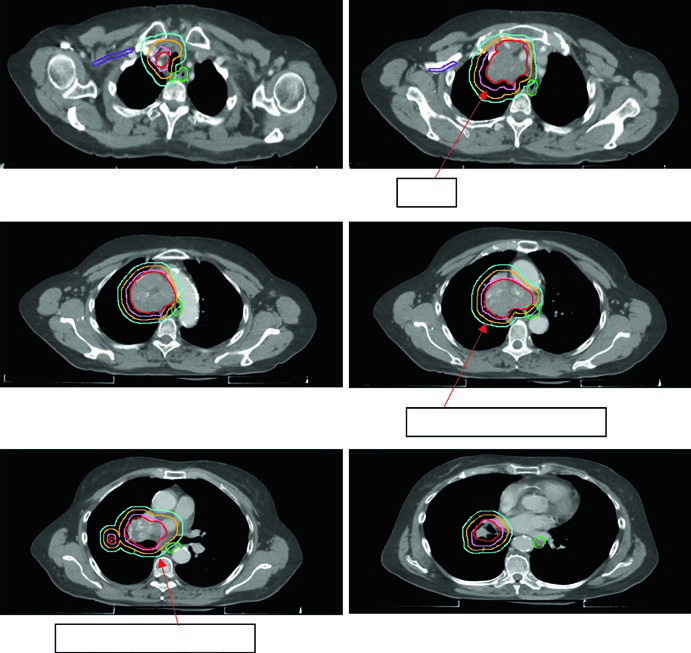
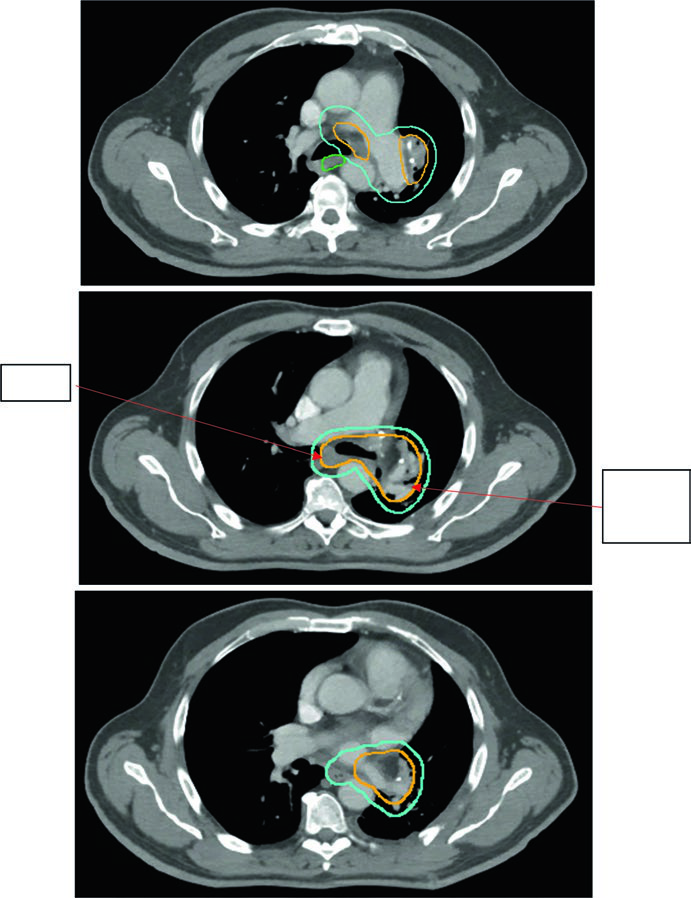
El ejemplo clínico es un SCLC de estadio limitado cT2N2 con masas paratraqueal derecha e hiliar derecha, afectación del mediastino anterior y extensión contigua hacia el hilio derecho y ganglios precarinales. Se utilizó un enfoque de campo involucrado que cubrió solo las regiones mediastínicas e hiliares apropiadas. La prescripción fue 45 Gy como 1,5 Gy x 30 fracciones BID, con expansión de 0,6 cm de iGTV a iCTV y otra de 0,5 cm hasta PTV.
Para enfermedad limitada, las dosis estándar siguen siendo 45 Gy en fracciones BID de 1,5 Gy con quimioterapia o 66 a 70 Gy en fracciones diarias de 2,0 Gy. Para enfermedad extensa tratada con intención de consolidación torácica, el capítulo indica 30 a 45 Gy en diez fracciones. La filosofía del campo sigue siendo la misma en ambos contextos; cambian la intención clínica y el fraccionamiento.
Dosis aceptadas por escenario clínico
La Tabla 13.1 resume la traducción práctica de todo el capítulo: una misma anatomía no implica el mismo esquema de prescripción. El estadiaje citado sigue la octava edición del AJCC, y el texto recuerda además que las restricciones de órganos sanos dependen de la dosis total y del número de fracciones, con apoyo en las publicaciones tipo QUANTEC.
Esquemas aceptados de radioterapia para cáncer de pulmón
La tabla siguiente reproduce de forma íntegra los regímenes incluidos por los autores para NSCLC y SCLC. Sirve como referencia rápida para cruzar escenario clínico, localización tumoral e intención terapéutica.
| Escenario clínico | Dosis aceptadas |
|---|---|
| NSCLC, estadio I, SBRT periférica | Variable: incluye 54 Gy en fracciones de 18 Gy, 48 Gy en fracciones de 12 Gy, 50 Gy en cuatro fracciones y 50 Gy en cinco fracciones |
| NSCLC, estadio I, SBRT central | Variable: incluye 50 Gy en cinco fracciones, 70 Gy en diez fracciones y 60 Gy en ocho fracciones |
| NSCLC, estadio II-III, fraccionamiento estándar | 60 Gy en fracciones diarias de 2 Gy |
| Posoperatorio | 50-54 Gy en fracciones de 1,8-2,0 Gy para resección R0 54-60 Gy en fracciones de 1,8-2,0 Gy para resección R1 60 Gy en fracciones de 2,0 Gy, con consideración de quimioterapia concomitante, para resección R2 |
| SCLC, estadio limitado | 45 Gy en fracciones BID de 1,5 Gy con quimioterapia O 66-70 Gy en fracciones diarias de 2,0 Gy |
| SCLC, estadio extenso | 30-45 Gy en fracciones de 3,0 Gy para radioterapia torácica de consolidación |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 13.1)
Cuándo el CBCT obliga a replantear
El CBCT no sirve solo para verificar el setup. En tórax puede mostrar que el plan inicial ya no representa la anatomía real del paciente. El capítulo termina con una lesión pulmonar metastásica obstructiva tratada con 45 Gy en 15 fracciones. Durante el tratamiento, la aireación pulmonar mejoró y el CBCT mostró que era necesario un replanteamiento adaptativo.
Ese ejemplo corto resume muy bien el mensaje del capítulo. El movimiento respiratorio, el posicionamiento diario y la anatomía torácica cambian. Si el pulmón se reexpande, la lesión se desplaza o cambia la relación con el esófago, aferrarse al plan original puede ser menos preciso que reconocer a tiempo que la anatomía ya es otra.
Referencias
- Chapet O, Kong FM, Quint LE, et al. Int J Radiat Oncol Biol Phys. 2005;63:170-8.
- Ritter T, Quint DJ, Senan S, et al. Int J Radiat Oncol Biol Phys. 2011;81(5):1442-57.
- Kong FM, Ritter T, Quint DJ, et al. Int J Radiat Oncol Biol Phys. 2011;81(5):1442-57.
- Rosenzweig KE, Sim SE, Mychalczak B, et al. Int J Radiat Oncol Biol Phys. 2001;50:681-5.
- Rosenzweig KE, Sura S, Jackson A, et al. J Clin Oncol. 2007;25:5557-61.
- Yuan S, Sun X, Li M, et al. Am J Clin Oncol. 2007;30:239-44.
- Giraud P, Antoine M, Larrouy A, et al. Int J Radiat Oncol Biol Phys. 2000;48:1015-24.
- Spoelstra FO, Senan S, Le Pechoux C, et al. Int J Radiat Oncol Biol Phys. 2009;76:1106-13.
- Marks LB, Yorke ED, Jackson A, et al. Int J Radiat Oncol Biol Phys. 2010;76:S10-9.
- American Joint Committee. Cancer staging manual. 8th ed. New York: Springer; 2010.
- Rusch VW, Asamura H, Watanabe H, et al. J Thorac Oncol. 2009;4(5):568-77.
- Watanabe Y, Shimizu J, Tsubota M, Iwa T. Chest. 1990;97(5):1059-65.