El sarcoma pediátrico comprende un grupo heterogéneo de neoplasias óseas y de tejidos blandos que requieren manejo multidisciplinario y delineación precisa de los volúmenes blanco. El sarcoma de Ewing (EWS) es el segundo tumor óseo pediátrico más frecuente, mientras que el rabdomiosarcoma (RMS) lidera entre los sarcomas de tejidos blandos en la infancia. Ambos comparten un algoritmo terapéutico que combina quimioterapia sistémica con terapia local — cirugía y/o radioterapia — pero difieren sustancialmente en estadificación, volúmenes de irradiación y dosis prescritas.
Este artículo detalla la delineación de volúmenes blanco y la planificación de radioterapia para EWS y RMS en pacientes pediátricos, abarcando desde la anatomía y patrones de diseminación hasta la simulación, inmovilización y evaluación del plan. Para una visión integral de todos los sitios anatómicos y técnicas de planificación en radioterapia, consulte nuestra guía completa sobre delineación de volúmenes blanco.
En Este Artículo
- Epidemiología y Patrones de Diseminación
- Imagen Diagnóstica para Definición de Volúmenes
- Delineación de Volúmenes en el Sarcoma de Ewing
- Delineación de Volúmenes en el Rabdomiosarcoma
- Clasificación Molecular e Implicaciones Dosimétricas
- Casos Clínicos Ilustrativos
- Simulación, Inmovilización y Localización Diaria
- Restricciones de Dosis y Evaluación del Plan
- Efectos Tardíos y Papel de la Protonterapia
Epidemiología y Patrones de Diseminación de los Sarcomas Pediátricos
El sarcoma de Ewing se presenta con mayor frecuencia en la pelvis (25% de los casos) y el fémur (16%). Los pacientes con tumores pélvicos generalmente no son candidatos a resección quirúrgica y suelen recibir radioterapia definitiva como control local. El osteosarcoma — el tumor óseo pediátrico más común — no depende tan centralmente de la radioterapia, lo que convierte al EWS en la principal indicación radioterápica entre las neoplasias óseas infantiles.
El rabdomiosarcoma tiene una distribución anatómica más amplia: cabeza y cuello representan el 35% de los casos, sistema genitourinario el 20% y extremidades el 20%. Una distinción fundamental en el RMS es la dicotomía entre sitios primarios favorables y desfavorables, que impacta directamente la estadificación y estratificación de riesgo. Dentro de las lesiones de cabeza y cuello, los tumores se clasifican como parameníngeos (15% de todos los RMS), orbitarios (10%) u otros sitios de cabeza y cuello (10%).
Las lesiones parameníngeas ocupan uno de ocho sitios específicos — oído medio, mastoides, cavidad nasal, nasofaringe, fosa infratemporal, fosa pterigopalatina, senos paranasales y espacio parafaríngeo (mnemónico «MMNNOOPP») — y conllevan riesgo aumentado de extensión intracraneal directa, clasificándose como sitios primarios desfavorables.
En cuanto a los patrones de diseminación local, el hueso no involucrado y las membranas interóseas funcionan como barreras anatómicas para la extensión microscópica. Sin embargo, la erosión e invasión ósea no son infrecuentes y deben evaluarse por imagen — especialmente tomografía computarizada. Como EWS y RMS frecuentemente reciben quimioterapia antes de la radioterapia, la reducción volumétrica posquimioterapia debe considerarse cuidadosamente: cuando la imagen pretratamiento muestra tumor «empujando» estructuras adyacentes (pulmón, vejiga, intestino) sin invasión directa, el volumen posquimioterapia refleja el retorno de estas estructuras a su posición normal. En contraste, la invasión directa identificada en la imagen prequimioterapia debe mantener cobertura en los campos posquimioterapia.
La diseminación ganglionar es infrecuente en la mayoría de los sarcomas pediátricos, pero merece atención en escenarios específicos. El RMS de extremidad presenta tasas más elevadas de metástasis nodales y se evalúa frecuentemente por biopsia de ganglio centinela. El RMS paratesticular puede requerir disección retroperitoneal ipsilateral con preservación nerviosa en pacientes mayores de 10 años. Cuando se confirman metástasis nodales, se recomienda cobertura radioterápica de toda la cadena ganglionar — no solo de los ganglios involucrados.
Imagen Diagnóstica para Definición de Volúmenes Blanco
La combinación de modalidades de imagen es esencial tanto para la definición de volúmenes blanco (GTV y CTV) como para la estadificación. La TC es particularmente útil para delinear el compromiso y erosión ósea, mientras que la RM ofrece excelente resolución de tejidos blandos para evaluar la extensión de la enfermedad, incluyendo invasión intracraneal. Ambas modalidades se utilizan rutinariamente para EWS y RMS.
El PET-TC se ha incorporado cada vez más en la estadificación inicial de ambas neoplasias, con literatura creciente que respalda su adopción frente a técnicas como la gammagrafía ósea. La fusión PET puede ayudar a identificar sitios de enfermedad inicialmente involucrados antes de la quimioterapia de inducción — información valiosa para la definición de volúmenes. Para principios de delineación en sarcomas de partes blandas en adultos, consulte nuestro artículo dedicado.
Delineación de Volúmenes en el Sarcoma de Ewing
La planificación en EWS utiliza dos conjuntos de volúmenes: uno basado en la extensión de la enfermedad al diagnóstico (GTV1/CTV1) y otro definido por la enfermedad residual posquimioterapia y, eventualmente, poscirugía (GTV2/CTV2). Los márgenes añadidos a los CTVs por incertidumbre de posicionamiento generan los respectivos PTVs.
Definición de Volúmenes Blanco en el Sarcoma de Ewing
La tabla siguiente resume las definiciones de volúmenes utilizadas en la planificación de radioterapia del sarcoma de Ewing, conforme al protocolo COG AEWS1031.
| Volumen | Definición |
|---|---|
| GTV1 | Extensión prequimioterapia de la enfermedad macroscópica (hueso y tejidos blandos), incluyendo ganglios sospechosos no resecados. El GTV1 puede modificarse si el tumor se extendía a cavidades corporales (pelvis, tórax) y regresó con quimioterapia. |
| CTV1 | GTV1 + 1–1,5 cm. Incluye cadenas ganglionares involucradas (clínica o patológicamente). |
| PTV1 | CTV1 + margen de setup (específico institucional y de guía por imagen, generalmente 3–5 mm). |
| GTV2 | Tumor residual tras quimioterapia de inducción; sin embargo, toda extensión ósea prequimioterapia se incluye típicamente en el GTV2. En postoperatorio, GTV2 corresponde a enfermedad residual (ósea o de tejidos blandos) y sitios de márgenes positivos. |
| CTV2 | GTV2 + 1–1,5 cm. |
| PTV2 | CTV2 + margen de setup (generalmente 3–5 mm). |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition
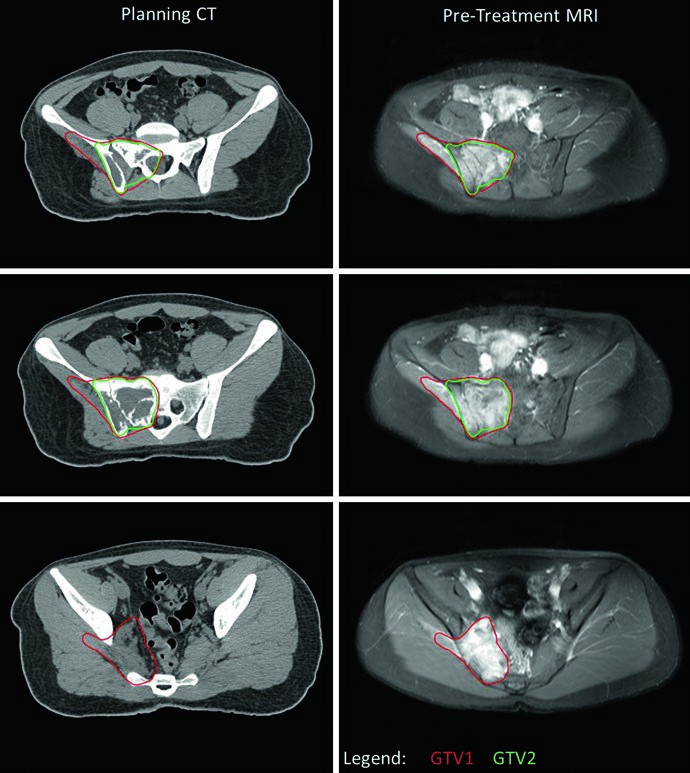
Una consideración práctica central es el manejo del GTV1 cuando el tumor se extiende a cavidades corporales. Si la imagen pretratamiento muestra tumor «empujando» pulmón o vísceras pélvicas sin invasión directa, el GTV1 puede adaptarse tras la quimioterapia de inducción para reflejar la regresión tumoral. Esto se ilustra claramente en el caso de EWS pélvico, donde el nivel más inferior no muestra enfermedad residual (GTV2) y la extensión del GTV1 hacia la pelvis fue reducida. El PTV1 recibió 45 Gy y el PTV2 recibió 10,8 Gy adicionales, totalizando 55,8 Gy.
Dosis en el Sarcoma de Ewing
Las prescripciones de dosis varían según el escenario clínico. Todas las fracciones son de 1,8 Gy/día.
| Escenario Clínico | PTV1 (Gy) | PTV2 (Gy) |
|---|---|---|
| RT definitiva (todos los sitios excepto vertebral) | 45 | 10,8 |
| RT definitiva — vertebral | 45 | 5,4 |
| EWS extraóseo con respuesta completa a quimioterapia | 50,4 | 0 |
| Postoperatorio con residuo microscópico (R1) y >90% necrosis tumoral | 0 | 50,4 |
| Postoperatorio con residuo microscópico (R1) y <90% necrosis tumoral | 50,4 | 0 |
| Postoperatorio con residuo macroscópico (R2) | 45 | 10,8 |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition
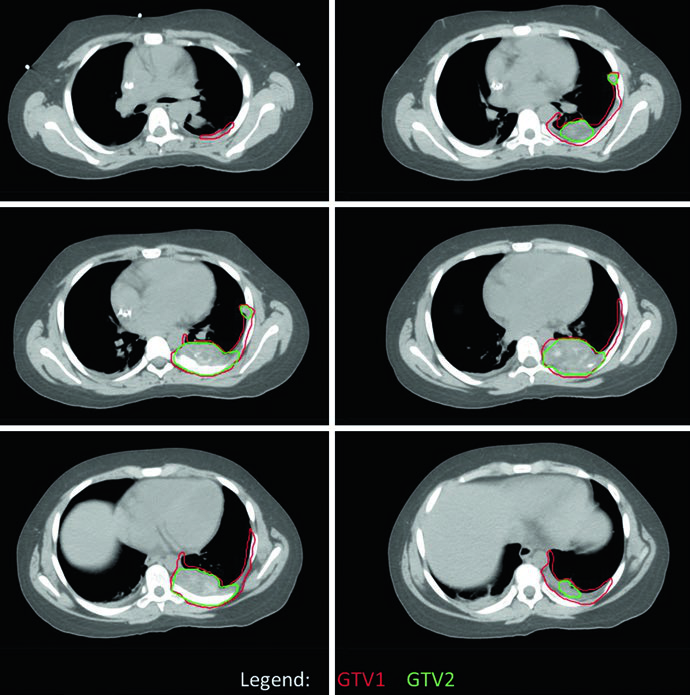
En el caso de EWS de pared torácica, se realizó simulación con TC de cuatro dimensiones (4DCT) para capturar la excursión respiratoria completa de los volúmenes blanco. El tumor original ocupaba la mitad posterior del hemitórax izquierdo, pero el GTV1 fue adaptado para reflejar el «empuje» tumoral en el espacio ahora ocupado por pulmón normal. La cobertura de los sitios de contacto e involucro originales fue mantenida. PTV1 recibió 45 Gy y PTV2 un boost adicional de 10,8 Gy.
Delineación de Volúmenes en el Rabdomiosarcoma
En el RMS, la radioterapia puede entregarse como volumen único o en dos niveles de dosis, similar al EWS. La reducción de volumen para dosis de boost superiores a 36 Gy se recomienda generalmente para tumores que «empujan» estructuras torácicas o pélvicas. Sin embargo, las lesiones invasivas de RMS pueden requerir cobertura completa del volumen prequimioterapia con la dosis máxima — frecuentemente 50,4 Gy para enfermedad macroscópica — independientemente de la respuesta a quimioterapia. Esta regla es particularmente relevante para el RMS parameníngeo de cabeza y cuello, donde el GTV2 debe incluir la extensión prequimioterapia de la enfermedad sin importar la respuesta a la quimioterapia de inducción.
Definición de Volúmenes Blanco en el Rabdomiosarcoma
El delineamiento de volúmenes en RMS sigue principios similares a los del EWS, con particularidades para tumores parameníngeos y lesiones que «empujan» estructuras adyacentes.
| Volumen | Definición |
|---|---|
| GTV1 | Extensión prequimioterapia de la enfermedad macroscópica (hueso y tejidos blandos), incluyendo ganglios sospechosos no resecados. |
| CTV1 | GTV1 + 1 cm. Incluye cadenas ganglionares involucradas. |
| PTV1 | CTV1 + margen de setup (generalmente 3–5 mm). |
| GTV2 | Tumor residual tras quimioterapia de inducción, excluyendo zonas donde el tumor «empujaba» estructuras (tórax, pelvis). Para RMS parameníngeo de cabeza y cuello, la enfermedad invasiva prequimioterapia debe incluirse en el GTV2 independientemente de la respuesta a quimioterapia. |
| CTV2 | GTV2 + 1 cm. |
| PTV2 | CTV2 + margen de setup (generalmente 3–5 mm). |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition
Dosis en el Rabdomiosarcoma
Las dosis prescritas dependen del grupo quirúrgico, estatus de fusión molecular y respuesta a la quimioterapia de inducción. Fracciones de 1,8 Gy/día.
| Grupo | Estatus de Fusión (Histología) | Dosis (Gy) |
|---|---|---|
| I (R0), ganglios negativos | Negativo (embrionario) | 0 |
| I (R0) | Positivo (alveolar) | 36,0 |
| II, ganglio-negativo (R1) | Cualquiera | 36,0 (enfermedad prequimioterapia) |
| II, ganglio-positivo (resecado) | Cualquiera | 41,4 (sitio + región nodal prequimioterapia) |
| III, no orbital / orbital con respuesta incompleta | Cualquiera | 50,4* |
| III, orbital con respuesta completa | Cualquiera | 45,0** |
| III, tumores >5 cm sin RC (ARST1431) | Cualquiera | 59,4* |
| III, RC comprobada en semana 9 (ARST1431) | Cualquiera | 36,0*** |
| Extremidad, N0, post-amputación | Cualquiera (incluido alveolar/fusión-positivo) | 0 |
*Reducción de volumen tras 36 Gy, cone-down de 14,4 o 23,4 Gy según tamaño tumoral (>5 cm). **RC en semana 9 permite dosis única de 36 Gy al PTV1 sin boost. ***RC radiográfica + metabólica o biopsia negativa en semana 9. Fuente: Target Volume Delineation and Field Setup, 2nd Edition
Clasificación Molecular e Implicaciones Dosimétricas en el RMS
La clasificación histológica del RMS está migrando de un modelo puramente morfológico — embrionario (menor riesgo) versus alveolar (mayor riesgo) — hacia una definición molecular basada en el estatus de fusión. Los protocolos actuales del COG utilizan el estatus de translocación involucrando FOX01 (cromosoma 13) como marcador de riesgo: las fusiones PAX3-FOX01 y PAX7-FOX01, representadas por t(2;13) y t(1;13), se asocian con comportamiento clínico de alto riesgo similar a la histología alveolar. Los datos respaldan que el RMS alveolar fusión-negativo se comporta de manera similar al RMS embrionario.
En la práctica, esta clasificación molecular impacta directamente la prescripción de dosis. Pacientes con resección completa (Grupo I, R0) y fusión negativa no necesitan radioterapia. En cambio, pacientes del Grupo I con fusión positiva reciben 36 Gy. Para enfermedad macroscópica residual (Grupo III), el protocolo ARST1431 introduce escalas de dosis que pueden alcanzar 59,4 Gy en tumores mayores de 5 cm sin respuesta completa a la quimioterapia de inducción.
Casos Clínicos Ilustrativos de Delineación
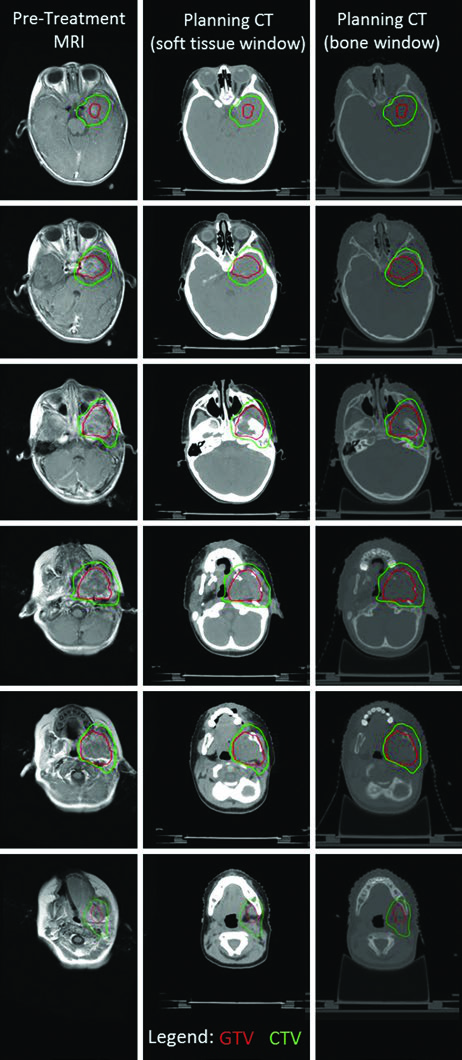
El caso de RMS parameníngeo de la fosa infratemporal ilustra la complejidad de la delineación en lesiones con extensión intracraneal. La fusión de RM T1 poscontraste con TC de simulación permitió identificar tanto la invasión intracraneal como la erosión ósea de la mandíbula y la placa pterigoidea izquierda. La extensión intracraneal motivó el inicio precoz de terapia local concurrente con quimioterapia, con tratamiento a dosis única. Máscara termoplástica y guía diaria por kV permitieron margen de PTV de solo 3 mm, y el PTV recibió 50,4 Gy.
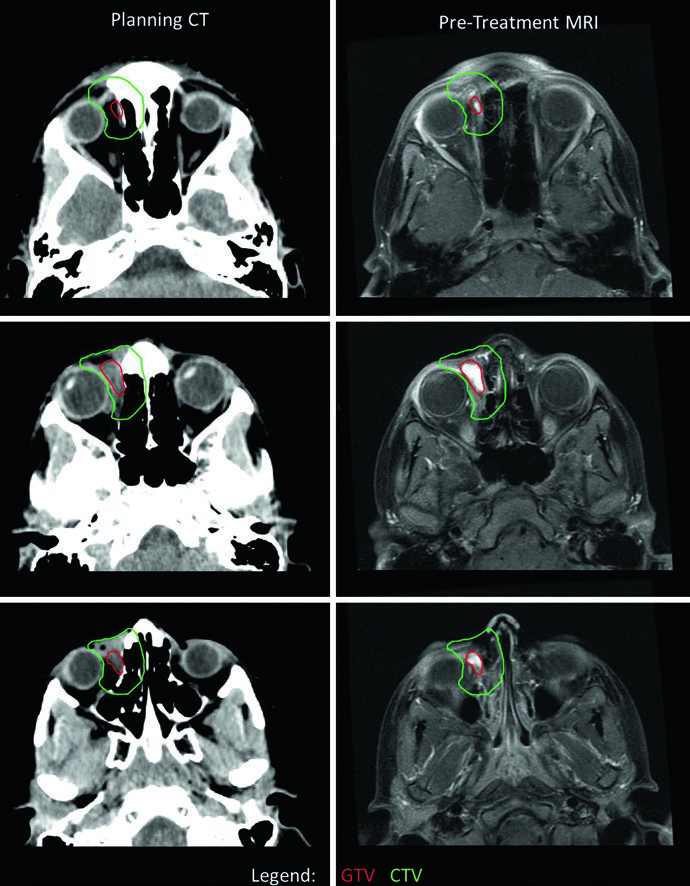
En el RMS orbital, la delineación exige atención cuidadosa a la preservación de estructuras oculares. En este caso, el CTV se extendió más allá de la órbita ósea en algunos cortes por sospecha de erosión ósea — en general, el CTV del RMS orbital no debe exceder los límites de la órbita ósea sin erosión confirmada. Se utilizó una desviación lateral del ojo derecho para optimizar la preservación del cristalino y nervio óptico. Como el tumor respondió mínimamente a la quimioterapia de inducción, se optó por dosis única de 50,4 Gy. Si hubiera respondido, se habrían utilizado dos niveles: 36 Gy con cone-down a 50,4 Gy. Para comparación con tumores del SNC que también requieren planificación cuidadosa orbital, consulte nuestro artículo sobre tumores malignos del SNC.
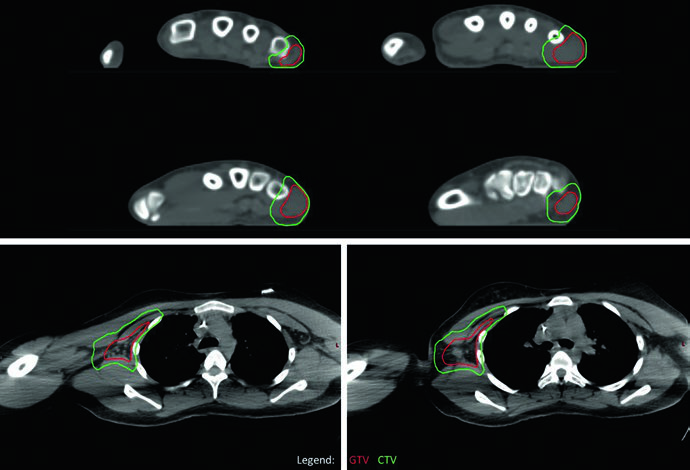
El caso de RMS alveolar (fusión-positivo) de extremidad superior con adenopatía axilar destaca el abordaje ante metástasis nodales regionales. Toda la cadena axilar derecha fue contorneada como GTV para garantizar cobertura completa, dado el compromiso extenso identificado por PET. El sitio primario en la mano respondió mínimamente y recibió dosis única de 50,4 Gy; la cadena axilar, a pesar de respuesta parcial, también recibió 50,4 Gy por la difusividad del compromiso. No se identificaron sitios de enfermedad en tránsito entre mano y axila, por lo que el brazo intermedio no fue tratado.
Simulación, Inmovilización y Localización Diaria
La inmovilización durante la simulación varía según la localización anatómica. Para lesiones de cabeza y cuello, la máscara termoplástica de cabeza y hombros es el estándar. Lesiones torácicas (incluyendo vertebrales torácicas) se simulan con brazos elevados, wingboard y VacLok o dispositivo similar. Tumores pélvicos se inmovilizan con VacLok para pelvis y extremidades inferiores. Las lesiones de extremidad pueden requerir VacLok personalizado, posicionamiento pies-primero y decúbito no supino en casos seleccionados.
Cuando existe preocupación por movimiento respiratorio, la simulación 4DCT permite evaluar la excursión de los volúmenes blanco con la respiración. Para lesiones pélvicas genitourinarias, el llenado vesical puede ser relevante — simulación con vejiga llena y vacía proporciona la extensión completa de la excursión del volumen blanco. En pacientes masculinos con sarcomas pélvicos o de pierna proximal, el posicionamiento en «piernas de rana» facilita el uso de blindaje testicular.
El tipo y frecuencia de guía por imagen determinan directamente la expansión CTV-PTV. Muchas instituciones utilizan kV diario con márgenes de PTV de 3 a 5 mm. Expansiones menores pueden ser apropiadas con guía por imagen más robusta o cuando estructuras críticas están próximas — escenario frecuente en sarcomas de cabeza y cuello cercanos a nervios ópticos, tronco encefálico y otras estructuras vitales. La simulación por RM puede complementar la TC para aportar datos en la posición de tratamiento. En pacientes más jóvenes — generalmente menores de 8 años — puede ser necesaria sedación o anestesia diaria. Para consideraciones de planificación en otros tumores pediátricos del SNC, consulte nuestro artículo sobre tumores cerebrales pediátricos.
Restricciones de Dosis y Evaluación del Plan
La evaluación del plan radioterápico en sarcomas pediátricos sigue principios generales de cobertura: al menos el 95% del PTV (o PTVs) debe recibir la dosis prescrita, con minimización de hotspots superiores al 110% — idealmente, no más del 10% del PTV recibiendo 110% o más.
Restricciones de Dosis a Órganos en Riesgo
Estas restricciones son referencias generales de los protocolos COG para EWS y RMS. Dada la vulnerabilidad de los pacientes pediátricos a toxicidades tardías, se recomienda encarecidamente optimizar la preservación de OARs más allá de estos límites.
| Órgano/Tejido | Volumen (%) | Dosis (Gy) |
|---|---|---|
| Tronco encefálico | Dosis máxima puntual | 54 |
| Quiasma/nervio óptico | Dosis máxima puntual | 54 |
| Médula espinal | Dosis máxima puntual | 45 |
| Cristalino | Dosis máxima puntual | 6 |
| Cóclea | Dosis máxima puntual | 35 |
| Corazón | 100 | 30 |
| Pulmones (bilateral) | V20 | 20 |
| Pulmones (bilateral) | 100 | 15 |
| Hígado | 100 | 23,4 |
| Hígado | 50 | 30 |
| Riñón (bilateral) | 50 | 24 |
| Riñón (bilateral) | 100 | 14,4 |
| Intestino delgado | 50 | 45 |
| Vejiga | 100 | 45 |
| Recto | 100 | 45 |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition
Es importante destacar que estas restricciones son puntos de partida. Los pacientes pediátricos conllevan riesgos profundos de toxicidades tardías de la radioterapia, y los esfuerzos adicionales para maximizar la preservación de los OARs deben realizarse siempre que sea posible.
Efectos Tardíos y Papel de la Protonterapia
La evaluación del plan debe orientar el asesoramiento de pacientes y familiares sobre efectos agudos y tardíos. El sarcoma de Ewing presenta una tasa de neoplasias secundarias superior a la de la mayoría de los cánceres pediátricos — un factor que debe pesar en la elección de la técnica de irradiación.
Los efectos tardíos son específicos del sitio. En sarcomas de cabeza y cuello: anomalías dentofaciales, xerostomía, xeroftalmía, disminución de la agudeza visual, cataratogénesis, asimetría facial, endocrinopatías y disfunción neurocognitiva. En extremidades: cierre epifisario prematuro y asimetría esquelética por disminución del crecimiento óseo. En pacientes que reciben RT vertebral: pérdida de talla y riesgo de cifosis, lordosis y escoliosis — minimizados con cobertura del cuerpo vertebral completo en niños prepúberes. En RT torácica: neumonitis y fibrosis pulmonar, cardiotoxicidad. En RT pélvica: cistitis, incontinencia urinaria o estenosis, e infertilidad — que también debe considerarse en relación con los quimioterápicos utilizados, en particular la ciclofosfamida.
En este contexto, la protonterapia merece consideración para pacientes pediátricos dado su potencial de reducir la dosis integral y preservar tejidos normales. Las consideraciones específicas de protones — incertidumbres de alcance, disposición de haces y selección de técnica — deben discutirse con físicos médicos y radioterapeutas experimentados en el uso de protonterapia para neoplasias pediátricas.




