Delineación de volúmenes blanco en tumores cerebrales pediátricos
La radioterapia pediátrica del sistema nervioso central exige precisión milimétrica y una comprensión profunda de las particularidades anatómicas y biológicas de cada tumor. El meduloblastoma, el ependimoma y el germinoma puro representan las tres entidades más frecuentes en este contexto, y cada una demanda estrategias de delineación distintas. La planificación volumétrica basada en tomografía computarizada es obligatoria independientemente de la técnica empleada — sea radioterapia conformacional 3D, IMRT, VMAT o protones.
Para una visión completa de todos los sitios anatómicos, consulte nuestra guía completa sobre delineación de volumen blanco en radioterapia.
Meduloblastoma: estadificación y simulación
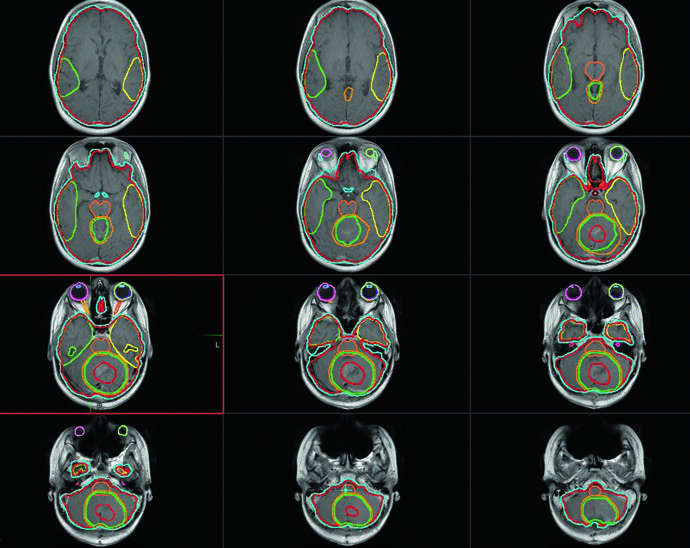
La estadificación integral determina las decisiones de dosis y volumen. Todo paciente necesita una RM cerebral con contraste en cortes finos de 1 a 3 mm — tanto pre como posoperatoria — además de RM espinal con contraste y análisis de líquido cefalorraquídeo. Los pacientes con citología positiva, metástasis macroscópica o residuo tumoral igual o mayor a 1,5 cm² en la RM posoperatoria se clasifican como alto riesgo. Aquellos con enfermedad M0 y residuo inferior a 1,5 cm² pertenecen al grupo de riesgo estándar.
La simulación por TC debe realizarse de forma reproducible, con o sin anestesia según la cooperación del niño. La inmovilización típica consiste en un VacLok o alpha cradle de cuerpo entero combinado con máscara craneal con múltiples marcas para triangulación y alineamiento longitudinal espinal. Algunos sistemas de TC permiten espesor de corte variable por región — más finos en el cerebro, más gruesos en la columna — para optimizar el detalle del contorneo sin excesiva carga de trabajo. El rango del escaneo debe abarcar desde la cima del cráneo hasta las gónadas.
Un detalle práctico que marca diferencia: la conversación temprana entre el radiooncólogo y el anestesiólogo sobre el manejo de la vía aérea es fundamental. Si el paciente comienza intubado pero se prevé la transición a máscara laríngea o cánula nasal, colocar una cánula oral durante la confección de la máscara garantiza una posición reproducible del mentón y evita re-simulaciones innecesarias.
Volúmenes blanco para irradiación craneoespinal
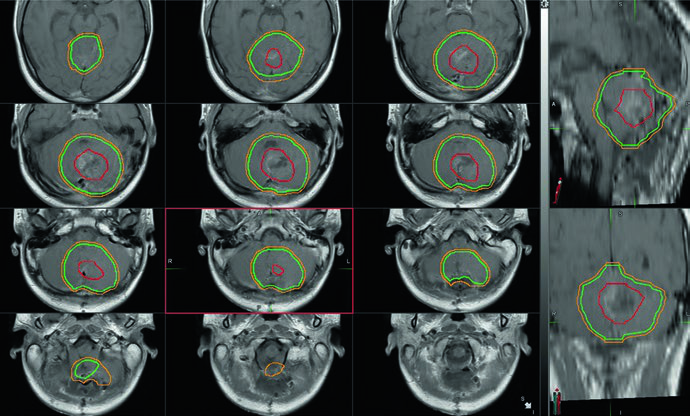
El contorneo debe realizarse corte por corte en la TC de planificación. Las tablas siguientes resumen las definiciones recomendadas.
Volúmenes recomendados para irradiación craneoespinal (CSI)
| Volumen | Definición |
|---|---|
| GTV | Lecho tumoral incluyendo toda enfermedad residual macroscópica y paredes de la cavidad de resección en RM, más áreas de preocupación señaladas por el neurocirujano. Los defectos quirúrgicos por la vía de acceso no forman parte del GTV. |
| CTVCSI | Todo el volumen contenido por la duramadre en contacto con el líquido cefalorraquídeo, incluido el pseudomeningocele posoperatorio. En niños en crecimiento, incluye el cuerpo vertebral completo y el canal; en individuos adultos, solo el canal. |
| PTVCSI | CTVCSI + 3 a 10 mm según la confianza en el posicionamiento diario y la experiencia institucional. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.1)
Volúmenes recomendados para el boost del lecho tumoral
| Volumen | Definición |
|---|---|
| GTV | Lecho tumoral con enfermedad residual macroscópica y paredes de la cavidad en RM, más áreas identificadas por el neurocirujano. |
| CTVboost | GTV + 1 a 1,5 cm de margen anatómicamente confinado. Excluir barreras de diseminación como el tentorio. Limitar el margen en el tronco cerebral a 2–3 mm en áreas de contacto tumoral. |
| PTVboost | CTVboost + 3 a 5 mm basado en imágenes diarias y experiencia institucional. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.2)
Dosis y estratificación por riesgo en meduloblastoma
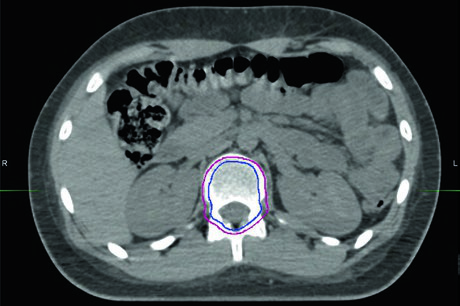
El brazo de 18 Gy del estudio ACNS0331 del Children’s Oncology Group mostró aumento de fracasos, y 23,4 Gy al eje craneoespinal sigue siendo el estándar para riesgo estándar. El mismo estudio demostró la equivalencia del boost de campo involucrado frente a la irradiación de toda la fosa posterior en estos pacientes. La recomendación vigente es 23,4 Gy craneoespinal seguido de boost de campo involucrado hasta 54 Gy.
Para enfermedad de alto riesgo o pacientes sin condiciones para quimioterapia (como algunos adultos), la dosis craneoespinal asciende a 36 Gy con boost hasta 54 Gy. Series retrospectivas respaldan el boost de lecho tumoral sin exceso de recaídas fuera del lecho en la fosa posterior, aunque no existen ensayos aleatorizados al respecto.
Con protonterapia en niños en crecimiento, se recomienda tratar el cuerpo vertebral completo hasta 30 Gy cuando la CSI es de 36 Gy, para prevenir asimetría en el crecimiento. Muchos radiooncólogos incluyen el hueso en el PTV sin expansión adicional para preservar esófago y pulmones. Datos preliminares sugieren que cubrir todo el cuerpo vertebral podría no ser estrictamente necesario, y el tema es objeto de un ensayo clínico activo (NCT03281889).
Los pacientes con enfermedad M2 pueden recibir boost hasta 54 Gy en áreas de enfermedad metastásica supratentorial o de la fosa posterior. La enfermedad M3 se subdivide en difusa y focal: la enfermedad espinal difusa recibe 39,6 Gy, la focal por encima de la médula 45 Gy, y la focal por debajo de la médula 50,4 Gy, según el protocolo ACNS 0332.
Volúmenes para boost de fosa posterior completa
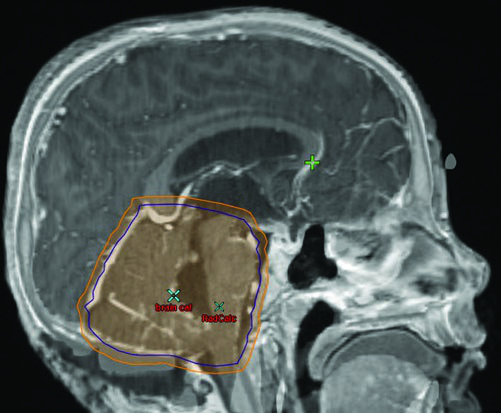
| Volumen | Definición |
|---|---|
| GTV | Lecho tumoral con enfermedad residual, paredes de la cavidad y áreas señaladas por el neurocirujano. |
| CTVFP | Toda la fosa posterior incluyendo el tronco cerebral completo. Límites: base del cráneo anteriormente, tentorio superiormente, foramen magno inferiormente. El hueso del cráneo restringe posterior y lateralmente. |
| PTVFP | CTVFP + 3 a 5 mm según frecuencia de imagen y experiencia institucional. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.3)
La identificación del fondo de saco tecal es esencial — generalmente se encuentra a nivel de S2, pero no siempre. Tratar más inferiormente de lo necesario incrementa la dosis de salida en las gónadas cuando se emplea un campo fotónico posterior único. Con protones esto no representa un problema.
Ependimoma: delineación y márgenes de CTV
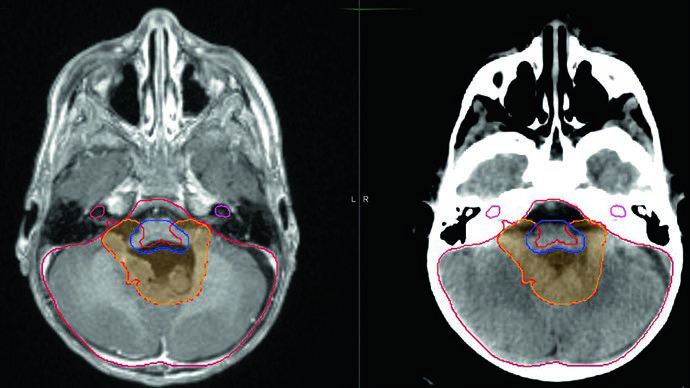
Al igual que en el meduloblastoma, la delineación volumétrica basada en TC es obligatoria. Todos los pacientes requieren RM pre y posoperatoria de alta calidad con cortes de 1–3 mm de cerebro y columna total. La diseminación por LCR es menos frecuente que en el meduloblastoma — inferior al 10% al diagnóstico — pero debe descartarse mediante RM espinal y citología del LCR.
La extensión de la resección es el factor pronóstico más importante. Si la RM posoperatoria muestra enfermedad residual, debe considerarse la re-resección cuando la morbilidad anticipada sea aceptable.
El GTV consiste en la cavidad de resección posoperatoria con atención especial a los forámenes de Luschka y Magendie, frecuentemente comprometidos. Consultar al neurocirujano aporta valor para identificar hallazgos intraoperatorios no evidentes en la imagen.
Los márgenes de GTV a CTV han disminuido durante la última década. El protocolo ACNS 0831 del COG trató con CTV = GTV + 0,5 cm hasta una dosis total de 54 Gy en 30 fracciones. Para minimizar la toxicidad del tronco cerebral, la expansión del CTV en el tronco se limitó a 3 mm. Un conedown adicional hasta 59,4 Gy (para niños mayores de 18 meses) excluye completamente el tronco cerebral, el quiasma óptico y la médula cervical del volumen de boost.
Volúmenes recomendados para ependimoma infratentorial
| Volumen | Definición |
|---|---|
| GTV | Lecho tumoral con enfermedad residual y paredes de la cavidad en RM. Atención especial a los forámenes de Magendie y Luschka. |
| CTV54 | GTV + 5 a 10 mm restringido por hueso y tentorio. No debe extenderse en el tronco cerebral más de 3 mm. |
| CTV59,4 | GTV + 5 mm excluyendo completamente tronco cerebral, quiasma óptico y médula cervical. |
| PTV | CTV + 3 a 5 mm. Se acepta subdosificación del PTV en regiones donde sea necesario respetar la tolerancia de la médula cervical y el quiasma óptico. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 34.4)
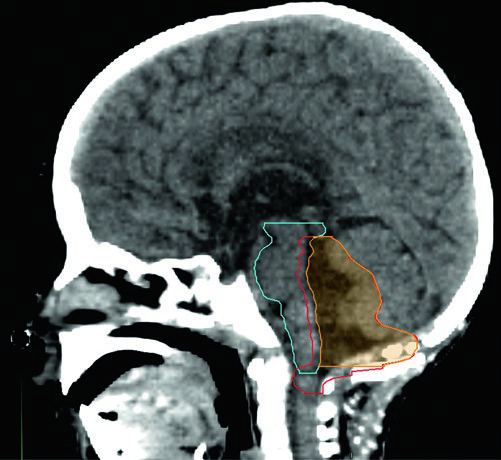
Muchos radiooncólogos pediátricos aún prefieren márgenes más amplios (CTV = GTV + 1 cm) con dosis total de 54 Gy fuera de protocolo, y este abordaje se considera aceptable. El protocolo ACNS 0831 estableció como objetivo que la D10% de la médula cervical no supere 57 Gy, y durante el tratamiento del PTV59,4, el volumen total de la médula espinal no debe recibir más del 70% — o 126 cGy por fracción — durante cada una de las últimas tres sesiones.
Cuando se trata hasta 59,4 Gy, se recomienda un abordaje en dos fases: el conedown a 54 Gy permite preservar dosis adicional en tronco cerebral, quiasma óptico y médula cervical. Independientemente de la extensión inferior del tumor, el PTV54 no debe extenderse por debajo del foramen magno.
Germinoma puro: irradiación ventricular y boost
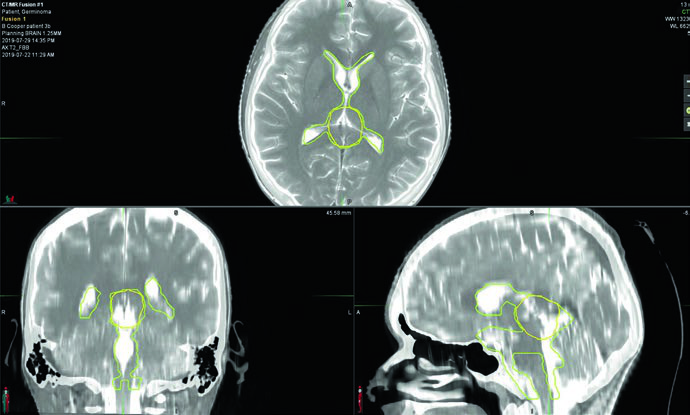
La planificación exige RM pre y posoperatoria de 1–3 mm de espesor de corte cubriendo cerebro y columna. Los marcadores séricos y en LCR de beta-hCG y alfa-fetoproteína son fundamentales para descartar componente no germinomatoso: cualquier elevación de AFP reclasifica el tumor como NGGCT. En el protocolo ACNS 1123, los pacientes con beta-hCG sérica o en LCR superior a 100 mIU/mL fueron tratados como NGGCT.
Los germinomas bifocales — compromiso simultáneo supraselar y pineal — se tratan como enfermedad localizada con irradiación ventricular total seguida de boost de campo involucrado. El volumen blanco incluye el tumor prequimioterapia, cualquier enfermedad residual y todo el sistema ventricular. Delinear la enfermedad prequimioterapia en el momento de la planificación inicial es crítico, porque el volumen de boost frecuentemente se extiende más allá de los límites ventriculares normales.
El boost CTV se define como GTV prequimioterapia + 1 a 1,5 cm. La inclusión de la cisterna prepontina es opcional, pero debe considerarse en pacientes sometidos a ventriculostomía o con tumores supraselares voluminosos.
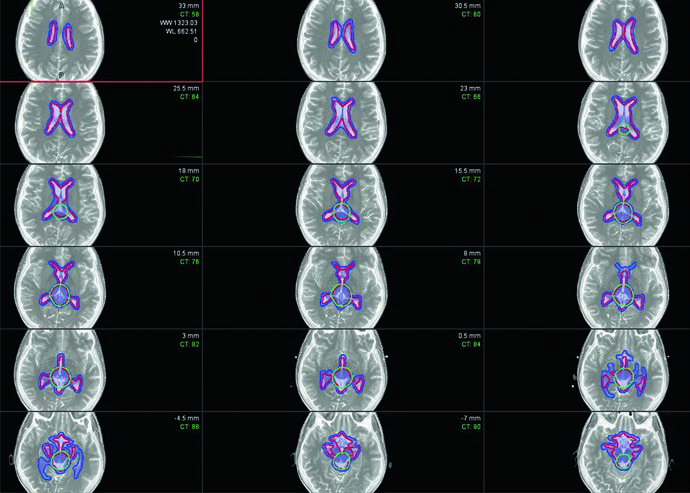
Esquemas de dosis para germinoma puro
Cuando la radioterapia es la modalidad única, el volumen ventricular recibe 21 a 24 Gy con boost hasta 45 Gy en el sitio tumoral prequimioterapia. Una fracción de 1,5 Gy es preferida por muchos centros dado el buen pronóstico y el deseo de minimizar la toxicidad neurocognitiva a largo plazo, aunque 1,8 Gy por fracción es igualmente razonable.
Con quimioterapia neoadyuvante y respuesta completa del primario, la dosis ventricular desciende a 21 Gy con boost de 9 a 15 Gy, totalizando 30 a 36 Gy en el tumor primario. El estudio ACNS 1123 investigó la reducción de la dosis ventricular a 18 Gy: no hubo fracasos ventriculares en los 74 pacientes evaluables, pero el estudio no logró demostrar no-inferioridad frente al umbral de 95% de supervivencia libre de progresión a 3 años. Los pacientes con respuesta parcial o enfermedad progresiva necesitan boost hasta 36 a 45 Gy en el tumor primario.
Para temas complementarios en delineación de SNC en adultos, consulte el artículo sobre tumores malignos del SNC que cubre gliomas de alto grado, y el artículo sobre tumores benignos del SNC que aborda meningiomas y schwannomas.




