Principios Generales de la Planificación Radioterápica en Tumores Malignos del SNC
La planificación de radioterapia para tumores malignos primarios del sistema nervioso central requiere un enfoque integral que comienza mucho antes de la simulación. El radioterapeuta necesita una historia clínica completa, un examen neurológico dirigido, evaluación hormonal basal, hemograma (fundamental para los candidatos a quimioterapia concomitante), campimetría, audiometría y evaluación neurocognitiva de base. Todo esto alimenta directamente las decisiones de planificación.
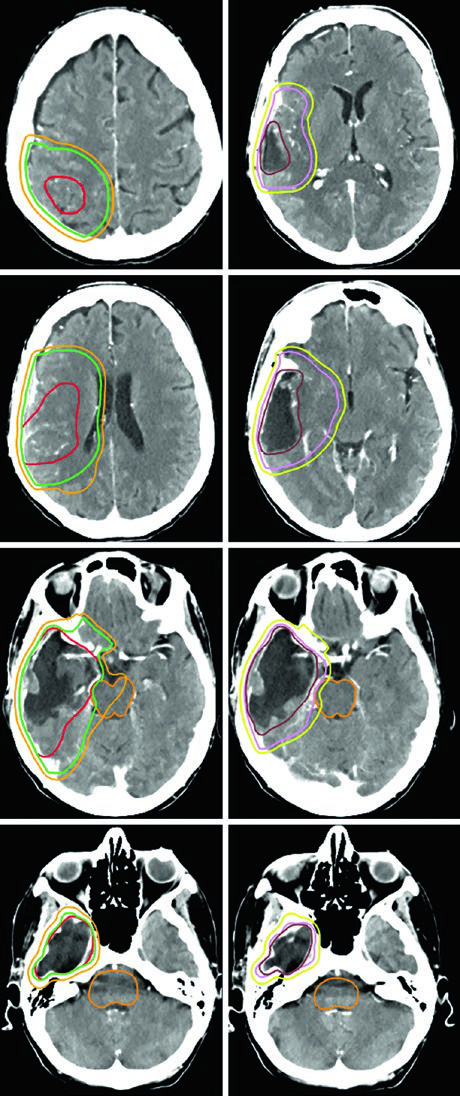
La resección quirúrgica máxima segura con el objetivo de lograr una resección macroscópica total sigue siendo el estándar de cuidado para tumores operables. Para pacientes inoperables, la radioterapia definitiva se aplica tras biopsia diagnóstica. La radioterapia adyuvante corresponde a la mayoría de los pacientes después de la resección.
Se utilizan diversas técnicas: radioterapia conformacional 3D (3D-CRT), radiocirugía estereotáxica fraccionada (FSRT), radioterapia de intensidad modulada (IMRT), arcoterapia volumétrica modulada (VMAT), radiocirugía estereotáxica (SRS) y protonterapia (PBT). La elección depende del tamaño tumoral, la localización y la proximidad a estructuras críticas. La delineación precisa de los volúmenes blanco y los órganos de riesgo es lo que permite determinar la mejor opción para cada paciente.
Un punto que no admite negociación: la corregistración de RM diagnóstica al CT de planificación es fundamental. Las secuencias T1 poscontraste y FLAIR muestran el tumor y el edema perilesional, mientras que T1 simple y secuencias 3D-T2/CISS permiten delinear el hipocampo y los nervios craneales. Para una visión global del tema, consulte nuestra guía completa sobre delineación de volumen blanco en radioterapia.
Posicionamiento, Inmovilización y Simulación
El posicionamiento estándar es decúbito supino con brazos paralelos al cuerpo y hombros relajados. Una máscara termoplástica indexada de 3 puntos proporciona la inmovilización para simulación y tratamiento basados en TC. Los tumores de base de cráneo o cercanos al aparato óptico pueden requerir una máscara de 5 puntos — la extensión cervical refuerza el posicionamiento del cuello. Para simulación por RM, se utiliza una máscara tipo clamshell.
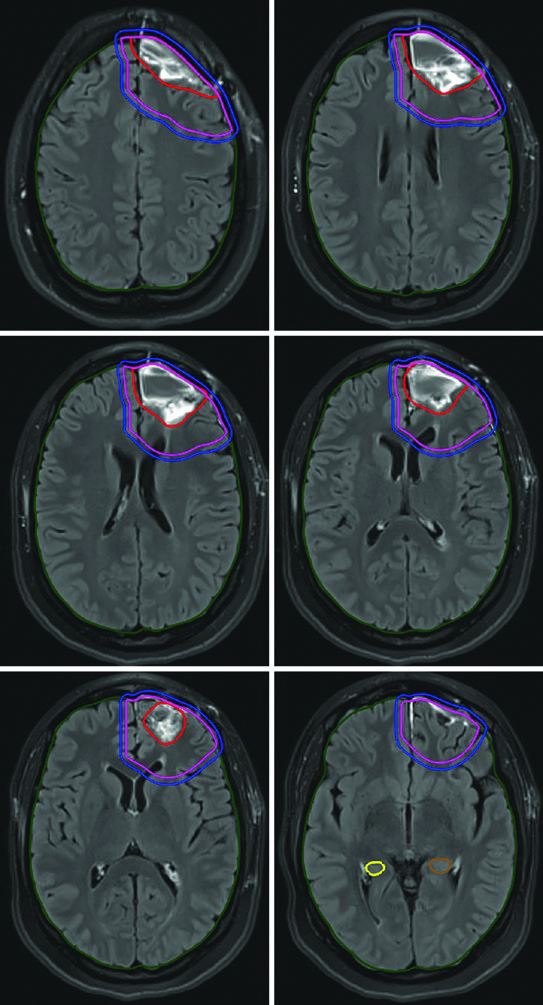
Cabeza y mentón permanecen en posición neutra salvo indicación contraria para base de cráneo. Los cortes axiales de TC se adquieren a 1 mm de espesor para SRS, FSRT o PBT, y a 2 mm para 3D-CRT, IMRT o VMAT — cubriendo desde el vértex hasta los hombros. El contraste IV puede ayudar a delinear cavidades quirúrgicas y facilitar la fusión con imágenes preoperatorias.
Estructuras Normales y Órganos de Riesgo
Los órganos de riesgo (OARs) se delinean en la TC de planificación con apoyo de la RM diagnóstica. Los volúmenes de riesgo de planificación (PRVs) sirven como margen dosimétrico adicional cuando el tumor se encuentra adyacente a estructuras críticas.
Lista de OARs sugeridos para tumores cerebrales primarios
| Estructura | Observación |
|---|---|
| Cerebro | Volumen total |
| Cerebro no involucrado | Cerebro menos GTV o CTV según escenario clínico |
| Tronco encefálico | Núcleo y superficie contorneados por separado |
| Médula espinal | — |
| Cócleas (D/I) | Bilateral |
| Globos oculares (D/I) | Bilateral |
| Cristalinos (D/I) | Bilateral |
| Nervios ópticos (D/I) | Bilateral |
| Quiasma óptico | — |
| Retinas (D/I) | Bilateral |
| Glándulas lagrimales (D/I) | Bilateral |
| Lóbulos temporales (D/I) | Bilateral |
| Hipocampos (D/I) | Se delinean preferiblemente en T1 poscontraste corregistrada |
| Hipotálamo | — |
| Hipófisis | — |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 30.1)
Glioma de Alto Grado: Volúmenes Blanco y Fraccionamiento
Los pacientes con astrocitoma de alto grado y oligodendroglioma se someten a resección quirúrgica máxima para diagnóstico y caracterización molecular. El tratamiento estándar combina radioterapia conformacional fraccionada a 59,4–60 Gy con quimioterapia concurrente o adyuvante.
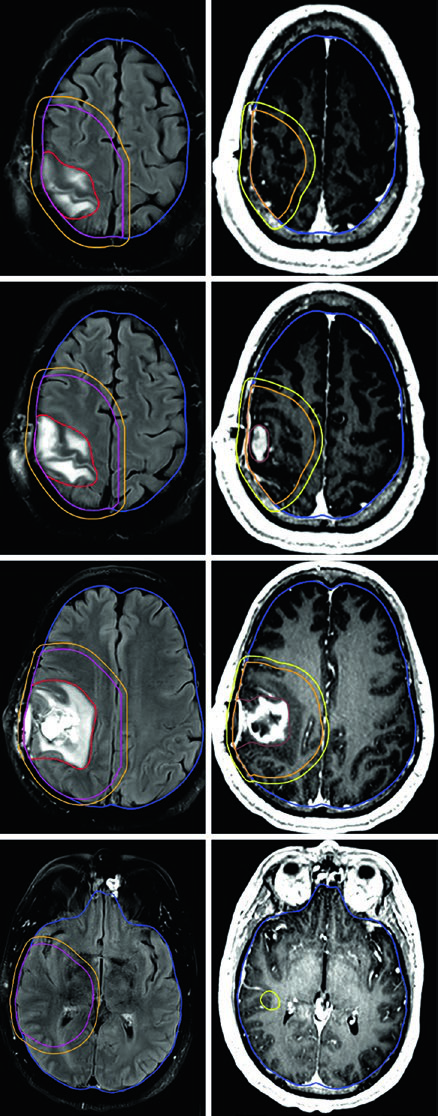
Para pacientes de alto riesgo, ancianos o frágiles, los esquemas hipofraccionados representan una alternativa validada: 40,05 Gy en 15 fracciones o 25 Gy en 5 fracciones, con márgenes reducidos de 0,5–1 cm, con o sin quimioterapia. El manejo del glioscarcoma replica el paradigma del glioblastoma.
Volúmenes blanco recomendados para glioma de alto grado
| Tipo tumoral | Dosis/Fraccionamiento | Definición del GTV | Expansión CTV | Expansión PTV |
|---|---|---|---|---|
| Glioma anaplásico (captante) | Cone-down secuencial: PTV1 50,4 Gy (1,8 Gy/fx), PTV2 59,4 Gy (1,8 Gy/fx); o SIB: PTV1 54,45 Gy (1,65 Gy/fx), PTV2 59,4 Gy (1,8 Gy/fx) | GTV1: volumen T2/FLAIR; GTV2: cavidad posoperatoria + tumor residual en T1 poscontraste | CTV1: 1,5 cm restringido anatómicamente; CTV2: 1,0 cm restringido | 0,3–0,5 cm |
| Glioma anaplásico (no captante) / Astrocitoma difuso IDH-wild type | PTV1: 59,4 Gy (1,8 Gy/fx) | GTV: cavidad posoperatoria + tumor residual en T2/FLAIR | CTV: 1,5 cm restringido anatómicamente | 0,3–0,5 cm |
| Glioblastoma | Cone-down: PTV1 46 Gy (2 Gy/fx), PTV2 60 Gy (2 Gy/fx); o SIB: PTV1 50–51 Gy (1,67–1,7 Gy/fx), PTV2 60 Gy (2 Gy/fx) | GTV1: volumen T2/FLAIR; GTV2: cavidad + tumor residual en T1 poscontraste | CTV1: 2 cm restringido; CTV2: 2 cm restringido | 0,3–0,5 cm |
| Gliosarcoma | Cone-down: PTV1 46 Gy (2 Gy/fx), PTV2 60 Gy (2 Gy/fx); o SIB: PTV1 50–51 Gy (1,67–1,7 Gy/fx), PTV2 60 Gy (2 Gy/fx) | GTV1: T2/FLAIR; GTV2: cavidad + tumor residual en T1 poscontraste | CTV1: 1,5–2 cm restringido; CTV2: 1,5–2 cm restringido | 0,3–0,5 cm |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 30.2)
Un punto práctico esencial: las expansiones anatómicamente restringidas implican que el CTV no cruza la línea media, no penetra en la cisterna prepontina, no invade el cráneo y no atraviesa el tentorio hacia la fosa posterior. Sin embargo, los tractos en riesgo de diseminación tumoral contralateral — como la rodilla del cuerpo calloso — deben incluirse explícitamente. Esta distinción resulta especialmente relevante en glioblastomas frontales que se aproximan a las fibras callosas.
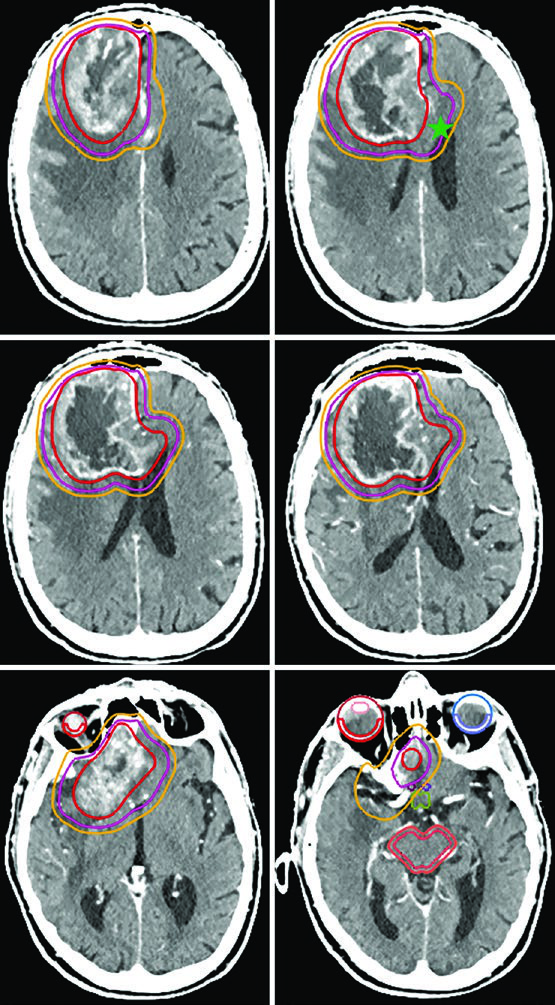
Esquemas Hipofraccionados para Pacientes de Alto Riesgo
El esquema de 40 Gy en 15 fracciones es adecuado cuando existe escaso volumen FLAIR fuera del tumor captante. El GTV abarca la cavidad de resección, el tumor residual y los nódulos satélite en T1 poscontraste, con un margen de CTV de solo 1,0 cm restringido anatómicamente al tentorio.
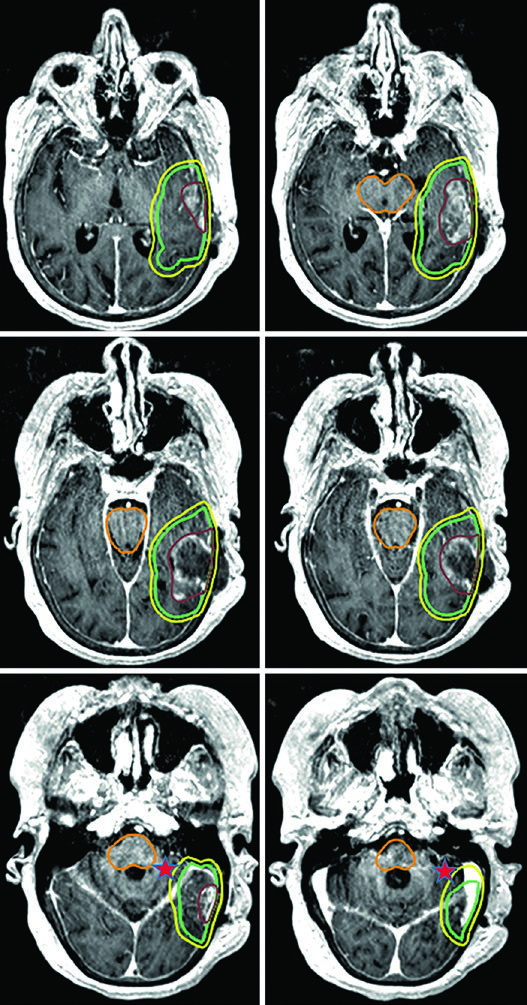
En los escenarios de pronóstico más desfavorable, la entrega ultrahipofraccionada — 25 Gy en 5 fracciones (o 30 Gy en 5 fracciones como en el caso ilustrado) — emplea márgenes de 0,5 cm del GTV al CTV. Un glioblastoma de fosa posterior ejemplifica este enfoque, donde la cóclea y el tronco encefálico sirven como referencias directas para la optimización dosimétrica.
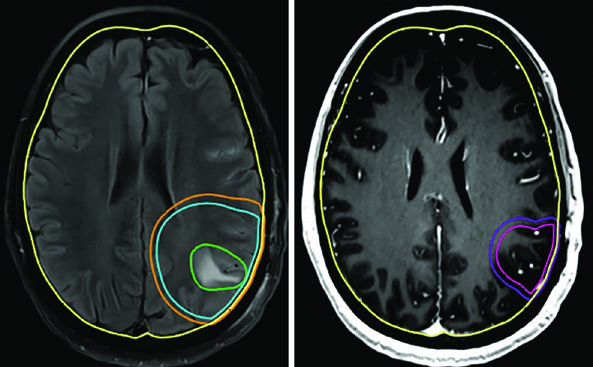
El gliosarcoma sigue el mismo paradigma que el glioblastoma. Se emplean habitualmente dos volúmenes secuenciales — el primero basado en FLAIR (46 Gy) y el segundo en T1 poscontraste (60 Gy), con expansiones de CTV de 1,5 cm anatómicamente restringidas.
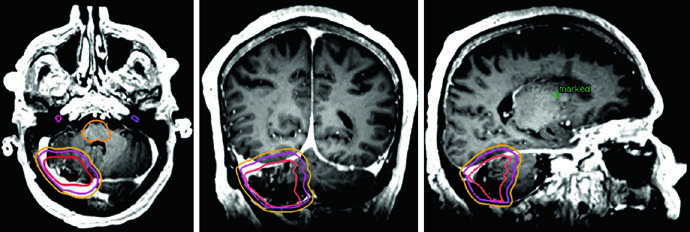
Meningioma Atípico y Maligno: Grados II y III de la OMS
Los meningiomas constituyen los tumores intracraneales primarios más frecuentes en adultos. Menos del 30% se clasifican como atípicos (OMS grado II) o malignos (OMS grado III). El abordaje radioterápico de estos subtipos difiere sustancialmente del meningioma benigno.
Para meningioma grado II, la radioterapia adyuvante puede considerarse tras resección macroscópica total y se recomienda tras resección subtotal. Para grado III, la radioterapia se recomienda para todos los pacientes independientemente de la extensión de la resección. Para el hemangiopericitoma, la radioterapia adyuvante está indicada en todos los casos posresección. Si desea conocer el manejo de los tumores benignos, consulte nuestro artículo dedicado sobre tumores benignos del SNC.
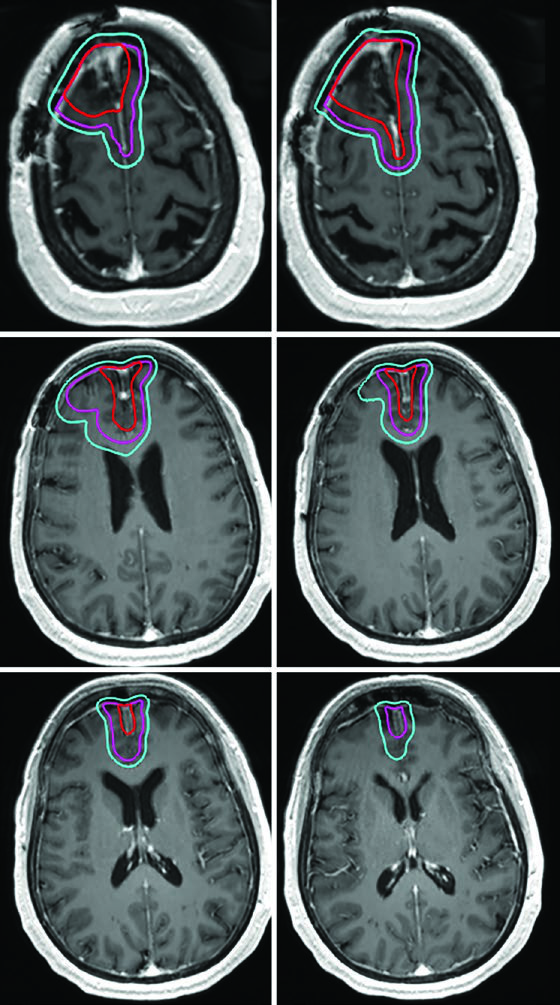
Una distinción crítica para los meningiomas de grado II/III: como estos tumores pueden invadir hueso y parénquima cerebral, el cráneo y el cerebro normal no funcionan necesariamente como barreras naturales a la diseminación tumoral. Si los hallazgos quirúrgicos o anatomopatológicos demuestran invasión cerebral, los márgenes del CTV deben incluir el parénquima en riesgo. Para lesiones recurrentes de grado II, es esencial evaluar el sitio de inserción dural original en el diagnóstico inicial.
Volúmenes blanco para meningioma grado II/III y hemangiopericitoma
| Tipo tumoral | Dosis/Fraccionamiento | Definición del GTV | Expansión CTV | Expansión PTV |
|---|---|---|---|---|
| Meningioma grado II (upfront) | 54–59,4 Gy (1,8 Gy/fx) | Cavidad posoperatoria, tumor residual incluyendo compromiso dural/óseo sospechoso en T1 poscontraste | 0,5 cm restringido anatómicamente | 0,3–0,5 cm |
| Meningioma grado II (recurrente) | 54–59,4 Gy (1,8 Gy/fx) | Ídem + evaluación de la inserción dural previa al diagnóstico inicial | 0,5–1,0 cm restringido | 0,3–0,5 cm |
| Meningioma grado III (upfront o recurrente) | 59,4–60 Gy (1,8–2 Gy/fx) | Ídem + inserción dural previa | 1,0–1,5 cm restringido | 0,3–0,5 cm |
| Hemangiopericitoma | 59,4–60 Gy (1,8–2 Gy/fx) | Cavidad posoperatoria, tumor residual, compromiso dural/óseo en T1 poscontraste | 1,5 cm restringido, pero incluir la totalidad del hueso comprometido | 0,3–0,5 cm |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 30.3)
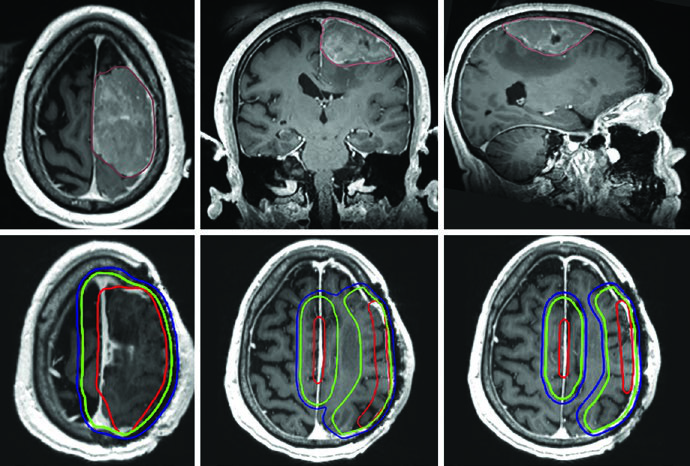
El hemangiopericitoma merece mención especial. La expansión de CTV de 1,5 cm sigue el patrón estándar, pero a diferencia de los meningiomas, la totalidad del hueso comprometido debe incluirse sin reducción en barreras óseas — la naturaleza infiltrativa de este tumor justifica una cobertura más agresiva.
Consideraciones Prácticas y Errores Frecuentes
Varios errores recurrentes en la planificación de tumores malignos del SNC merecen atención. El más común es aplicar expansiones isotrópicas sin respetar las barreras anatómicas. El CTV de un glioblastoma frontal no debe cruzar la línea media — a menos que la rodilla del cuerpo calloso esté en riesgo, en cuyo caso debe incluirse explícitamente. Otro error frecuente es confundir las secuencias de RM: el GTV1 debe basarse en FLAIR (edema peritumoral), mientras que el GTV2 utiliza la T1 poscontraste (enfermedad captante residual).
Para SRS y FSRT, el espesor de corte de 1 mm es obligatorio — cortes más gruesos comprometen la precisión geométrica. En cuanto a los márgenes de PTV: 0,3 cm es suficiente con IGRT diaria, mientras que 0,5 cm resulta más prudente sin verificación de imagen frecuente.
Artículos relacionados de esta serie pueden aportar contexto adicional: consulte nuestro artículo sobre metástasis cerebrales y WBRT/SRS para principios complementarios de radiocirugía, y el artículo sobre tumores cerebrales pediátricos para consideraciones específicas en la población más joven.




