La delineacion del carcinoma hepatocelular en radioterapia empieza antes del primer contorno. El capitulo lo plantea desde la primera pagina: un buen plan depende de TC trifasica con contraste, evaluacion clinica completa, lectura disciplinada de la invasion vascular, inmovilizacion fiable y una estrategia respiratoria capaz de reproducir la posicion del higado durante todo el tratamiento. Para situar este capitulo dentro del panorama general, conviene volver a nuestra guia completa sobre delineacion del volumen blanco y campos en radioterapia.
Ese arranque importa porque el higado no es un blanco inmovil. La fase arterial muestra mejor el tumor viable, la fase portal ayuda a fijar limites anatomicos a partir de los vasos intrahepaticos, la fase tardia define mejor la extension hacia la vena cava inferior y la respiracion desplaza todo ese escenario durante la simulacion y el tratamiento. El capitulo de HCC trabaja exactamente en esa interseccion entre imagen multifasica, control del movimiento y riesgo microscopico. Por eso sigue siendo tan util en la planificacion diaria: convierte la margen en una decision clinica y no en una costumbre.
Carcinoma hepatocelular: principios de delineacion
La respuesta central del capitulo es directa. En carcinoma hepatocelular, la tecnica elegida debe proteger higado sano sin perder credibilidad anatomica. Por eso step-and-shoot IMRT y la terapia de arco volumetrico modulado siguen siendo tecnicas estandar cuando se limita el numero de angulos o el rango del arco para reducir la dispersion de dosis baja sobre el parenquima no comprometido.
El texto tambien delimita cuando SBRT pasa a ser la opcion preferida. El tratamiento con 5 o 6 fracciones o menos se favorece cuando existe proteccion intestinal segura, disponibilidad de alta tasa de dosis, inmovilizacion adecuada e image guidance fiable. No se presenta como una defensa general de SBRT. El capitulo la vincula a un escenario en el que el equipo puede verificar la posicion hepatica y respetar la cercania entre el blanco y los tejidos gastrointestinales luminales. El esquema hipofraccionado puede utilizarse precisamente porque algunos tumores estan muy proximos a esas estructuras.
Esa forma de abrir el tema organiza todo lo que viene despues. La eleccion tecnica no llega al final del contorneo. Ya depende de volumen, organos de riesgo y reproducibilidad. Por eso el capitulo insiste tanto en coordinacion respiratoria, posicion de tratamiento y fusion de imagenes. Si esas piezas fallan, la margen deja de expresar el caso real y se convierte en una cifra defensiva.
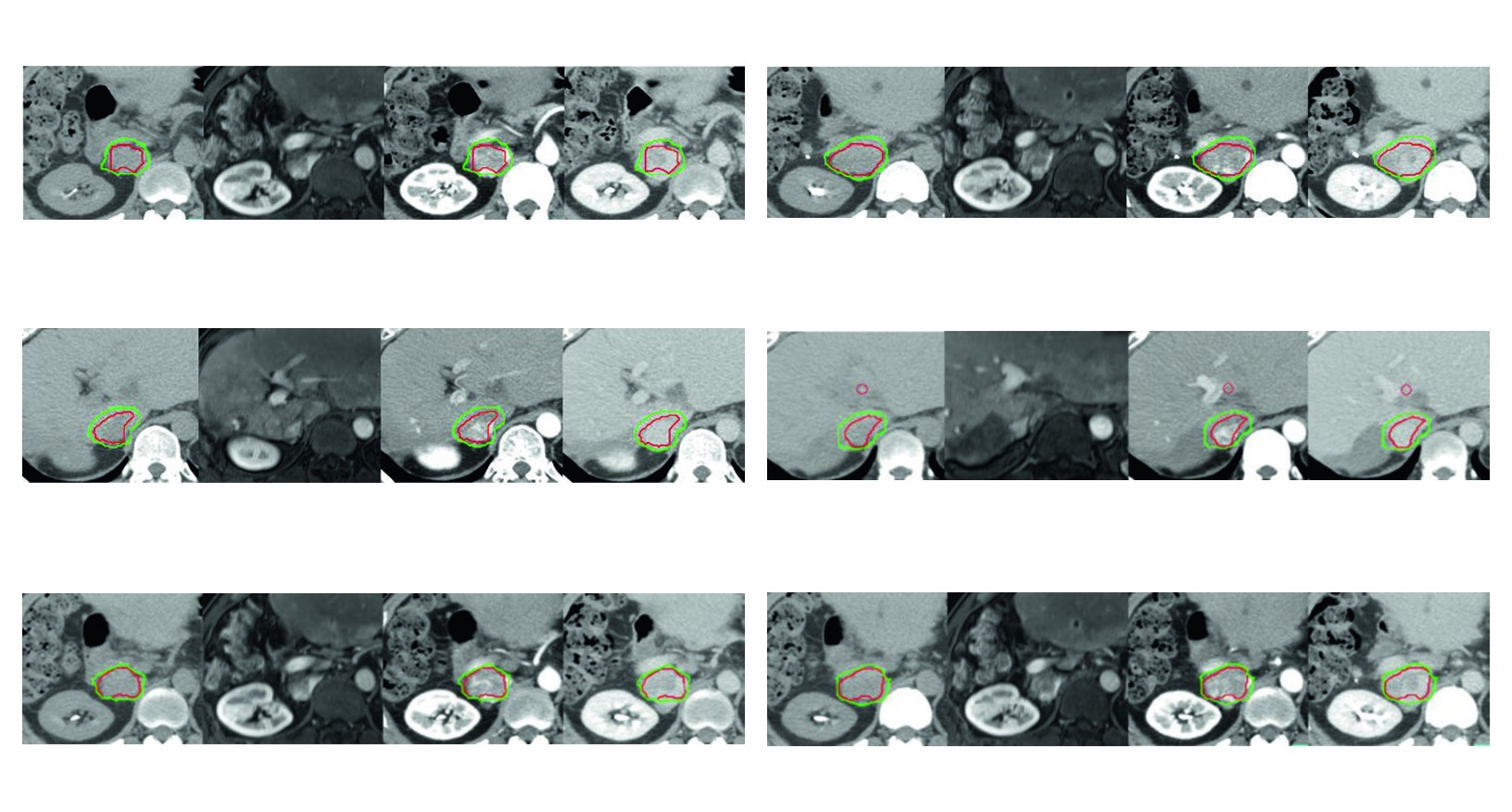
La Figura 17.1 muestra esa logica de forma concreta. En el caso de tumor residual tras quimioembolizacion arterial transcateter y radiofrecuencia, el GTV incluye tanto el tumor que realza como la trombosis invadida de la vena cava inferior. El CTV agrega despues un margen de 5 mm dentro del limite hepatico y un margen intravascular de 3 mm alrededor del GTV. El libro no presenta la expansion como automatica. Presenta una margen que sigue la geometria de una recidiva ya tratada.
Imagen trifasica y estadificacion antes de planificar
El capitulo exige una base clinica completa antes de la simulacion. Historia clinica, examen fisico, estudios de laboratorio, valoracion de la funcion hepatica y pruebas de imagen forman parte del mismo paso porque todos influyen en diagnostico, estadificacion y diseno del tratamiento. En HCC, separar esas decisiones suele debilitar la definicion del blanco, ya que el volumen a tratar depende tanto de la extension de la enfermedad como de la reserva hepatica restante.
El estudio principal es una TC hepatica con contraste, idealmente trifasica, con fases arterial, portal-venosa y tardia, obtenida con grosor de corte de 3 a 5 mm. Ese detalle numerico importa. Un grosor en ese rango permite leer el patron de realce y las relaciones vasculares con suficiente detalle y, al mismo tiempo, sigue siendo adecuado para fusion y planificacion. El capitulo no trata la TC trifasica como un lujo. La presenta como el eje de la definicion del blanco.
La resonancia magnetica dinamica multifasica entra cuando el paciente puede sostener la apnea necesaria para la adquisicion, o cuando el contraste de la TC esta contraindicado. Con fusion de imagenes, la RM puede complementar a la TC en la delineacion. Esa palabra, complementar, es importante. El capitulo no sustituye un estudio por otro. Utiliza cada modalidad para responder una pregunta distinta dentro del mismo caso.
El PET se reserva para escenarios mas concretos. Las imagenes con 18F-FDG y con otros trazadores, como 11C-acetato y 11C-colina, pueden ayudar a localizar tumor viable en casos individuales, sobre todo cuando existe enfermedad residual o recurrente en zonas previas de retencion de lipiodol y o en regiones tratadas con radiofrecuencia. Esa limitacion es util porque evita convertir el PET en una rutina automatica. El capitulo lo deja como herramienta de resolucion de problemas cuando la duda principal es donde persiste tumor viable.
Si quiere contrastar esta logica con otro sitio del abdomen superior dentro de la misma serie, puede revisar tambien nuestro articulo sobre cancer de pancreas y delineacion en radioterapia. La utilidad de esa comparacion es clara: en abdomen superior, la seleccion de imagen y la estrategia respiratoria suelen pesar tanto como la disposicion de los campos.
Otra virtud del capitulo es que asigna una tarea distinta a cada fase de contraste. En lugar de pedir que un solo conjunto de imagenes resuelva todas las dudas del contorneo, reparte funciones entre las fases. Eso vuelve la planificacion mas coherente y evita un error frecuente en los casos hepaticos: aumentar margen porque la interpretacion de la imagen fue incompleta.
Inmovilizacion y control del movimiento del higado
El capitulo no trata el manejo del movimiento como un refinamiento optativo. Afirma de forma explicita que se necesita inmovilizacion de medio cuerpo o de cuerpo entero con control respiratorio para mejorar la reproducibilidad. Se pueden usar dispositivos como vacuum bag o chest board, idealmente con los brazos elevados, tanto en la simulacion como a lo largo del tratamiento.
La recomendacion tiene dos fundamentos. Uno es geometrico: mantener consistencia diaria. El otro es practico: preservar acceso de haces. El texto agrega ademas un requisito que muchas revisiones resumidas pasan por alto. El sistema de inmovilizacion no debe atenuar la dosis ni interferir con posiciones de gantry necesarias para haces coplanares o no coplanares.
Despues el capitulo entra en el aspecto mas delicado del tratamiento hepatico: el movimiento respiratorio. La apnea activa ayuda a reducir el volumen tratado y es preferible en pacientes que pueden mantener la respiracion durante mas de 30 segundos. Ese numero funciona como un umbral practico. Indica cuando la apnea probablemente producira imagenes utiles y administracion reproducible, y cuando solo generara concesiones repetidas.
Si la apnea no se tolera, puede utilizarse compresion abdominal. El texto, sin embargo, no la idealiza. La compresion puede deformar el abdomen o cambiar la forma de los organos. Es decir, reducir amplitud de movimiento tambien puede introducir un nuevo problema geometrico. Por eso la delineacion se realiza con mayor frecuencia sobre imagenes multifasicas y multimodales obtenidas en apnea, reproduciendo la forma en que habitualmente se interpreta la imagen diagnostica del HCC.
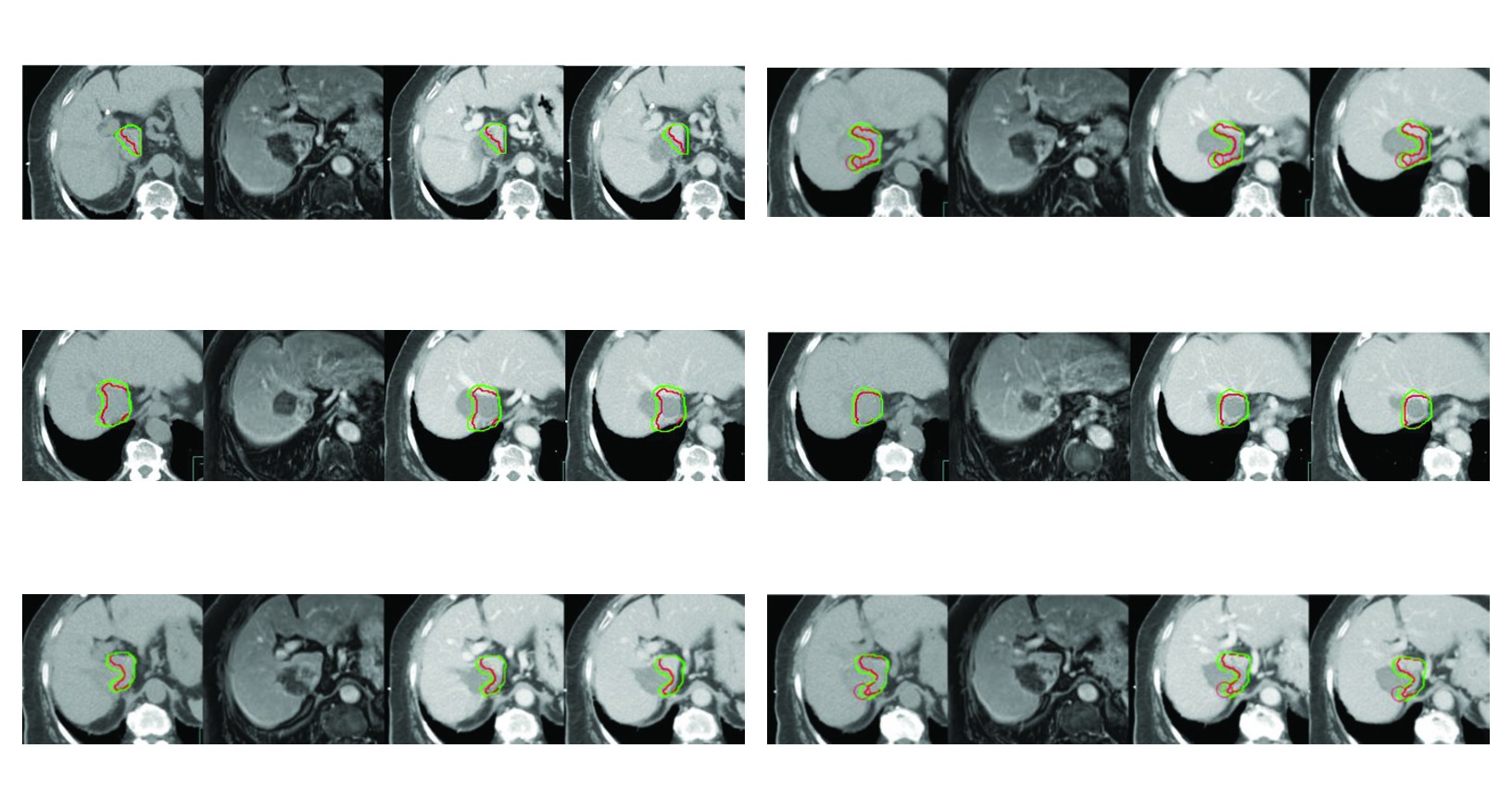
Image-guided radiation therapy se considera necesaria porque la posicion del higado cambia tanto dentro de una fraccion como entre fracciones. En pacientes que no toleran control respiratorio voluntario, la compresion abdominal pasiva combinada con 4DCT aporta informacion sobre movimiento interno y puede compensar cambios de posicion hepatica. El tratamiento con gating tambien puede ser util, aunque prolonga la sesion al trabajar dentro de una ventana inspiratoria o espiratoria seleccionada.
La Figura 17.2 deja ver por que todo esto importa. En la recurrencia con trombosis parcial de la vena cava inferior despues de radiofrecuencia repetida, la simulacion trifasica se obtiene con coordinacion en apnea para inmovilizacion hepatica. El CTV incluye el tumor que realza y el trombo tumoral representados por el GTV, ademas de un margen de 5 mm alrededor del GTV dentro del limite del higado y dentro de la zona previamente ablacionada cuando existe necesidad clinica. El control del movimiento y la historia de tratamiento previo cambian el blanco final.
TC de simulacion y funcion de cada fase de contraste
La simulacion debe realizarse con contraste intravenoso y adquisicion multifasica, con el paciente ya en posicion de tratamiento y bajo coordinacion respiratoria. El capitulo insiste en esto porque el blanco no debe nacer de una anatomia generica. Debe dibujarse en la misma geometria que despues sera tratada. Esa alineacion entre interpretacion diagnostica, posicion de simulacion y estrategia respiratoria es una de las enseñanzas mas practicas del texto.
La fusion entre las distintas fases de la simulacion, y cuando hace falta con imagenes diagnosticas, ayuda a definir el GTV. El HCC viable suele verse mejor y mas brillante en la fase arterial. En las fases venosa y tardia presenta menos realce en relacion con el higado. Ese patron de realce arterial seguido de washout no solo sirve para diagnostico. Durante la planificacion ayuda a separar tumor viable de cambios adyacentes por tratamientos previos.
La fase portal cumple otra tarea. El capitulo explica que aprovecha la distribucion de los vasos intrahepaticos para definir los limites anatomicos del tumor tratado, sobre todo cuando la inmovilizacion y el control respiratorio deforman la forma del higado. La invasion tumoral de estructuras vasculares se observa mejor en la fase portal-venosa. Si la pregunta clinica es la extension del compromiso de la vena cava inferior, la fase tardia lo demuestra mejor.
Esa distribucion de funciones entre fases es una de las mejores lecciones practicas del capitulo. No le pide a la fase arterial que resuelva todas las dudas del contorneo ni reduce la fase portal a una simple confirmacion. Cada fase responde a una parte del problema: demostrar tumor viable, definir barreras anatomicas o mostrar extension venosa mayor. En planificacion de carcinoma hepatocelular, esa disciplina suele ser mas valiosa que añadir margen sin una base clara de imagen.
GTV, CTV, riesgo microscopico y PTV
El capitulo reconoce que, en circunstancias seleccionadas de SBRT, solo el tumor visible puede tratarse como GTV. Ese es el escenario acotado. Lo mas frecuente es ampliar el GTV para formar un CTV segun el riesgo clinico de diseminacion microscopica dentro del parenquima hepatico, incluyendo areas alrededor de radiofrecuencia previa o zonas embolizadas.
Al mismo tiempo, el texto advierte que el CTV no es un objeto fijo. Puede cambiar de tamano y de posicion por movimiento respiratorio y por dinamica de organos. Esa advertencia modifica la forma de leer toda la tabla de margenes. Un numero solo tiene sentido si esta vinculado al control respiratorio realmente logrado y al comportamiento geometrico del higado en ese paciente.
Tabla 17.1. Volumenes sugeridos en las regiones de GTV y CTV
Esta tabla concentra el nucleo operativo del capitulo. Separa enfermedad macroscopica visible, extension macroscopica contigua, riesgo microscopico opcional y expansion final de planificacion. Leida con calma, demuestra que el capitulo no mezcla enfermedad evidente y cobertura electiva por costumbre.
| Volumen blanco | Definicion y descripcion |
|---|---|
| GTVa | Tumor hepatico: tumor intrahepatico con realce en la TC contrastada en fase arterial y washout en la TC venosa o tardia. Tumor con retencion de lipiodol: lipiodol blanco contiguo al tumor que realza. Tumor refractario tras ablacion: tumor con realce arterial adyacente a la zona ablacionada hipodensa. Trombo tumoral vascular: trombo con realce arterial y washout en la fase venosa. |
| CTVmacroscopica | Tumor hepatico: el tumor intrahepatico con realce en la fase arterial. Zona embolizada contigua al tumor que realza incluida en el GTV. Tumor con realce arterial adyacente a la zona ablacionada hipodensa. Trombo tumoral vascular con realce arterial. |
| CTVmicroscopic electivob | Margen de 3 a 5 mm alrededor del GTV intrahepatico. Margen opcional de 2 a 3 mm alrededor del GTV de trombo tumoral dentro del vaso, segun indicacion clinica o protocolo. Trombo bland adyacente al GTV de trombo tumoral. Zona de radiofrecuencia adyacente al GTV. Zona embolizada no directamente adyacente al GTV. El CTV no debe cruzar barreras naturales, como la superficie o el limite del higado. |
| PTV | CTV, o GTV/CTVmacroscopic, mas 5 a 20 mm, con posibilidad de asimetria segun inmovilizacion y control respiratorio. El movimiento interno de organos y el error de setup constituyen la base del PTV. El 4DCT adquirido en todas las fases respiratorias puede ayudar a definir el PTV y cubrir la extension del movimiento interno. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 17.1)
Notas de la tabla: a GTV y CTV macroscopico pueden tratarse, por ejemplo, con 45 a 54 Gy en 3 a 6 fracciones, recordando que la dosis segura puede necesitar reduccion si los tejidos normales limitan el plan. b El CTV electivo o microscopico puede tratarse, por ejemplo, con 24 a 30 Gy en 3 a 6 fracciones; el propio texto añade que la autora L.A.D. no recomienda de rutina un CTV microscopico alrededor del GTV. c El margen adicional alrededor del GTV intrahepatico puede recibir dosis macroscopicas o mas altas si eso es seguro.
Estas notas son clinicamente decisivas porque impiden convertir la tabla en un protocolo rigido. El capitulo ofrece un marco de referencia, pero admite que el CTV microscopico es opcional y puede no formar parte de la rutina. Tambien recuerda que dosis y margenes siguen respondiendo a la tolerancia de los tejidos normales. En HCC, ese equilibrio pesa tanto como el deseo de cubrir extension subclinica.
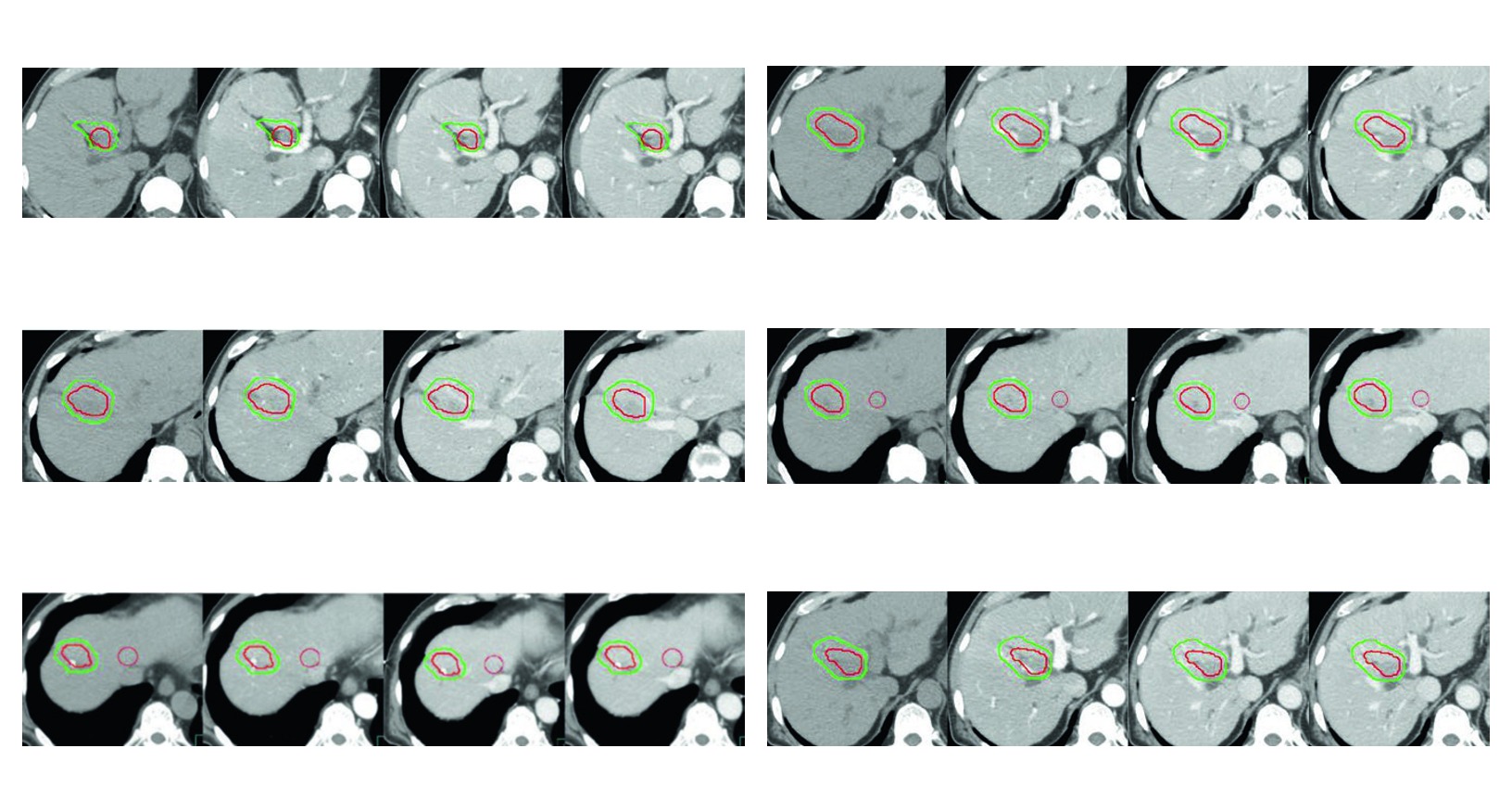
La Figura 17.3 representa muy bien esa filosofia. En la recidiva despues de cirugia y radiofrecuencia, con alto riesgo de lesion del conducto biliar por la ablacion, la simulacion utiliza fases sin contraste, arterial, portal y venosa tardia, todas obtenidas con coordinacion en apnea. El CTV incluye el tumor que realza mostrado como GTV, un margen de 5 mm en parenquima hepatico y un margen intravascular de 3 mm alrededor del GTV. No hay expansion rutinaria. Hay una respuesta a un escenario clinico definido.
Que enseñan las cuatro figuras clinicas
Las cuatro figuras del capitulo funcionan como ejemplos aplicados de la misma logica de delineacion. Todas utilizan simulacion multifasica con coordinacion en apnea para inmovilizacion hepatica. Todas muestran GTV en rojo y CTV en verde. Y todas dejan ver que la seleccion de margenes cambia cuando entran en juego trombo tumoral, tejido previamente ablacionado, territorio embolizado o extension vascular.
Figura 17.1
En el primer caso, la enfermedad residual despues de quimioembolizacion y radiofrecuencia incluye trombosis invadida de la vena cava inferior. La leccion es clara. Cuando la enfermedad sale del parenquima e invade el compartimento vascular, la planificacion debe incorporar esa geometria y no limitarse al nodulo intrahepatico.
Figura 17.2
En el segundo caso, la recidiva despues de radiofrecuencia repetida muestra como un territorio previamente tratado puede necesitar inclusion cuando existe indicacion clinica. El margen de 5 mm alrededor del GTV dentro del limite hepatico y de la region ablacionada no es exceso. Responde a riesgo contiguo en un sitio ya tratado.
Figura 17.3
En el tercer caso, el riesgo biliar despues de cirugia y radiofrecuencia refuerza que delineacion y planificacion no pueden separarse. El contorno ya nace condicionado por una historia local que cambia tanto la seguridad como la distribucion de dosis.
Figura 17.4
En el cuarto caso, el HCC refractario a sorafenib con progresion de trombosis en vena porta y vena hepatica media resume muy bien el capitulo. El CTV incluye el tumor que realza, el GTV en rojo y un margen tridimensional de 5 mm alrededor del GTV dentro del limite hepatico. Incluso con compromiso vascular mayor, la expansion sigue respetando la frontera anatomica del higado.
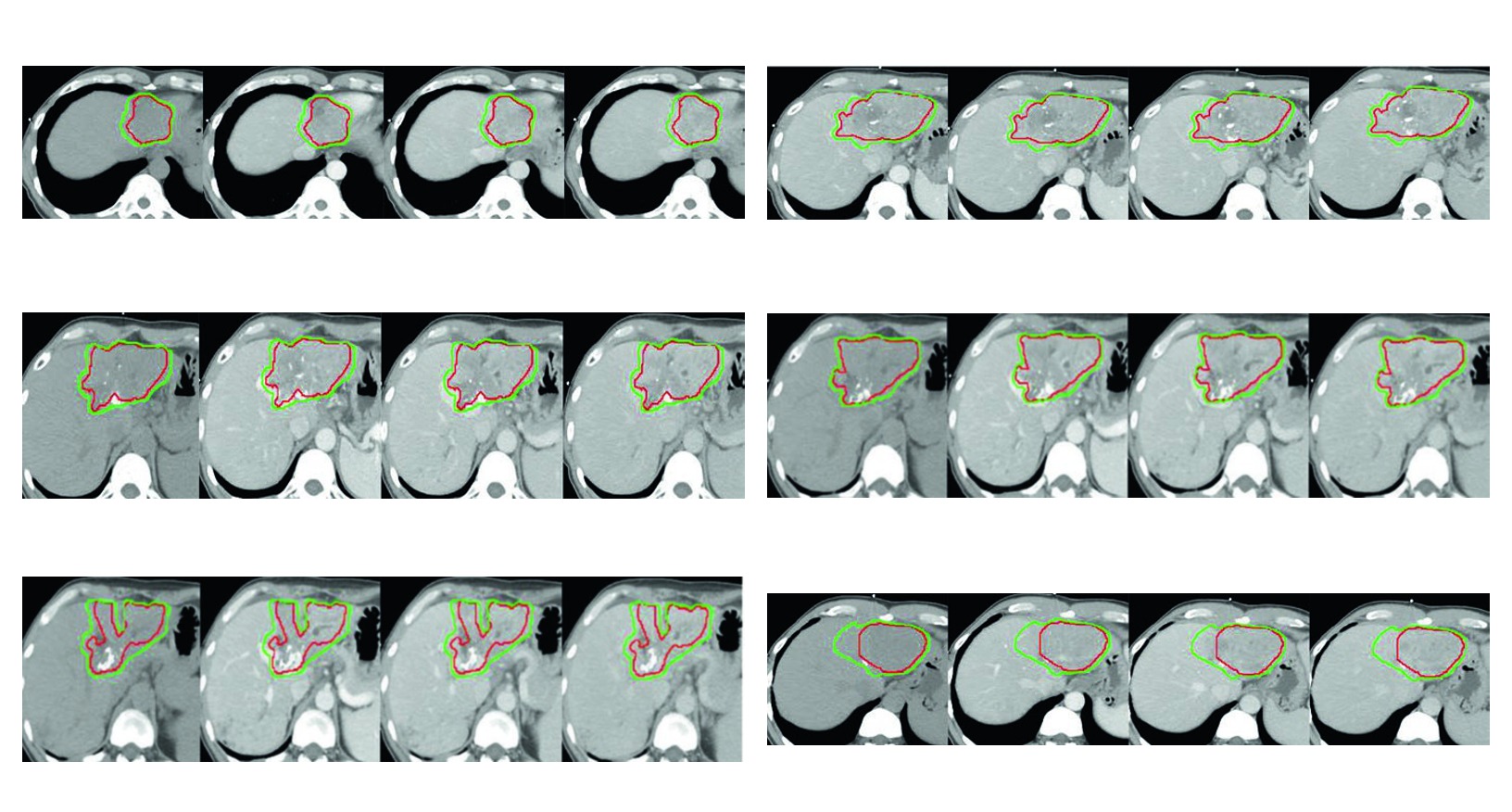
Si se observan juntas, las figuras sostienen un mensaje muy consistente. La expansion intraparenquimatosa cubre riesgo adyacente dentro del higado. La expansion intravascular aparece cuando el trombo tumoral forma parte real del problema geometrico. Las zonas ablacionadas o embolizadas entran en el volumen cuando el caso lo exige, no por defecto. Probablemente sea la parte mas util del capitulo para quien necesita defender el diseño final del volumen en revision entre pares o en una discusion multidisciplinaria.
Como cierra el capitulo en la practica
Las referencias finales no añaden nuevos contornos, pero muestran de donde sale la logica del capitulo. La lista incluye radioterapia local con o sin quimioembolizacion transarterial en enfermedad irresecable, variabilidad interobservador y consensos para definicion de blanco con y sin trombo portal, atlas de organos de riesgo del abdomen superior, comparacion entre protonterapia y radiofrecuencia en recurrencia, consensos APPLE sobre radioterapia y SBRT, SBRT individualizada, factores relacionados con microinvasion y un ensayo aleatorizado que comparo quimioembolizacion transarterial mas radioterapia externa frente a sorafenib en invasion vascular macroscopica.
La regla practica que permanece es muy clara. En carcinoma hepatocelular, delinear bien significa asociar la fase de contraste correcta a la pregunta correcta de contorneo, controlar el movimiento respiratorio de forma reproducible y elegir margenes defendibles tanto por anatomia como por historia de tratamiento. Cuando esas tres capas se mantienen alineadas, GTV, CTV y PTV dejan de ser siglas abstractas y pasan a describir la enfermedad real del paciente. Para recuperar la vision amplia del tema, vuelva a la guia principal sobre delineacion del volumen blanco y campos en radioterapia.




