Delineación de Volumen Blanco en Cáncer Gástrico
El cáncer gástrico sigue siendo una de las neoplasias que más desafían la planificación radioterápica adyuvante. El estómago se extiende desde la unión gastroesofágica hasta el píloro, con la curvatura mayor formando el borde izquierdo convexo y la curvatura menor constituyendo el borde derecho cóncavo. Anatómicamente se divide en cuatro regiones — cardias, fondo, cuerpo y antro — y su pared presenta cinco capas histológicas: mucosa, submucosa, muscular externa, subserosa y serosa. Para una visión integral de todos los sitios anatómicos abordados en esta serie, consulte nuestra guía completa sobre delineación de volumen blanco.
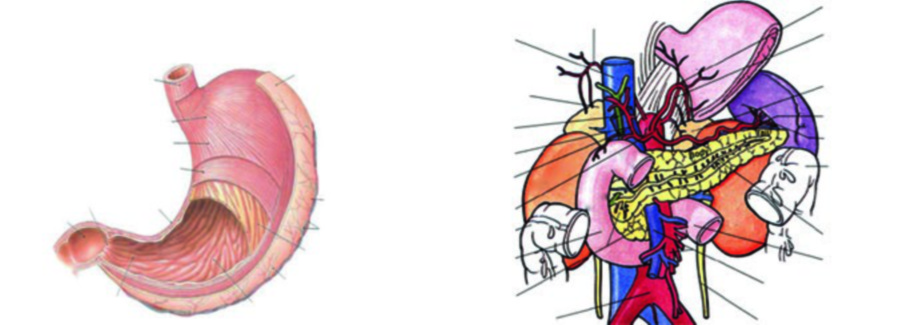
En cuanto a la localización primaria, los tumores de la unión gastroesofágica, cardias y fondo representan aproximadamente el 35% de los casos; los del cuerpo abarcan cerca del 25%; y los del antro y estómago distal conforman alrededor del 40%. Esta distribución tiene implicación directa en la planificación, ya que los volúmenes de CTV cambian sustancialmente según el subsitio de origen.
En la extensión local, el tumor puede invadir directamente hígado, duodeno, páncreas, colon transverso, omento y diafragma. Los tumores proximales frecuentemente se extienden superiormente hacia el esófago. La invasión perineural constituye otra vía de diseminación que no debe ser subestimada.
Estaciones Ganglionares y Patrones de Diseminación
El compromiso ganglionar en el cáncer gástrico es extremadamente prevalente — hasta el 80% de los pacientes ya presentan metástasis ganglionares al momento del diagnóstico. En la práctica, esto significa que la delineación de los volúmenes nodales es tan crítica como la cobertura del lecho tumoral.
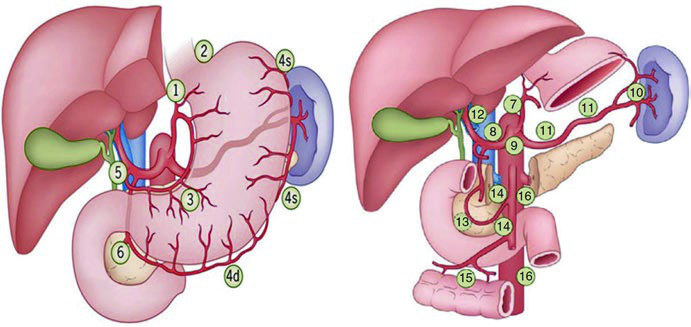
La clasificación japonesa (JRSGC) organiza las estaciones en cuatro niveles. La siguiente tabla reproduce fielmente la distribución publicada en el libro de texto, con la correspondencia anatómica de cada estación.
Estaciones Ganglionares — Clasificación JRSGC
| Grupo | Estación | Descripción |
|---|---|---|
| N1 | 1 | Ganglios cardiales derechos |
| N1 | 2 | Ganglios cardiales izquierdos |
| N1 | 3 | Ganglios a lo largo de la curvatura menor |
| N1 | 4 | Ganglios a lo largo de la curvatura mayor |
| N1 | 5 | Ganglios suprapilóricos |
| N1 | 6 | Ganglios infrapilóricos |
| N2 | 7 | Ganglios a lo largo de la arteria gástrica izquierda |
| N2 | 8 | Ganglios a lo largo de la arteria hepática común |
| N2 | 9 | Ganglios a lo largo del eje celíaco |
| N2 | 10 | Ganglios en el hilio esplénico |
| N2 | 11 | Ganglios a lo largo de la arteria esplénica |
| N3 | 12 | Ganglios en el ligamento hepatoduodenal |
| N3 | 13 | Ganglios en la cara posterior de la cabeza pancreática |
| N3 | 14 | Ganglios en la raíz del mesenterio |
| N4 | 15 | Ganglios en el mesocolon transverso |
| N4 | 16 | Ganglios paraaórticos |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 15.1). Adaptado de Hartgrink & Van De Velde (2005).
Clínicamente, los tumores proximales y de la UGE tienden a diseminarse hacia los ganglios paraesofágicos inferiores. Los tumores del cuerpo pueden afectar prácticamente todas las estaciones. Los tumores distales y antrales tienen mayor tendencia a comprometer ganglios periduodenales y de la porta hepática. Esta lógica de diseminación constituye la base para la selección de los volúmenes nodales en el CTV.
Estudio Diagnóstico para la Delineación
Antes de la planificación radioterápica, es imperativo revisar los informes quirúrgico y patológico y discutir con el cirujano para identificar las áreas de mayor riesgo de recurrencia. Debe anotarse si la cirugía fue gastrectomía total o parcial, ya que esto modifica completamente la anatomía postoperatoria.
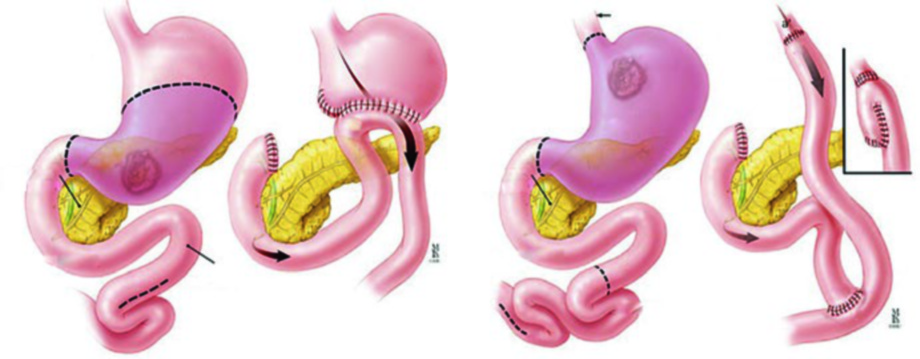
La TC preoperatoria debe revisarse para localizar el tumor primario y las cadenas ganglionares comprometidas. Cabe señalar que el PET con FDG como único método no es adecuado para la estadificación del cáncer gástrico, dado que los subtipos difuso y mucinoso presentan baja captación de FDG — una trampa diagnóstica frecuente.
Debe considerarse un estudio cuantitativo de perfusión renal bilateral antes de la radioterapia. La TC diagnóstica postoperatoria con contraste oral e intravenoso es obligatoria, con identificación precisa de: esófago y remanente gástrico, anastomosis (gastroyeyunal o esofagoyeyunal), muñón duodenal, porta hepática, hilio esplénico, páncreas, y arteria celíaca y arteria mesentérica superior.
Principios Generales de Planificación y CTV Adyuvante
Los pacientes deben ayunar durante 2 a 3 horas antes de la TC de simulación y antes de cada fracción de tratamiento. La TC de planificación, con cortes de 3–5 mm de espesor, debe adquirirse con el paciente en decúbito supino y brazos por encima de la cabeza, extendiéndose desde la parte superior del diafragma (o la carina para tumores de la UGE o cardias) hasta la base de L4.
La inmovilización con bolsa de vacío tipo VacLok se recomienda para el tratamiento con IMRT. Se prefiere el contraste intravenoso para visualizar los vasos sanguíneos y guiar la delineación del CTV, particularmente para los volúmenes nodales.
Definición de los Volúmenes Blanco
| Volumen | Definición y Descripción |
|---|---|
| GTV | Enfermedad residual macroscópica definida por imagen (TC) y hallazgos quirúrgicos |
| PTV (enfermedad residual) | GTV residual / márgenes positivos + 1,5 cm. Boost tipo cone-down después de 45 Gy hasta dosis total de 50,4–54 Gy en fracciones de 1,8 Gy |
| CTV45 | Cobertura de los grupos nodales según subsitio (Tablas 15.5–15.8). Incluye remanente gástrico, anastomosis (gastroyeyunal o esofagoyeyunal), muñón duodenal |
| PTV45 | CTV45 + 1 cm de margen. Un margen mayor puede ser necesario por movimiento de órgano e incertidumbres de posicionamiento |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 15.2)
Tres áreas deben identificarse como CTV en la radioterapia adyuvante: el lecho tumoral gástrico, la anastomosis o muñones, y las cadenas linfáticas regionales. Además, el ligamento hepatogástrico debe tratarse preferentemente en todos los casos, pues presenta alto riesgo de recurrencia — representa la parte del omento menor que conecta la curvatura menor con el hígado y contiene los ganglios gástricos izquierdos y derechos que no siempre son completamente resecados en la cirugía.
La dosis total recomendada para radioterapia adyuvante con quimioterapia concurrente es de 45 Gy en 25 fracciones, utilizando fotones de alta energía (≥6 MV). Deben administrarse boosts de 50,4–54 Gy para márgenes positivos o enfermedad residual, siempre que las dosis en los órganos críticos adyacentes permanezcan dentro de la tolerancia.
Impacto del Estadio T y N en los Volúmenes de Tratamiento
| Categoría TN (AJCC 8ª edición) | Estómago remanente | Lecho tumoral | Ganglios |
|---|---|---|---|
| T1-2N0 (sin invasión de subserosa) | No | No | No |
| T2N0 (invasión de subserosa) | Variable | Sí | No |
| T3N0 | Variable | Sí | No |
| T4N0 | Variable | Sí | Variable |
| T1-2N+ | Sí | No | Sí |
| T3-4N+ | Sí | Sí | Sí |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 15.4). Adaptado de Clinical Radiation Oncology, 4ª edición.
CTV por Subsitio: Unión Gastroesofágica
Para los tumores de la UGE, el estómago remanente debe incluirse siempre que permita la exclusión de dos tercios del riñón derecho. La cobertura del lecho tumoral depende del estadio T: para T2N0 con invasión de la subserosa, se incluyen el hemidiafragma izquierdo medial y el cuerpo del páncreas adyacente. Para T3N0, el abordaje es similar. Para T4N0, se añaden los sitios de adherencia con margen de 3–5 cm.
Los volúmenes nodales para la UGE incluyen ganglios perigástricos (PG), perioesofágicos (PEN), celíacos (CN) y mediastínicos (MN), según el estadio N. Un margen de 4 cm del esófago debe incluirse en el CTV para tumores de la UGE. La inclusión nodal opcional para T2-3N0 es aceptable cuando se ha realizado una disección D2 adecuada con al menos 10–15 ganglios examinados.
CTV por Subsitio: Cardias y Tercio Proximal
Para tumores del cardias y tercio proximal, el estómago remanente debe incluirse respetando dos tercios de un riñón, generalmente el derecho. El lecho tumoral para T2N0 incluye el hemidiafragma izquierdo medial y el cuerpo del páncreas adyacente, con o sin cola. En la enfermedad T1-2N+, los volúmenes nodales se expanden para incluir PG, CN, esplénico, suprapancreático (SP), con posibilidad de mediastínico (MN), pancreaticoduodenal (PD) y porta hepática (PH). Es importante señalar que PD y PH presentan bajo riesgo cuando la positividad ganglionar es mínima (1–2 ganglios positivos con 10–15 examinados).
CTV por Subsitio: Cuerpo y Tercio Medio
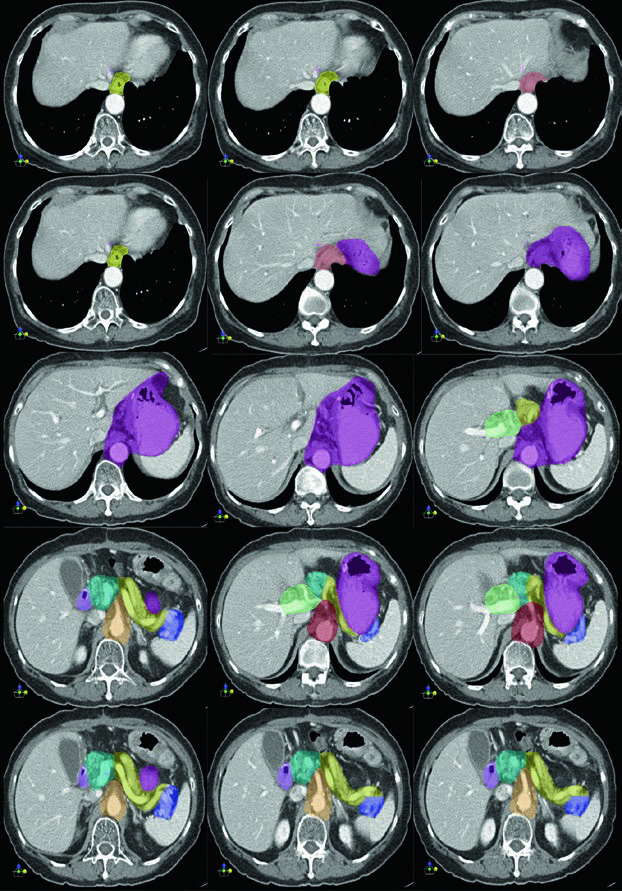
En los tumores del cuerpo gástrico, el estómago remanente siempre se incluye, preservando dos tercios de un riñón. El lecho tumoral para T2-3N0 corresponde al cuerpo del páncreas con o sin cola. Los volúmenes nodales para enfermedad T1-2N+ incluyen PG, CN, esplénico, SP, PD y PH — prácticamente todas las estaciones perigástricas y retroperitoneales relevantes.
CTV por Subsitio: Antro, Píloro y Tercio Distal
Para tumores del antro y píloro, el estómago remanente se incluye preservando dos tercios del riñón izquierdo (nota: el lado opuesto comparado con la UGE). El lecho tumoral para T2-3N0 comprende la cabeza del páncreas con o sin cuerpo, además de la primera y segunda porciones del duodeno. Los volúmenes nodales para T1-2N+ incluyen PG, CN, SP, PD y PH, con inclusión opcional del hilio esplénico.
Casos Clínicos: CTV en la Práctica
Caso 1: T1N1M0 Adenocarcinoma del Cardias — Gastrectomía Total
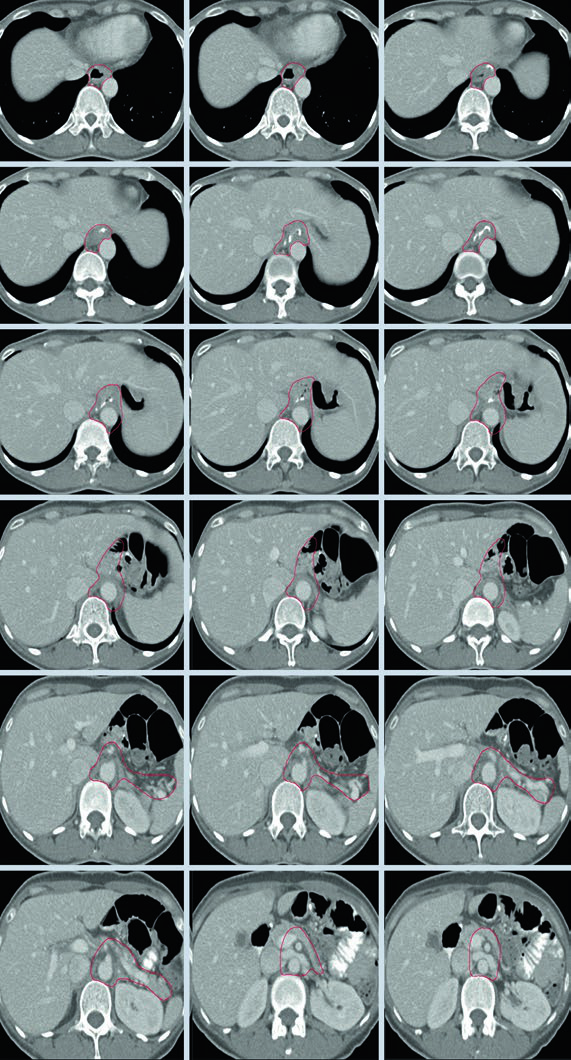
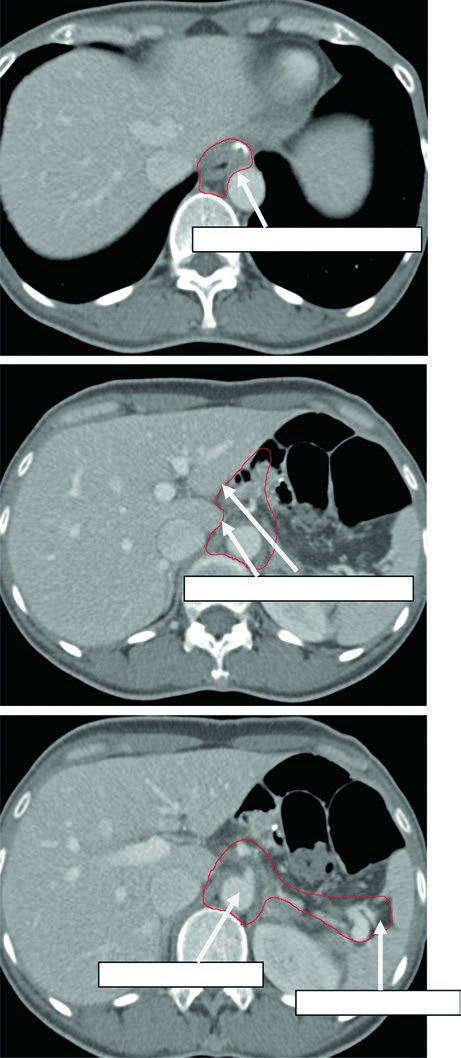
En este caso, el CTV abarca la anastomosis esofagoyeyunal, el ligamento hepatogástrico, la arteria celíaca y el hilio esplénico. Al tratarse de una gastrectomía total en un tumor del cardias con ganglio positivo, no hay remanente gástrico que incluir, pero los volúmenes nodales deben ser amplios.
Caso 2: T3N3M0 Adenocarcinoma del Cuerpo — Gastrectomía Distal
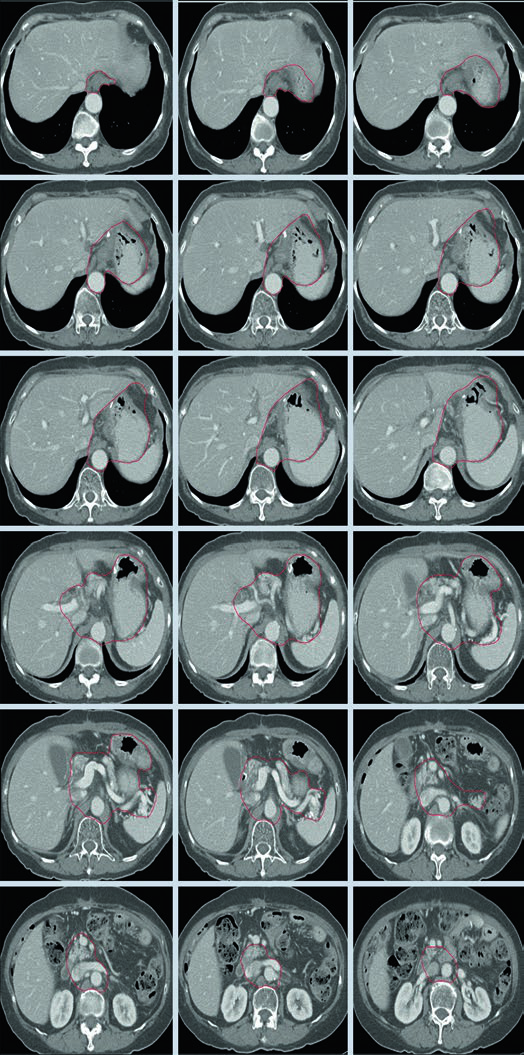
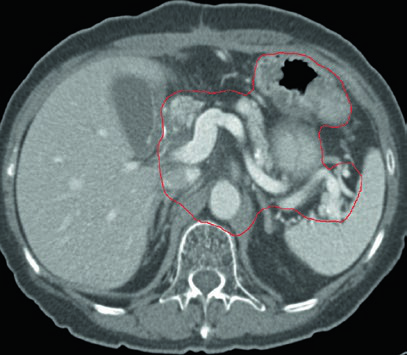
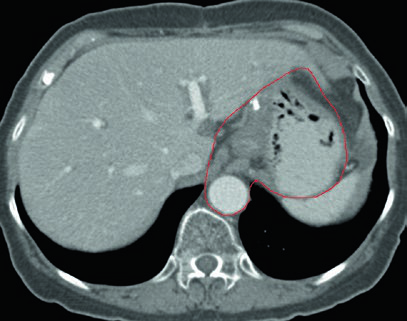
Con enfermedad T3N3, el CTV es extenso: incluye la anastomosis gastroyeyunal, el estómago remanente, la arteria celíaca, el hilio esplénico y el lecho tumoral pancreático. Este escenario exige atención especial a las restricciones de dosis en los órganos de riesgo — particularmente riñones e hígado — dado el considerable volumen de tratamiento.
Caso 3: T2N1M0 Adenocarcinoma de Antro/Píloro — Gastrectomía Distal
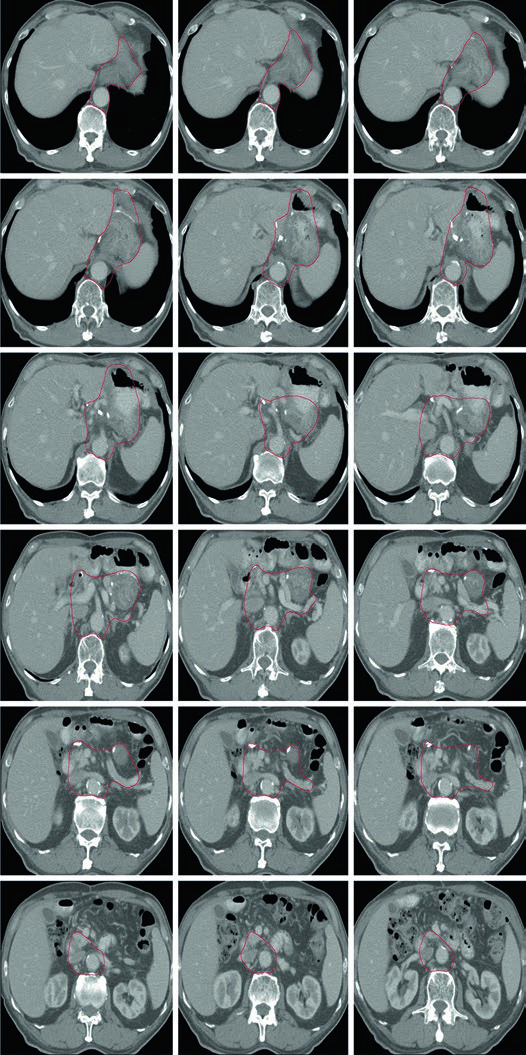
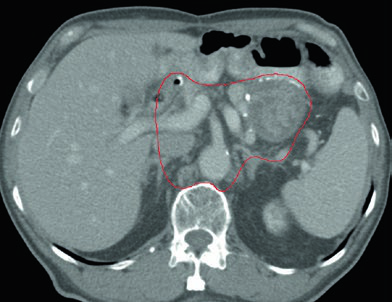
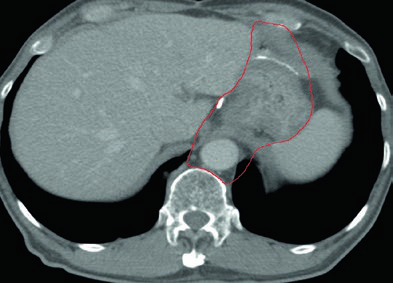
En el adenocarcinoma de antro/píloro, el CTV cubre la anastomosis gastroyeyunal, el estómago remanente, el ligamento hepatogástrico y el muñón duodenal. La cobertura del hilio esplénico es opcional en este escenario. La inclusión del muñón duodenal es preferencial en gastrectomías parciales por tumores distales/antrales, pero no debe incluirse en pacientes con tumores proximales sometidos a gastrectomía total.
Evaluación del Plan y Restricciones de Dosis
En casos avanzados, el equipo típicamente prioriza las restricciones de dosis en las estructuras normales — específicamente médula espinal, riñones e hígado — sobre la cobertura completa del tumor. Con técnica 3D conformada, el 100% del PTV45 debe recibir ≥42,75 Gy (95% de la dosis prescrita), según ICRU 62. Con IMRT, el 98% del PTV debe recibir ≥42,75 Gy, según ICRU 83.
Restricciones de Dosis para OAR en Tumores Abdominales Superiores
| Órgano de Riesgo | Restricción de Dosis | Desenlace | Tasa (%) |
|---|---|---|---|
| Médula espinal | Dmáx = 50 Gy | Mielopatía | 0,2 |
| Médula espinal | Dmáx = 60 Gy | Mielopatía | 6 |
| Médula espinal | Dmáx = 69 Gy | Mielopatía | 50 |
| Hígado completo | Dosis media 30–32 Gy | RILD clásica | <5 |
| Hígado completo | Dosis media <42 Gy | RILD clásica | <50 |
| Intestino delgado | V45 < 195 cc (cavidad peritoneal completa) | Toxicidad aguda grado ≥3 | <10 |
| Corazón | Dosis media <26 Gy (pericardio) | Pericarditis | <15 |
| Corazón | V30 < 46% (pericardio) | Mortalidad cardíaca tardía | <15 |
| Corazón | V25 < 10% (corazón completo) | Mortalidad cardíaca | <1 |
| Riñones bilaterales | Dosis media <15–18 Gy | Disfunción renal clínicamente relevante | <5 |
| Riñones bilaterales | Dosis media <28 Gy | Disfunción renal clínicamente relevante | <50 |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 15.9)
La preservación renal merece atención particular en la planificación del cáncer gástrico. Para tumores de la UGE y cardias, el plan busca preservar dos tercios del riñón derecho; para tumores del antro y píloro, se preservan dos tercios del riñón izquierdo. Esta asimetría refleja la anatomía de la extensión tumoral y del lecho quirúrgico.
Consideraciones Generales del CTV Adyuvante
La siguiente tabla resume las consideraciones generales que orientan la inclusión del muñón duodenal, la anastomosis, los ganglios paraaórticos y los ganglios paraesofágicos.
| Volumen Blanco | Definición y Descripción |
|---|---|
| Muñón duodenal | Preferentemente cubierto en gastrectomía parcial por tumores distales/antrales. No incluir en gastrectomía total por tumores proximales/cardias |
| Anastomosis | Gastroyeyunal (gastrectomía parcial para tumores distales) o esofagoyeyunal (gastrectomía total para tumores proximales/UGE) — deben ser tratadas |
| Ganglios paraaórticos | Deben incluirse en toda la extensión del CTV |
| Ganglios paraesofágicos | Margen de 4 cm del esófago incluido en el CTV para tumores de la unión gastroesofágica |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 15.3)
Los beneficios de la IMRT en la radioterapia gástrica adyuvante han sido sugeridos por múltiples publicaciones. Cuando se utiliza IMRT, tanto el lecho tumoral como los volúmenes subclínicos — incluyendo las regiones de drenaje linfático — deben delinearse individualmente. El PTV se genera expandiendo el CTV con un margen mínimo de 1 cm, considerando el movimiento de órgano y las incertidumbres de posicionamiento.
Otros artículos de esta serie abordan técnicas relevantes para planificaciones abdominales complejas — como la delineación del cáncer de esófago y la planificación del cáncer de páncreas, que comparten desafíos similares de manejo del movimiento de órgano y protección renal.




