O câncer de pulmão delineamento de volume alvo é uma das tarefas mais exigentes da radioterapia. O planejamento envolve heterogeneidade de densidade tecidual, movimento respiratório significativo, múltiplas cadeias linfonodais e cenários clínicos que vão do SBRT até a irradiação pós-operatória. Este artigo cobre cada um desses cenários com margens, doses e raciocínio clínico retirados diretamente do capítulo de Wijetunga, Liao e Gomez no Target Volume Delineation and Field Setup, 2nd Edition.
O guia completo de delineamento de volume alvo contextualiza este artigo dentro de uma série que cobre pulmão, mama, esôfago e outros sítios torácicos. Para comparação com o manejo de cadeia nodal em mama, consulte também o artigo sobre irradiação nodal regional de mama.
Qual técnica de planejamento usar no câncer de pulmão?
A resposta depende do estádio e do volume tumoral. SBRT para estádio inicial, IMRT ou 3D-CRT com quimioterapia concomitante para doença localmente avançada, e campos limitados no cenário pós-operatório. Em todos os casos, o controle do movimento respiratório não é opcional — é pré-requisito para margens racionais.
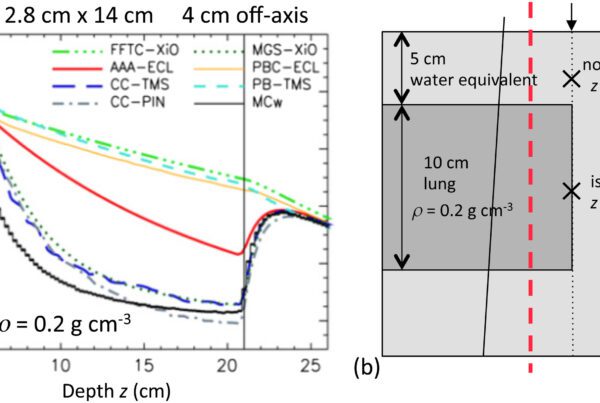
A TC com contraste é a base do planejamento. A TC 4D captura o envelope de movimento do tumor ao longo do ciclo respiratório e gera o GTV interno (iGTV) ou o volume interno de tumor (ITV), dependendo da abordagem escolhida. PET-CT acrescenta informação metabólica crítica para diferenciar colapso pós-obstrutivo de tumor viável — situação frequente no pulmão. Mediastinoscopia e EBUS completam o estadiamento dos linfonodos quando a imagem é equívoca.
O planejamento baseado em TC exige contorno cuidadoso das estruturas de risco: pulmões (ipsilateral e contralateral), coração, medula espinhal, esôfago, parede torácica, grandes vasos, plexo braquial (especialmente em tumores do sulco superior) e a árvore brônquica proximal (PBT). As restrições de dose para esses órgãos seguem a publicação QUANTEC (Marks et al., 2010).
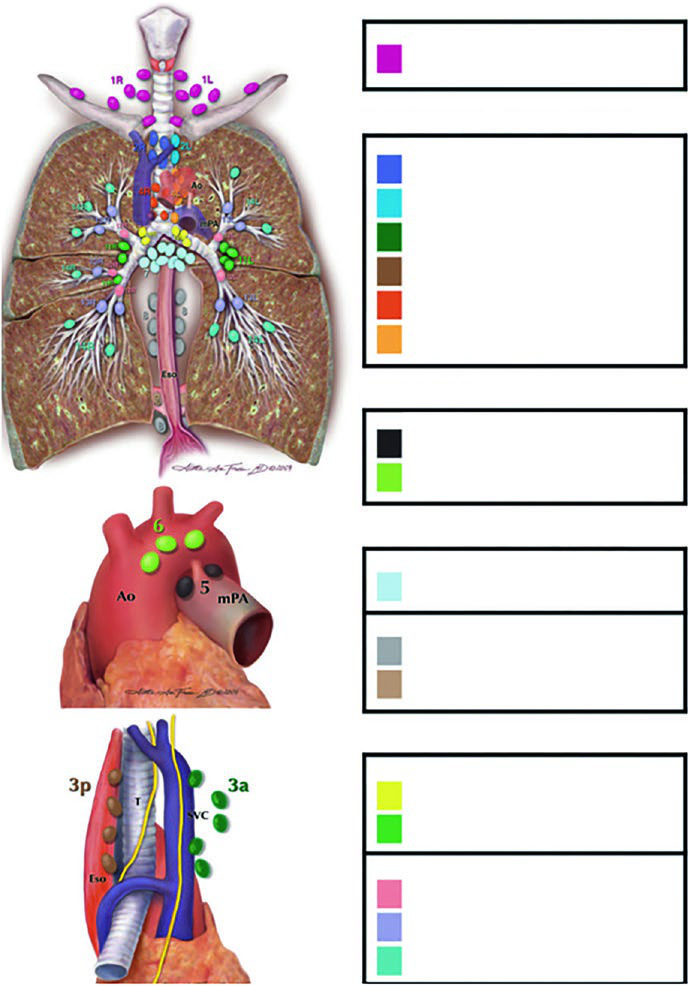
Estações linfonodais: atlas de Michigan como referência
Todo planificador que trabalha com pulmão precisa dominar o atlas linfonodal de Michigan. Sem esse mapa mental, as decisões sobre campo envolvido versus eletivo se tornam arbitrárias.
As estações são organizadas em zonas anatômicas:
- Supraclavicular: Estação 1
- Mediastino superior: 2R, 2L, 3a, 3p, 4R, 4L
- Aórtica: 5, 6
- Mediastino inferior: 7, 8, 9
- N1 (intrapulmonares): 10, 11, 12, 13, 14
A tabela abaixo, baseada nos dados da Figura 13.1b do capítulo, mostra o risco de acometimento por estação conforme a localização do tumor primário. Esses percentuais orientam a decisão de incluir ou excluir regiões eletivas do campo.
Risco de acometimento linfonodal por lobo tumoral
| Estação | LSD (%) | LMD (%) | LID (%) | LSE (%) | LIE (%) |
|---|---|---|---|---|---|
| 1 (Supraclavicular) | 11 | 4 | 3 | 17 | 3 |
| 2R | 31 | 26 | 12 | 5 | 3 |
| 2L | 3 | 0 | 2 | 21 | 7 |
| 3a | 4 | 7 | 5 | 3 | 3 |
| 4R | 64 | 59 | 26 | 8 | 4 |
| 4L | 6 | 4 | 5 | 56 | 18 |
| 5 | 4 | 0 | 2 | 71 | 22 |
| 6 | 2 | 0 | 2 | 32 | 8 |
| 7 (Subcarinal) | 20 | 48 | 35 | 19 | 33 |
| 8 | 2 | 11 | 15 | 5 | 50 |
| 9 | 2 | 4 | 5 | 2 | 17 |
| 10 (Hilar ipsilateral) | 59 | 63 | 49 | 56 | 46 |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition. LSD=lobo superior direito, LMD=lobo médio direito, LID=lobo inferior direito, LSE=lobo superior esquerdo, LIE=lobo inferior esquerdo.
Abordagem de campo envolvido: por que não irradiar eletivamente?
A irradiação nodal eletiva foi abandonada como rotina porque os estudos mostraram taxa baixa de falha nodal eletiva e toxicidade esofagiana e pulmonar inaceitável quando campos grandes eram usados para cobrir todo o mediastino. O ensaio randomizado que comparou campo envolvido versus campo eletivo demonstrou melhora de desfechos com o campo envolvido — dado consistente com a biologia: a irradiação de nodos clinicamente negativos agrega dose sem benefício comprovado.
A lógica da abordagem de campo envolvido é simples: irradiar o que se vê na imagem. GTV inclui tumor primário e linfonodos PET-positivos ou com critério de tamanho por TC. As regiões eletivas ficam de fora, salvo situações específicas como CPPC de estádio limitado com doença hilar.
Expansões GTV → PTV: duas abordagens práticas
O texto descreve duas abordagens para incorporar o movimento respiratório nas expansões:
Abordagem 1 — iGTV como base: GTV → iGTV (envelope de movimento da TC 4D) → iCTV (expansão isotrópica sobre o iGTV) → PTV (margem de setup). Esta abordagem é mais comum no SBRT, onde o controle preciso do iGTV é crítico para respeitar a NFZ peribrônquica.
Abordagem 2 — CTV convencional com ITV: GTV → CTV (expansão microscópica) → ITV (CTV movido pelo envelope da TC 4D) → PTV. Esta abordagem é preferida no cenário pós-operatório, onde não há GTV grosseiro, e no CPNPC localmente avançado tratado com IGRT sistemático.
Simulação: posicionamento e aquisição antes do contorno
O posicionamento reprodutível é pré-condição para margens racionais. Braços acima da cabeça reduz a dose no plexo braquial em tumores superiores e retira os braços dos feixes. Um dispositivo de imobilização — molde personalizado ou tábua com apoios — deve ser utilizado de forma consistente ao longo de todo o tratamento.
A TC 4D exige treino de respiração regular e adequado. Respiração irregular durante a TC 4D gera artefatos na reconstrução de fase que se traduzem diretamente em definição imprecisa do iGTV. Se o treino não estiver disponível, a TC lenta (tempo de rotação prolongado captando o movimento médio) é uma alternativa razoável para casos não-SBRT.
A TC com contraste na sessão de simulação é preferível para o contorno mediastinal: esclarece os limites vasculares nas estações 4R, 4L, 5 e 6, onde distinguir linfonodos de estruturas vasculares adjacentes pode ser genuinamente difícil na imagem sem contraste. A fusão com PET afina ainda mais a definição do GTV quando há atelectasia: o pulmão colapsado deve ser excluído do GTV salvo captação PET dentro do colapso.
SBRT no CPNPC estádio inicial: precisão máxima
SBRT é o tratamento de escolha para CPNPC estádio I em pacientes inoperáveis e cresce como alternativa em operáveis de alto risco. O objetivo é BED > 100 Gy no tumor, com dose mínima possível nos tecidos normais circundantes.
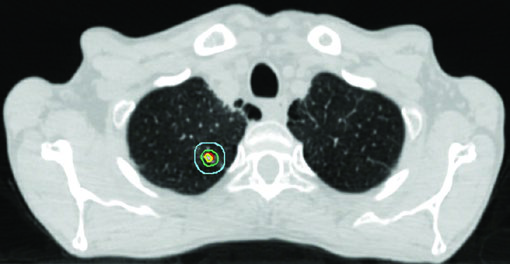
A expansão iGTV → iCTV no estádio inicial é pequena: 0 a 0,2 cm. O raciocínio é que, no tumor pequeno e periférico, a extensão microscópica é mínima e a margem de setup domina a expansão final. A margem PTV adicional depende da tecnologia de IGRT disponível.
A árvore brônquica proximal (PBT) — definida como os 2 cm distais da traqueia, carina, brônquios principais, brônquios lobares e os primeiros segmentos dos brônquios segmentares — é a estrutura mais crítica no SBRT. Define-se uma zona de não irradiação (NFZ) de 2 cm além da PBT. Tumores dentro ou adjacentes à NFZ são considerados centrais e demandam fracionamento menos ablativo.
Os esquemas de dose variam por localização:
- Periférico: 54 Gy/3fx (18 Gy/fx), 48 Gy/4fx (12 Gy/fx), 50 Gy/4fx ou 50 Gy/5fx
- Central: 50 Gy/5fx, 70 Gy/10fx ou 60 Gy/8fx
A dose máxima em ponto da PBT é restrita a 55 Gy em qualquer esquema. A Figura 13.2 do texto mostra três casos de estádio inicial: tumor periférico clássico tratado com 54 Gy/3fx, tumor próximo à PBT com 48 Gy/4fx e tumor central com 50 Gy/5fx.
CPNPC localmente avançado (estádios II-III): controle nodal e integração com quimioterapia
No estádio localmente avançado, a expansão iGTV → iCTV aumenta para 0,5 a 0,8 cm, reflexo dos dados histológicos que mostram extensão microscópica significativa no CPNPC. A margem PTV depende do nível de controle de movimento e IGRT implementado:
- 1,0–1,5 cm sem controle de movimento/IGRT
- 0,5–1,0 cm com TC 4D ou CBCT, mas não ambos
- 0,3–0,5 cm com TC 4D + kV/CBCT (abordagem preferida)
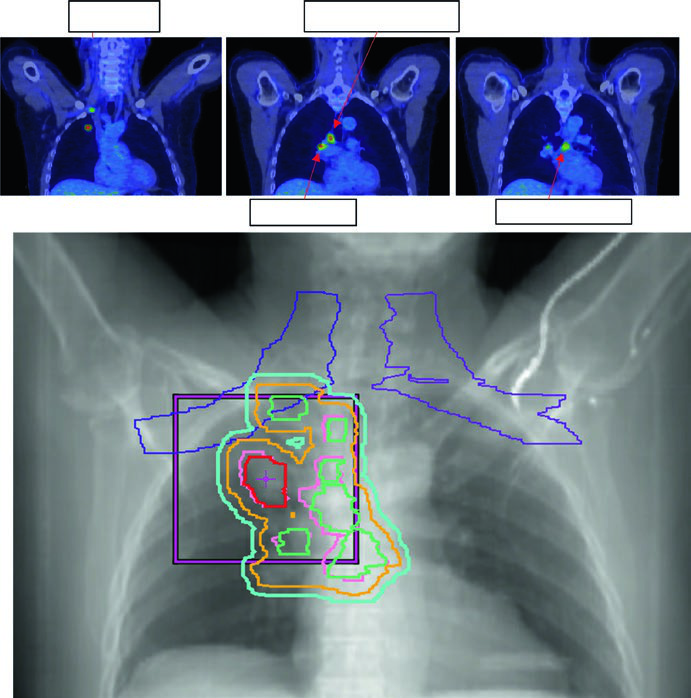
A dose padrão para CPNPC estádio II-III com quimioterapia concomitante é 60 Gy em 30 frações (2 Gy/fx). Doses de escalada acima de 60 Gy não demonstraram benefício em ensaios randomizados e aumentaram toxicidade. O GTV inclui tumor primário e linfonodos acometidos visíveis em TC ou PET.
A Figura 13.3 do texto ilustra um caso cT1cN3M0 IIIB: tumor no LSD com linfonodo hilar direito, subcarinal, paratraqueal e SCV direita acometidos. O plano de 60 Gy/30fx cobre todos os sítios PET-positivos com exclusão das cadeias eletivas contralaterais. A Figura 13.4 mostra um caso cT4N3M0 IIIC com SCV bilateral comprometida e síndrome de veia cava superior, exigindo campo que inclui mediastino superior bilateral.
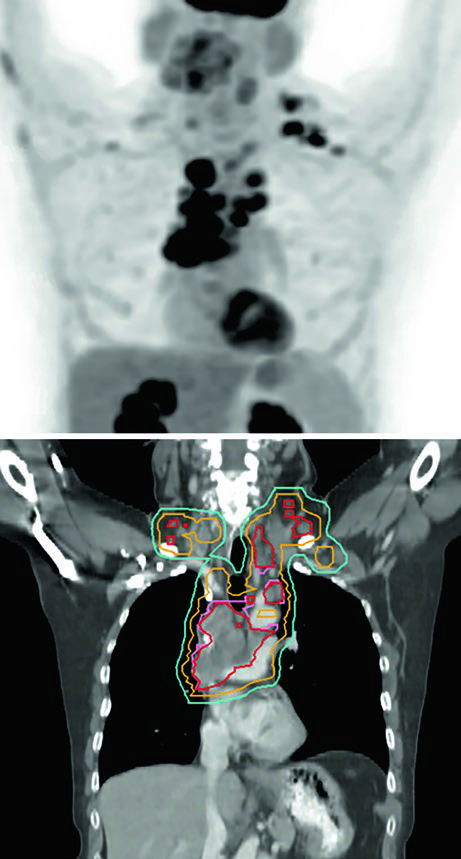
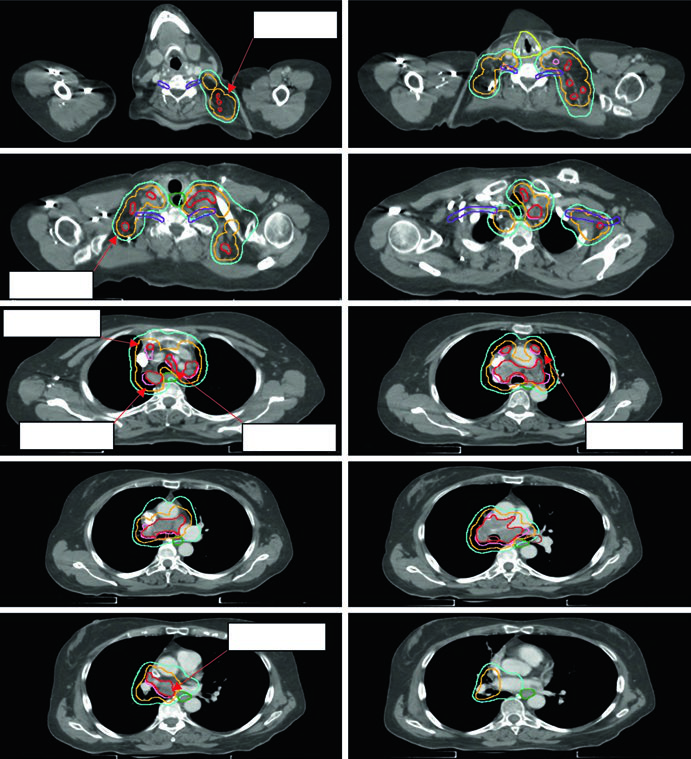
CPNPC pós-operatório: campo limitado é o novo padrão
A radioterapia pós-operatória no CPNPC é uma área de evolução rápida. A abordagem histórica irradiava campos extensos — leito tumoral, linfonodos comprometidos, mediastino bilateral, coto ipsilateral e SCV — com toxicidade pulmonar e cardíaca relevante. O ensaio Lung ART reformulou esse paradigma.
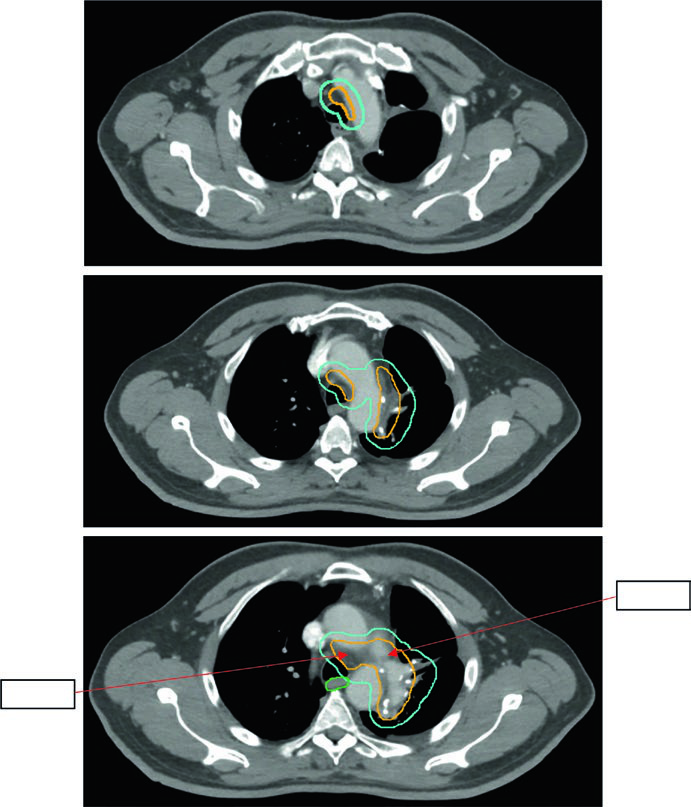
A abordagem atual é limitada: regiões linfonodais comprometidas comprovadas mais o coto brônquico ipsilateral, com a opção de incluir um nível acima e abaixo dos níveis positivos. Não há GTV — o delineamento começa no CTV. A expansão CTV → ITV (movimento respiratório) → PTV (~0,5 cm de margem de setup) é a sequência padrão.
As doses são estratificadas pela margem cirúrgica:
- R0 (margens livres): 50–54 Gy em 1,8–2,0 Gy/fx
- R1 (margem microscópica positiva): 54–60 Gy em 1,8–2,0 Gy/fx
- R2 (doença macroscópica residual): 60 Gy com quimioterapia concomitante
A Figura 13.5 do capítulo mostra um tumor de 5,8 cm no LSE com positividade nos níveis 5 e 10L. O campo limitado conforme Lung ART é o utilizado, com 54 Gy/30fx.
CPPC: irradiação de campo envolvido em doença limitada e extensiva
O carcinoma de pequenas células apresenta radiorresistência relativa e crescimento rápido, mas é sensível à irradiação combinada à quimioterapia. A abordagem de campo envolvido é aceita em ambos os estádios.
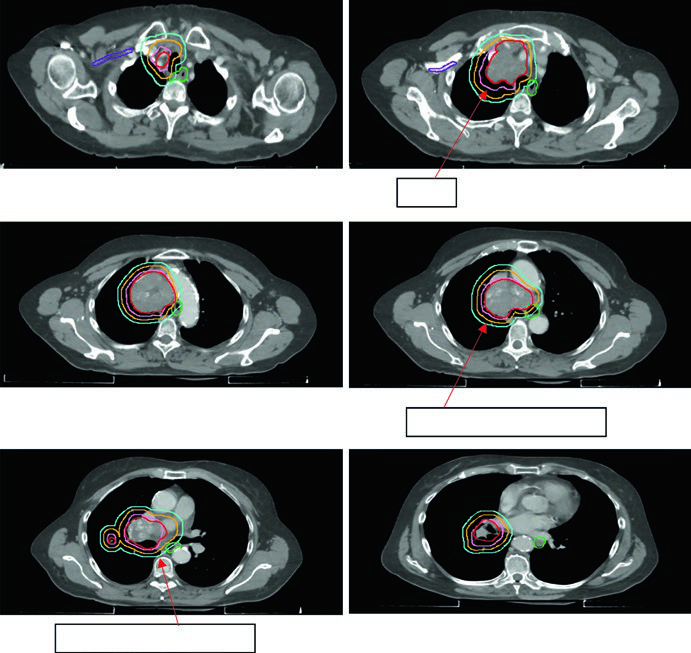
A expansão GTV → CTV no CPPC é de 0,5 a 1,0 cm, frequentemente incluindo o hilo ipsilateral mesmo sem captação PET demonstrada, dado o padrão de drenagem linfática. As margens CTV → PTV seguem as mesmas diretrizes do CPNPC, calibradas pelo sistema de IGRT disponível.
Os esquemas de dose diferem por estádio:
- Estádio limitado: 45 Gy em 1,5 Gy duas vezes ao dia (30 frações) — o esquema clássico de Turrisi — ou 66–70 Gy em 2,0 Gy diário como alternativa de dose mais alta
- Estádio extensivo (consolidação): 30–45 Gy em 3,0 Gy/fx no sítio de doença volumosa
A Figura 13.6 mostra um caso cT2N2 de estádio limitado com o campo envolvido cobrindo tumor primário e linfonodos mediastinais comprometidos, mas excluindo cadeias eletivas. O esquema utilizado foi 45 Gy/30fx BID.
Replanejamento adaptativo: quando a anatomia muda durante o tratamento
Tumores obstrutivos que causam atelectasia podem resolver parcialmente durante o tratamento à medida que a radioterapia reduz o volume tumoral e o pulmão reaeração. Esse fenômeno, documentado nas CBCT de verificação, pode expor tecido pulmonar previamente colapsado à dose prevista para o tumor, alterando dramaticamente a distribuição de dose.
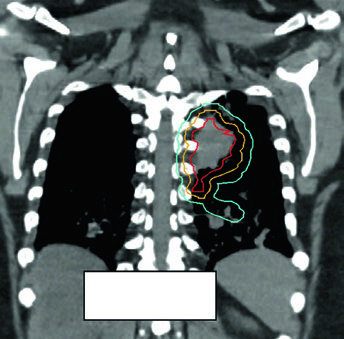
O replanejamento adaptativo deve ser considerado quando a CBCT mostra mudança anatômica significativa — expansão pulmonar ipsilateral, redução de derrame ou colapso em resolução. O caso da Figura 13.7 ilustra uma lesão metastática tratada com 45 Gy/15fx: a reaer ação pulmonar durante o tratamento exigiu replanejamento para proteger o pulmão recém-arejado.
Não existe protocolo universal para o gatilho do replanejamento adaptativo. Na prática, CBCT semanal com revisão pelo planificador e pelo oncologista é o mínimo razoável. Qualquer mudança visual significativa no contorno pulmonar ou mediastinal justifica recalcular os DVHs antes de continuar.
Delineamento do iCTV e cobertura de dose
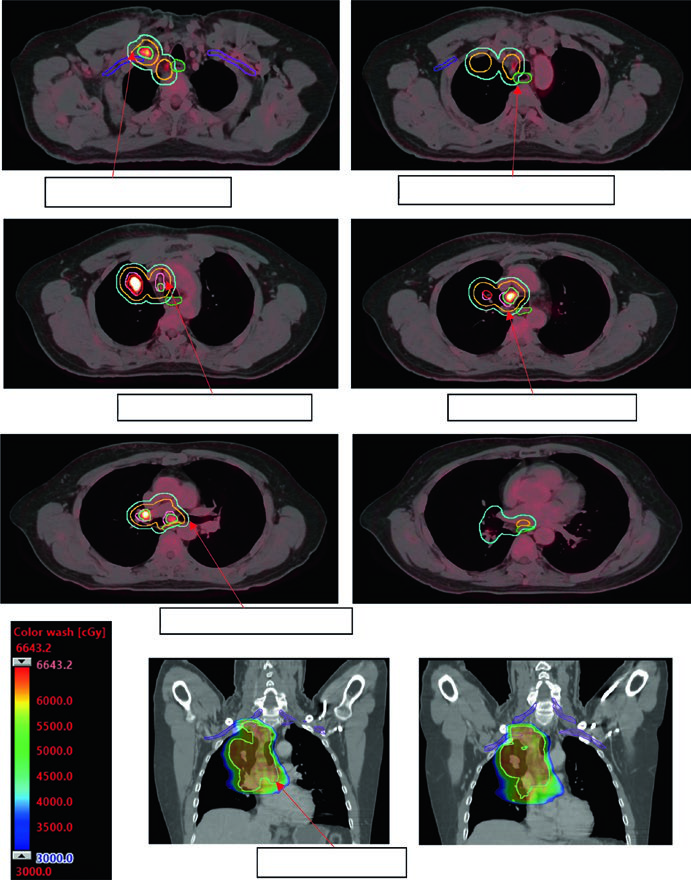
O iCTV é editado a partir do iGTV com atenção às barreiras anatômicas: pleura, parede torácica, mediastino e grandes vasos limitam a extensão microscópica e permitem retrair a margem nessas direções. Essa edição reduz o volume irradiado sem comprometer o controle tumoral — desde que a reconstrução de fase média da TC 4D seja feita com rigor.
A cobertura de dose adequada no iCTV e PTV é verificada pelos DVHs: V95 ≥ 95% do PTV, Dmin ≥ 90% da dose prescrita. Em SBRT, a conformidade é avaliada pelo índice PITV (razão volume de isodose prescrita / volume PTV) e pelo índice de gradiente de dose (GI). Uma curva de isodose que abrace o PTV com queda rápida para os tecidos normais circundantes é o objetivo.
Tabela de regimes de dose — Resumo prático
| Cenário | Dose Total | Fracionamento | Observações |
|---|---|---|---|
| CPNPC estádio I SBRT periférico | 54 Gy / 48 Gy / 50 Gy / 50 Gy | 3 fx / 4 fx / 4 fx / 5 fx | BED >100 Gy; máx PBT 55 Gy |
| CPNPC estádio I SBRT central | 50 Gy / 70 Gy / 60 Gy | 5 fx / 10 fx / 8 fx | Dentro ou adjacente à NFZ |
| CPNPC estádio II-III | 60 Gy | 30 fx (2 Gy/fx) | Com quimioterapia concomitante |
| Pós-operatório R0 | 50–54 Gy | 1,8–2,0 Gy/fx | Margem cirúrgica livre |
| Pós-operatório R1 | 54–60 Gy | 1,8–2,0 Gy/fx | Margem microscópica positiva |
| Pós-operatório R2 | 60 Gy | 2,0 Gy/fx | Com quimioterapia concomitante |
| CPPC estádio limitado | 45 Gy ou 66–70 Gy | 1,5 Gy BID (30 fx) ou 2,0 Gy diário | Campo envolvido |
| CPPC estádio extensivo (consolidação) | 30–45 Gy | 3,0 Gy/fx | Doença volumosa residual |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition — Capítulo 13 (Wijetunga, Liao, Gomez).
Restrições de OAR e avaliação do plano de tratamento
As restrições de dose nos OARs pulmonares não são parâmetros de referência — ultrapassá-las resulta em eventos clínicos documentados. Coração, pulmões, esôfago e medula espinhal são as quatro estruturas que mais frequentemente limitam a qualidade do plano.
Para os pulmões, os parâmetros mais usados são a dose média pulmonar (DMP) e o V20 (volume recebendo 20 Gy ou mais). DMP abaixo de 20 Gy e V20 abaixo de 35% são os limiares convencionais para tratamento com fracionamento convencional. No SBRT, o V20 perde relevância; o V12,5 Gy e a dose média do pulmão contralateral passam a ser os parâmetros-chave. O pulmão ipsilateral recebe dose elevada por design no SBRT lobar — o trabalho de restrição foca no pulmão contralateral e no pulmão global menos o volume do GTV.
A toxicidade esofagiana é o OAR mais limitante no CPNPC localmente avançado com quimioterapia concomitante. O QUANTEC recomenda dose média esofagiana abaixo de 34 Gy, com V50 < 40% e V60 < 30%. Na prática, a cobertura de linfonodos mediastinais frequentemente empurra o esôfago além desses limites; quando isso ocorre, uma discussão franca sobre risco de toxicidade versus benefício de controle local é necessária.
As restrições cardíacas incluem V30 pericárdico e dose média cardíaca. Tumores volumosos do lobo inferior esquerdo irradiados com quimioterapia concomitante produzem frequentemente doses médias cardíacas acima de 20 Gy; há evidência crescente associando isso a eventos cardíacos tardios. A otimização de arcos IMRT para poupar a base cardíaca é recomendada quando tecnicamente viável.
Integração clínica e decisão no dia a dia
O pulmão concentra praticamente todos os desafios do planejamento em radioterapia: heterogeneidade de tecido, movimento, múltiplas cadeias nodais, proximidade a estruturas críticas e cenários que vão do ablativo ao paliativo. O profissional que domina esses princípios consegue adaptar o protocolo ao paciente real — não ao caso ideal do ensaio clínico.
Para quem trabalha com câncer torácico de forma mais ampla, o artigo sobre câncer de esôfago: campos e delineamento traz princípios complementares para o mediastino inferior e junção gastroesofágica. O guia completo de delineamento oferece o contexto sistemático para todos os sítios. Para mama com comprometimento nodal, o artigo sobre irradiação nodal regional é o complemento natural para entender as estações supraclaviculares e mamárias internas que se sobrepõem anatomicamente ao mediastino superior.