No câncer de pulmão, o contorno só começa a fazer sentido quando três problemas são colocados na mesma mesa: movimento respiratório, mediastino e definição coerente entre GTV, ITV e PTV. Se uma dessas peças entra errada, o restante do plano apenas formaliza o erro com mais sofisticação.
É por isso que o tema perde qualidade quando vira lista automática de siglas e cenários clínicos. O valor do artigo está em organizar esses elementos como uma lógica única.
Movimento respiratório muda o plano de verdade
O texto acerta ao insistir em iGTV, iCTV, ITV e PTV como conceitos operacionais e não apenas teóricos. Em pulmão, o movimento respiratório não é detalhe de refinamento; ele altera diretamente o que será tratado e como a dose será distribuída.
Quando o artigo explica isso com clareza, ele se afasta muito do tom de conteúdo automatizado.
Mediastino e estações linfonodais seguem centrais
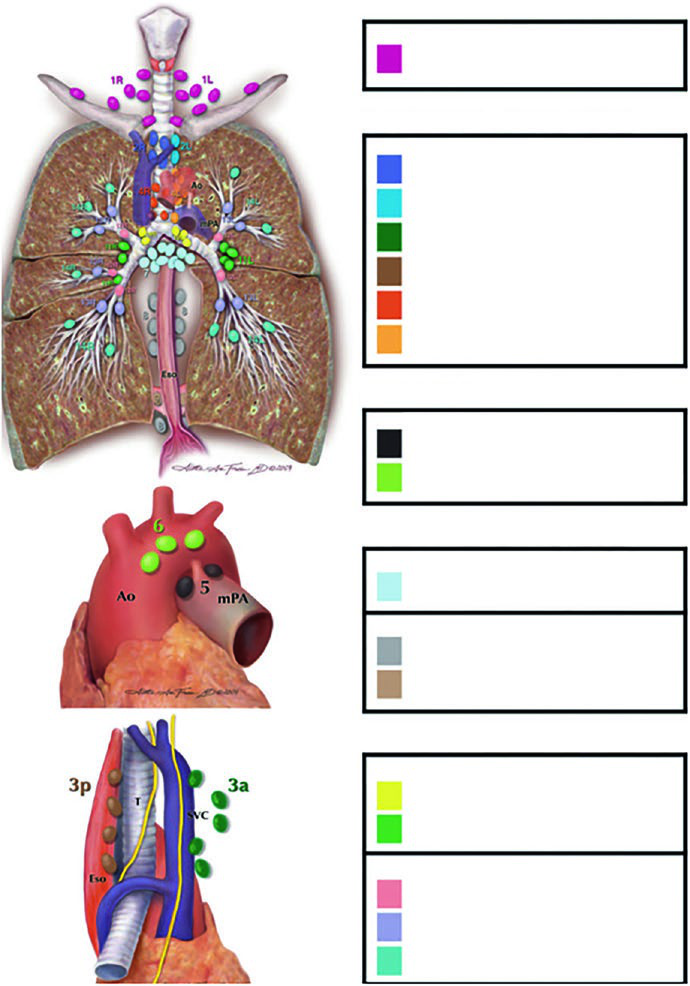
Outro ponto forte é a atenção às estações linfonodais e ao risco mediastinal conforme a localização tumoral. Em NSCLC e SCLC, a leitura dessas cadeias faz diferença real no volume, no estadiamento e no raciocínio de dose. Não é um item acessório do capítulo.
É também aqui que a integração entre CT, PET e estadiamento invasivo ganha valor prático.
SBRT, pós-operatório e consolidação pedem contextos distintos
O artigo percorre desde NSCLC inicial com SBRT até doença localmente avançada, pós-operatório e SCLC com radioterapia torácica de consolidação. Essa amplitude só funciona quando o texto deixa claro que cada cenário responde a uma pergunta clínica diferente. Do contrário, tudo parece um empilhamento artificial de subtópicos.
Ao reescrever com mais contexto, o conteúdo fica muito mais humano.
Como a RT Medical Systems enxerga isso
- Em pulmão, manejo do movimento respiratório é parte central do contorno e não mero refinamento.
- Mediastino e estações linfonodais continuam determinantes para volume e estratégia.
- SBRT, pós-operatório e consolidação torácica precisam ser apresentados como cenários clínicos distintos.
O que muda na prática
- Definição entre GTV, ITV e PTV deve ser explicitamente amarrada ao movimento.
- PET, EBUS e estadiamento mediastinal precisam entrar cedo no planejamento.
- Cada cenário clínico deve puxar dose e margens coerentes com sua intenção terapêutica.
Reescrever esse artigo em tom mais humano ajuda a tirar o tema da aparência de manual gerado e devolvê-lo ao seu problema real: precisão em um alvo móvel, cercado por estruturas críticas e mediado por risco nodal. Quando isso aparece no texto, a confiança do leitor sobe imediatamente.
Para discutir movimento respiratório, mediastino e planejamento em câncer de pulmão, fale com nossos especialistas.
Transparência editorial
Revisão editorial: Equipe RT Medical Systems
Fonte editorial: capítulo clínico do artigo original e Target Volume Delineation and Field Setup
Atualizado em: 26/03/2026
- Reescrita integral com foco em movimento, mediastino e definição de volumes.
- Redução do tom automático e da enumeração excessiva de cenários.
- Ênfase em contexto clínico para NSCLC, SBRT e SCLC.