Neste Artigo
Princípios Gerais de Planejamento e Simulação
O planejamento radioterápico do câncer de esôfago exige domínio da anatomia cervical, mediastinal e abdominal, além de técnicas confiáveis de compensação de movimento. Tanto a IMRT quanto a 3D-CRT conformacional demandam delineamento preciso dos volumes-alvo, estruturas normais e órgãos de risco (OARs), com avaliação rigorosa dos histogramas dose-volume durante o planejamento.
Na simulação, o paciente idealmente posiciona os braços acima da cabeça para maximizar as possibilidades de arranjos de feixes sem atravessar os membros superiores. Para tumores distais ou da junção gastroesofágica (JGE), medidas de compensação de movimento respiratório são fundamentais: TC 4D, gating respiratório ou técnicas de breath-hold. Um detalhe que faz diferença na prática: o paciente deve permanecer em jejum (NPO) por pelo menos 2 a 3 horas antes da simulação e de cada sessão de tratamento. Isso limita a variação diária da anatomia causada por gás gástrico e intestinal.
Para planejamentos com IMRT, contraste intravenoso no momento da simulação ajuda a delinear melhor os campos nodais. A TC de planejamento com contraste melhora a distinção entre linfonodos e estruturas vasculares adjacentes — algo particularmente relevante no mediastino.
Para uma visão completa sobre delineamento de volumes-alvo em diversas localizações anatômicas, confira nosso artigo dedicado ao câncer gástrico, que compartilha vários princípios de planejamento abdominal com o esôfago distal.
Subdivisões Anatômicas do Esôfago
O esôfago começa no pescoço, na borda inferior da cartilagem cricoide (anterior à sexta vértebra cervical), e desce pelo mediastino, atravessando o diafragma até o abdome. Usando a distância padrão de 40 cm dos incisivos até a JGE, as subdivisões ficam assim:
- Esôfago cervical: dos incisivos até aproximadamente 15–20 cm
- Esôfago torácico superior (proximal): de 18–20 cm até 25 cm
- Esôfago torácico inferior (médio/distal): de 25 cm até 30–32 cm
- Esôfago abdominal: de 30–32 cm até 40 cm
Essa subdivisão anatômica orienta diretamente o contorno do CTV e a escolha das estações nodais eletivas. Tumores que abrangem múltiplas subdivisões devem seguir as diretrizes de todos os subconjuntos envolvidos.
Independentemente da localização tumoral, os pulmões inteiros devem ser contornados para análise adequada do DVH. Em neoplasias do esôfago superior, o plexo braquial e a laringe precisam ser delineados. Já em tumores do esôfago inferior, coração, fígado, rins, estômago e alças intestinais adjacentes devem ser incluídos como OARs.
Delineamento do GTV, CTV e PTV
As seguintes estruturas-alvo devem ser delineadas: GTV (volume tumoral macroscópico), CTV (volume-alvo clínico) e PTV (volume-alvo de planejamento). A definição de um ITV — volume que engloba o movimento interno do GTV observado na TC 4D — é rotina institucional. O ITV é expandido para CTV e depois para PTV.
O GTV deve ser delineado com referência à TC, ao PET e aos achados da endoscopia digestiva alta e do ultrassom endoscópico (EUS). O EUS é particularmente valioso para estadiar a profundidade de invasão tumoral e classificar linfonodos periesofágicos pequenos — difíceis de avaliar apenas por TC ou PET. Se o tumor for superior à carina, uma broncoscopia é recomendada para afastar fístula traqueoesofágica, que pode postergar a radioterapia.
As expansões padrão de ITV para CTV são 1 cm radialmente (para englobar linfonodos periesofágicos) e 3–4 cm na direção craniocaudal (orientada ao longo da mucosa esofágica), considerando a disseminação submucosa e a possibilidade de lesões skip. A expansão para CTV pode ser reduzida a 0,5 cm em áreas de sobreposição com o coração e fígado não envolvido, desde que haja manejo de movimento adequado.
Para tumores distais e de JGE, uma margem caudal de 4 cm incluiria grandes volumes de estômago ou vísceras abdominais. A recomendação é de apenas 2 cm de margem para CTV ao longo da mucosa gástrica clinicamente não envolvida — exceto em doses com intenção pré-operatória (≤4500 cGy), onde 4 cm ou mais de margem gástrica podem ser apropriados, especialmente em tumores com extensão gástrica significativa.
Corpos vertebrais não envolvidos e rins são excluídos do CTV. Para linfonodos envolvidos, uma margem de GTV para CTV de 0,5–1,0 cm é utilizada. Se houver linfonodos periesofágicos grosseiramente envolvidos, o CTV deve cobrir pelo menos 1 cm cranialmente aos nodos envolvidos. A expansão de CTV para PTV recomendada é de 0,5 cm.
Cobertura Nodal por Localização Tumoral
A inclusão de linfonodos regionais no CTV depende da localização do tumor primário no esôfago. Na prática, esse é o ponto onde muitos planejamentos falham — seja por cobertura excessiva gerando toxicidade, seja por cobertura insuficiente comprometendo o controle regional.
Esôfago cervical e torácico proximal: inclui-se as estações nodais supraclaviculares bilaterais. O limite cranial é a borda inferior da cartilagem cricoide; as bordas anterior, posterior e lateral são definidas pelo músculo esternocleidomastóideo. Para tumores torácicos proximais, linfonodos mediastinais são incluídos além dos periesofágicos — englobando a traqueia inteira, níveis 2 e 4, com extensão em direção ao esterno e cabeças claviculares para cobrir o nível 3.
Esôfago torácico distal: o CTV deve incluir os linfonodos celíacos, limitados à direita pela face lateral de T12, à esquerda por 0,5–1 cm além da face lateral da aorta, posteriormente pelos corpos vertebrais e anteriormente pelo pâncreas. Não é necessário incluir as estações nodais mediastinais superiores eletivamente, exceto pela sobreposição com as expansões craniais.
Tumores de JGE: o CTV deve incluir linfonodos para-aórticos e do ligamento gastro-hepático, delimitados pelo fígado à direita e pelo estômago à esquerda. Para tumores que também demandam planejamento abdominal, consulte nosso artigo sobre câncer de pâncreas, que discute anatomia do eixo celíaco e manejo de movimento em detalhe.
Classificação de Siewert–Stein para Tumores de JGE
Quando tumores de JGE sobrepõem significativamente a cárdia gástrica, a origem — esofágica ou gástrica — torna-se ambígua. A classificação de Siewert–Stein resolve essa questão definindo os tumores de JGE pelo epicentro em relação à junção:
- Tipo I: epicentro 1–5 cm acima da junção
- Tipo II: epicentro de 1 cm proximal a 2 cm distal à junção
- Tipo III: epicentro 2–5 cm abaixo da junção
O ponto de corte razoável para câncer de esôfago é o tipo II de Siewert. A oitava edição do estadiamento AJCC define tumores esofágicos como aqueles cujo epicentro se estende no máximo 2 cm para dentro da cárdia gástrica. Para tumores Siewert tipo II, parte ou todo o hilo esplênico e a região nodal da grande curvatura podem ser incluídos no CTV.
Com base nas diretrizes vigentes para cânceres gástricos, laparoscopia diagnóstica, colocação de jejunostomia, quimiorradioterapia pré-operatória ou pós-operatória podem ser consideradas. Para mais detalhes sobre planejamento gástrico, veja nosso artigo dedicado ao câncer gástrico.
Tabela de Recomendações por Subdivisão Esofágica
A tabela a seguir resume as margens, cobertura nodal eletiva e doses recomendadas para cada subdivisão anatômica do esôfago. Esses dados são a espinha dorsal do planejamento — vale mantê-los acessíveis durante o contorno.
| Subdivisão | Definição | Margem ITV→CTV | Margem CTV→PTV | Cobertura Nodal Eletiva | Dose |
|---|---|---|---|---|---|
| Cervical | Incisivos até ~15–20 cm | 3 cm sup/inf (mucosa), 1 cm radial | 0,5 cm | Periesofágicos, supraclaviculares, ± mediastinais anteriores | 50,4 Gy em 1,8 Gy/fr, com boost a 60–70 Gy para CEC |
| Torácico superior | 18–20 cm até ~25 cm | 3 cm sup/inf (mucosa), 1 cm radial | 0,5 cm | Periesofágicos, supraclaviculares, ± mediastinais anteriores | 50,4 Gy em 1,8 Gy/fr |
| Torácico inferior | 25 cm até ~37 cm | 3 cm sup/inf (mucosa), 1 cm radial | 0,5 cm | Periesofágicos | 50,4 Gy (definitivo); 41,4–50,4 Gy (pré-operatório) |
| Abdominal (JGE) | ~37 até 42 cm | 3 cm sup (mucosa esof.) + 1–2 cm inf (mucosa gástrica); ≥4 cm gástrica se pré-op ≤4500 cGy | 0,5 cm | Periesofágicos, lig. gastro-hepático (paracárdicos + gástricos esquerdos), eixo celíaco, ± hilo esplênico | 50,4 Gy (definitivo); 41,4–50,4 Gy (pré-operatório) |
Fonte: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 14.1)
Casos Clínicos Ilustrados
Os casos a seguir, extraídos diretamente do livro-texto, ilustram a aplicação prática dessas diretrizes em cenários reais. Cada caso demonstra como integrar PET, endoscopia e EUS no contorno dos volumes.
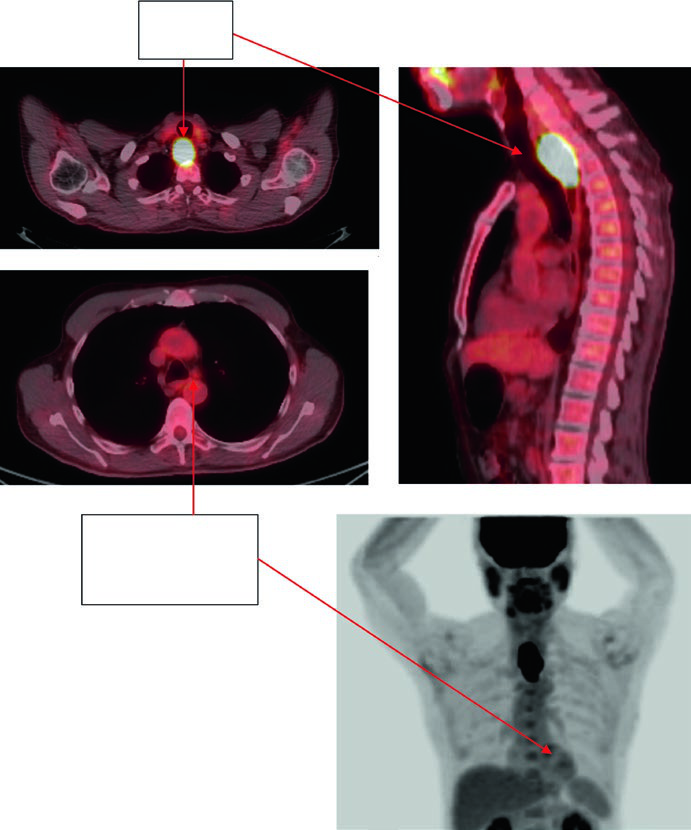
Caso 1: CEC Cervical/Torácico Superior — 69 anos
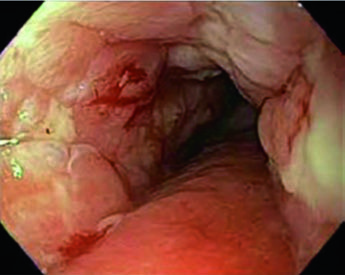
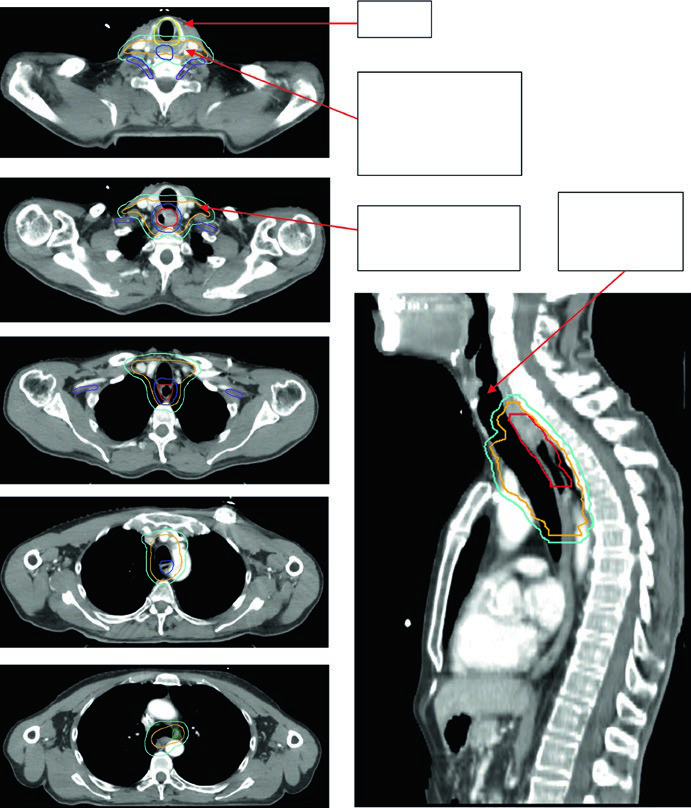
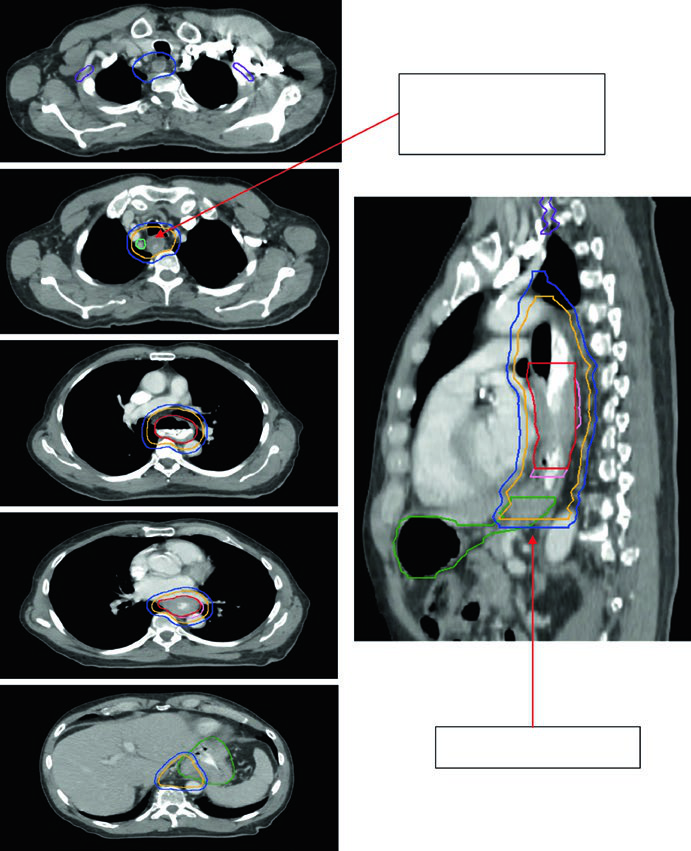
Paciente de 69 anos com CEC do esôfago cervical/torácico superior. O PET-CT revelou captação de FDG no tumor primário e linfonodos paratraqueais discretamente captantes. A EGD demonstrou massa ulcerada submucosa entre 15 e 23 cm dos incisivos. Os volumes delineados incluíram: plexo braquial (roxo), laringe (amarelo), GTV esofágico (vermelho), GTV nodal (verde), CTV (laranja), PTV 54 Gy (ciano) e PTV 60 Gy (azul escuro). O borda superior do campo supraclavicular foi posicionada na borda inferior da cartilagem cricoide, com cobertura nodal supraclavicular bilateral eletiva.
Caso 2: Adenocarcinoma Torácico Inferior — 81 anos, uT3N1
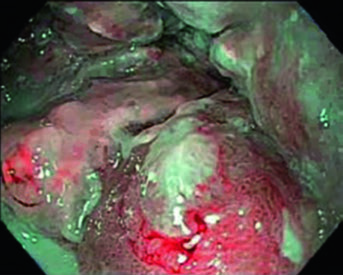
Paciente de 81 anos com adenocarcinoma esofágico torácico inferior uT3N1. O PET demonstrou captação no primário e no linfonodo paratraqueal nível 4R. A endoscopia revelou adenocarcinoma circunferencial parcialmente obstrutivo entre 31 e 35 cm dos incisivos. O EUS confirmou doença T3 com linfonodo nível 4R suspeito. Os contornos aplicaram margem de 0,5 cm de GTV para CTV no linfonodo 4R e cobertura inferior de 3–4 cm. Volumes: plexo braquial (roxo), estômago (verde escuro), GTV esofágico (vermelho), ITV (rosa), GTV nodal (verde claro), CTV (laranja), PTV 50,4 Gy (azul escuro).
Caso 3: Adenocarcinoma de JGE — 75 anos, uT3N0
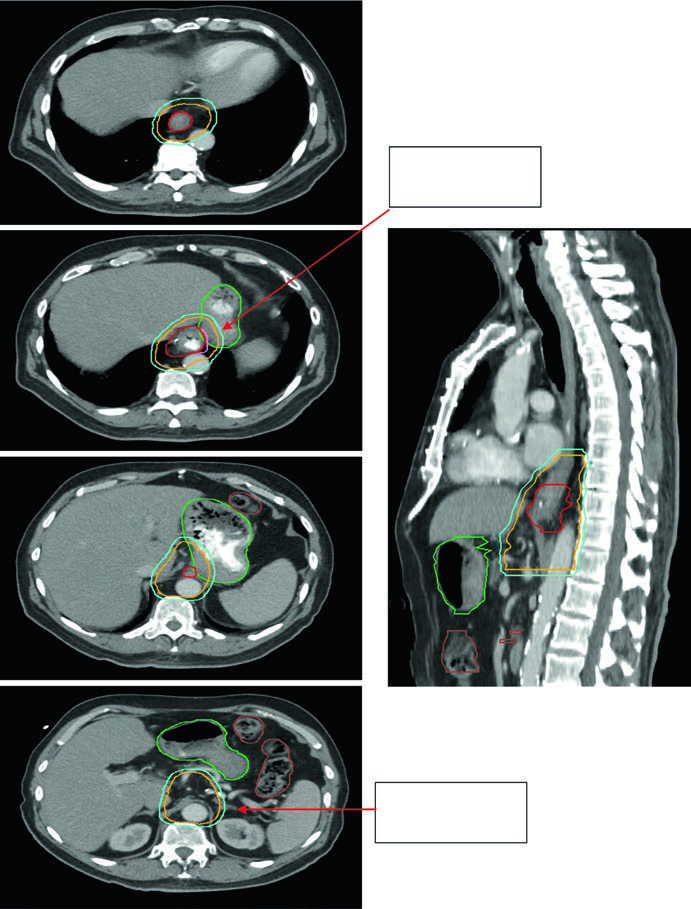
Paciente de 75 anos com adenocarcinoma de junção gastroesofágica uT3N0. Os contornos demonstram extensão do CTV para o estômago proximal, com cobertura até o eixo celíaco. Volumes delineados: estômago (verde escuro), intestino grosso (marrom), GTV esofágico (vermelho), CTV (laranja), PTV 50,4 Gy (ciano). A inclusão do eixo celíaco é mandatória para tumores distais e de JGE.
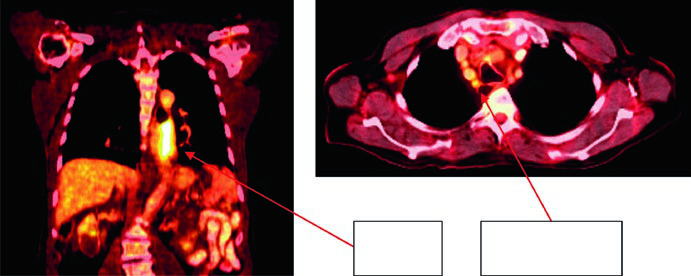
Caso 4: Adenocarcinoma de JGE — 59 anos, uT3N2
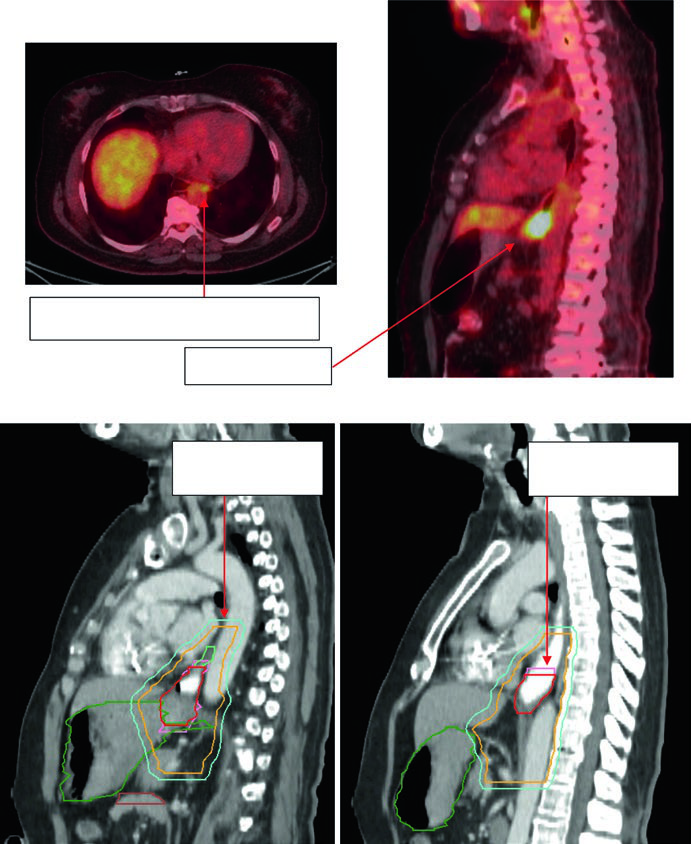
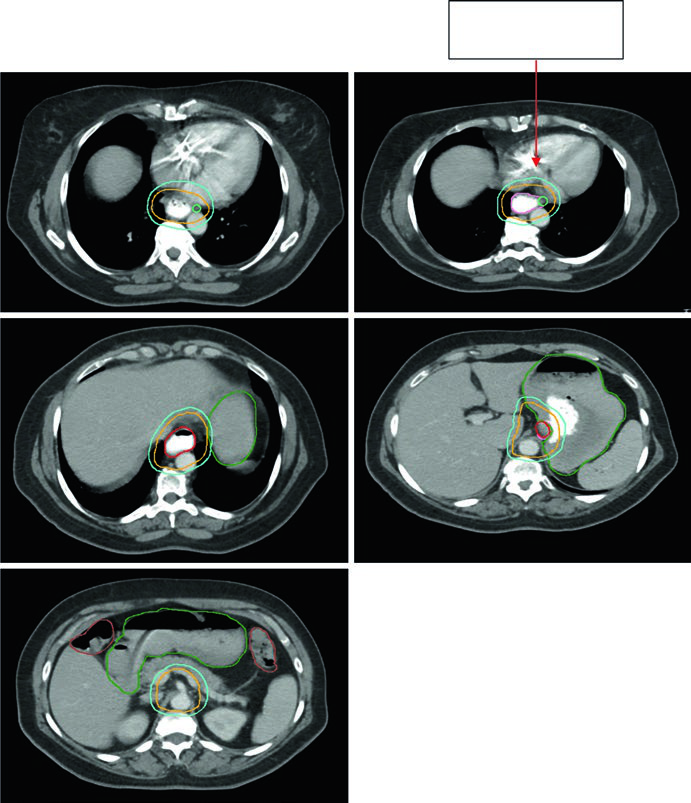
Paciente de 59 anos com adenocarcinoma de JGE uT3N2. O PET demonstrou linfonodos paraesofágicos captantes e tumor primário localizado entre 36 e 40 cm dos incisivos. O corte sagital da TC de planejamento mostra o ITV refletindo o movimento do GTV, com CTV cobrindo 3–4 cm acima do ITV. Volumes: estômago/duodeno (verde escuro), GTV nodal (verde claro), GTV esofágico (vermelho), ITV (rosa), CTV (laranja), PTV 50,4 Gy (ciano). Os linfonodos paraesofágicos foram incluídos no campo de tratamento.
Para explorar princípios semelhantes aplicados a outros sítios torácicos e abdominais, confira nosso artigo sobre câncer de pulmão e a discussão sobre câncer retal, que abordam respectivamente manejo de movimento respiratório e delineamento pélvico.


![Imagem fundida PET/TC com captação de [89Zr]girentuximab em massa renal posterior](https://rtmedical.com.br/wp-content/uploads/2026/05/article10_pet-600x403.jpg)