Neste Artigo
- 1. O Que é TSET e Por Que Monte Carlo Faz Diferença
- 2. Simulação Monte Carlo dos Feixes Utilizados em TSET
- 3. Validação dos Feixes na Geometria de Entrega TSET
- 4. A Controvérsia do Bremsstrahlung a Distâncias Estendidas
- 5. Uniformidade de Dose: Fantoma Oval e Distribuição no Paciente
- 6. Monte Carlo na Braquiterapia: Superando as Limitações do TG-43
- 7. Impacto Clínico da Transição TG-43 para Monte Carlo
- 8. Ferramentas de Cálculo MC para Braquiterapia
- 9. O Papel da Imagem na Atribuição de Tecidos para MC
- 10. Especificação de Dose: $D_{w,m}$ versus $D_{m,m}$
O Que é TSET e Por Que Monte Carlo Faz Diferença

A irradiação total de pele com elétrons (TSET) permanece como um dos tratamentos mais eficazes para linfoma cutâneo de células T (micose fungoide). Na prática, trata-se de um procedimento especial que exige modificações substanciais no equipamento e uma geometria de campo absolutamente fora do convencional — campos compostos de aproximadamente 200 cm de altura por 80 cm de largura, com SSDs nominais entre 300 e 500 cm para cobrir o maior paciente possível com uniformidade adequada.
Guia completo da série: para uma visão abrangente de todas as técnicas e artigos relacionados, confira nosso guia completo sobre Monte Carlo em radioterapia.
A população de pacientes que necessita de TSET é relativamente pequena, e a técnica costuma estar disponível apenas em centros acadêmicos ou hospitais de grande porte. Conforme as recomendações do AAPM Report 23, a dose máxima deve ocorrer na superfície, o nível de 80% da dose prescrita precisa estar a profundidade superior a 0,4 cm, e a dose deve cair para menos de 20% a 2 cm de profundidade. A energia nominal do feixe de elétrons mais utilizada varia entre 4 e 9 MeV.
As técnicas de entrega em TSET visam fornecer dose uniforme à pele inteira do paciente com máximo na superfície. Duas técnicas são predominantes atualmente: campos duplos estáticos (seis posições) e campos duplos rotacionais, nos quais o paciente fica sobre uma plataforma giratória. Na técnica de 6 campos estáticos, o paciente assume seis orientações distintas: anterior, posterior, lateral direita, lateral esquerda e duas posições anguladas. Estudos em fantomas indicaram que a rotação do paciente proporciona a melhor uniformidade de dose, embora a técnica de oito campos seja quase equivalente e a de seis campos seja adequada e mais simples de executar.
O método Monte Carlo trouxe para esse cenário algo que décadas de dosimetria experimental não alcançaram: a visualização completa das distribuições de dose na pele do paciente, incluindo análise DVH em diferentes profundidades — informações inacessíveis por métodos experimentais tradicionais baseados em filmes, TLDs e câmaras de ionização.
Simulação Monte Carlo dos Feixes Utilizados em TSET
Os campos de elétrons utilizados em TSET são definidos pelos colimadores (jaws) do LINAC, sem aplicador de elétrons acoplado. A simulação desses feixes utiliza o sistema EGSnrc, partindo da geometria detalhada do cabeçote do acelerador. Ding et al. modelaram feixes de 6 MeV a partir de dois aceleradores distintos: o Varian Clinac 21EX e o Varian TrueBeam — cada um com abordagem de simulação própria.
Para o Clinac 21EX, a simulação começa com elétrons saindo da janela de vácuo do cabeçote. Os detalhes da geometria do cabeçote — incluindo folhas de espalhamento de elétrons e o sistema de definição de campo — foram obtidos diretamente do fabricante. A energia e o tamanho do spot do feixe de elétrons antes de atingir a janela de saída são ajustados iterativamente para obter a melhor concordância entre medidas e cálculos.
O TrueBeam segue lógica diferente. A simulação parte de arquivos de phase-space fornecidos pela Varian, registrados no plano logo acima dos colimadores x-y, sem necessidade de ajuste manual. Essa abordagem elimina a incerteza associada à modelagem do cabeçote, transferindo a responsabilidade da precisão para o fabricante.
Em todos os casos, os parâmetros padrão do EGSnrc foram empregados:
$$AE = ECUT = 0{,}521 \text{ MeV}, \quad AP = PCUT = 0{,}010 \text{ MeV}$$
Não houve forçamento de interação de fótons nem espalhamento Rayleigh — configuração consistente com estudos anteriores. Os feixes simulados foram armazenados em phase-space files a SSD = 100 cm, contendo posição, energia, ângulo, carga e peso de cada partícula. Esses arquivos alimentam o código DOSXYZnrc para os cálculos de dose subsequentes.
A validação mostrou excelente concordância entre curvas de porcentagem de dose em profundidade (PDD) medidas e calculadas, além de perfis de dose em água para feixes de 6 MeV com campos de 36 × 36 cm² e 40 × 40 cm² a SSD = 100 cm. As medidas utilizaram detector diodo. Essa concordância confirma a acurácia da modelagem Monte Carlo para os feixes de TSET.
Validação dos Feixes na Geometria de Entrega TSET
Embora o Monte Carlo seja considerado padrão-ouro para cálculo de dose, a acurácia depende de muitos fatores. A validação experimental da simulação torna-se essencial, especialmente quando a radiação é entregue por feixes duplos combinados à geometria rotacional.
A técnica utiliza uma grande placa de acrílico transparente (90 cm × 200 cm), montada em um quadro de madeira sobre rodas, posicionada entre o feixe incidente e a plataforma giratória. Essa placa funciona como degradador de feixe — reduz a energia dos elétrons e aumenta o espalhamento, contribuindo para a uniformidade da dose na pele.
As medidas de validação empregaram dosímetros nanoDot fabricados pela LANDAUER, baseados em tecnologia de Luminescência Opticamente Estimulada (OSL). Esses dosímetros foram posicionados sobre um fantoma cilíndrico equivalente a água (29 cm de diâmetro, 30 cm de comprimento) revestido com duas camadas de bolus de 5 mm de espessura equivalente a água. Os dosímetros ficaram na superfície do fantoma e entre as camadas de bolus.
Para validar os feixes simulados na direção vertical, dosímetros nanoDot foram colocados na superfície da placa de espalhamento. O retroespalhamento da placa é proporcional à dose de superfície, portanto a forma dos perfis não é afetada pelo retroespalhamento. A comparação entre perfis medidos e calculados mostrou concordância excelente.
Um achado importante: os perfis de dose são extremamente sensíveis ao tamanho de campo do feixe de elétrons. Para o campo de 40 × 40 cm², a dose nas bordas é menor do que para 36 × 36 cm². A explicação é geométrica — no centro, ambos os campos duplos contribuem para a dose, enquanto nas extremidades apenas um campo contribui. A boa concordância entre simulação e medida valida a acurácia do modelo, resultados consistentes com a literatura existente.
A Controvérsia do Bremsstrahlung a Distâncias Estendidas
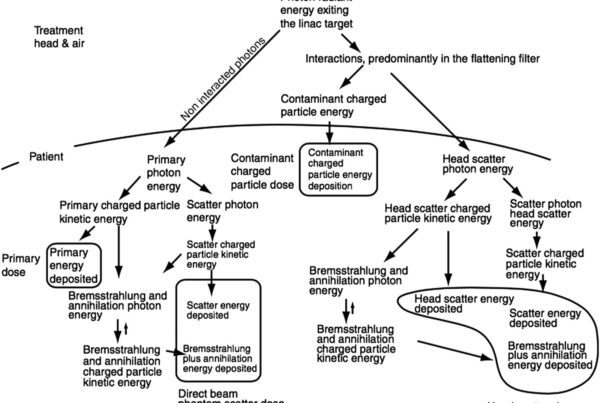
Um dos resultados mais impactantes dos estudos Monte Carlo em TSET diz respeito à dose de bremsstrahlung. Durante décadas, a percepção comum na comunidade de física médica era que a dose de bremsstrahlung de um feixe de 6 MeV atingia 5% a distâncias estendidas de ~500 cm, conforme reportado por Das et al. Essa estimativa, se correta, limitaria significativamente o uso clínico do TSET.
Os resultados Monte Carlo de Ding et al. desafiaram essa percepção de forma definitiva. As simulações mostraram que a dose de bremsstrahlung para feixes de 6 MeV ficou entre 0,5% e 1% para SSDs de 100 a 700 cm — uma ordem de grandeza abaixo do valor previamente aceito. Chen et al. também encontraram doses de bremsstrahlung de apenas ~1% mesmo a SSD > 500 cm para um feixe de 6 MeV do Varian 21EX-S.
Ding et al. avaliaram a validade dos 5% reportados e concluíram que os erros nas medidas originais provavelmente decorreram de um detector cuja leitura era dominada por baixa relação sinal/ruído a distâncias estendidas. Os feixes simulados a distâncias estendidas também foram utilizados por Ding para investigar as razões de poder de frenagem (stopping-power ratios) para dosimetria precisa em TSET.
Essa descoberta tem impacto direto na prática clínica. Uma dose de bremsstrahlung de 5% contribuiria significativamente para irradiação de tecidos profundos — um efeito indesejado em TSET, onde o objetivo é tratar exclusivamente a pele. Ao demonstrar que o valor real é inferior a 1%, o Monte Carlo removeu uma barreira potencial à expansão do uso da técnica. Como discutido em nosso artigo sobre cálculo de dose Monte Carlo no paciente, a precisão na modelagem do feixe é fundamental para resultados clínicos confiáveis.
Uniformidade de Dose: Fantoma Oval e Distribuição no Paciente
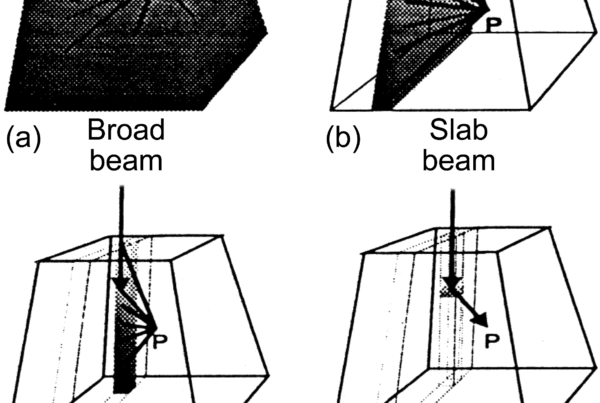
O torso humano se assemelha a um oval, o que torna a análise com fantoma cilíndrico oval mais realista que com geometrias circulares. Simulações Monte Carlo em um fantoma cilíndrico oval equivalente a água (eixo longo de 40 cm, eixo curto de 20 cm, comprimento vertical de 150 cm) revelam diferenças importantes em relação à geometria circular.
Na geometria circular, a dose é uniforme em toda a superfície. No cilindro oval, doses significativamente menores são observadas nas superfícies do eixo curto — correspondendo às regiões anterior e posterior do torso do paciente. Embora a dose seja menor na superfície do eixo curto, a profundidade onde a dose cai para 50% do valor de superfície permanece aproximadamente a mesma. Isso ocorre porque as doses em profundidades maiores são contribuídas por feixes de incidência quase normal, enquanto feixes oblíquos não penetram significativamente.
A espessura da placa degradadora influencia diretamente a cobertura em profundidade. Comparações entre placas de 3 mm, 9 mm e sem placa mostram que o máximo de dose ocorre na superfície mesmo sem degradador — resultado da incidência de elétrons de múltiplas direções durante a rotação do fantoma. Quando o fantoma está estacionário, observa-se buildup de dose, consistente com curvas de PDD medidas por Chen et al. Com base nos resultados Monte Carlo, Ding et al. recomendam placa degradadora de 3 mm em vez de 9 mm, com campo de 40 × 40 cm² para cobertura ótima de dose em profundidade na pele.
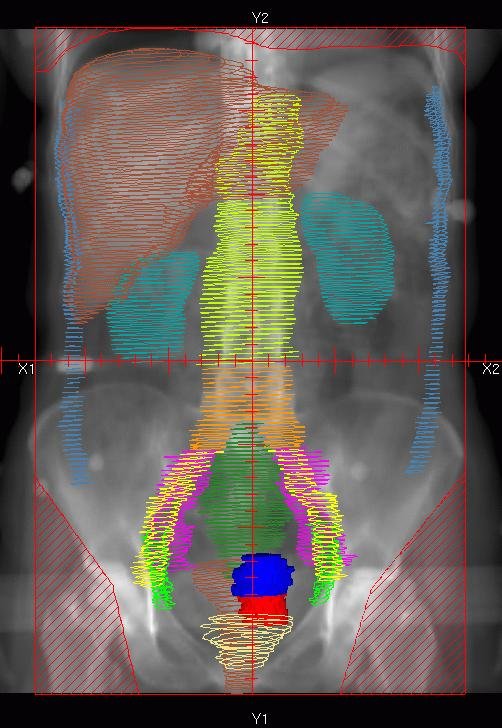
As distribuições de dose na anatomia real do paciente — obtidas por cálculo Monte Carlo em imagens CT — revelam variações superiores a 20% na dose cutânea, consistentes com medidas in vivo da literatura. As linhas de isodose de 90% (vermelho), 75% (branco) e 50% (azul) revelam blindagem parcial pelos braços elevados, gerando descontinuidades na cobertura entre cabeça e braço. A distância entre as isodoses de 90% e 50% é de aproximadamente 5 mm.
As análises DVH em três intervalos de profundidade — 0–5 mm, 5–10 mm e 10–15 mm da superfície — tanto para o torso quanto para a pele inteira demonstram o impacto da espessura da placa de espalhamento (3 mm versus 9 mm) na cobertura de dose. Essas informações detalhadas sobre a distribuição volumétrica de dose são absolutamente inacessíveis por métodos experimentais e representam a contribuição singular do Monte Carlo ao planejamento de TSET.
No Vanderbilt University Medical Center, dosímetros OSLD (nanoDot) são posicionados na pele do paciente durante a primeira fração de tratamento em localizações específicas. As variações de dose in vivo medidas em diferentes localizações corporais foram consistentes com as variações de 20% preditas pelo cálculo Monte Carlo. Resultados terapêuticos de pacientes tratados com o degradador de 3 mm são objeto de estudo prospectivo em andamento para avaliar eficácia clínica. Tanto a técnica de campos duplos rotacionais quanto a de 6 campos estáticos duplos produzem distribuições de dose cutânea comparáveis.
Monte Carlo na Braquiterapia: Superando as Limitações do TG-43
O formalismo TG-43, com mais de 1.500 citações até agosto de 2020, representou avanço fundamental na dosimetria de braquiterapia. Ele substituiu métodos semiempíricos baseados em atividade aparente e equivalente em massa de rádio por parâmetros dosimétricos que dependem da geometria detalhada da fonte — distribuição de radioatividade, encapsulamento e marcadores de imagem. Essa padronização melhorou a consistência e comparabilidade dos cálculos de dose entre instituições mundialmente.
Entretanto, o TG-43 baseia-se na superposição de distribuições de dose de fonte única derivadas em esferas de água de referência (raios de 15 cm para fontes de baixa energia, 40 cm para alta energia). Quando a geometria real se desvia significativamente dessa esfera de referência, cinco fenômenos geram erros:
| Sítio Anatômico | Energia | Absorção | Atenuação | Blindagem | Espalhamento | Dose ≠ Kerma |
|---|---|---|---|---|---|---|
| Próstata | Alta | N | N | N | N | N |
| Próstata | Baixa | Y | Y | Y | N | N |
| Mama | Alta | N | N | N | Y | N |
| Mama | Baixa | Y | Y | Y | N | N |
| GYN | Alta | N | N | Y | N | N |
| GYN | Baixa | Y | Y | N | N | N |
| Pele | Alta | N | N | Y | Y | N |
| Pele | Baixa | Y | N | Y | Y | N |
| Pulmão | Alta | N | N | N | Y | Y |
| Pulmão | Baixa | Y | Y | N | Y | N |
| Pênis | Alta | N | N | N | Y | N |
| Pênis | Baixa | Y | N | N | Y | N |
| Olhos | Alta | N | N | Y | Y | Y |
| Olhos | Baixa | Y | Y | Y | Y | N |
Fonte: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022), Table 16.1, adaptada de Rivard et al.
Para fontes de baixa energia, o coeficiente de absorção mássica de energia $\mu_{en}/\rho$ varia significativamente entre tecidos devido à dependência aproximada de $Z^{3-4}$ da seção de choque fotoelétrica. Sob condições de equilíbrio de partículas carregadas (CPE) em uma cavidade grande, a relação entre dose no tecido e dose em água é:
$$\frac{D_{tecido}}{(\mu_{en}/\rho)_{tecido}} = \frac{D_{água}}{(\mu_{en}/\rho)_{água}}$$
Essa razão $(\mu_{en}/\rho)_{tecido} / (\mu_{en}/\rho)_{água}$ difere substancialmente da unidade para a maioria dos tecidos na faixa de energia de fontes de baixa energia. Em energias mais altas de fótons, as razões convergem para a unidade à medida que o espalhamento Compton se torna dominante.
A blindagem (shielding) é relevante em implantes multi-sementes, onde fótons de uma fonte podem ser absorvidos por marcadores radiopacos (Au, Ag, Pb) ou componentes de fontes adjacentes — a chamada atenuação intersementes (ISA). Para fontes HDR de alta energia como $^{192}$Ir, a ISA entre sementes não é problema, pois uma única fonte percorre os canais do aplicador. Contudo, materiais do aplicador como aço inoxidável e blindagens de tungstênio (usadas para proteger órgãos de risco) podem causar desvios significativos.
A quebra da aproximação kerma = dose ocorre quando os alcances dos elétrons secundários são significativos. Para fontes de alta energia, essa aproximação pode introduzir diferenças maiores que 1% a distâncias inferiores a 7 mm ($^{60}$Co), 3,5 mm ($^{137}$Cs) e 2 mm ($^{192}$Ir) da fonte. Para fontes de baixa energia, o equilíbrio eletrônico é atingido dentro de 0,1 mm e a aproximação permanece acurada. Para mais detalhes sobre modelagem de fontes, veja nosso artigo sobre Monte Carlo em elétrons e braquiterapia.
Impacto Clínico da Transição TG-43 para Monte Carlo
Os números do impacto clínico são eloquentes. Meigooni et al. foram os primeiros a investigar ISA em 1992, estimando reduções de dose de 6% na borda de implantes prostáticos de $^{125}$I. Chibani et al. e Carrier et al. publicaram simulações Monte Carlo em geometrias reais de implantes de $^{125}$I e $^{103}$Pd em próstata em 2005 e 2006, encontrando reduções no $D_{90}$ de 2%–5% devidas à ISA.
Carrier et al. realizaram estudo retrospectivo com 28 pacientes de câncer de próstata implantados com $^{125}$I usando dados de CT pós-implante. Encontraram redução média de 7% no $D_{90}$ pela combinação de ISA e heterogeneidades teciduais. Chibani et al. também investigaram o impacto de calcificações intraprostáticas e encontraram reduções no $D_{90}$ de até 37%. No maior estudo da literatura (613 pacientes), Miksys et al. demonstraram que o $D_{90}$ é 6% menor, em média, para simulações Monte Carlo paciente-específicas comparadas ao TG-43. Pacientes com calcificações intraprostáticas podem apresentar subdosagem significativa em subvolumes sombreados pelas calcificações, com reduções no $D_{90}$ de até 25%.
Para implantes de mama, os resultados são ainda mais dramáticos. Landry et al. investigaram a sensibilidade das distribuições de dose em implantes prostáticos com $^{125}$I e mamários com $^{103}$Pd. Duas composições elementais de próstata da literatura resultaram em variações de 3,5% no $D_{w,m,90\%}$. Para mama, a proporção adipose:glandular variou de 70:30 a 30:70, gerando variações de 10% no $D_{w,m,90\%}$ (ou cerca de 6% em $D_{m,m}$). A variabilidade na composição elemental do tecido para uma dada proporção resultou em variações de dose de 10%. Afsharpour et al. encontraram reduções no $D_{90\%}$ de 4% para mama inteiramente glandular até 35% para mama inteiramente adiposa com implantes de $^{103}$Pd.
Em braquiterapia ocular com placas de $^{103}$Pd, $^{125}$I ou $^{131}$Cs, as discrepâncias são igualmente expressivas. Para uma placa COMS de 16 mm de diâmetro com dezesseis sementes de $^{103}$Pd, a dose média no tumor foi até 17% menor pelo MC comparado ao TG-43. Para estruturas normais como o cristalino, a dose MC foi até 34% menor que o TG-43.
Miksys et al. demonstraram, em braquiterapia mamária com $^{103}$Pd, que o TG-43 superestima doses no alvo ($D_{90\%}$ em média 10%, até 27%) e subestima doses na pele ($D_{1 cm^3}$ em média 29%, até 48%) comparado ao MC com modelos teciduais completos do paciente.
Ferramentas de Cálculo MC para Braquiterapia
Várias plataformas de cálculo Monte Carlo foram desenvolvidas para dosimetria paciente-específica em braquiterapia, cada uma com abordagens distintas para tornar os tempos de cálculo clinicamente viáveis.
| Ferramenta | Base MC | Resolução de Voxel | Tempo de Cálculo | Incerteza Estatística | Características Distintivas |
|---|---|---|---|---|---|
| MCPI | GEPTS | 2 mm³ | ~1 min | 2% | Modelo híbrido voxel+cilíndrico; ray tracing analítico |
| PTRAN_CT | EGSnrc | 2 mm³ | ~3 s | 2% | Correlated sampling generalizado; ganho de eficiência 2–40× |
| BrachyDose | EGSnrc | 2 mm³ | ~30 s | <2% | Multi-geometry package; múltiplas fontes e aplicadores |
| ALGEBRA | GEANT4 | 2 mm³ | 6–12 min | 2% | DICOM-RT nativo; scoring em parallel world independente |
| egs_brachy | EGSnrc (egs++) | 2 mm³ / 1 mm³ | 13–39 s | 2% | Código aberto; biblioteca benchmarked; GUI integrada |
Fonte: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
O MCPI (Monte Carlo dose calculation tool for prostate implants), desenvolvido por Chibani et al. em 2005, utiliza transporte apenas de fótons para fontes de baixa energia (<50 keV). Emprega um modelo híbrido onde voxels retangulares e geometrias cilíndricas das sementes coexistem — voxels que intersectam sementes são sinalizados, evitando a necessidade de consultar cada semente durante o transporte. O código utiliza ray tracing no lugar de transporte analógico, projetando trajetórias de fótons primários e secundários através de toda a malha de voxels, independentemente de interação, aumentando a frequência de deposição de energia em voxels distantes.
O PTRAN_CT implementa a técnica de correlated sampling generalizado: histórias de fótons são construídas inicialmente em água homogênea, depois os pesos das partículas são recalculados para a geometria heterogênea. Em vez de pontuar dose absoluta, o código pontua a diferença entre a dose na geometria heterogênea e a dose TG-43, aumentando a eficiência por fatores de 2 a 40. Tempos de cálculo de cerca de 3 segundos para implantes de próstata com incerteza de 2% em voxels de 2 mm³ foram reportados. O código importa imagens CT DICOM e utiliza o CTcreate do EGSnrc para atribuição de seções de choque.
O BrachyDose é um código de usuário do EGSnrc que utiliza o multi-geometry package. Modela tanto fótons quanto elétrons de 1 keV a MeV, incluindo fontes LDR e HDR de diversas energias, aplicadores de placas oculares e modelos virtuais de pacientes baseados em CT. Foi extensivamente benchmarked gerando parâmetros TG-43 para múltiplas fontes comerciais de $^{125}$I, $^{103}$Pd e $^{192}$Ir.
O ALGEBRA (ALgorithm for heterogeneous dosimetry based on GEANT4 for BRAchytherapy) é baseado no GEANT4 e no padrão DICOM-RT. Importa dados do sistema de planejamento e imagens CT, com método semiautomático de segmentação. Uma funcionalidade importante é o scoring independente da geometria de transporte, usando o “parallel world” do GEANT4 — a resolução da malha de transporte e da malha de scoring podem ser diferentes.
O egs_brachy é a aplicação mais moderna do grupo, distribuída como software livre e de código aberto. Utiliza o egs++ (biblioteca C++ do EGSnrc) para modelagem geométrica e emprega técnicas variadas para aumentar eficiência: track-length estimator para kerma de colisão, fontes de phase-space, reciclagem de partículas e técnicas específicas de redução de variância para braquiterapia eletrônica. Para implantes de próstata e mama com voxels de 2 mm³ e placas oculares com voxels de 1 mm³, os tempos de simulação ficam entre 13 e 39 segundos para 2% de incerteza média no alvo. O código pode ser executado em múltiplos núcleos para tempos ainda menores. Para mais sobre simulações e ferramentas de QA, confira nosso artigo sobre prótons e QA avançado com Monte Carlo.
O Papel da Imagem na Atribuição de Tecidos para MC
A precisão do cálculo Monte Carlo em braquiterapia depende criticamente da atribuição voxel a voxel das seções de choque de fótons, o que exige conhecimento detalhado da composição tecidual. A tomografia computadorizada (CT) é o input padrão porque sua intensidade acompanha o coeficiente de atenuação linear relativo do tecido. A conversão de unidades Hounsfield (HU) para densidade eletrônica ou mássica é razoavelmente direta.
Para fontes de alta energia, onde os efeitos de composição tecidual são menores e o espalhamento Compton domina, as imagens CT fornecem informação suficiente para calcular a dose absorvida com poucos pontos percentuais de erro. Melhus e Rivard mostraram que heterogeneidades de composição tecidual têm efeitos desprezíveis (<5%) para $^{192}$Ir em distâncias clinicamente relevantes em tecidos moles.
Para fontes de baixa energia, a situação muda completamente. A forte dependência $Z^{3-4}$ da seção de choque fotoelétrica exige determinação precisa da composição elemental — algo que a CT convencional de energia única não fornece diretamente. Estudos recentes demonstram que a CT de energia dupla (DECT) pode fornecer estimativas mais precisas da composição elemental, reduzindo incertezas nas simulações MC.
A ressonância magnética (MRI) oferece contraste superior em tecidos moles, particularmente vantajoso para delineação da próstata. Porém, não fornece diretamente informações de densidade eletrônica. Distorções geométricas devidas a não-homogeneidades do campo magnético, não-linearidade de gradiente e efeitos de susceptibilidade representam desafios adicionais, embora a braquiterapia possa ser menos sensível a essas distorções do que a radioterapia externa.
A sensibilidade das distribuições de dose à composição tecidual é significativa. Para implantes prostáticos com $^{125}$I, duas composições elementais de próstata encontradas na literatura resultaram em variações de 3,5% no $D_{w,m,90\%}$. Para mama, a variabilidade na composição tecidual resultou em variações de dose de até 10%. Maughan et al. encontraram grande variação no conteúdo de carbono (8%–32% em peso) e cinza mineral (0,9%–3,0% em massa) em tumores de vários sítios, resultando em variações de 20% na razão $(\mu_{en}/\rho)_{tumor} / (\mu_{en}/\rho)_{água}$ a 30 keV — indicando a necessidade de mais estudos nessa área.
Especificação de Dose: $D_{w,m}$ versus $D_{m,m}$
Um tema de debate na transição para cálculos Monte Carlo em braquiterapia é a grandeza dosimétrica utilizada. O TG-43 reporta dose em água em água ($D_{w,w}$). Com o MC, duas opções surgem: dose no meio em meio ($D_{m,m}$) — fótons transportados e dose pontuada no tecido real — e dose em água no meio ($D_{w,m}$) — fótons transportados no tecido real, mas dose convertida para água.
A diferença entre essas grandezas depende das dimensões da cavidade (volume de interesse) em relação ao alcance dos elétrons secundários. Carlsson-Tedgren e Carlsson aplicaram a teoria de cavidade de Burlin para avaliar quando cavidades podem ser consideradas pequenas, intermediárias ou grandes. Para fontes de baixa energia, cavidades de dimensões típicas de voxels de cálculo comportam-se como cavidades grandes, simplificando a conversão. Para fontes de alta energia, a situação é mais complexa e os métodos MC tornam-se a única ferramenta verdadeiramente adequada para resolver a questão.
O avanço contínuo dessas técnicas aponta para um futuro onde o cálculo Monte Carlo será ferramenta de rotina no planejamento de braquiterapia, oferecendo dosimetria verdadeiramente paciente-específica. Para conhecer as tendências emergentes, confira nosso artigo sobre IA e futuro do Monte Carlo em radioterapia.