Sarcoma pediátrico engloba um grupo heterogêneo de neoplasias de osso e partes moles que exigem abordagem multidisciplinar e delineamento preciso dos volumes-alvo. O sarcoma de Ewing (EWS) é o segundo tumor ósseo pediátrico mais frequente, enquanto o rabdomiossarcoma (RMS) lidera entre os sarcomas de partes moles na infância. Ambos compartilham um algoritmo terapêutico que combina quimioterapia sistêmica e terapia local — cirurgia e/ou radioterapia — mas diferem substancialmente em relação a estadiamento, volumes de irradiação e doses prescritas.
Este artigo detalha o delineamento de volumes-alvo e o planejamento radioterápico para EWS e RMS em pacientes pediátricos, abordando desde a anatomia e padrões de disseminação até a simulação, imobilização e avaliação do plano. Para uma visão abrangente de todas as localizações anatômicas e técnicas de planejamento em radioterapia, confira nosso guia completo sobre delineamento de volumes-alvo.
Neste Artigo
- Epidemiologia e Padrões de Disseminação
- Imagem Diagnóstica para Definição de Volumes
- Delineamento de Volumes no Sarcoma de Ewing
- Delineamento de Volumes no Rabdomiossarcoma
- Classificação Molecular e Implicações na Dosimetria
- Casos Clínicos Ilustrativos
- Simulação, Imobilização e Localização Diária
- Restrições de Dose e Avaliação do Plano
- Efeitos Tardios e Papel da Próton-Terapia
Epidemiologia e Padrões de Disseminação dos Sarcomas Pediátricos
O sarcoma de Ewing predomina na pelve (25% dos casos) e no fêmur (16%). Pacientes com tumores pélvicos geralmente não são candidatos à ressecção cirúrgica e acabam recebendo radioterapia definitiva como controle local. Já o osteossarcoma — tumor ósseo pediátrico mais comum — não costuma depender da radioterapia de maneira tão central, tornando o EWS a principal indicação radioterápica entre as neoplasias ósseas da infância.
O rabdomiossarcoma apresenta distribuição anatômica mais dispersa: cabeça e pescoço respondem por 35% dos casos, sistema geniturinário por 20% e extremidades por 20%. Uma distinção fundamental no RMS é a dicotomia entre sítios primários favoráveis e desfavoráveis, que impacta diretamente o estadiamento e a estratificação de risco. Dentro das lesões de cabeça e pescoço, os tumores são classificados como parameníngeos (15% de todos os RMS), orbitais (10%) ou outros sítios de cabeça e pescoço (10%).
As lesões parameníngeas ocupam um dos oito sítios específicos — ouvido médio, mastoide, cavidade nasal, nasofaringe, fossa infratemporal, fossa pterigopalatina, seios paranasais e espaço parafaríngeo (mnemônico “MMNNOOPP”) — e carregam risco aumentado de extensão intracraniana direta, sendo classificadas como sítios desfavoráveis.
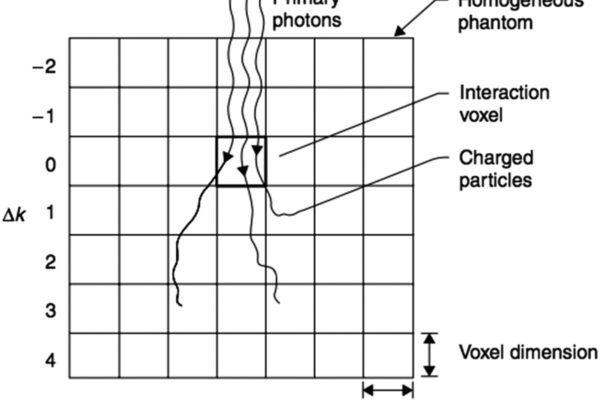
Quanto aos padrões de disseminação local, osso não envolvido e membranas interósseas funcionam como barreiras anatômicas para a extensão microscópica. Entretanto, erosão e invasão óssea não são incomuns e devem ser avaliadas por imagem — especialmente tomografia computadorizada. Como EWS e RMS frequentemente recebem quimioterapia antes da radioterapia, a redução volumétrica pós-quimioterapia precisa ser considerada: quando a imagem pré-tratamento mostra tumor “empurrando” estruturas adjacentes (pulmão, bexiga, alça intestinal), o volume pós-quimioterapia geralmente reflete o retorno dessas estruturas à posição normal. Em contraste, invasão direta identificada no exame pré-quimioterapia deve manter cobertura nos campos de irradiação pós-indução.
A disseminação linfonodal é incomum na maioria dos sarcomas pediátricos, mas merece atenção em cenários específicos. O RMS de extremidade apresenta taxas mais elevadas de metástases nodais e frequentemente é avaliado por biópsia de linfonodo sentinela. O RMS paratesticular pode exigir dissecção retroperitoneal ipsilateral com preservação de nervos em pacientes acima de 10 anos. Quando há metástases nodais confirmadas, recomenda-se cobertura radioterápica de toda a bacia linfonodal — não apenas dos linfonodos envolvidos.
Imagem Diagnóstica para Definição de Volumes-Alvo
A combinação de modalidades de imagem é essencial tanto para a definição de volumes-alvo (GTV e CTV) quanto para o estadiamento. A tomografia computadorizada é particularmente útil para delinear envolvimento e erosão óssea, enquanto a ressonância magnética oferece excelente resolução de partes moles para avaliar a extensão da doença, inclusive invasão intracraniana. Ambas são rotineiramente utilizadas para EWS e RMS.
O PET-CT tem sido cada vez mais incorporado no estadiamento inicial de ambas as neoplasias, com literatura crescente favorecendo sua adoção em detrimento de técnicas como a cintilografia óssea. A fusão PET pode ajudar a identificar sítios de doença inicialmente envolvidos antes da quimioterapia de indução — informação valiosa para a definição de volumes, especialmente ao comparar extensão pré e pós-quimioterapia. Para princípios de delineamento em sarcomas de partes moles em adultos, consulte nosso artigo dedicado.
Delineamento de Volumes no Sarcoma de Ewing
O planejamento no EWS utiliza dois conjuntos de volumes: um baseado na extensão da doença ao diagnóstico (GTV1/CTV1) e outro definido pela doença residual pós-quimioterapia e, eventualmente, pós-cirurgia (GTV2/CTV2). As margens adicionadas aos CTVs para incerteza de posicionamento resultam nos respectivos PTVs.
Definição de Volumes-Alvo no Sarcoma de Ewing
A tabela abaixo resume as definições de volumes utilizadas no planejamento radioterápico do sarcoma de Ewing, conforme o protocolo COG AEWS1031.
| Volume | Definição |
|---|---|
| GTV1 | Extensão pré-quimioterapia da doença macroscópica (osso e partes moles), incluindo linfonodos suspeitos não ressecados. O GTV1 pode ser modificado se o tumor inicial se estendia para cavidades corporais (pelve, tórax) e houve regressão com quimioterapia. |
| CTV1 | GTV1 + 1–1,5 cm. Inclui bacias linfonodais envolvidas (clínica ou patologicamente). |
| PTV1 | CTV1 + margem de setup (específica da instituição e do tipo de guiamento por imagem, geralmente 3–5 mm). |
| GTV2 | Tumor residual após quimioterapia de indução; contudo, toda extensão óssea pré-quimioterapia é tipicamente incluída no GTV2. No pós-operatório, o GTV2 corresponde à doença residual (óssea ou de partes moles) e sítios de margens positivas. |
| CTV2 | GTV2 + 1–1,5 cm. |
| PTV2 | CTV2 + margem de setup (geralmente 3–5 mm). |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition
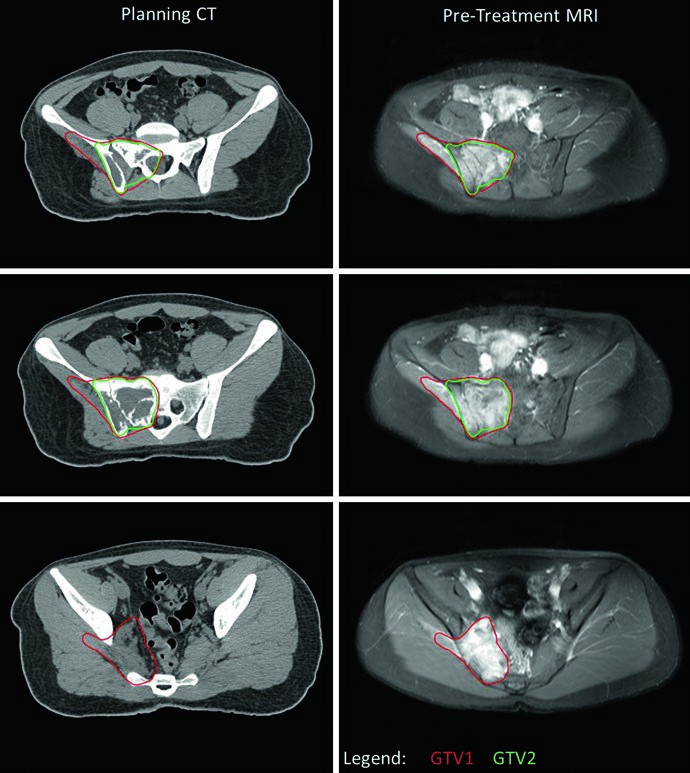
Um ponto prático central é o manejo do GTV1 quando o tumor se estende para cavidades corporais. Se a imagem pré-tratamento mostra tumor “empurrando” pulmão ou vísceras pélvicas — sem invasão direta — o GTV1 pode ser adaptado após a quimioterapia de indução para refletir a regressão tumoral nesses espaços. Essa adaptação aparece claramente no caso de EWS pélvico, onde o nível inferior não apresenta doença residual (GTV2) e a extensão do GTV1 para a pelve foi reduzida para compensar a resposta à quimioterapia. O PTV1 recebeu 45 Gy e o PTV2 recebeu 10,8 Gy adicionais, totalizando 55,8 Gy.
Doses no Sarcoma de Ewing
Os esquemas de dose variam conforme o cenário clínico. Todas as frações são de 1,8 Gy por dia.
| Cenário Clínico | PTV1 (Gy) | PTV2 (Gy) |
|---|---|---|
| RT definitiva (todos os sítios exceto vertebral) | 45 | 10,8 |
| RT definitiva — vertebral | 45 | 5,4 |
| EWS extraósseo com resposta completa à quimioterapia | 50,4 | 0 |
| Pós-operatório com doença residual microscópica (R1) e >90% de necrose tumoral | 0 | 50,4 |
| Pós-operatório com doença residual microscópica (R1) e <90% de necrose tumoral | 50,4 | 0 |
| Pós-operatório com doença residual macroscópica (R2) | 45 | 10,8 |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition
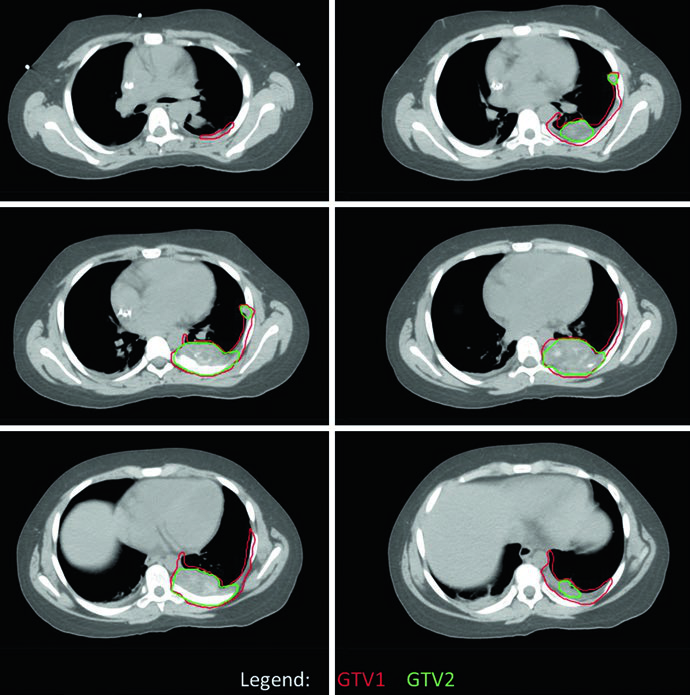
No caso de EWS de parede torácica, a simulação com TC de quatro dimensões (4DCT) foi realizada para capturar a excursão respiratória completa dos volumes-alvo. O tumor original ocupava a metade posterior do hemitórax esquerdo, mas o GTV1 foi adaptado para refletir o “pushing” tumoral no espaço agora ocupado por pulmão normal. A cobertura dos sítios de contato e envolvimento originais foi mantida. Da mesma forma, PTV1 recebeu 45 Gy e PTV2 um boost adicional de 10,8 Gy.
Delineamento de Volumes no Rabdomiossarcoma
No RMS, a radioterapia pode ser entregue como volume único ou em dois níveis de dose, similar ao EWS. A redução de volume para doses de boost acima de 36 Gy é geralmente recomendada para tumores que “empurram” estruturas torácicas ou pélvicas. No entanto, lesões invasivas podem exigir cobertura completa do volume pré-quimioterapia com a dose máxima — frequentemente 50,4 Gy para doença macroscópica — independentemente da resposta à quimioterapia. Essa regra é particularmente relevante para o RMS parameníngeo de cabeça e pescoço, onde o GTV2 deve incluir a extensão pré-quimioterapia da doença, mesmo que a quimioterapia de indução tenha produzido resposta.
Definição de Volumes-Alvo no Rabdomiossarcoma
O delineamento de volumes no RMS segue princípios semelhantes aos do EWS, mas com particularidades para tumores parameníngeos e lesões que “empurram” estruturas adjacentes.
| Volume | Definição |
|---|---|
| GTV1 | Extensão pré-quimioterapia da doença macroscópica (osso e partes moles), incluindo linfonodos suspeitos não ressecados. |
| CTV1 | GTV1 + 1 cm. Inclui bacias linfonodais envolvidas (clínica ou patologicamente). |
| PTV1 | CTV1 + margem de setup (geralmente 3–5 mm). |
| GTV2 | Tumor residual pós-quimioterapia de indução, excluindo áreas onde o tumor “empurrava” estruturas como tórax ou pelve. Para RMS parameníngeo de cabeça e pescoço, a doença invasiva pré-quimioterapia deve ser incluída no GTV2 independentemente da resposta à quimioterapia. |
| CTV2 | GTV2 + 1 cm. |
| PTV2 | CTV2 + margem de setup (geralmente 3–5 mm). |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition
Doses no Rabdomiossarcoma
As doses prescritas dependem do grupo cirúrgico, status de fusão molecular e resposta à quimioterapia de indução. Frações de 1,8 Gy/dia.
| Grupo | Status de Fusão (Histologia) | Dose (Gy) |
|---|---|---|
| I (R0), linfonodo-negativo | Negativo (embrionário) | 0 |
| I (R0) | Positivo (alveolar) | 36,0 |
| II, linfonodo-negativo (R1) | Qualquer | 36,0 (doença pré-quimioterapia) |
| II, linfonodo-positivo (ressecado) | Qualquer | 41,4 (sítio + região nodal pré-quimioterapia) |
| III, não orbital / orbital com resposta incompleta | Qualquer | 50,4* |
| III, orbital com resposta completa | Qualquer | 45,0** |
| III, tumores >5 cm sem RC (ARST1431) | Qualquer | 59,4* |
| III, RC comprovada na semana 9 (ARST1431) | Qualquer | 36,0*** |
| Extremidade, N0, pós-amputação | Qualquer (incluindo alveolar/fusão-positivo) | 0 |
*Redução de volume pode ser feita após 36 Gy, com cone-down de 14,4 ou 23,4 Gy dependendo do tamanho tumoral (>5 cm). **RC na semana 9 permite dose única de 36 Gy ao PTV1 sem boost. ***RC radiográfica + metabólica ou biópsia negativa na semana 9. Fonte: Target Volume Delineation and Field Setup, 2nd Edition
Classificação Molecular e Implicações na Dosimetria do RMS
A classificação histológica do RMS está migrando de um modelo puramente morfológico — embrionário (menor risco) versus alveolar (maior risco) — para uma definição molecular baseada no status de fusão. Os protocolos atuais do COG utilizam o status de translocação envolvendo FOX01 (cromossomo 13) como marcador de risco: as fusões PAX3-FOX01 e PAX7-FOX01, representadas por t(2;13) e t(1;13), associam-se a comportamento clínico de alto risco semelhante à histologia alveolar. Dados suportam que o RMS alveolar fusão-negativo se comporta de maneira similar ao RMS embrionário.
Na prática, essa classificação molecular impacta diretamente a prescrição de dose. Pacientes com ressecção completa (Grupo I, R0) e fusão negativa não necessitam de radioterapia. Em contrapartida, pacientes com ressecção completa mas fusão positiva recebem 36 Gy. Para doença macroscópica residual (Grupo III), o protocolo ARST1431 introduz escalas de dose que podem atingir 59,4 Gy em tumores maiores que 5 cm sem resposta completa à quimioterapia de indução.
Casos Clínicos Ilustrativos de Delineamento
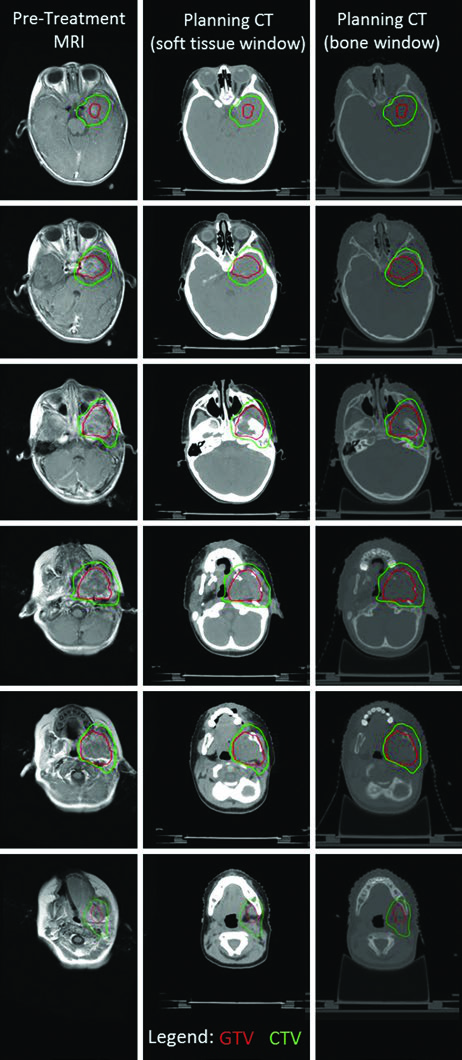
O caso de RMS parameníngeo da fossa infratemporal ilustra a complexidade do delineamento em lesões com extensão intracraniana. A fusão de RM T1 pós-contraste com TC de simulação permitiu identificar tanto a invasão intracraniana quanto a erosão óssea da mandíbula e da placa pterigoide esquerda. A extensão intracraniana motivou o início precoce da terapia local concomitante à quimioterapia, com tratamento em dose única. Máscara termoplástica e guiamento diário por kV permitiram margem de PTV de apenas 3 mm, e o PTV recebeu 50,4 Gy.
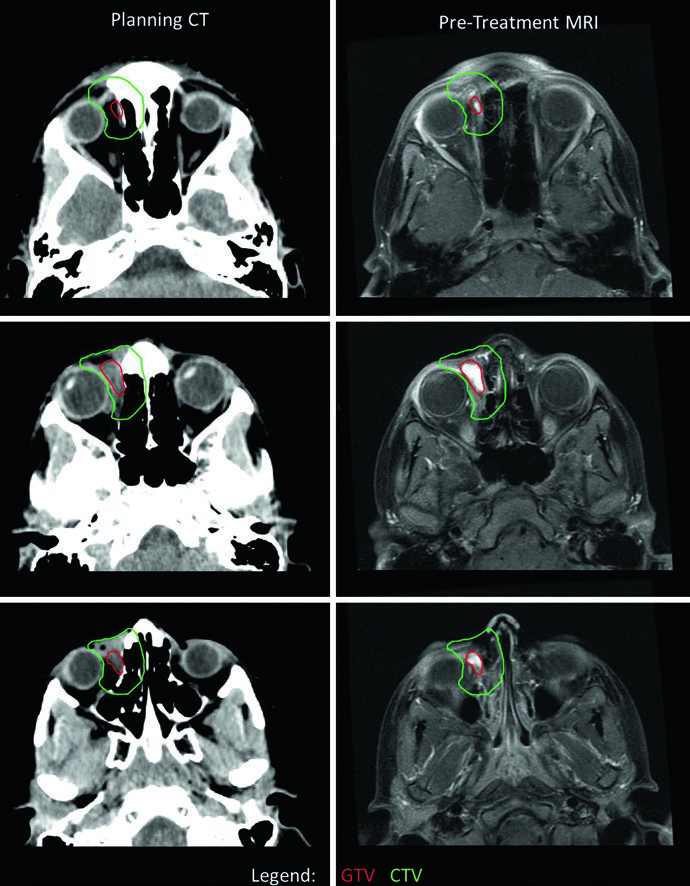
No RMS orbital, o delineamento exige atenção à preservação de estruturas oculares. Neste caso, a CTV se estendeu além da órbita óssea em alguns cortes por suspeita de erosão óssea — em geral, o CTV de RMS orbital não deve exceder os limites da órbita óssea na ausência de erosão. Um desvio lateral do olho direito foi utilizado para otimizar a preservação do cristalino e do nervo óptico. Como o tumor respondeu minimamente à quimioterapia de indução, optou-se por dose única de 50,4 Gy. Se houvesse resposta, seriam utilizados dois níveis: 36 Gy com cone-down para 50,4 Gy. Para comparação com tumores benignos e malignos do SNC que também exigem planejamento cuidadoso ao redor de estruturas oculares, consulte nosso artigo sobre tumores malignos do SNC.
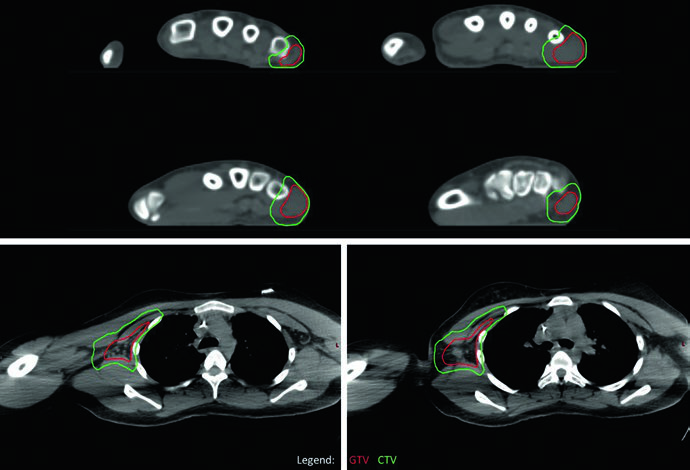
O caso de RMS alveolar (fusão-positivo) de extremidade superior com adenopatia axilar bilateral destaca a abordagem quando há metástases nodais regionais. Toda a bacia axilar direita foi contornada como GTV para garantir cobertura completa, dado o envolvimento extenso identificado no PET. O sítio primário na mão respondeu minimamente e recebeu dose única de 50,4 Gy; a bacia axilar, apesar de resposta parcial, também recebeu 50,4 Gy em nível único pela difusividade do envolvimento. Não foram identificados sítios de doença em trânsito entre mão e axila, e portanto o braço intermediário não foi tratado.
Simulação, Imobilização e Localização Diária
A imobilização durante a simulação varia conforme a localização anatômica. Para lesões de cabeça e pescoço, máscara termoplástica de cabeça e ombro é o padrão. Lesões torácicas (incluindo vertebrais torácicas) posicionam os braços elevados com wingboard e VacLok ou dispositivo semelhante. Tumores pélvicos são imobilizados com VacLok para pelve e membros inferiores. Lesões de extremidade podem exigir VacLok customizado, posicionamento pés-primeiro e, em casos selecionados, decúbito não supino.
Quando há preocupação com movimento respiratório, a simulação 4DCT é indicada para avaliar a excursão dos volumes-alvo com a respiração. Para lesões pélvicas geniturinárias, o enchimento vesical pode ser relevante — simulação com bexiga cheia e vazia pode fornecer a extensão completa da excursão do volume-alvo. Em pacientes masculinos com sarcomas pélvicos ou de perna proximal, o posicionamento em “pernas de rã” pode ser utilizado se escudo testicular for empregado.
O tipo e frequência de guiamento por imagem determinam a margem CTV-PTV. Muitas instituições utilizam kV diário e consequentemente margens de PTV de 3 a 5 mm. Margens menores podem ser consideradas em cenários com guiamento mais robusto ou proximidade de estruturas críticas — situação frequente em sarcomas de cabeça e pescoço, onde nervos ópticos, tronco encefálico e outras estruturas estão próximas aos volumes-alvo. A simulação por RM pode complementar a TC para fornecer dados de RM na posição de tratamento. Em pacientes mais jovens — geralmente abaixo de 8 anos — sedação ou anestesia diária pode ser necessária. Para planejamento de outros tumores pediátricos no SNC que também requerem imobilização rigorosa, confira nosso artigo sobre tumores cerebrais pediátricos.
Restrições de Dose e Avaliação do Plano
A avaliação do plano radioterápico nos sarcomas pediátricos segue princípios gerais de cobertura: ao menos 95% do PTV (ou PTVs) deve receber a dose prescrita, com minimização de hotspots acima de 110% — idealmente, no máximo 10% do PTV recebendo 110% ou mais.
Restrições de Dose aos Órgãos em Risco
Estas restrições são referências gerais dos protocolos COG para EWS e RMS. Dada a vulnerabilidade da população pediátrica a toxicidades tardias, esforços adicionais de preservação de OARs são fortemente encorajados.
| Órgão/Tecido | Volume (%) | Dose (Gy) |
|---|---|---|
| Tronco encefálico | Dose máxima pontual | 54 |
| Quiasma/nervo óptico | Dose máxima pontual | 54 |
| Medula espinhal | Dose máxima pontual | 45 |
| Cristalino | Dose máxima pontual | 6 |
| Cóclea | Dose máxima pontual | 35 |
| Coração | 100 | 30 |
| Pulmões (bilateral) | V20 | 20 |
| Pulmões (bilateral) | 100 | 15 |
| Fígado | 100 | 23,4 |
| Fígado | 50 | 30 |
| Rim (bilateral) | 50 | 24 |
| Rim (bilateral) | 100 | 14,4 |
| Intestino delgado | 50 | 45 |
| Bexiga | 100 | 45 |
| Reto | 100 | 45 |
Fonte: Target Volume Delineation and Field Setup, 2nd Edition
É importante salientar que essas restrições são pontos de partida. Pacientes pediátricos carregam riscos profundos de toxicidades tardias da radioterapia, e esforços adicionais para maximizar a preservação dos órgãos em risco devem ser feitos sempre que possível.
Efeitos Tardios e Papel da Próton-Terapia
A avaliação do plano deve orientar o aconselhamento de pacientes e familiares sobre efeitos agudos e tardios. O sarcoma de Ewing carrega taxa de malignidades secundárias superior à da maioria dos cânceres pediátricos — um fator que deve pesar na escolha da técnica de irradiação.
Os efeitos tardios são sítio-específicos. Em sarcomas de cabeça e pescoço: anormalidades dentofaciais, xerostomia, xeroftalmia, diminuição da acuidade visual, cataratogênese, assimetria facial, endocrinopatias e disfunção neurocognitiva. Em extremidades: fechamento epifisário precoce e assimetria esquelética por diminuição do crescimento ósseo. Em pacientes recebendo RT vertebral: perda de altura e risco de cifose, lordose e escoliose — minimizados com cobertura do corpo vertebral completo em crianças pré-púberes. Em RT torácica: pneumonite e fibrose pulmonar, cardiotoxicidade. Em RT pélvica: cistite, incontinência urinária ou estenose, e infertilidade — que também deve ser considerada em função dos quimioterápicos utilizados, em particular a ciclofosfamida.
Nesse contexto, modalidades como a próton-terapia podem ser consideradas para pacientes pediátricos, com potencial de reduzir a dose integral e preservar tecidos normais. Técnicas de feixe de prótons, incertezas de alcance, arranjos de feixes e demais particularidades devem ser discutidas com físicos médicos e médicos experientes no uso dessa tecnologia em malignidades pediátricas.