O Monte Carlo deixou de ser exclusividade de centros de pesquisa. Hoje, sistemas de planejamento como Monaco (Elekta), iPlan (BrainLab) e até opções dentro do Eclipse (Varian) oferecem cálculo de dose baseado em simulação estocástica — e a alternativa determinística Acuros XB traz precisão comparável com tempo de cálculo drasticamente menor. Neste artigo, exploramos como o método Monte Carlo funciona no contexto clínico, quais códigos MC sustentam os TPS comerciais e por que a equação de transporte de Boltzmann resolvida pelo Acuros XB representa uma virada de jogo para a rotina do físico médico.
Para uma visão completa da evolução dos algoritmos — dos métodos empíricos até as técnicas de convolução — confira nosso guia completo sobre algoritmos de cálculo de dose por fótons.
Monte Carlo na Radioterapia: Por Que Simular Partícula por Partícula?
O Monte Carlo resolve numericamente a equação de transporte de Boltzmann rastreando milhões de partículas individuais. Diferente dos algoritmos analíticos que aproximam o transporte com kernels ou pencil beams, o MC reproduz cada interação fóton–elétron segundo as seções de choque conhecidas. O resultado é a distribuição de dose mais precisa que se pode obter computacionalmente.
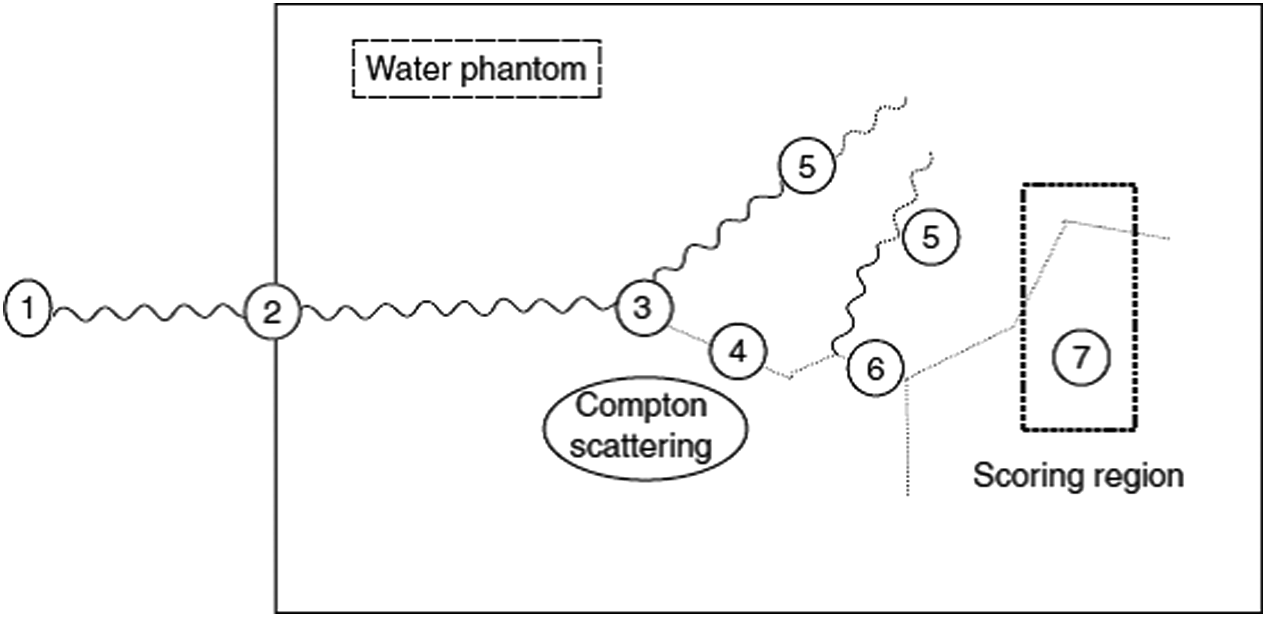
A simulação começa com o espaço de fase (phase-space) — energia, posição e direção de cada partícula. Um fóton de 1 MeV sofre em média 14–15 interações em água antes da absorção fotoelétrica. Cada interação é selecionada por amostragem aleatória da função de distribuição de probabilidade cumulativa (CPD): produção de pares, espalhamento Compton, absorção fotoelétrica e espalhamento Rayleigh. A distância até a próxima interação segue:
$$x = -\frac{1}{\mu_{tot}} \ln(1 – R)$$
Onde:
- $\mu_{tot}$ = coeficiente de atenuação total do meio (soma de todos os processos de interação)
- $R$ = número aleatório uniformemente distribuído entre 0 e 1
Para elétrons, a situação muda radicalmente. Um elétron de 10 MeV em oxigênio tem alcance CSDA de 5,6 g/cm² e sofre entre $10^5$ e $10^6$ interações antes de perder toda sua energia cinética. Simular cada uma dessas interações individualmente seria computacionalmente proibitivo.
Transporte de Elétrons por História Condensada
A solução veio com Berger (1963): o método de história condensada. A ideia é agrupar milhares de interações de pequeno efeito em poucos “passos” virtuais de grande efeito. Na prática, entre as chamadas colisões “catastróficas” — criação de raios delta e fótons de bremsstrahlung acima de certos limiares — o elétron perde energia continuamente segundo o stopping power restrito.
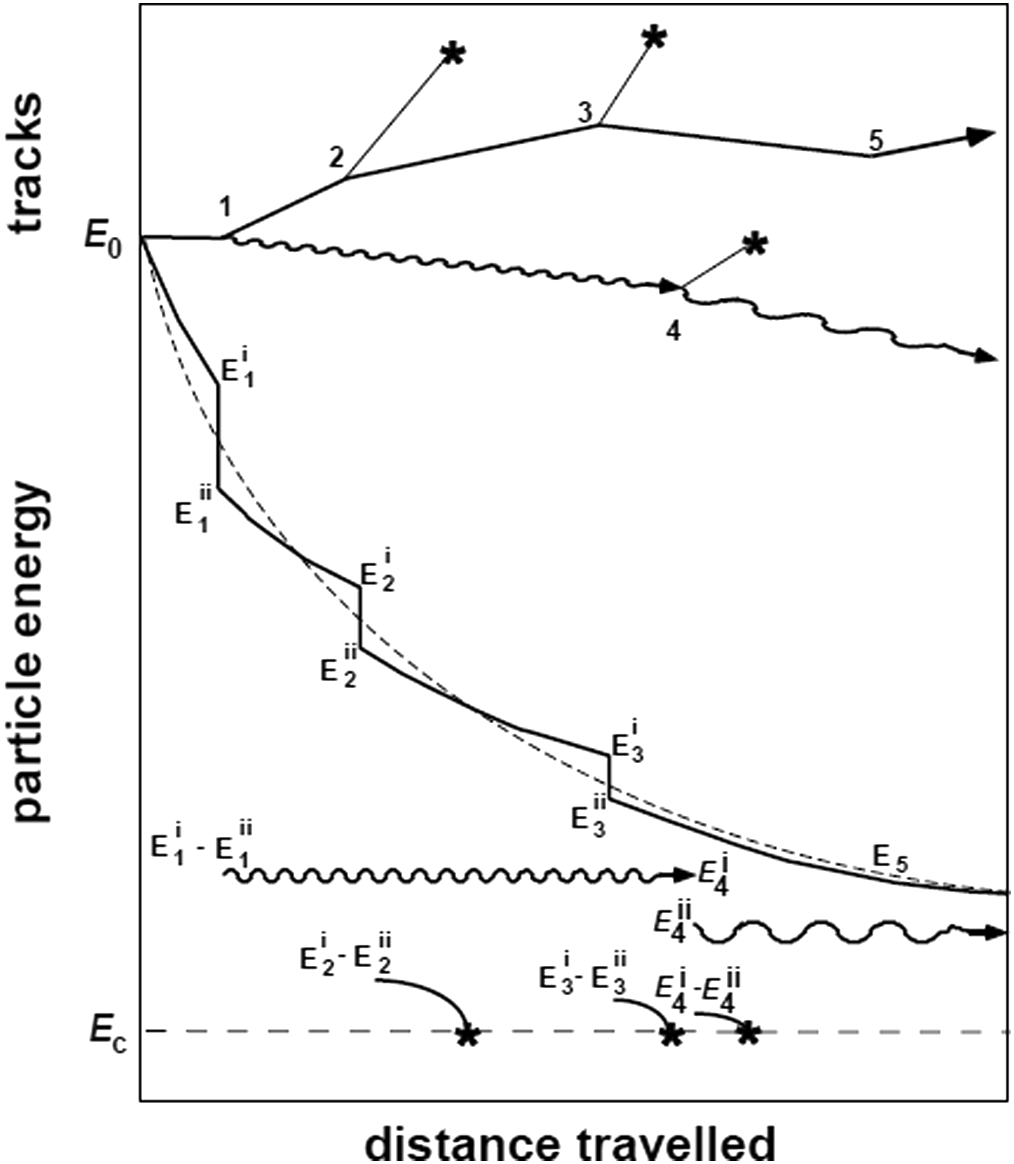
Berger classificou essa abordagem como simulação “Classe II”: híbrida entre transporte contínuo e amostragem analógica de eventos discretos. Os cutoffs de energia controlam o balanço entre precisão e velocidade. No EGSnrc, o parâmetro ECUT define a energia cinética abaixo da qual o elétron é “absorvido localmente” — tipicamente escolhido para que o alcance CSDA nessa energia seja cerca de 1/3 da menor dimensão do voxel. Já o ESTEPE limita a fração máxima de perda de energia por passo condensado (valor típico: 4%).
Sem história condensada, o transporte de partículas carregadas exigiria recursos da ordem de teraflops ($10^{12}$ operações/segundo) para a maioria dos problemas práticos. Na prática, a história condensada é a técnica de redução de variância mais importante em aplicações de radioterapia.
Transporte Acoplado Fóton–Elétron
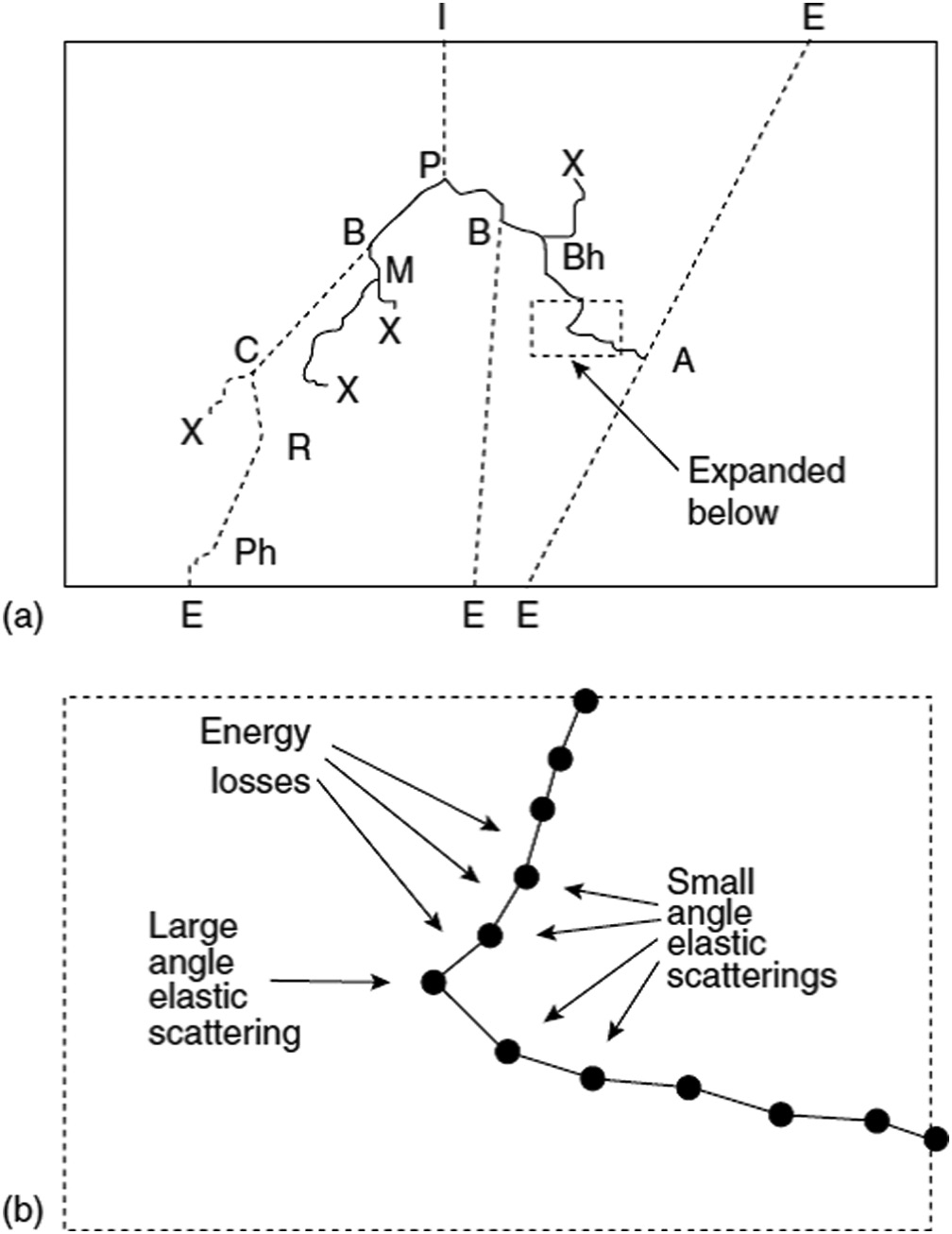
Fótons transferem energia através de elétrons secundários — logo o transporte dos dois tipos de partícula precisa ser acoplado. A Figura 30.5 ilustra uma história completa: um fóton entra na geometria e sofre produção de pares (P). O elétron resultante gera bremsstrahlung (B), enquanto o fóton espalhado sofre Compton (C), Rayleigh (R) e absorção fotoelétrica (Ph). O pósitron aniquila-se (A) gerando dois fótons de 511 keV que escapam da geometria.
Na prática clínica, esse acoplamento é o que permite ao Monte Carlo capturar corretamente efeitos como a falta de equilíbrio de partículas carregadas em campos pequenos e interfaces de densidade — situações onde algoritmos como pencil beam e AAA podem falhar significativamente.
Técnicas de Redução de Variância no Monte Carlo
A incerteza estatística de uma simulação MC diminui com $1/\sqrt{N}$, onde $N$ é o número de histórias. Dobrar a precisão exige quadruplicar o tempo de cálculo. As técnicas de redução de variância (VRT) contornam esse gargalo modificando a simulação para obter menor variância sem aumentar o número de histórias.
A eficiência $\varepsilon$ de uma simulação é definida como:
$$\varepsilon = \frac{1}{[s(N)]^2 \cdot T(N)}$$
Onde $[s(N)]^2$ é a variância estimada e $T(N)$ o tempo total de cálculo. O objetivo das VRTs é aumentar $\varepsilon$ reduzindo $s(N)$, $T(N)$, ou ambos.
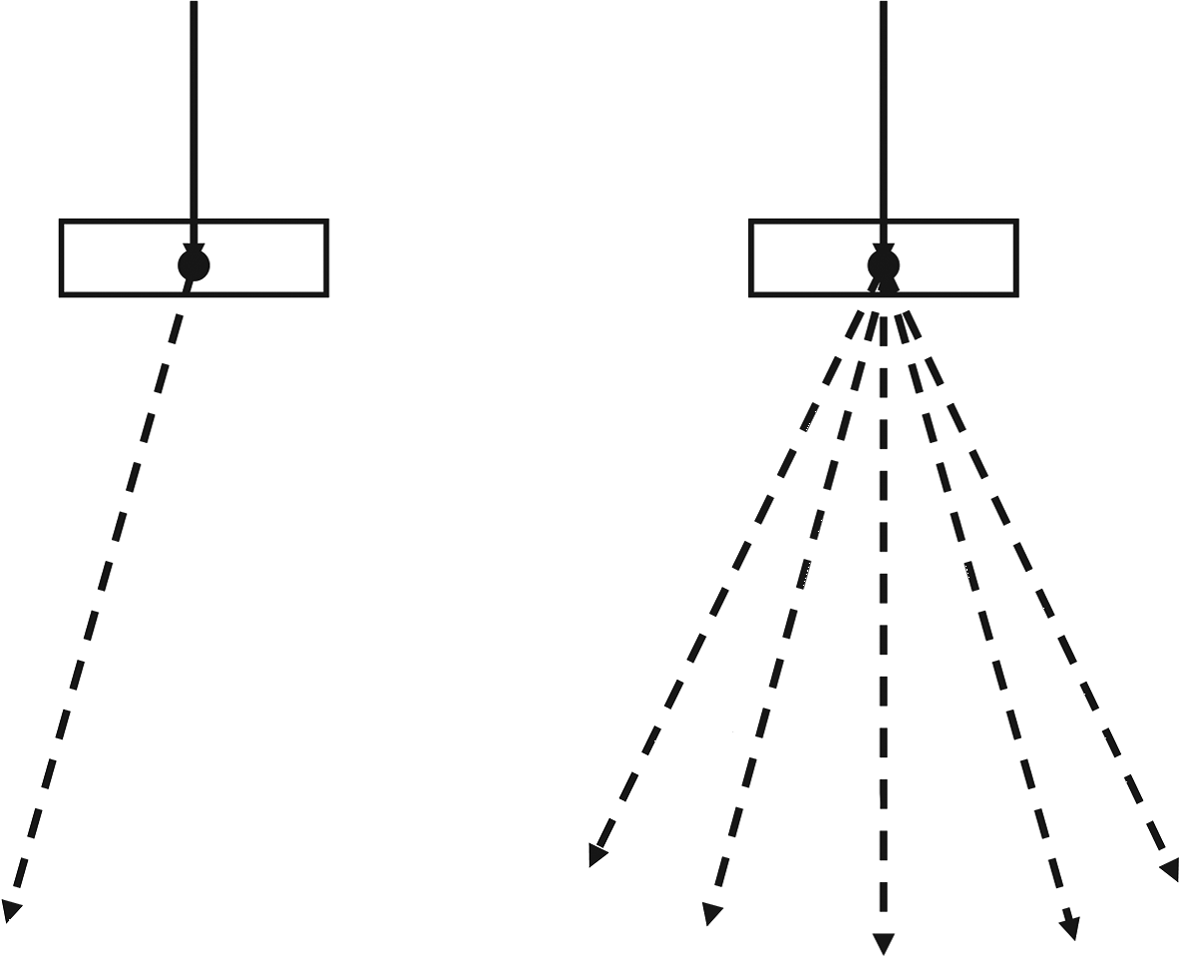
As VRTs mais utilizadas na simulação de cabeçotes de aceleradores incluem:
- Splitting uniforme de partículas: em vez de gerar 1 fóton de bremsstrahlung com peso $w = 1$, geram-se $N_{split}$ fótons independentes com peso $w = 1/N_{split}$ cada. A Figura 30.7 mostra o conceito com $N_{split} = 5$.
- Forçamento de interação (interaction forcing): fótons são forçados a interagir dentro da região de interesse. O número de caminhos livres médios $\lambda$ até o ponto de interação é dado por: $\lambda = -\ln\left[1 – R(1 – e^{-\Lambda})\right]$, onde $\Lambda = \sum_{Start}^{Stop} \mu_i s_i$.
- Amostragem correlacionada: pré-calcula-se o transporte na região externa (constante) e repete-se apenas o transporte na região variável para cada geometria diferente.
- Roleta russa: elimina partículas de baixo peso estatístico, compensando com aumento proporcional do peso dos sobreviventes.
Códigos MC e Implementações em TPS Comerciais
O físico médico moderno não precisa escrever seu próprio código MC. Décadas de desenvolvimento resultaram em pacotes poderosos, muitos deles gratuitos. A tabela abaixo resume os principais códigos utilizados em física médica.
Principais Códigos Monte Carlo em Física Médica
| Código | Características Principais | Aplicação |
|---|---|---|
| EGSnrc / BEAMnrc | Código mais citado em física médica; transporte elétron–fóton com controle fino de história condensada | Pesquisa; modelagem de cabeçotes (BEAMnrc); dose no paciente (DOSXYZnrc) |
| MCNP | Inclui transporte de nêutrons; uso extensivo em indústria nuclear | Física médica; blindagem; braquiterapia |
| GEANT4 | Toolkit multi-partícula abrangente; crescente uso médico | Pesquisa; protonterapia; PET/SPECT |
| VMC++ / XVMC | Otimizado para velocidade com “electron-track repeating” | Oncentra/Masterplan (Elekta); Monaco; XiO |
| PENELOPE | Transporte eletrônico sofisticado | Pesquisa; PRIMO (verificação livre) |
| DPM | Passos condensados grandes cruzando interfaces de materiais | TPS Pinnacle (Philips) |
| MMC (Macro MC) | Semi-numérico, transporte híbrido rápido de elétrons | Eclipse (Varian) — feixes de elétrons |
| PEREGRINE | Desenvolvido para planejamento em radioterapia | Corvus (Best NOMOS) |
Fonte: Handbook of Radiotherapy Physics: Theory and Practice, 2nd Ed. (CRC Press, 2020) (Table 30.1)
Os TPS comerciais geralmente usam um modelo de fonte virtual (VSM) em vez de simular o cabeçote inteiro do acelerador. O VSM reconstrói o espaço de fase a partir de parâmetros ajustados durante o commissioning, evitando a necessidade de arquivos de phase-space de vários gigabytes.
TPS Comerciais com Monte Carlo
| TPS / Sistema | Tipo | Simulação do LINAC | Dose no Paciente | Disponibilidade |
|---|---|---|---|---|
| Monaco (Elekta) | Planejamento | VSM | XVMC (rápido) | Comercial |
| Eclipse — elétrons (Varian) | Planejamento | VSM | MMC (pré-calculado) | Comercial |
| iPlan (BrainLab) | Planejamento | VSM | XVMC (rápido) | Comercial |
| Oncentra (Elekta) | Planejamento | VSM | VMC++ (rápido) | Comercial |
| Pinnacle (Philips) | Planejamento | — | DPM (rápido) | Comercial |
| XiO (Elekta) | Planejamento | VSM | XVMC (rápido) | Comercial |
| PRIMO | Verificação | PENELOPE (completo) | PENELOPE | Gratuito |
| PLanUNC | Verificação | EGSnrc (completo) | EGSnrc | Gratuito |
Fonte: Handbook of Radiotherapy Physics: Theory and Practice, 2nd Ed. (CRC Press, 2020) (Table 30.2, adaptada)
Monte Carlo Clínico: Dose por MU e Dose-to-Medium
Duas questões práticas distinguem o MC clínico do MC de pesquisa. A primeira é a relação dose por unidade monitora (MU). No MC, a dose é calculada por partícula simulada — para converter em Gy/MU, é necessário normalizar usando a dose em condições de referência (campo 10×10 cm², profundidade de referência, SSD ou SAD definida). Essa calibração garante consistência com a dosimetria absoluta do serviço.
A segunda questão é a escolha entre dose-to-medium ($D_m$) e dose-to-water ($D_w$). O MC naturalmente calcula $D_m$ — a dose depositada no material real do voxel (osso, pulmão, tecido mole). Para converter em $D_w$, aplica-se a razão de stopping powers água/meio:
$$D_w = D_m \cdot \left(\frac{S}{\rho}\right)_{meio}^{água}$$
Na prática, a diferença entre $D_w$ e $D_m$ é clinicamente significativa apenas em osso (até 5–10%) e pode influenciar a interpretação de DVHs em casos de cabeça e pescoço ou coluna.
Por Que o MC Ainda Não Domina a Rotina Clínica?
Precisão sem precedentes tem um preço: tempo de cálculo. Por volta de 1990, estimava-se que um plano de tratamento por fótons levaria centenas de horas com o hardware disponível. Hoje, com processadores multicore e GPUs, o MC clínico é viável para feixes de elétrons e aproxima-se da viabilidade plena para fótons.
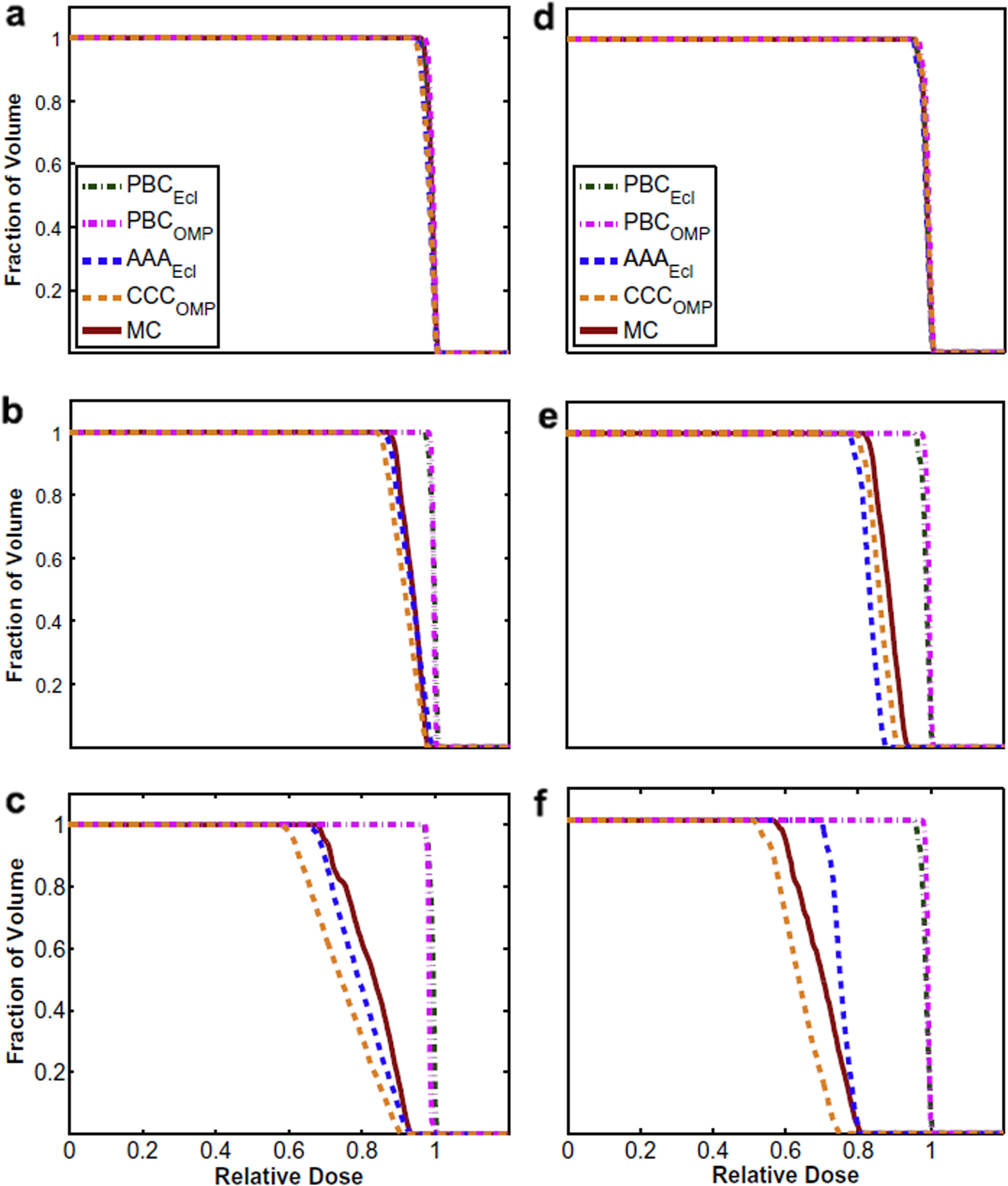
A Figura 30.13 mostra DVHs para um tumor pulmonar calculados com diferentes algoritmos. Com densidade pulmonar de 1,0 g/cm³, todos concordam. À medida que a densidade cai para 0,4 e depois 0,1 g/cm³, os algoritmos pencil beam superestimam severamente a dose tumoral, enquanto MC e Collapsed Cone Convolution convergem para o mesmo resultado. Em 18 MV e densidade 0,1 g/cm³, a discrepância do pencil beam ultrapassa 20%.
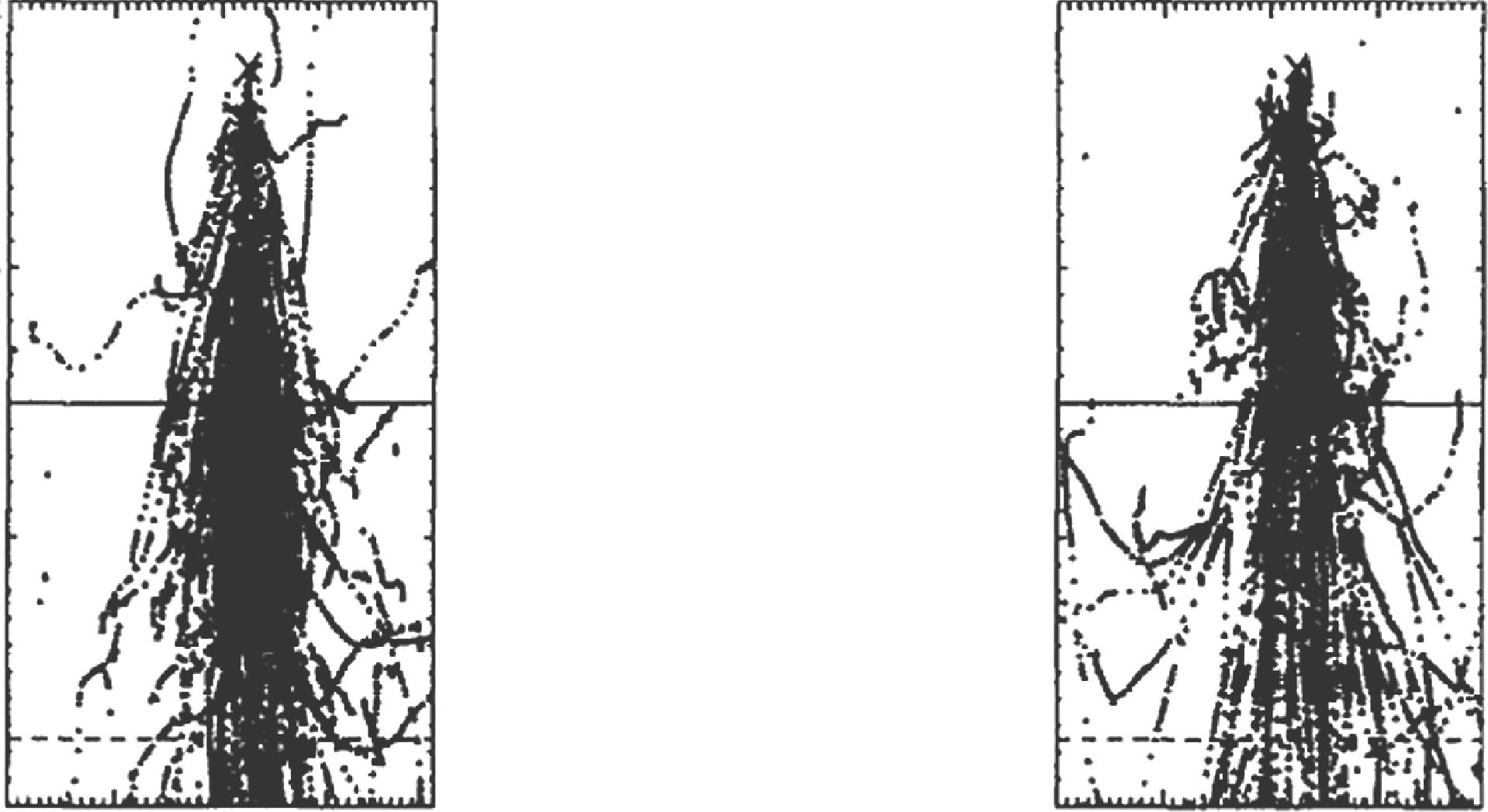
A razão fundamental dessa superioridade está na Figura 30.12: o scaling retilíneo de kernels (usado por algoritmos de convolução) assume que a distribuição de dose depende apenas da densidade média entre o ponto de interação e o de deposição. O MC mostra que a ordem das densidades importa — um fóton que cruza primeiro tecido denso e depois pulmão gera um padrão de elétrons diferente do caminho inverso. Para saber mais sobre os fundamentos da superposição e TERMA, confira nosso artigo dedicado.
A Equação Linear de Transporte de Boltzmann (LBTE): Fundamentos Matemáticos
Enquanto o Monte Carlo resolve a equação de transporte de forma estocástica — simulando histórias individuais de partículas —, o Acuros XB adota a abordagem determinística: resolve a LBTE diretamente sobre uma grade computacional. Para compreender o Acuros, é essencial entender a equação que ele resolve.
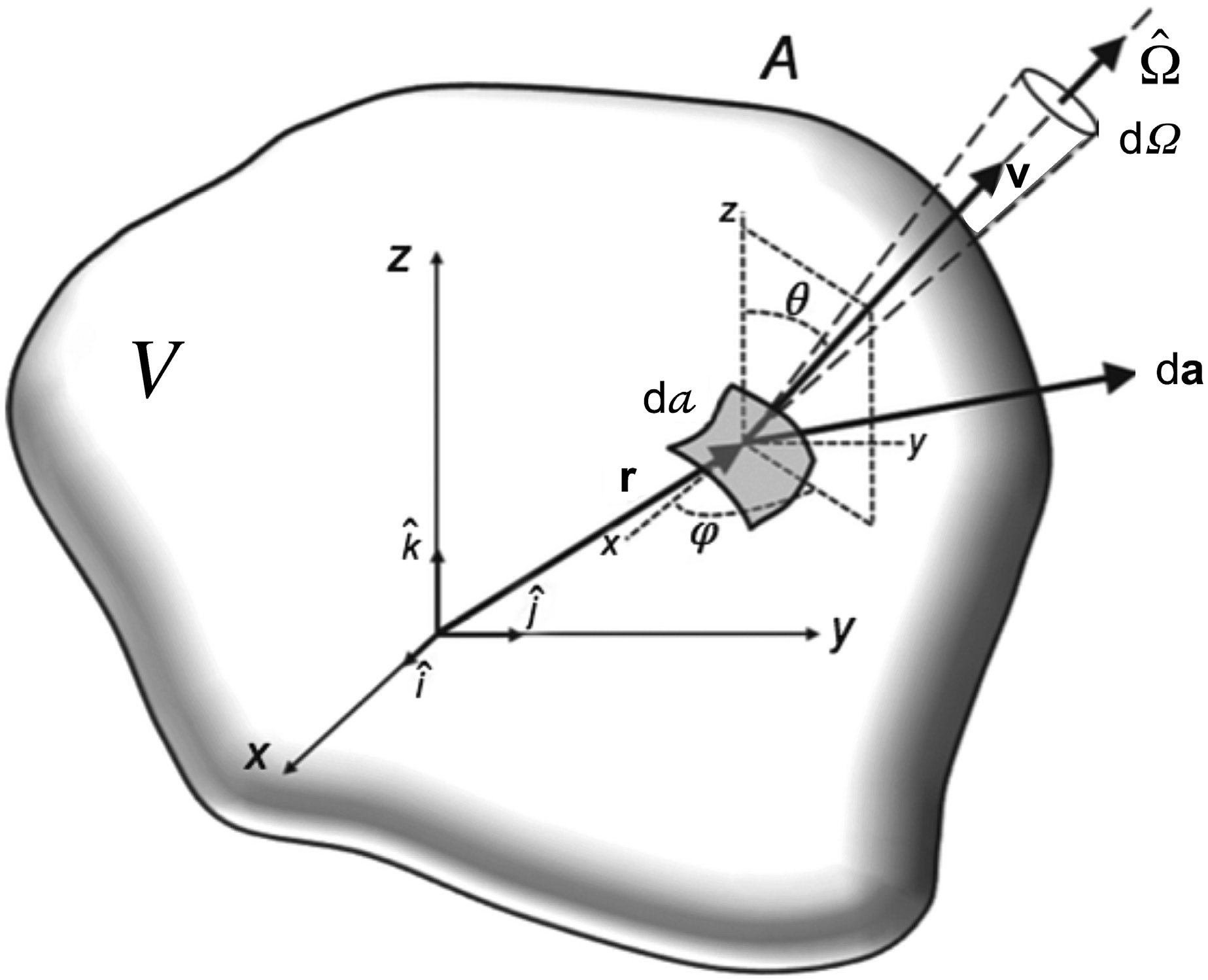
A equação linear de transporte de Boltzmann descreve a conservação de partículas em um meio. Na sua forma mais geral, para uma partícula de tipo $p$ com energia $E$ viajando na direção $\hat{\Omega}$ a partir da posição $\vec{r}$:
$$\hat{\Omega} \cdot \nabla \psi_p(\vec{r}, E, \hat{\Omega}) + \sigma_{t,p}(\vec{r}, E)\, \psi_p(\vec{r}, E, \hat{\Omega}) = q_p(\vec{r}, E, \hat{\Omega})$$
Onde:
- $\psi_p(\vec{r}, E, \hat{\Omega})$ = fluência angular da partícula tipo $p$ (fótons ou elétrons) na posição $\vec{r}$, energia $E$ e direção $\hat{\Omega}$
- $\sigma_{t,p}(\vec{r}, E)$ = seção de choque macroscópica total (probabilidade de interação por unidade de caminho)
- $q_p(\vec{r}, E, \hat{\Omega})$ = termo-fonte total, que inclui espalhamento (scattering-in), produção de partículas secundárias e fontes externas
- $\hat{\Omega} \cdot \nabla$ = operador de streaming (deriva espacial ao longo da direção de voo)
O primeiro termo ($\hat{\Omega} \cdot \nabla \psi$) descreve o transporte livre de partículas ao longo da direção $\hat{\Omega}$. O segundo termo ($\sigma_t \psi$) representa as perdas por interação — tanto absorção quanto espalhamento para fora do feixe angular considerado. O lado direito ($q_p$) agrupa todas as fontes de partículas naquele ponto do espaço de fase.
O termo-fonte é a peça mais complexa da equação, pois acopla diferentes tipos de partículas e diferentes energias:
$$q_p(\vec{r}, E, \hat{\Omega}) = \sum_{p’} \int_0^{\infty} \int_{4\pi} \sigma_{s,p’ \to p}(\vec{r}, E’ \to E, \hat{\Omega}’ \to \hat{\Omega})\, \psi_{p’}(\vec{r}, E’, \hat{\Omega}’)\, d\hat{\Omega}’\, dE’ + q_{ext,p}(\vec{r}, E, \hat{\Omega})$$
Aqui, $\sigma_{s,p’ \to p}$ é o kernel de espalhamento diferencial que descreve a probabilidade de uma partícula de tipo $p’$ com energia $E’$ e direção $\hat{\Omega}’$ produzir uma partícula de tipo $p$ com energia $E$ e direção $\hat{\Omega}$. O somatório sobre $p’$ acopla fótons e elétrons: fótons Compton geram elétrons, elétrons geram bremsstrahlung, e assim por diante.
Transporte Acoplado Fóton–Elétron na LBTE
Para feixes clínicos de megavoltagem, a LBTE se desdobra em um sistema acoplado. O transporte de fótons segue:
$$\hat{\Omega} \cdot \nabla \psi_\gamma + \sigma_{t,\gamma}\, \psi_\gamma = \int_0^{\infty} \int_{4\pi} \sigma_{s,\gamma \to \gamma}\, \psi_\gamma\, d\hat{\Omega}’\, dE’ + \int_0^{\infty} \int_{4\pi} \sigma_{s,e \to \gamma}\, \psi_e\, d\hat{\Omega}’\, dE’ + q_{ext,\gamma}$$
O primeiro termo integral no lado direito representa fótons espalhados (Compton, Rayleigh). O segundo representa bremsstrahlung e aniquilação — fótons criados por elétrons. O transporte de elétrons é análogo, mas com termos-fonte vindos das interações fotoelétrica, Compton e produção de pares:
$$\hat{\Omega} \cdot \nabla \psi_e + \sigma_{t,e}\, \psi_e = \int_0^{\infty} \int_{4\pi} \sigma_{s,e \to e}\, \psi_e\, d\hat{\Omega}’\, dE’ + \int_0^{\infty} \int_{4\pi} \sigma_{s,\gamma \to e}\, \psi_\gamma\, d\hat{\Omega}’\, dE’$$
Este acoplamento bidirecional fóton ⇌ elétron é o que torna a LBTE tão poderosa — e tão difícil de resolver. O Monte Carlo resolve esse sistema amostrando histórias aleatórias; o Acuros XB o resolve discretizando todas as variáveis e iterando numericamente.
Da Fluência à Dose
Uma vez resolvida a fluência angular $\psi_e(\vec{r}, E, \hat{\Omega})$, a dose absorvida no material real do voxel é calculada integrando a fluência eletrônica sobre todas as energias e direções, ponderada pelo stopping power mássico de colisão:
$$D_m(\vec{r}) = \int_0^{\infty} \left(\frac{S_{col}(E)}{\rho}\right)_m \phi_e(\vec{r}, E)\, dE$$
Onde $\phi_e(\vec{r}, E) = \int_{4\pi} \psi_e(\vec{r}, E, \hat{\Omega})\, d\hat{\Omega}$ é a fluência escalar de elétrons e $(S_{col}/\rho)_m$ é o stopping power mássico de colisão no material $m$ do voxel. Para obter $D_w$, substitui-se o stopping power do material pelo da água:
$$D_w(\vec{r}) = \int_0^{\infty} \left(\frac{S_{col}(E)}{\rho}\right)_w \phi_e(\vec{r}, E)\, dE$$
Essa formulação é idêntica à usada pelo Monte Carlo para reportar dose — a diferença está apenas em como a fluência $\phi_e$ foi obtida: por amostragem estocástica (MC) ou por solução determinística (Acuros XB).
Monte Carlo vs. LBTE: Dois Caminhos para a Mesma Equação
É fundamental compreender que Monte Carlo e Acuros XB resolvem a mesma equação física — a LBTE. A diferença é metodológica:
- Monte Carlo (estocástico): gera histórias aleatórias de partículas, amostra interações segundo distribuições de probabilidade, e acumula dose em voxels de scoring. A precisão depende do número de histórias ($N$) — a incerteza estatística cai com $1/\sqrt{N}$. Cada história é independente, tornando o algoritmo naturalmente paralelizável.
- Acuros XB (determinístico): discretiza o espaço de fase em variáveis angulares, energéticas e espaciais, e resolve o sistema de equações resultante por iteração. Não há ruído estatístico — a solução converge para o resultado exato da LBTE discretizada conforme a malha é refinada. O erro é puramente de discretização, não estatístico.
Na prática, ambos produzem resultados concordantes dentro de 1–2% em cenários clínicos típicos. A escolha entre eles é guiada por considerações de velocidade, tipo de problema e infraestrutura disponível.
Acuros XB: Implementação e Discretização da LBTE
O Acuros XB (External Beam), desenvolvido originalmente pela Transpire Inc. e adquirido pela Varian para integração no Eclipse, resolve a LBTE através de uma cascata de etapas cuidadosamente ordenadas. A implementação decompõe o problema de transporte em componentes que são resolvidos sequencialmente.
Etapa 1: Transporte de Fótons Não-Colididos
A fluência primária — fótons que não sofreram nenhuma interação — é calculada por ray-tracing analítico a partir do modelo de fonte do acelerador. Cada raio é atenuado exponencialmente conforme atravessa os voxels do paciente, usando as seções de choque macroscópicas do material atribuído a cada voxel. A atenuação segue:
$$\psi_\gamma^{unc}(\vec{r}, E, \hat{\Omega}) = \psi_\gamma^{src}(E, \hat{\Omega}) \cdot \exp\left(-\int_0^s \sigma_{t,\gamma}(\vec{r}’, E)\, ds’\right)$$
Onde $s$ é a distância percorrida ao longo da direção $\hat{\Omega}$ desde a fonte até o ponto $\vec{r}$.
Etapa 2: Discretização Angular — Ordenadas Discretas ($S_N$)
A variável angular $\hat{\Omega}$ é discretizada usando o método de ordenadas discretas ($S_N$). A esfera unitária de direções é subdividida em um conjunto finito de direções $\hat{\Omega}_n$ com pesos de quadratura $w_n$, de modo que integrais sobre o ângulo sólido são aproximadas por:
$$\int_{4\pi} f(\hat{\Omega})\, d\hat{\Omega} \approx \sum_{n=1}^{N_{dir}} w_n\, f(\hat{\Omega}_n)$$
O Acuros XB utiliza tipicamente conjuntos de quadratura com 80 a 128 direções discretas — suficiente para capturar a anisotropia do transporte em feixes de radioterapia, incluindo espalhamento lateral e retrodifusão.
Etapa 3: Discretização Energética — Método Multigrupo
O espectro contínuo de energia é dividido em grupos discretos ($G$ grupos tipicamente). Para cada grupo $g$, as seções de choque são pré-calculadas e tabuladas como constantes $\sigma_{t,g}$ e $\sigma_{s,g’ \to g}$. A equação de transporte para o grupo $g$ na direção $\hat{\Omega}_n$ torna-se:
$$\hat{\Omega}_n \cdot \nabla \psi_g^n(\vec{r}) + \sigma_{t,g}(\vec{r})\, \psi_g^n(\vec{r}) = \sum_{g’=1}^{G} \sum_{n’=1}^{N_{dir}} w_{n’}\, \sigma_{s,g’ \to g}(\vec{r}, \hat{\Omega}_{n’} \to \hat{\Omega}_n)\, \psi_{g’}^{n’}(\vec{r}) + q_{ext,g}^n(\vec{r})$$
A estrutura multigrupo das seções de choque é derivada de bibliotecas nucleares padrão (semelhantes às usadas em reatores nucleares), adaptadas para as energias de interesse em radioterapia (keV a MeV). Materiais do paciente são atribuídos a partir de densidades CT usando tabelas de conversão HU-para-material com composições químicas conhecidas.
Etapa 4: Discretização Espacial — Diferenças Finitas na Grade do Paciente
O volume do paciente é discretizado na grade de cálculo do Eclipse (tipicamente 2,5 mm de resolução, embora resolução fina de até 1 mm esteja disponível). Para cada voxel, as equações multigrupo de ordenadas discretas são resolvidas usando esquemas de diferenças finitas que garantem conservação de partículas e positividade da fluência.
A varredura (sweep) espacial procede octante por octante: para cada direção discreta $\hat{\Omega}_n$, os voxels são varridos na sequência upstream-to-downstream, de modo que a fluência incidente em cada voxel já foi calculada nos voxels precedentes. Esse procedimento é altamente eficiente e pode ser paralelizado por octante.
Etapa 5: Transporte de Fótons Espalhados
A fonte de fótons espalhados é calculada a partir da fluência de fótons não-colididos (Etapa 1). Fótons Compton, Rayleigh e de aniquilação são transportados iterativamente: a cada iteração, a nova fluência espalhada contribui para uma nova fonte de espalhamento, até que a convergência é atingida.
Etapa 6: Fonte de Elétrons e Transporte Eletrônico
As interações fotoelétrica, Compton e produção de pares geram elétrons secundários. O Acuros XB calcula essa fonte de elétrons a partir da fluência total de fótons e então resolve a LBTE para elétrons, incluindo a perda contínua de energia (CSDA) e a produção de bremsstrahlung. A fluência eletrônica resultante é integrada para produzir a distribuição de dose final.
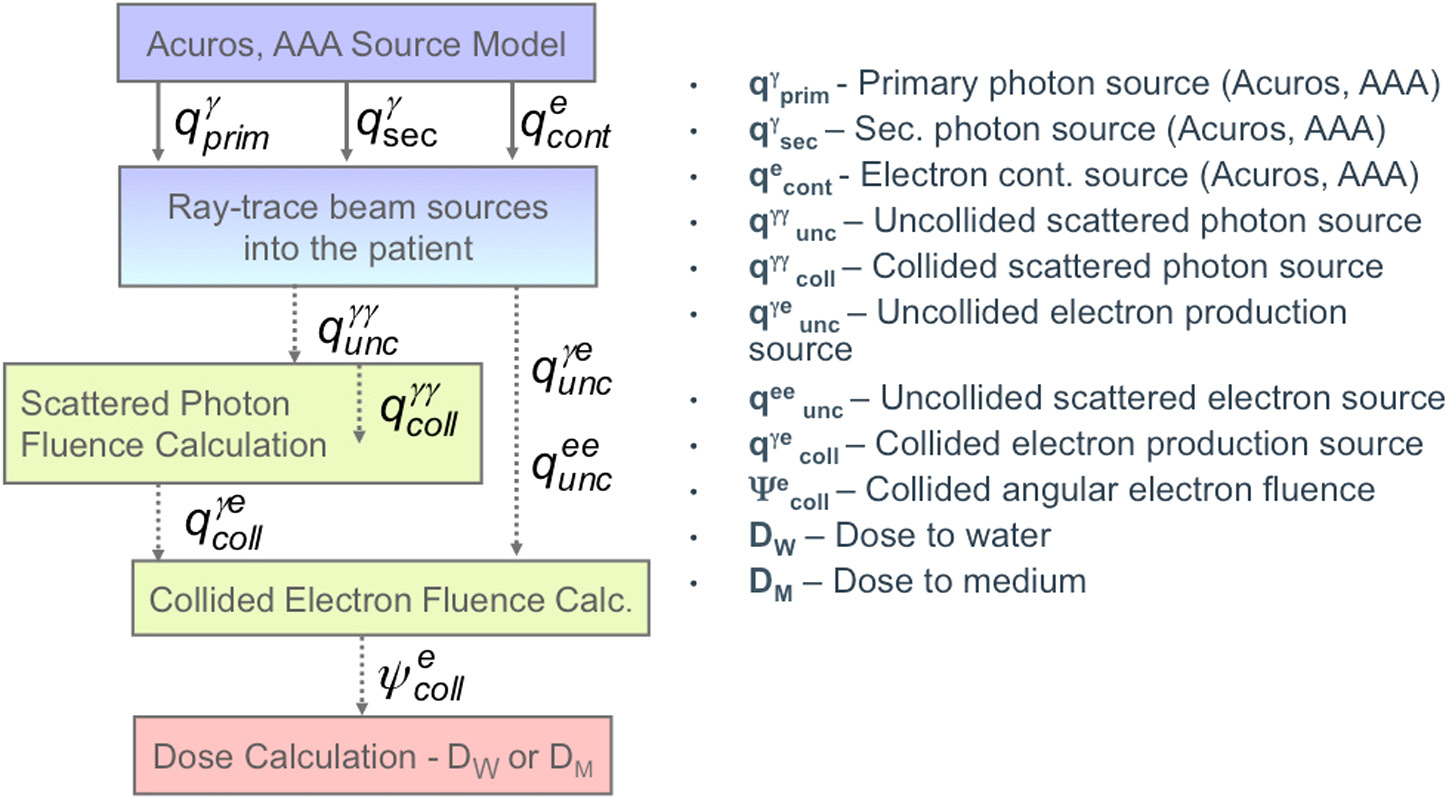
Modelo de Fonte e Commissioning
O Acuros XB utiliza o mesmo modelo de fonte de múltiplas fontes virtuais (multi-source model) do AAA: fonte primária (alvo), fonte de espalhamento extraprimário (filtro achatador, colimadores) e fonte de transmissão dos jaws/MLC. Os parâmetros são ajustados durante o commissioning a partir de dados dosimétricos medidos — PDDs, perfis e fatores de campo. Isso significa que clínicas que já comissionaram o AAA podem migrar para o Acuros XB sem necessidade de medidas adicionais.
Comparação Detalhada: Monte Carlo vs. Acuros XB
A tabela abaixo apresenta uma comparação direta entre Monte Carlo e Acuros XB nos aspectos que mais importam para a prática clínica:
| Aspecto | Monte Carlo | Acuros XB |
|---|---|---|
| Método | Estocástico — amostragem aleatória de histórias de partículas | Determinístico — solução numérica da LBTE em grade discreta |
| Ruído estatístico | Presente; diminui com $1/\sqrt{N}$. Requer ~$10^9$ histórias para incerteza < 1% | Ausente. Erro é de discretização (tamanho do voxel, quadratura angular, grupos de energia) |
| Tempo de cálculo (IMRT típico) | 5–30 min (GPU-acelerado) a horas (CPU) | 1–5 min (CPU multi-core padrão) |
| Precisão em meio homogêneo | Referência (gold standard) | Equivalente ao MC (< 1% diferença) |
| Precisão em pulmão | Referência | Dentro de 1–2% do MC na maioria dos cenários |
| Precisão em osso | Referência | Dentro de 1–2% do MC |
| Interfaces ar–tecido | Excelente (resolve desequilíbrio CPE) | Excelente (resolve LBTE explicitamente) |
| Campos pequenos (< 3×3 cm²) | Excelente | Excelente |
| Reporte $D_w$ / $D_m$ | Ambos (nativo $D_m$) | Ambos (nativo $D_m$) |
| Implantes metálicos | Excelente (composição real do material) | Bom (atribuição de material limitada a materiais da biblioteca) |
| Efeito de campo magnético (MR-LINAC) | Excelente (EGSnrc, GEANT4 com extensão magnética) | Suportado no Acuros XB v15.6+ para Unity (Elekta) |
| Geometrias muito complexas | Superior (sem aproximações de discretização angular) | Boa (resolução angular finita pode suavizar detalhes) |
| Pesquisa e cenários não-padrão | Flexibilidade total (geometrias arbitrárias, scoring personalizado) | Limitado ao que o TPS oferece |
| TPS comerciais | Monaco, iPlan, Oncentra, XiO, Pinnacle | Eclipse (Varian) — exclusivo |
Aplicações Clínicas Avançadas do Acuros XB
Estereotaxia Pulmonar (SBRT)
Na SBRT de pulmão, os campos são pequenos, as heterogeneidades são extremas (ar → tumor → ar) e o equilíbrio de partículas carregadas (CPE) não existe nas bordas do tumor. Estudos como Bush et al. (2011) e Fogliata et al. (2011) demonstraram que o Acuros XB concorda com o Monte Carlo dentro de 1–2% nessas condições, enquanto o AAA pode superestimar a cobertura tumoral em até 5–10% dependendo da densidade pulmonar e do tamanho do campo. O Acuros XB reportando dose-to-medium ($D_m$) captura corretamente a redução de dose nas interfaces ar–tumor.
Planejamento com MR-LINAC
Sistemas MR-LINAC como o Unity (Elekta) e o ViewRay MRIdian geram um campo magnético de 0,35–1,5 T que desvia a trajetória dos elétrons secundários via força de Lorentz. Isso altera a distribuição de dose, especialmente em interfaces ar–tecido — o chamado efeito de retorno eletrônico (electron return effect, ERE). O Acuros XB versão 15.6+ para Eclipse inclui extensão para campos magnéticos, resolvendo a LBTE com termos adicionais de deflexão. A força de Lorentz modifica o operador de transporte eletrônico:
$$\hat{\Omega} \cdot \nabla \psi_e + \sigma_{t,e}\, \psi_e + \frac{e}{p}(\vec{v} \times \vec{B}) \cdot \nabla_{\hat{\Omega}} \psi_e = q_e$$
Onde $\vec{B}$ é o campo magnético, $\vec{v}$ a velocidade do elétron, $e$ a carga elementar e $p$ o momento. O termo adicional $\nabla_{\hat{\Omega}}$ representa a rotação da direção de voo no espaço angular — essencial para capturar o ERE corretamente.
Implantes Metálicos de Alta Densidade
Próteses de quadril (titânio, cromo-cobalto), implantes dentários e marcadores fiduciais introduzem heterogeneidades extremas ($Z$ efetivo alto, densidade 4–8 g/cm³). O Acuros XB atribui composições de material a partir de tabelas HU-para-material e calcula seções de choque específicas para cada material. Para implantes com densidade muito alta (acima do range típico do CT), a atribuição pode ser limitada pela biblioteca de materiais do Acuros. Nesses casos, o Monte Carlo com geometria explícita do implante pode ser preferível.
Cabeça e Pescoço: Interfaces Osso–Ar
Tumores em cavidades nasais, seios paranasais e base de crânio envolvem interfaces frequentes entre osso, ar e tecido mole. O Acuros XB captura os efeitos de backscatter e perda de equilíbrio nessas interfaces com precisão muito superior à do AAA — e com tempo de cálculo compatível com a otimização inversa de IMRT/VMAT.
Por Que o Acuros XB Está Substituindo o AAA no Eclipse
Desde a versão 13.6 do Eclipse, a Varian posiciona o Acuros XB como o algoritmo preferencial para fótons. As razões são claras:
- Precisão: resolve a LBTE explicitamente, capturando heterogeneidades com precisão de MC.
- Velocidade: 2–5x mais rápido que MC para planos VMAT típicos.
- Sem ruído: resultado determinístico, sem artefatos de subamostragem.
- Dose-to-medium: reporta $D_m$ nativamente, alinhado com recomendações atuais.
- Commissioning simplificado: usa o mesmo modelo de fonte do AAA.
Na prática, serviços que migram do AAA para o Acuros XB frequentemente observam diferenças clinicamente relevantes (2–5%) em planos de pulmão, especialmente em SBRT com campos pequenos. Essa diferença pode afetar a cobertura do PTV e os limites de dose em OAR, justificando a recalibração de protocolos institucionais.
Comparação Completa: Monte Carlo vs. Acuros vs. Algoritmos Analíticos
| Característica | Monte Carlo | Acuros XB (LBTE) | AAA/CCC | Pencil Beam |
|---|---|---|---|---|
| Princípio | Simulação estocástica | Solução determinística da LBTE | Convolução/Superposição | Convolução 1D + correções |
| Precisão em heterogeneidades | Referência (gold standard) | Excelente (~1–2% do MC) | Boa (CCC > AAA) | Limitada |
| Campos pequenos | Excelente | Excelente | Boa (com limitações) | Pobre |
| Tempo de cálculo | Minutos–horas | Minutos | Segundos–minutos | Segundos |
| Ruído estatístico | Presente (diminui com mais histórias) | Ausente | Ausente | Ausente |
| $D_w$ vs $D_m$ | Ambos (nativo $D_m$) | Ambos | $D_w$ (nativo) | $D_w$ (nativo) |
| TPS disponíveis | Monaco, iPlan, Oncentra, XiO | Eclipse (Varian) | Eclipse (AAA), Oncentra (CCC) | Vários (legado) |
Compilação baseada no Handbook of Radiotherapy Physics: Theory and Practice, 2nd Ed. (CRC Press, 2020)
O Futuro do Cálculo de Dose em Radioterapia
A convergência de hardware cada vez mais barato — GPUs com milhares de cores, processadores multithread, cloud computing — está tornando o MC clinicamente viável para a rotina diária. O relatório TG-157 da AAPM (2020) já considera o MC como padrão-ouro para feixes de elétrons e próximo da viabilidade plena para fótons.
Na prática, dois cenários coexistem. Para clínicas que utilizam Eclipse, o Acuros XB oferece o melhor equilíbrio entre precisão e velocidade para cálculo de dose em fótons — especialmente em pulmão, cabeça e pescoço e estereotaxia. Para serviços com Monaco ou outros TPS baseados em XVMC/VMC++, o Monte Carlo já faz parte da rotina com tempos de cálculo aceitáveis.
O relatório TG-268 da AAPM (2018) estabeleceu diretrizes para relatar estudos baseados em MC, padronizando a documentação de parâmetros como cutoffs de energia, VRTs utilizadas e incertezas estatísticas. Essa padronização é essencial para garantir reprodutibilidade e comparabilidade entre estudos — e para que os resultados de pesquisa se traduzam de forma confiável na prática clínica.
O futuro aponta para algoritmos híbridos que combinam a robustez determinística do Acuros com aceleração por GPU e técnicas de deep learning para estimativa inicial de dose, reduzindo ainda mais o tempo de cálculo sem comprometer a precisão. Projetos de pesquisa em Monte Carlo acelerado por GPU (como gDPM e ARCHER) já demonstram cálculos de planos VMAT completos em menos de 1 minuto, aproximando o MC da viabilidade em tempo real para radioterapia adaptativa.
Para explorar outros aspectos do Monte Carlo em radioterapia, incluindo aplicações em protonterapia, braquiterapia e QA avançado, confira nossos artículos dedicados. Para uma introdução completa ao método Monte Carlo na radioterapia, veja nosso guia completo sobre Monte Carlo. E para entender como os métodos empíricos de cálculo de dose pavimentaram o caminho para essas técnicas sofisticadas, leia nossa análise da evolução dos algoritmos.
Este artigo faz parte da nossa série sobre algoritmos de cálculo de dose por fótons.


