Neste Artigo
Origem do Método Monte Carlo
O método Monte Carlo fornece soluções numéricas para problemas que podem ser descritos como a evolução temporal de objetos — no caso da física médica, partículas quânticas como fótons, elétrons, nêutrons e prótons — interagindo com outros objetos segundo relações de seção de choque. Na prática, o método simula diretamente a dinâmica microscópica de um sistema, reproduzindo aleatoriamente as interações até que os resultados convirjam para estimativas confiáveis de médias e variâncias.
Guia completo da série: para visão geral e links dos artigos relacionados, volte ao guia completo sobre Monte Carlo em radioterapia.
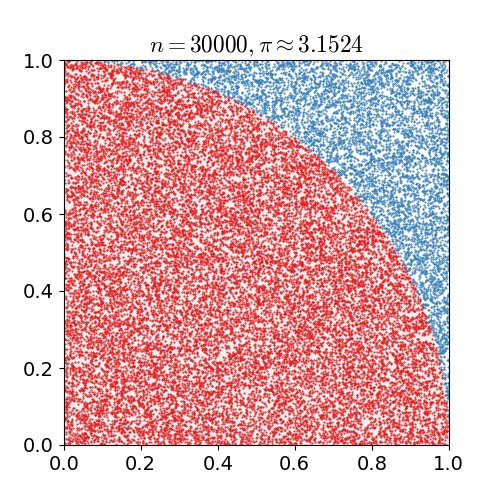
A ideia de amostragem estocástica não nasceu com os computadores. O Conde de Buffon propôs em 1777 um experimento que consistia em lançar repetidamente uma agulha sobre uma folha pautada para determinar a probabilidade de cruzar uma das linhas. Essa probabilidade é dada por:
$$p = \frac{2L}{\pi d}$$
Onde:
- $p$ = probabilidade de a agulha cruzar uma linha
- $L$ = comprimento da agulha
- $d$ = distância entre as linhas paralelas ($d > L$)
Laplace sugeriu mais tarde que esse procedimento poderia ser usado para determinar o valor de $\pi$, embora de forma bastante lenta. Mas o verdadeiro impulso veio de Stan Ulam. Recuperando-se de uma doença, ele jogava paciência repetidamente e se perguntou se poderia calcular a probabilidade de sucesso por análise combinatória — ou simplesmente jogando um número grande de partidas e contabilizando os resultados.
Ulam comunicou a ideia a John von Neumann, que na época trabalhava em cálculos teóricos para o desenvolvimento de armas termonucleares em Los Alamos. A primeira sugestão documentada de usar amostragem estocástica em cálculos de transporte de radiação surgiu em uma carta de von Neumann a Richtmyer em 11 de março de 1947. Pouco depois, Metropolis e Ulam publicaram o artigo fundador “The Monte Carlo Method” em 1949 — o primeiro trabalho não classificado a utilizar o nome “Monte Carlo” associado a amostragem estocástica.
Uma ironia notável emerge dessa história: um método matemático criado para o projeto da arma mais terrível da história — a bomba termonuclear, que nunca foi usada em conflito — acabou beneficiando milhões de pessoas através de suas aplicações na medicina.
Por Que Monte Carlo na Física Médica?
O método Monte Carlo é frequentemente visto como “competidor” dos métodos determinísticos e analíticos. Na realidade, um cientista pragmático deve sempre perguntar: o que quero realizar? Qual o caminho mais eficiente? Às vezes a resposta será “determinístico”; outras vezes, “Monte Carlo”.
Duas realidades são inescapáveis. A teoria de transporte fornece intuição profunda sobre como campos macroscópicos de partículas se comportam — nesse quesito, Monte Carlo não compete bem. Praticantes de Monte Carlo operam muito mais como experimentalistas, descobrindo propriedades por tentativa e erro. Contudo, quando a complexidade aumenta, simulações Monte Carlo tornam-se a abordagem mais vantajosa.
A ascensão dos aceleradores lineares de elétrons (LINACs) na radioterapia impulsionou diretamente a necessidade de desenvolver métodos Monte Carlo para predição e dosimetria. LINACs produzem fótons energéticos e penetrantes que entram profundamente no tecido, poupando a superfície e atenuando-se menos rapidamente que feixes de $^{60}\text{Co}$ ou $^{137}\text{Cs}$.
Elétrons relativísticos têm alcance de aproximadamente 1 cm para cada 2 MeV de energia cinética em água. No seu máximo, a deposição de energia a partir de um feixe pencil de elétrons forma uma “pluma” em formato de pera cujo diâmetro também é de cerca de 1 cm por 2 MeV de energia cinética inicial. Essas dimensões são comparáveis aos órgãos tratados e aos órgãos em risco. As áreas de tratamento são heterogêneas, com diferenças de composição e densidade — e é verdade hoje, como era então, que o método Monte Carlo fornece a única predição de grandezas radiométricas que satisfaz a demanda de precisão da radioterapia.
Códigos Monte Carlo: EGS, MCNP e GEANT
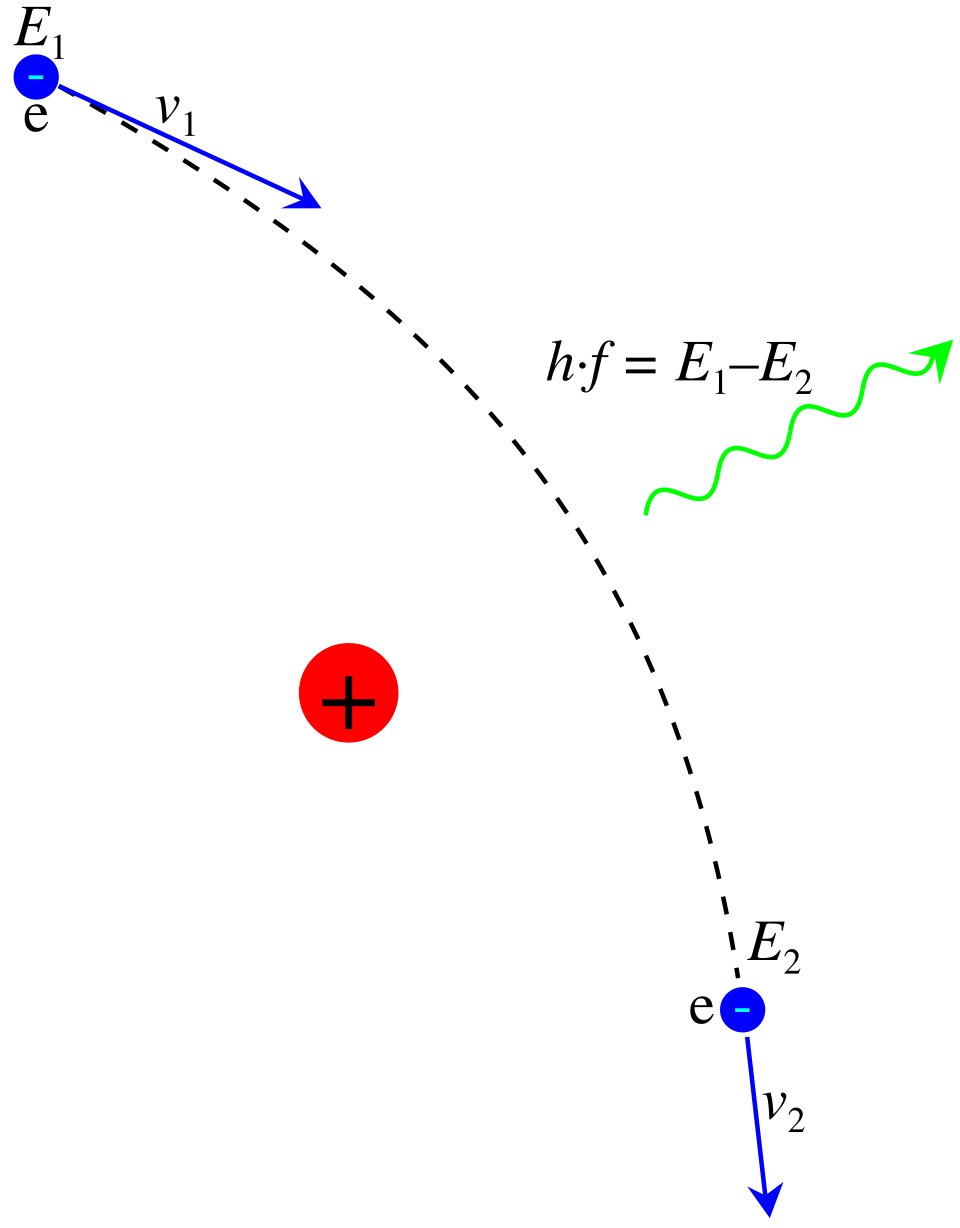
Três sistemas de códigos dominam historicamente as simulações Monte Carlo em física médica e radioterapia: EGS, MCNP e GEANT. Cada um tem características e origens distintas.
EGS (Electron Gamma Shower)
O código EGS originou-se da necessidade de simular cascatas eletromagnéticas para fins de blindagem e detecção no Stanford Linear Accelerator Center (SLAC). O programa SHOWER1 de Nagel, escrito em FORTRAN, simulava elétrons de alta energia (até 1000 MeV) incidindo sobre chumbo, tratando seis interações significativas: bremsstrahlung, espalhamento elétron-elétron, perda por ionização, produção de pares, espalhamento Compton e efeito fotoelétrico, além de espalhamento múltiplo de Coulomb.
O SLAC publicou o EGS3 em 1978, e Rogers o empregou em publicações importantes a partir de 1982. Uma contribuição decisiva foi a implementação de uma técnica emprestada do ETRAN para tornar cálculos dependentes de elétrons mais confiáveis, encurtando os passos de interações virtuais. Os artefatos de tamanho de passo, porém, permaneceram um desafio até o desenvolvimento do algoritmo PRESTA por Bielajew e Rogers em 1987.
As versões subsequentes — EGS4, EGSnrc e EGS5 — corrigiram progressivamente essas limitações. O EGSnrc, em particular, eliminou artefatos de tamanho de passo e tornou-se referência para dosimetria de câmaras de ionização com precisão melhor que 0,1%.
MCNP (Monte Carlo N-Particle)
O código MCNP reivindica ser descendente direto dos códigos escritos pelos fundadores do método Monte Carlo: Fermi, von Neumann, Ulam, Metropolis e Richtmyer. Sua linhagem passa pelos códigos MCS (1957), MCN (1967), MCC, MCP, MCNG (1973), até a Versão 1 em 1977. O transporte de elétrons foi adicionado apenas na Versão 4, em 1990 — a partir daí, o MCNP tornou-se um player importante em pesquisa médica.
GEANT
Na última década, o GEANT tem feito contribuições significativas e atualmente é comparável ao MCNP em frequência de uso na área médica. Se considerarmos toda a literatura não médica, MCNP e GEANT são os códigos mais citados, com quase o dobro de citações em relação ao EGS.
| Código | Origem | Transporte de Elétrons | Área Principal |
|---|---|---|---|
| EGS (1978+) | SLAC / NRC Canada | Desde EGS3 | Física médica e dosimetria |
| MCNP (1977+) | Los Alamos (LANL) | Desde Versão 4 (1990) | Ciências nucleares e radiológicas |
| GEANT (1982+) | CERN | Desde o início | Física de altas energias e medicina |
| PENELOPE | Espanha | Desde 1995 | Penetração e perda de energia |
| FLUKA (1964+) | CERN / INFN | Desde o início | Blindagem e dosimetria |
Fonte: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
Transporte de Elétrons e Condensed History
O transporte de elétrons exige tratamento especial nas simulações Monte Carlo. Elétrons relativísticos sofrem da ordem de $10^6$ interações individuais durante sua trajetória. Simular cada interação discreta seria computacionalmente proibitivo.
A contribuição fundadora de Martin Berger em 1963 — um artigo de 81 páginas — estabeleceu o framework para toda a geração seguinte de físicos computacionais em Monte Carlo. Berger introduziu o método de condensed history: teorias cumulativas de espalhamento condensam $10^3$ a $10^5$ eventos individuais de espalhamento elástico e inelástico em eventos “virtuais” únicos, proporcionando um speedup por fatores da ordem de centenas.
Nelson, o criador do sistema EGS, comentou: “Se eu soubesse do trabalho de Berger, talvez não tivesse empreendido o trabalho no EGS!” O código de Berger foi eventualmente liberado como ETRAN em 1968, embora versões internas existissem no NBS (hoje NIST) desde o início dos anos 1960.
O ETRAN deu origem a uma família inteira de códigos via adaptações nos laboratórios Sandia: EZTRAN, SANDYL, TIGER, CYLTRAN, SPHERE, ACCEPT, e finalmente o sistema ITS (Integrated TIGER Series). O transporte de elétrons do ITS foi posteriormente incorporado ao MCNP na Versão 4.
Dosimetria de Câmaras de Ionização
O artigo fundador para a aplicação de Monte Carlo à resposta de câmaras de ionização é atribuído a Bond et al. (1978), que calcularam a resposta de câmaras em função da espessura da parede para irradiação com $^{60}\text{Co}$. Ao validar o código EGS para essa aplicação, descobriu-se que o código tinha dificuldades algorítmicas fundamentais nesse regime de baixa energia.
Nahum, interessado em modelar resposta de câmaras de ionização, visitou o laboratório de Rogers na primavera de 1984. Usando o EGS4, obteve respostas até 60% abaixo do esperado. Nas palavras de Nahum: “Como pode um cálculo que se poderia esboçar no verso de um envelope, acertando dentro de 5%, errar em 60% usando Monte Carlo?”
A redução do tamanho de passo resolveu o problema, mas a busca por uma solução definitiva resultou no algoritmo PRESTA. O problema subjacente era sutil: trajetórias de elétrons interrompidas em fronteiras de materiais, onde seções de choque mudam, geravam singularidades espúrias de fluência. Foote e Smythe (1995) descreveram elegantemente esse mecanismo.
Atualmente, o cálculo de correções de câmaras de ionização é uma operação refinada, com resultados calculados com precisão melhor que 0,1%. Para uma visão completa do tema, confira nosso guia completo sobre técnicas de Monte Carlo em radioterapia.
Primeiras Aplicações em Radioterapia
As aplicações iniciais de Monte Carlo na radioterapia seguiram uma progressão natural. A modelagem de unidades de Cobalto-60 foi mencionada pela primeira vez no ICRU Report #18 (1971), com trabalho mais completo por Rogers et al. (1985) e Han et al. (1987). A modelagem de LINACs terapêuticos foi realizada inicialmente por Petti et al. (1983) e logo depois por Mohan et al. (1985).
Mackie et al. pioneiraram o método de convolução em 1985 e geraram o primeiro banco de dados de “kernels” ou “dose-spread arrays” para uso em radioterapia em 1988. Esses kernels continuam em uso até hoje. A modelagem de feixes de elétrons de LINACs médicos foi realizada por Teng et al. (1986) e Hogstrom et al. (1986).
O projeto OMEGA (Ottawa Madison Electron Gamma Algorithm), proposto por Mackie et al. em 1990, representou um marco: a primeira proposta de usar Monte Carlo para cálculo de dose “do alvo do acelerador ao paciente”. Cedo no projeto, adotou-se uma abordagem “dividir e conquistar” — os outputs fixos da máquina (phase-space files) serviam como inputs para o cálculo específico no paciente. Essa bifurcação gerou duas indústrias: a modelagem de cabeçote (com o código BEAM/EGS como o mais refinado e o artigo mais citado com “Monte Carlo” no título e “radioterapia” como tópico) e o desenvolvimento de algoritmos rápidos de cálculo de dose baseados em Monte Carlo, como o VMC++.
Monte Carlo vs. Métodos Determinísticos
O apêndice do primeiro capítulo do livro apresenta uma prova matemática elegante de que o método Monte Carlo é mais eficiente que métodos determinísticos de primeira ordem para estimar tallies em três dimensões espaciais.
O transporte de partículas é descrito pela equação de transporte de Boltzmann linear:
$$\left(\frac{\partial}{\partial s} + \hat{p} \cdot \frac{\partial}{\partial x} + \mu(x,p)\right) \psi(x,p,s) = \int dx’ \int dp’ \, \mu(x,p,p’) \, \psi(x’,p’,s)$$
Onde $\psi(x,p,s)$ é a fluência em fase, $\mu(x,p)$ a seção de choque macroscópica total e $s$ o comprimento de caminho. O ponto central é que a solução envolve uma integral de dimensão $N_x + N_p$ — tipicamente 6 ou 7 dimensões para problemas de radioterapia.
A convergência dos métodos determinísticos obedece a $N_{cell}^{-2/D}$, onde $D$ é a dimensionalidade do espaço de fase e $N_{cell}$ o número de células da malha. Já o método Monte Carlo converge segundo o teorema do limite central: $\sigma_{MC}(x) / \sqrt{N_{hist}}$, onde $N_{hist}$ é o número de histórias simuladas.
Comparando as taxas de convergência:
$$\frac{\Delta T_{MC}(x)}{\Delta T_{NMC}(x)} \propto t^{(4-D)/2D}$$
Monte Carlo é sempre mais vantajoso para $D > 4$. Como problemas de radioterapia operam em dimensão 6 ou 7, o método Monte Carlo oferece uma vantagem intrínseca sobre os métodos determinísticos nessa classe de problemas. Obviamente, essa conclusão depende da eficiência relativa das implementações e da forma das funções-resposta — para distribuições que variam rapidamente, Monte Carlo tende a ser ainda mais favorecido.
Essa base teórica explica por que, até 2020, cerca de 900.000 artigos foram publicados sobre o método Monte Carlo, com quase 55.000 deles relacionados à medicina — uma contribuição consistente de 10% a 20% ao longo do tempo. Para mais detalhes sobre as aplicações avançadas dessas técnicas, confira nosso guia completo sobre Monte Carlo em radioterapia.