Tumores benignos del SNC y el rol de la radioterapia
Los tumores benignos del sistema nervioso central — meningiomas, schwannomas vestibulares, adenomas hipofisarios y tumores glómicos — constituyen un grupo heterogéneo de lesiones que, a pesar de su histología benigna, frecuentemente requieren radioterapia precisa. La delineación correcta de los volúmenes blanco y la selección de la técnica adecuada determinan el control local a largo plazo y la preservación funcional del paciente.
El manejo de estos pacientes comienza con una evaluación clínica detallada: historia neurológica, examen físico focalizado, evaluación hormonal, campo visual, agudeza visual, audiometría y función neurocognitiva basal. La resección quirúrgica máxima segura permanece como estándar de atención para pacientes operables con tumores accesibles. Para los demás, la radioterapia definitiva representa la alternativa de primera línea. Este artículo detalla la lógica de contorneo, dosis, fraccionamientos y planificación para cada subtipo, basándose en nuestra guía completa sobre delineación de volúmenes blanco.
Posicionamiento, inmovilización y simulación
El paciente se simula en decúbito supino, brazos paralelos al cuerpo y hombros en posición natural. La inmovilización estándar emplea máscara termoplástica indexada de 3 puntos. Cuando el tumor se localiza en la base del cráneo o cerca del aparato óptico, la máscara de 5 puntos refuerza la fijación del cuello. Los pacientes simulados por RM utilizan máscara tipo clamshell. La cabeza y el mentón se colocan en posición neutral, salvo que se requiera posicionamiento específico para base de cráneo.
Las imágenes axiales de TC se adquieren con espesor de corte de 1 mm para SRS, FSRT y protonterapia, o 2 mm para 3D-CRT, IMRT y VMAT, cubriendo toda la cabeza hasta el nivel de los hombros. El co-registro con RM diagnóstica es altamente recomendado — secuencias T1 poscontraste o FLAIR para visualización tumoral, y T1 nativo o 3D T2/CISS para delinear nervios craneales e hipocampo. Se emplea contraste IV salvo contraindicación.
Delineación de órganos de riesgo
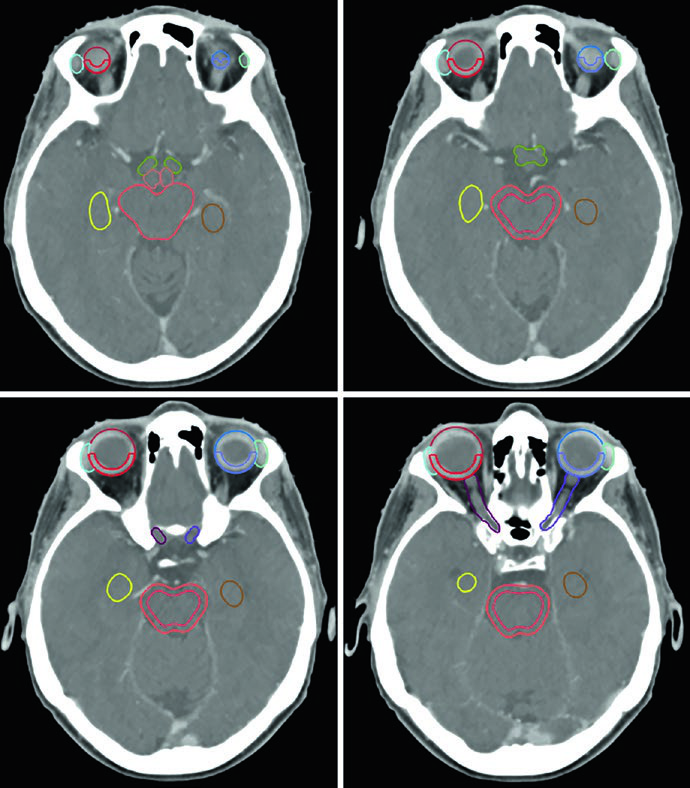
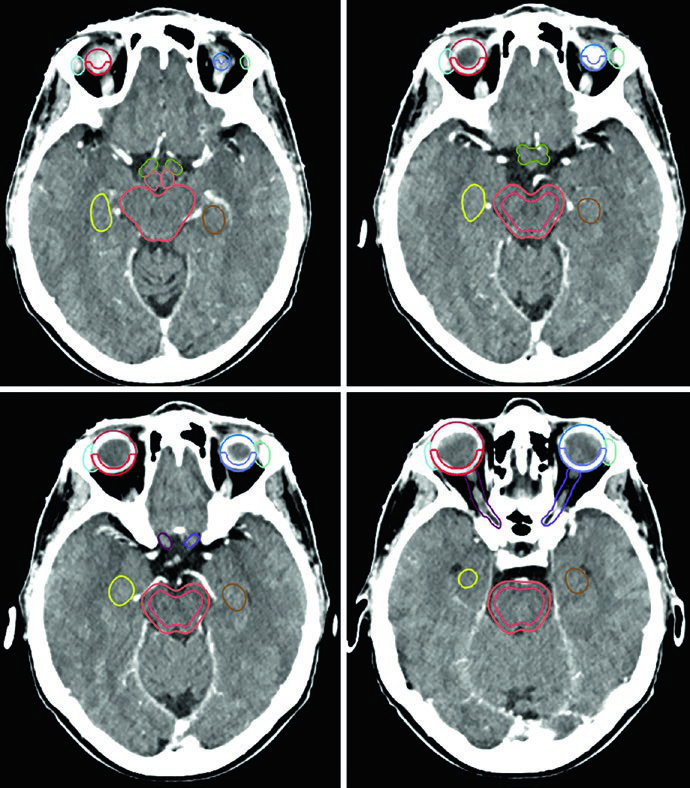
La lista de estructuras normales a contornear es extensa. Para la mayoría de los tumores cerebrales primarios benignos, los OARs incluyen: encéfalo completo, encéfalo no involucrado (encéfalo menos GTV o CTV según el escenario), tronco encefálico dividido en core y superficie (anillo periférico de 3 mm), médula espinal, cócleas bilaterales, globos oculares, cristalinos, nervios ópticos, quiasma óptico, retinas, glándulas lagrimales, lóbulos temporales, hipocampos, hipotálamo y glándula pituitaria. Los volúmenes de riesgo planificado (PRVs) pueden crearse para tumores adyacentes a estructuras críticas, facilitando la evaluación dosimétrica.
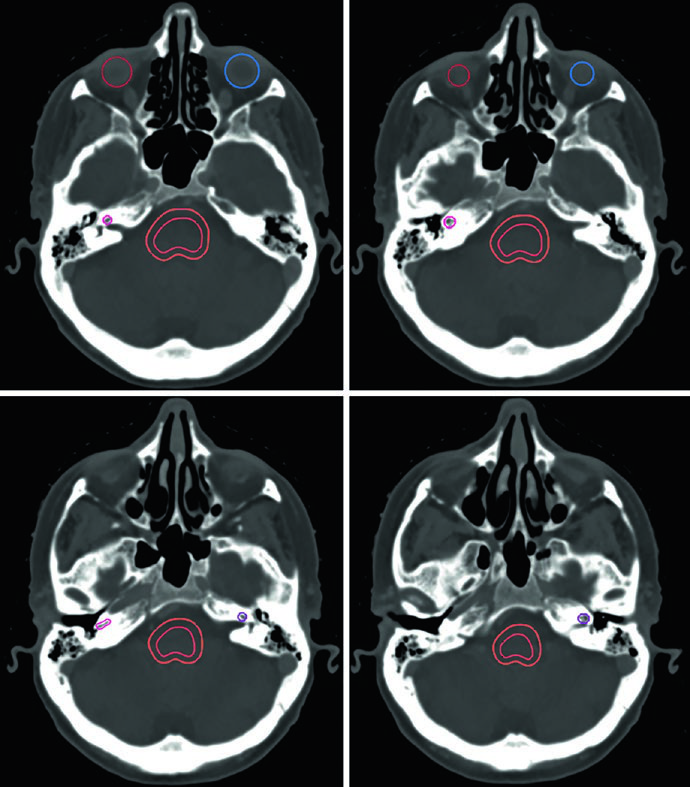
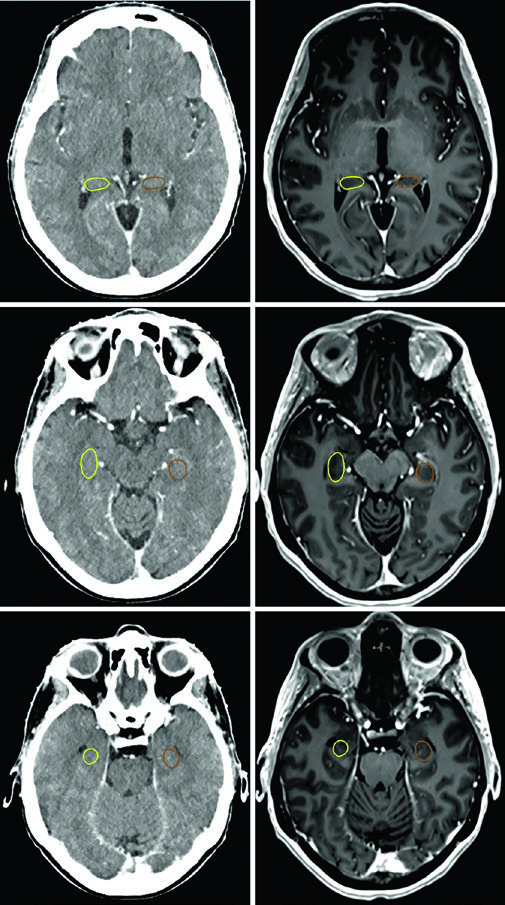
Cada OAR tiene una ventana de visualización óptima. El tronco encefálico, quiasma óptico y componentes intracraneales de los nervios ópticos se ven mejor en ventana cerebral. Los nervios ópticos en los canales ópticos y sus componentes orbitarios son más nítidos en ventana de partes blandas. Las cócleas solo se identifican con precisión en ventana ósea — y según la posición de la cabeza, pueden no encontrarse en el mismo corte axial. El hipocampo — específicamente la zona subgranular — se delinea en T1 de RM y se visualiza como sustancia gris hipointensa, desde el nivel donde limita con el atrio del ventrículo lateral superiormente hasta la extensión inferior del cuerno temporal.
Gliomas de bajo grado: astrocitomas y oligodendrogliomas
Los pacientes con astrocitomas difusos de bajo grado (IDH-mutados) y oligodendrogliomas deben someterse a resección máxima segura para diagnóstico y caracterización molecular. La dosis estándar con radioterapia convencional fraccionada es de 54 Gy en 30 fracciones. La quimioterapia se recomienda para tumores grado 2 o superior con características de alto riesgo. Los tumores IDH wild-type reciben tratamiento multimodal análogo a los gliomas malignos, dada su historia natural desfavorable.
La radiocirugía estereotáxica no está indicada para estos tumores como tratamiento inicial, excepto en casos seleccionados de astrocitomas pilocíticos.
Volúmenes blanco para gliomas astrocíticos y oligodendrogliales
| Tipo tumoral | Definición del GTV | Expansión CTV sugerida | Expansión PTV |
|---|---|---|---|
| Astrocitoma pilocítico grado I | No resecado: RM T1 poscontraste; resecado: cavidad posoperatoria | 0–0,5 cm, reducido junto a barreras anatómicas | 0–0,3 cm según técnica; 0–1 mm para SRS/HSRT; 1–3 mm para RT convencional |
| Ganglioglioma | No resecado: RM T2 o FLAIR poscontraste; resecado: cavidad + tumor residual | 1 cm, reducido junto a barreras naturales | 0,3–0,5 cm según IGRT y técnica |
| Glioma difuso de bajo grado (IDH-mutado, grado II) | No resecado: RM T2 o FLAIR; resecado: cavidad + tumor residual | 1 cm, reducido junto a barreras naturales | 0,3–0,5 cm según IGRT y técnica |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.2)
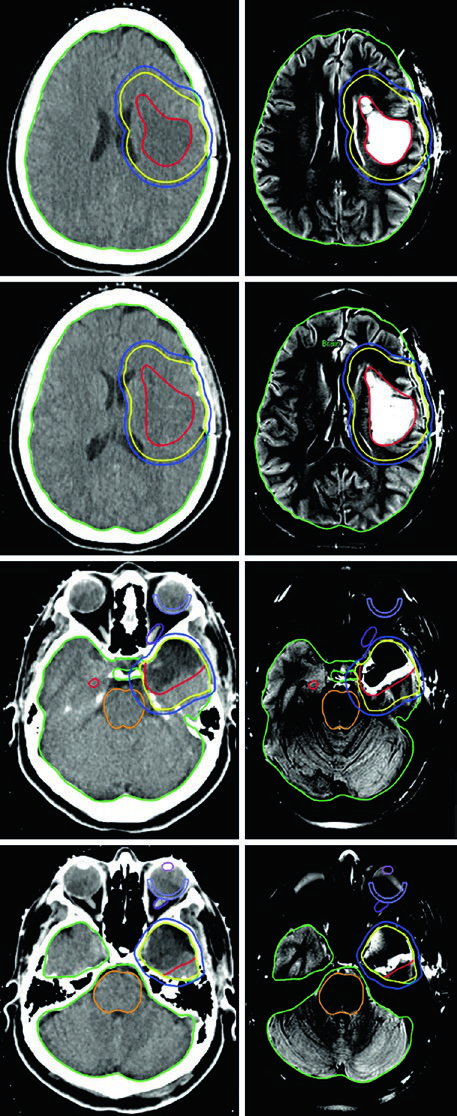
El caso del oligodendroglioma de la Figura 29.5 muestra un paciente tras craneotomía frontotemporal izquierda con resección parcial que involucra la ínsula izquierda, porciones del opérculo y extensión hacia el centrum semiovale izquierdo. El GTV (rojo) abarca la enfermedad residual en FLAIR y la cavidad operatoria. La expansión de 1,0 cm genera el CTV (amarillo), con restricción anatómica fuera de la fosa posterior, cráneo y estructuras de línea media. El PTV (azul) recibe un margen adicional de 0,3 cm.
Meningiomas grado 1: dosis, técnicas y contorneo
Los meningiomas representan los tumores intracraneales primarios más frecuentes en adultos — más del 70% son benignos y candidatos a radioterapia definitiva. Para pacientes grado 1 con resección subtotal en áreas de alto riesgo de progresión sintomática, se considera la terapia adyuvante. En los demás casos, la cirugía de rescate y la radioterapia se reservan para la recurrencia.
Dosis y fraccionamientos recomendados
| Técnica de radiación | Dosis/fraccionamiento sugerido |
|---|---|
| SRS | 14–16 Gy en fracción única |
| FSRT | 20–24 Gy en 4 fracciones; 25 Gy en 5 fracciones |
| RT convencional fraccionada | 52,2–54 Gy a 1,8–2 Gy/fracción; 50,4 Gy a 1,8 Gy/fracción para meningiomas de vaina del nervio óptico |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.3)
Volúmenes blanco para meningiomas
| Escenario clínico | Definición del GTV | Expansión CTV | Expansión PTV |
|---|---|---|---|
| Grado 1 no resecado | Tumor delineado en RM de planificación y TC de simulación | 0–0,5 cm, reducido junto a barreras anatómicas | 0–1 mm (SRS/HSRT); 1–3 mm (RT convencional) |
| Grado 1 recurrente | Cavidad posoperatoria, tumor residual realzado, compromiso dural/óseo sospechoso e inserción dural previa | 0–0,5 cm con restricción anatómica | 0–1 mm (SRS/HSRT); 1–3 mm (RT convencional) |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.4)
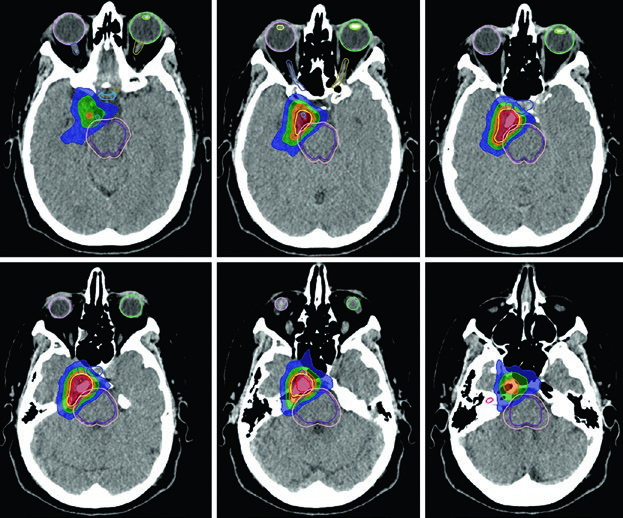
Un punto práctico fundamental: la evaluación por TC es esencial para decidir si los cambios periósticos y óseos deben incluirse en el GTV. En el ejemplo del meningioma del seno cavernoso (Figura 29.7), el tumor fue delineado con RM de planificación, recibió margen de 2 mm para el PTV y fue tratado a 52,2 Gy en 29 fracciones. Las líneas de isodosis muestran conformación estrecha alrededor del tronco encefálico, quiasma, nervios craneales adyacentes, arteria carótida y cóclea derecha.
Los meningiomas selares y supraselares voluminosos con resección incompleta — como en la Figura 29.8 — pueden requerir expansión de PTV de 3 mm debido a la enfermedad residual extensa. La relación íntima con ambos globos oculares y el tronco encefálico exige una planificación dosimétrica cuidadosa, frecuentemente con IMRT o VMAT para conformar la dosis y proteger estas estructuras críticas.
Schwannomas vestibulares y no vestibulares
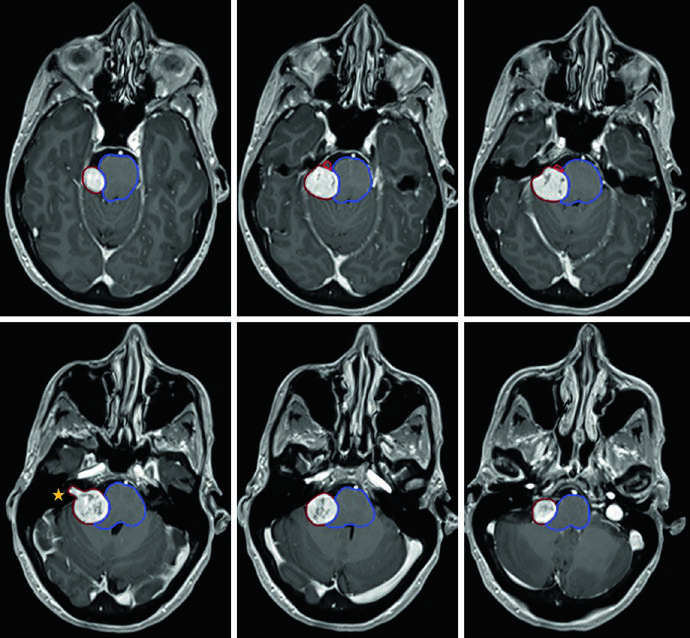
Los schwannomas vestibulares y no vestibulares pueden tratarse con radioterapia como tratamiento definitivo, adyuvante tras resección parcial o, en casos raros, para recurrencia. Una característica distintiva: no se añade margen de CTV. El GTV se delinea directamente en RM T1 poscontraste y TC de simulación, y únicamente se aplica un margen de PTV dependiente de la técnica.
Técnicas y volúmenes blanco para schwannomas
| Técnica | Dosis/fraccionamiento | GTV | CTV | PTV |
|---|---|---|---|---|
| SRS | 12–13 Gy en fracción única | Tumor en RM + TC | Ninguno | 0–1 mm |
| FSRT | 20 Gy/4 fracciones o 25 Gy/5 fracciones | Tumor en RM + TC | Ninguno | 0–1 mm |
| RT convencional | 46,8–54 Gy a 1,8–2 Gy/fracción | Tumor en RM + TC | Ninguno | 0–3 mm |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.5)
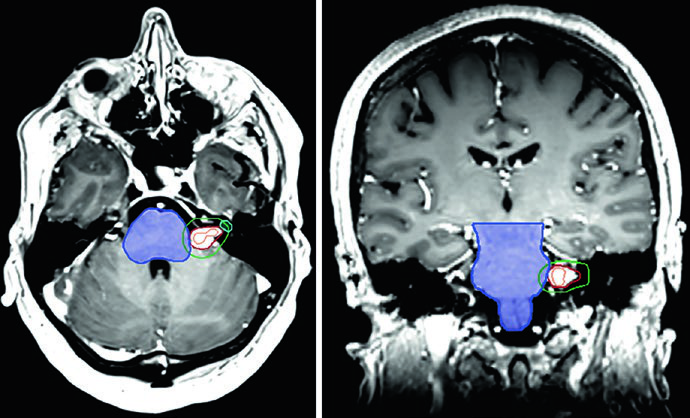
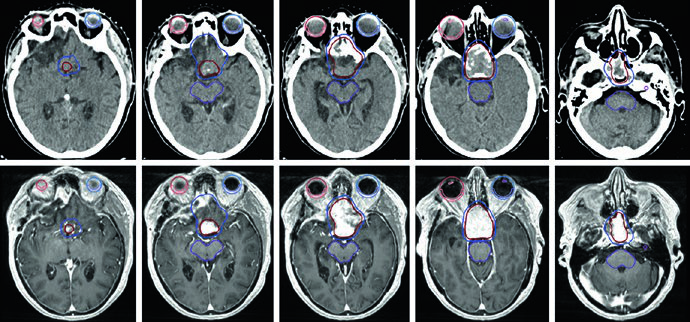
El caso de la Figura 29.9 ilustra un schwannoma vestibular derecho en el ángulo cerebelopontino que comprime el pedúnculo cerebeloso medio y el puente, extendiéndose hasta el fondo del canal auditivo interno. Existe compresión del tronco encefálico y del nervio trigémino cisternal, con borramiento parcial moderado del cuarto ventrículo. En la Figura 29.10, el tratamiento de un schwannoma del APC izquierdo con SRS a 12,5 Gy de prescripción muestra la isodosis de prescripción cubriendo el tumor, con isodosis de 20 Gy en el centro y 5 Gy en la periferia, preservando tronco encefálico y cóclea como OARs.
Adenomas hipofisarios: contorneo y planificación
Los adenomas no funcionales se tratan habitualmente con SRS, HSRT o RT convencional fraccionada en el escenario adyuvante o de rescate tras resección. Los adenomas funcionales pueden recibir terapia hormonal o cirugía antes de considerar la radioterapia, dependiendo del subtipo tumoral. Imágenes de RM de alta resolución con cortes finos en planos coronal y sagital son esenciales para delinear los volúmenes blanco. Los adenomas se visualizan mejor en la fase temprana del gadolinio dinámico, apareciendo como lesión hipointensa contra el fondo hiperintenso de la glándula hipofisaria normal.
Dosis recomendadas para adenomas hipofisarios
| Técnica | Dosis/fraccionamiento |
|---|---|
| SRS — No funcional | 15–16 Gy en fracción única |
| SRS — Funcional/secretor | 18–25 Gy en fracción única (preferible >20 Gy), según tolerancia del nervio óptico/quiasma |
| RT convencional — No funcional | 45–50,4 Gy a 1,8–2 Gy/fracción |
| RT convencional — Funcional/secretor | 54–55,8 Gy a 1,8–2 Gy/fracción |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.6)
Volúmenes blanco para adenomas hipofisarios
| Escenario clínico | Definición del GTV | Expansión CTV | Expansión PTV |
|---|---|---|---|
| No resecado / residual focal / recurrente focal | Tumor delineado en RM de planificación y TC de simulación | 0–0,5 cm, reducido junto a barreras anatómicas | 0–1 mm (SRS/HSRT); 1–3 mm (RT convencional) |
| Resecado con residual o recurrente | Tumor delineado en RM de planificación y TC de simulación | 0–0,5 cm, reducido junto a barreras anatómicas y extensión preoperatoria | 0,3–0,5 cm según IGRT y técnica |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.7)
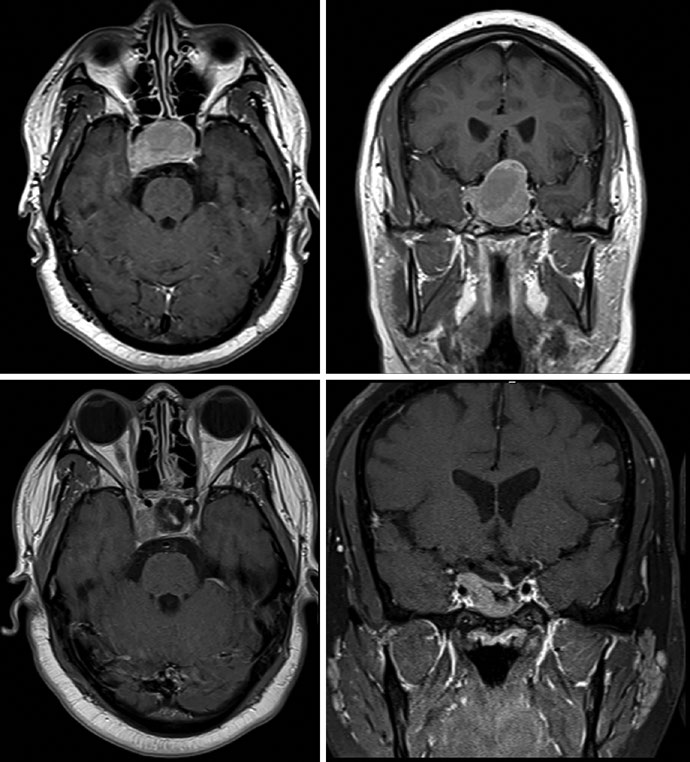
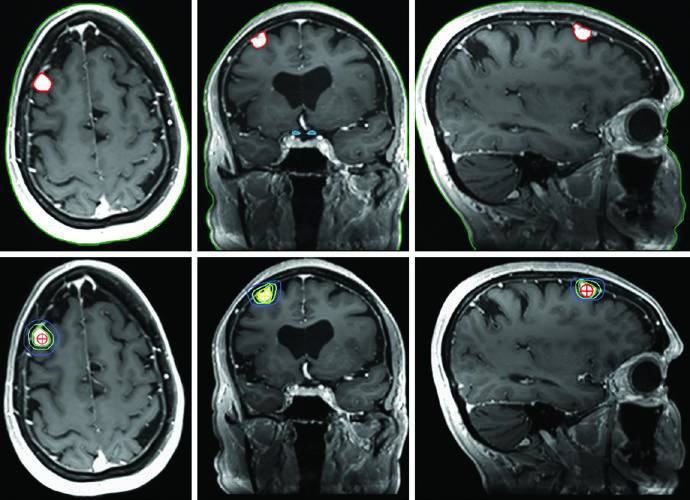
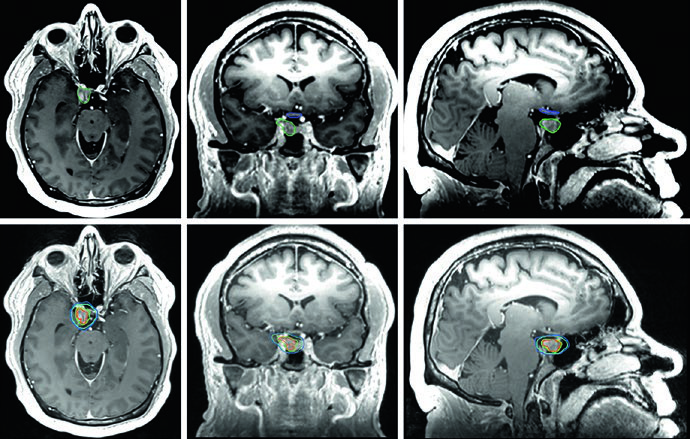
El adenoma secretor de GH de la Figura 29.11 demuestra tratamiento con SRS a 24 Gy. El tumor toca el margen medial de la carótida cavernosa y se extiende lateralmente entre las asas de la carótida, con compromiso del seno cavernoso. La dosis al quiasma, nervios ópticos y tronco encefálico se mantuvo por debajo de 8 Gy. En la Figura 29.12, el adenoma no secretor muestra invasión del seno cavernoso derecho y extensión supraselar — tras la resección, el tumor residual en la silla turca y el seno cavernoso persistió.
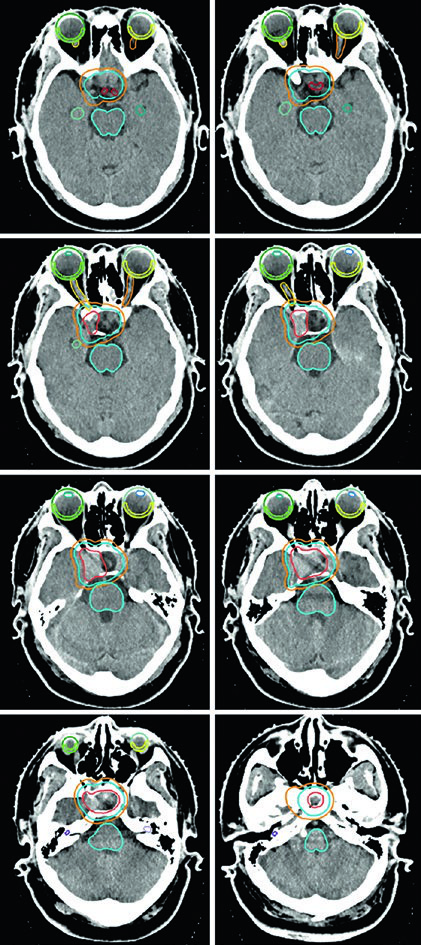
La Figura 29.13 muestra la planificación fraccionada del mismo paciente: GTV en coral, CTV con margen de 0,5 cm anatómicamente restringido en teal, PTV con expansión adicional de 0,3 cm. Tronco encefálico, quiasma y nervios ópticos aparecen como OARs delineados. Para macroadenomas, cuando la invasión del seno cavernoso es difícil de visualizar, se recomienda incluir el seno cavernoso completo en el GTV. Conocer el tipo de material implantado en la silla turca (músculo, grasa o colgajo de tabique nasal) ayuda a diferenciarlo del tumor residual.
Tumores glómicos y paragangliomas
Los tumores glómicos son neoplasias neuroendocrinas raras que pueden originarse en la base del cráneo, cabeza y cuello, tórax y abdomen, nombrados según su sitio de origen. Las opciones terapéuticas incluyen embolización, resección y radioterapia, con altas tasas de control local. La evaluación detallada por RM y TC es indispensable para detectar invasión de la cavidad timpánica, foramen yugular, región petroclival, seno cavernoso o canal del hipogloso. La TC en ventana ósea complementa la RM al revelar erosión ósea.
Dosis y volúmenes para tumores glómicos
| Técnica | Dosis/fraccionamiento |
|---|---|
| SRS | 14–16 Gy en fracción única |
| FSRT | 25 Gy en 5 fracciones |
| RT convencional | 50,4–54 Gy a 1,8–2 Gy/fracción |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.8)
| Definición del GTV | Expansión CTV | Expansión PTV |
|---|---|---|
| Tumor delineado en RM de planificación y TC de simulación | 0–0,5 cm, reducido junto a barreras anatómicas | 0–1 mm (SRS/HSRT); 1–3 mm (RT convencional) |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Tabla 29.9)
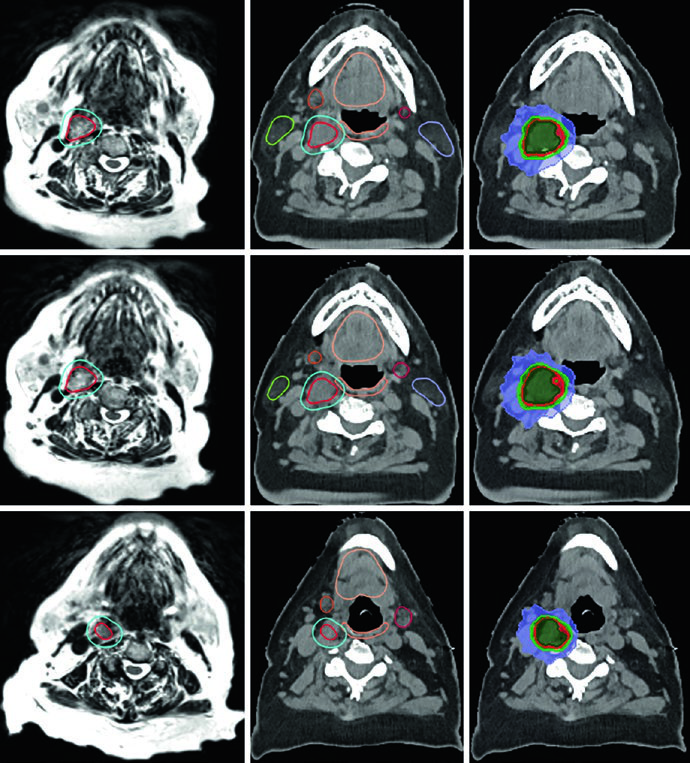
La Figura 29.14 muestra un tumor glómico carotídeo derecho que separa las arterias carótidas interna y externa. El GTV (rojo) fue delineado en RM T2 SPACE co-registrada a la TC, con expansión de 3 mm para PTV. El paciente recibió 25 Gy en 5 fracciones con líneas de isodosis de prescripción (25 Gy), 110% (27,5 Gy), 80% (20 Gy) y 50% (12,5 Gy), preservando parótidas, glándulas submandibulares, cavidad oral y pared orofaríngea.
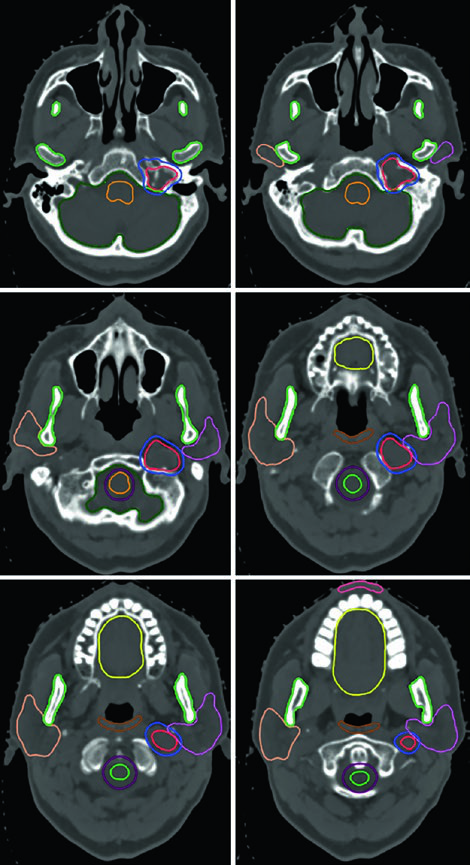
El caso de la Figura 29.15 presenta un escenario más complejo: tumor glómico recurrente en el bulbo yugular izquierdo tras embolización y resección, tratado con 54 Gy en 30 fracciones. El GTV fue generado co-registrando imágenes de RM del diagnóstico inicial y la recurrencia, abarcando la extensión original de la enfermedad, cambios posoperatorios, lecho tumoral y enfermedad recurrente con cobertura hasta la base del cráneo. Un margen de 0,3 cm definió el PTV. Múltiples OARs — tronco encefálico, mandíbula, parótidas bilaterales, médula con PRV, pared orofaríngea, cavidad oral y labios — fueron meticulosamente delineados.
Consideraciones finales e integración clínica
La delineación de tumores benignos del SNC exige integración multimodal de imagen — TC en diferentes ventanas complementada por RM con secuencias específicas para cada patología. La decisión entre SRS, FSRT y RT convencional fraccionada depende del tamaño tumoral, proximidad a estructuras críticas (especialmente el aparato óptico) y escenario clínico (definitivo, adyuvante o rescate). Para una visión integral de las técnicas de delineación en radioterapia, consulte nuestra guía completa sobre delineación de volúmenes blanco y configuración de campos.
Schwannomas y meningiomas compactos son candidatos ideales para SRS o FSRT, mientras que tumores de mayor tamaño o cercanos al quiasma óptico frecuentemente requieren fraccionamiento convencional para respetar las tolerancias de las estructuras críticas. Los gliomas de bajo grado, por su naturaleza infiltrativa, demandan márgenes de CTV más amplios y el uso criterioso de RM FLAIR para capturar la extensión de la enfermedad. Los tumores glómicos exigen atención especial a la anatomía de la base del cráneo y la potencial invasión vascular. Artículos relacionados que pueden complementar su lectura incluyen nuestro material sobre metástasis cerebrales y SRS y sobre tumores malignos del SNC.




