En Este Artículo
- 1. Qué es TSET y Por Qué Monte Carlo Marca la Diferencia
- 2. Simulación Monte Carlo de los Haces Utilizados en TSET
- 3. Validación de Haces en la Geometría de Entrega TSET
- 4. La Controversia del Bremsstrahlung a Distancias Extendidas
- 5. Uniformidad de Dosis: Fantoma Oval y Distribuciones en el Paciente
- 6. Monte Carlo en Braquiterapia: Más Allá de las Limitaciones del TG-43
- 7. Impacto Clínico de la Transición TG-43 a Monte Carlo
- 8. Herramientas de Cálculo MC para Braquiterapia
- 9. El Papel de la Imagen en la Asignación de Tejidos para MC
- 10. Especificación de Dosis: $D_{w,m}$ versus $D_{m,m}$
Qué es TSET y Por Qué Monte Carlo Marca la Diferencia

La irradiación total de piel con electrones (TSET) sigue siendo uno de los tratamientos más eficaces para el linfoma cutáneo de células T (micosis fungoide). Se trata de un procedimiento especial que exige modificaciones sustanciales en el equipo y una geometría de campo fuera de lo convencional — campos compuestos de aproximadamente 200 cm de altura por 80 cm de ancho, con SSDs nominales entre 300 y 500 cm para cubrir al paciente más grande con uniformidad adecuada.
Guía completa de la serie: para una visión integral de todas las técnicas y artículos relacionados, consulta nuestra guía completa sobre Monte Carlo en radioterapia.
La población de pacientes que requiere TSET es relativamente pequeña, y la técnica suele estar disponible solo en centros académicos u hospitales de gran tamaño. Según las recomendaciones del AAPM Report 23, la dosis máxima debe ocurrir en la superficie, el nivel del 80% de la dosis prescrita debe encontrarse a una profundidad mayor de 0,4 cm, y la dosis debe caer por debajo del 20% a los 2 cm de profundidad. La energía nominal del haz de electrones más utilizada varía entre 4 y 9 MeV.
Las técnicas de entrega en TSET buscan proporcionar dosis uniforme a toda la piel del paciente con el máximo en la superficie. Actualmente predominan dos técnicas: campos duales estáticos (seis posiciones) y campos duales rotacionales, donde el paciente se coloca sobre una plataforma giratoria. En la técnica de 6 campos estáticos, el paciente asume seis orientaciones distintas: anterior, posterior, lateral derecho, lateral izquierdo y dos posiciones anguladas. Estudios en fantomas indicaron que la rotación del paciente proporciona la mejor uniformidad de dosis, aunque la técnica de ocho campos resulta casi equivalente y la de seis campos es adecuada y más sencilla de ejecutar.
El método Monte Carlo aportó a este escenario algo que décadas de dosimetría experimental no lograron: la visualización completa de las distribuciones de dosis en la piel del paciente, incluyendo análisis DVH a diferentes profundidades — información inaccesible por métodos experimentales tradicionales basados en películas, TLDs y cámaras de ionización.
Simulación Monte Carlo de los Haces Utilizados en TSET
Los campos de electrones utilizados en TSET se definen por los colimadores (jaws) del LINAC, sin aplicador de electrones acoplado. La simulación de estos haces utiliza el sistema EGSnrc, partiendo de la geometría detallada del cabezal del acelerador. Ding et al. modelaron haces de 6 MeV a partir de dos aceleradores distintos: el Varian Clinac 21EX y el Varian TrueBeam — cada uno con un enfoque de simulación propio.
Para el Clinac 21EX, la simulación comienza con electrones saliendo de la ventana de vacío del cabezal. Los detalles de la geometría del cabezal — incluyendo las láminas de dispersión de electrones y el sistema de definición del campo — fueron proporcionados directamente por el fabricante. La energía y el tamaño del spot del haz de electrones antes de impactar la ventana de salida se ajustan iterativamente para obtener la mejor concordancia entre medidas y cálculos.
El TrueBeam sigue una lógica diferente. La simulación parte de archivos de phase-space proporcionados por Varian, registrados en el plano justo encima de los colimadores x-y, sin necesidad de ajuste manual. Este enfoque elimina la incertidumbre asociada al modelado del cabezal, transfiriendo la responsabilidad de la precisión al fabricante.
En todos los casos se emplearon los parámetros estándar del EGSnrc:
$$AE = ECUT = 0{,}521 \text{ MeV}, \quad AP = PCUT = 0{,}010 \text{ MeV}$$
No se utilizó forzamiento de interacción de fotones ni dispersión Rayleigh — configuración consistente con estudios anteriores. Los haces simulados se almacenaron en archivos de phase-space a SSD = 100 cm, conteniendo posición, energía, ángulo, carga y peso de cada partícula. Estos archivos alimentan el código DOSXYZnrc para los cálculos de dosis subsecuentes.
La validación mostró excelente concordancia entre curvas de porcentaje de dosis en profundidad (PDD) medidas y calculadas, así como perfiles de dosis en agua para haces de 6 MeV con campos de 36 × 36 cm² y 40 × 40 cm² a SSD = 100 cm. Las medidas utilizaron detector de diodo. Esta concordancia confirma la precisión de las simulaciones Monte Carlo para los haces de TSET.
Validación de Haces en la Geometría de Entrega TSET
Aunque Monte Carlo se considera el estándar de oro para cálculos de dosis, la precisión depende de muchos factores. La validación experimental de la simulación se vuelve esencial, especialmente cuando la radiación se entrega mediante haces duales combinados en geometría de fantoma rotacional.
La técnica emplea una placa grande de acrílico transparente (90 cm × 200 cm), montada en un marco de madera sobre ruedas, posicionada entre el haz incidente y la plataforma giratoria. Esta placa funciona como degradador de haz — reduce la energía de los electrones y aumenta la dispersión, contribuyendo a la uniformidad de dosis en la piel.
Las mediciones de validación emplearon dosímetros nanoDot fabricados por LANDAUER, basados en tecnología de Luminiscencia Ópticamente Estimulada (OSL). Estos dosímetros fueron posicionados sobre un fantoma cilíndrico equivalente a agua (29 cm de diámetro, 30 cm de longitud) revestido con dos capas de bolus de 5 mm de espesor equivalente a agua. Los dosímetros se colocaron en la superficie del fantoma y entre las capas de bolus.
Para confirmar la precisión de los haces duales simulados en la dirección vertical, se colocaron dosímetros nanoDot en la superficie de la placa de dispersión. La retrodispersión de la placa es proporcional a la dosis superficial, por lo que la forma de los perfiles no se ve afectada por la retrodispersión. La comparación entre perfiles medidos y calculados mostró excelente concordancia.
Un hallazgo clave: los perfiles de dosis son extremadamente sensibles al tamaño de campo del haz de electrones. Para el campo de 40 × 40 cm², la dosis en los bordes es menor que para 36 × 36 cm². La explicación es geométrica — en el centro, ambos campos duales contribuyen a la dosis, mientras que en los extremos solo contribuye un campo. La buena concordancia entre simulación y medida valida la precisión del modelo, con resultados consistentes con la literatura existente.
La Controversia del Bremsstrahlung a Distancias Extendidas
Uno de los resultados más impactantes de los estudios Monte Carlo en TSET se refiere a la dosis de bremsstrahlung. Durante décadas, la percepción común en la comunidad de física médica era que la dosis de bremsstrahlung de un haz de 6 MeV alcanzaba el 5% a distancias extendidas de ~500 cm, según lo reportado por Das et al. De ser correcta, esta estimación limitaría significativamente el uso clínico del TSET.
Los resultados Monte Carlo de Ding et al. desafiaron definitivamente esta percepción. Las simulaciones mostraron que la dosis de bremsstrahlung para haces de 6 MeV se situó entre 0,5% y 1% para SSDs de 100 a 700 cm — un orden de magnitud por debajo del valor previamente aceptado. Chen et al. también encontraron dosis de bremsstrahlung de solo ~1% incluso a SSD > 500 cm para un haz de 6 MeV del Varian 21EX-S.
Ding et al. evaluaron la validez del 5% reportado y concluyeron que los errores en las medidas originales probablemente se debían a un detector cuyas lecturas estaban dominadas por una baja relación señal/ruido a distancias extendidas. Los haces simulados a distancias extendidas también fueron utilizados por Ding para investigar las razones de poder de frenado (stopping-power ratios) para dosimetría precisa en TSET.
Este hallazgo impacta directamente la práctica clínica. Una dosis de bremsstrahlung del 5% contribuiría significativamente a la irradiación de tejidos profundos — un efecto indeseado en TSET, donde el objetivo es tratar exclusivamente la piel. Al demostrar que el valor real es inferior al 1%, el Monte Carlo eliminó una barrera potencial para la expansión de la técnica. Como se discute en nuestro artículo sobre cálculo de dosis Monte Carlo en el paciente, la precisión en el modelado del haz es fundamental para resultados clínicos confiables.
Uniformidad de Dosis: Fantoma Oval y Distribuciones en el Paciente
El torso humano se asemeja a un óvalo, lo que convierte al fantoma cilíndrico oval en una geometría más realista que la circular. Simulaciones Monte Carlo en un fantoma cilíndrico oval equivalente a agua (eje largo de 40 cm, eje corto de 20 cm, longitud vertical de 150 cm) revelan diferencias importantes respecto a la geometría circular.
En la geometría circular, la dosis es uniforme en toda la superficie. En el cilindro oval, se observan dosis significativamente menores en las superficies del eje corto — correspondientes a las regiones anterior y posterior del torso del paciente. Aunque la dosis es menor en la superficie del eje corto, la profundidad donde la dosis cae al 50% del valor superficial permanece aproximadamente igual. Esto ocurre porque las dosis a mayores profundidades son contribuidas por haces de incidencia casi normal, mientras que los haces oblicuos no penetran significativamente desde la superficie.
El espesor de la placa degradadora influye directamente en la cobertura de dosis en profundidad. Las comparaciones entre placas de 3 mm, 9 mm y sin placa muestran que el máximo de dosis ocurre en la superficie incluso sin degradador — resultado de la incidencia de electrones desde múltiples direcciones durante la rotación del fantoma. Cuando el fantoma está estacionario, se observa buildup de dosis, consistente con curvas de PDD medidas por Chen et al. Con base en los resultados Monte Carlo, Ding et al. recomiendan una placa degradadora de 3 mm en lugar de 9 mm, con campo de 40 × 40 cm² para cobertura óptima de dosis en profundidad en la piel.
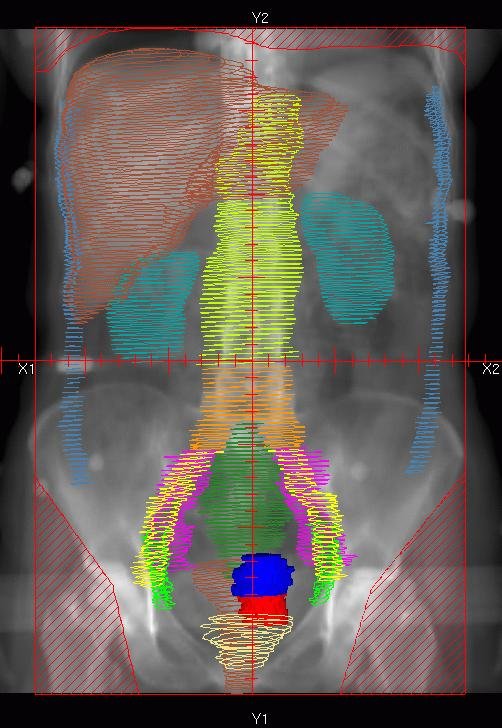
Las distribuciones de dosis en la anatomía real del paciente — obtenidas por cálculo Monte Carlo en imágenes CT — revelan variaciones superiores al 20% en la dosis cutánea, consistentes con medidas in vivo de la literatura. Las líneas de isodosis del 90% (rojo), 75% (blanco) y 50% (azul) revelan blindaje parcial por los brazos elevados, generando discontinuidades en la cobertura entre cabeza y brazo. La distancia entre las isodosis del 90% y 50% es de aproximadamente 5 mm.
Los análisis DVH en tres intervalos de profundidad — 0–5 mm, 5–10 mm y 10–15 mm de la superficie — tanto para el torso como para la piel completa demuestran el impacto del espesor de la placa de dispersión (3 mm versus 9 mm) en la cobertura de dosis. Esta información sobre la distribución volumétrica de dosis es completamente inaccesible por métodos experimentales y representa la contribución singular del Monte Carlo a la planificación de TSET.
En el Vanderbilt University Medical Center, dosímetros OSLD (nanoDot) se colocan en la piel del paciente durante la primera fracción de tratamiento en localizaciones específicas. Las variaciones de dosis in vivo medidas fueron consistentes con las variaciones del 20% predichas por Monte Carlo. Los resultados terapéuticos de pacientes tratados con el degradador de 3 mm son objeto de un estudio prospectivo en curso. Tanto la técnica de campos duales rotacionales como la de 6 campos estáticos duales producen distribuciones de dosis cutánea comparables.
Monte Carlo en Braquiterapia: Más Allá de las Limitaciones del TG-43
El formalismo TG-43, con más de 1.500 citaciones hasta agosto de 2020, representó un avance fundamental en la dosimetría de braquiterapia. Sustituyó métodos semiempíricos basados en actividad aparente y equivalente en masa de radio por parámetros dosimétricos que dependen de la geometría detallada de la fuente — distribución de radiactividad, encapsulamiento y marcadores de imagen. Esta estandarización mejoró la consistencia y comparabilidad de los cálculos de dosis entre instituciones a nivel mundial.
Sin embargo, el TG-43 se basa en la superposición de distribuciones de dosis de fuente única derivadas en esferas de agua de referencia (radios de 15 cm para fuentes de baja energía, 40 cm para alta energía). Cuando la geometría real se desvía significativamente de esta esfera de referencia, cinco fenómenos generan errores:
| Sitio Anatómico | Energía | Absorción | Atenuación | Blindaje | Dispersión | Dosis ≠ Kerma |
|---|---|---|---|---|---|---|
| Próstata | Alta | N | N | N | N | N |
| Próstata | Baja | Y | Y | Y | N | N |
| Mama | Alta | N | N | N | Y | N |
| Mama | Baja | Y | Y | Y | N | N |
| GYN | Alta | N | N | Y | N | N |
| GYN | Baja | Y | Y | N | N | N |
| Piel | Alta | N | N | Y | Y | N |
| Piel | Baja | Y | N | Y | Y | N |
| Pulmón | Alta | N | N | N | Y | Y |
| Pulmón | Baja | Y | Y | N | Y | N |
| Pene | Alta | N | N | N | Y | N |
| Pene | Baja | Y | N | N | Y | N |
| Ojos | Alta | N | N | Y | Y | Y |
| Ojos | Baja | Y | Y | Y | Y | N |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022), Table 16.1, adaptada de Rivard et al.
Para fuentes de baja energía, el coeficiente de absorción másica de energía $\mu_{en}/\rho$ varía significativamente entre tejidos debido a la dependencia aproximada de $Z^{3-4}$ de la sección eficaz fotoeléctrica. Bajo condiciones de equilibrio de partículas cargadas (CPE) en una cavidad grande, la relación entre dosis en tejido y dosis en agua es:
$$\frac{D_{tejido}}{(\mu_{en}/\rho)_{tejido}} = \frac{D_{agua}}{(\mu_{en}/\rho)_{agua}}$$
Esta razón $(\mu_{en}/\rho)_{tejido} / (\mu_{en}/\rho)_{agua}$ difiere sustancialmente de la unidad para la mayoría de los tejidos en el rango de energía de fuentes de baja energía. A energías más altas de fotones, las razones convergen a la unidad conforme la dispersión Compton se vuelve dominante.
El blindaje es relevante en implantes multi-semilla donde fotones de una fuente pueden ser absorbidos por marcadores radiopacos (Au, Ag, Pb) o componentes de fuentes adyacentes — la denominada atenuación entre semillas (ISA). Para fuentes HDR de alta energía como $^{192}$Ir, la ISA entre semillas no es un problema, ya que una sola fuente recorre los canales del aplicador. Sin embargo, materiales del aplicador como acero inoxidable y blindajes de tungsteno (para proteger órganos en riesgo) pueden causar desviaciones significativas. Las geometrías de voxels no cartesianos (mallas 3D) ya son soportadas en varios códigos MC como MCNP6 y GEANT4, permitiendo modelar aplicadores complejos como el Fletcher-Williamson.
La ruptura de la aproximación kerma = dosis ocurre cuando los alcances de los electrones secundarios se vuelven significativos. Para fuentes de alta energía, esta aproximación puede introducir diferencias mayores al 1% a distancias menores de 7 mm ($^{60}$Co), 3,5 mm ($^{137}$Cs) y 2 mm ($^{192}$Ir) de la fuente. Para fuentes de baja energía, el equilibrio electrónico se alcanza dentro de 0,1 mm y la aproximación permanece precisa. Para más detalles sobre modelado de fuentes, consulta nuestro artículo sobre Monte Carlo para electrones y braquiterapia.
Impacto Clínico de la Transición TG-43 a Monte Carlo
Las cifras del impacto clínico son elocuentes. Meigooni et al. fueron los primeros en investigar la ISA en 1992, estimando reducciones de dosis del 6% en el borde de implantes prostáticos de $^{125}$I. Chibani et al. y Carrier et al. publicaron simulaciones Monte Carlo en geometrías reales de implantes de $^{125}$I y $^{103}$Pd en próstata en 2005 y 2006, encontrando reducciones del $D_{90}$ de 2%–5% debidas a ISA.
Carrier et al. realizaron un estudio retrospectivo con 28 pacientes de cáncer de próstata implantados con $^{125}$I usando datos de CT post-implante. Encontraron una disminución promedio del 7% en el $D_{90}$ por la combinación de ISA y heterogeneidades de composición tisular. Chibani et al. también investigaron el impacto de calcificaciones intraprostáticas y encontraron reducciones del $D_{90}$ de hasta 37%. En el estudio más grande de la literatura (613 pacientes), Miksys et al. demostraron que el $D_{90}$ es 6% menor en promedio para simulaciones MC específicas del paciente comparadas con cálculos TG-43. Pacientes con calcificaciones intraprostáticas pueden presentar subdosificación significativa en subvolúmenes sombreados por las calcificaciones, con reducciones del $D_{90}$ de hasta 25%.
Para implantes de mama, los resultados son aún más dramáticos. Landry et al. investigaron la sensibilidad de las distribuciones de dosis en implantes prostáticos con $^{125}$I y mamarios con $^{103}$Pd. Dos composiciones elementales de próstata de la literatura resultaron en variaciones de 3,5% en el $D_{w,m,90\%}$. Para mama, la proporción adiposo:glandular varió de 70:30 a 30:70, generando variaciones de 10% en el $D_{w,m,90\%}$ (cerca de 6% en $D_{m,m}$). La variabilidad en la composición elemental del tejido para una proporción dada resultó en variaciones de dosis del 10%. Afsharpour et al. encontraron reducciones del $D_{90\%}$ de 4% para mama totalmente glandular hasta 35% para mama totalmente adiposa con implantes de $^{103}$Pd.
En braquiterapia ocular con placas de $^{103}$Pd, $^{125}$I o $^{131}$Cs, las discrepancias son igualmente significativas. Para una placa COMS de 16 mm de diámetro con dieciséis semillas de $^{103}$Pd, la dosis promedio al tumor fue hasta 17% menor por MC comparado con TG-43. Para estructuras normales como el cristalino, la dosis MC fue hasta 34% menor que TG-43.
Miksys et al. demostraron, en braquiterapia mamaria con $^{103}$Pd, que el TG-43 sobreestima dosis en el blanco ($D_{90\%}$ en promedio 10%, hasta 27%) y subestima dosis en la piel ($D_{1 cm^3}$ en promedio 29%, hasta 48%) comparado con MC con modelos tisulares completos del paciente.
Herramientas de Cálculo MC para Braquiterapia
Diversas plataformas de cálculo Monte Carlo fueron desarrolladas para dosimetría específica del paciente en braquiterapia, cada una con enfoques distintos para lograr tiempos de cálculo clínicamente viables.
| Herramienta | Motor MC | Tamaño de Voxel | Tiempo de Cálculo | Incertidumbre Estadística | Características Clave |
|---|---|---|---|---|---|
| MCPI | GEPTS | 2 mm³ | ~1 min | 2% | Modelo híbrido voxel+cilíndrico; ray tracing analítico |
| PTRAN_CT | EGSnrc | 2 mm³ | ~3 s | 2% | Correlated sampling generalizado; ganancia de eficiencia 2–40× |
| BrachyDose | EGSnrc | 2 mm³ | ~30 s | <2% | Multi-geometry package; múltiples fuentes y aplicadores |
| ALGEBRA | GEANT4 | 2 mm³ | 6–12 min | 2% | DICOM-RT nativo; scoring en parallel world independiente |
| egs_brachy | EGSnrc (egs++) | 2 mm³ / 1 mm³ | 13–39 s | 2% | Código abierto; biblioteca verificada; GUI integrada |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
El MCPI (Monte Carlo dose calculation tool for prostate implants), desarrollado por Chibani et al. en 2005, utiliza transporte solo de fotones para fuentes de baja energía (<50 keV). Emplea un modelo híbrido donde voxels rectangulares y geometrías cilíndricas de las semillas coexisten — los voxels que intersecan semillas se marcan, evitando la necesidad de consultar cada semilla durante el transporte. El código utiliza ray tracing en lugar de transporte análogo, proyectando trayectorias de fotones primarios y secundarios a través de toda la malla de voxels, independientemente de la interacción, aumentando la frecuencia de deposición de energía en voxels distantes mediante el estimador de valor esperado de longitud de trayectoria.
El PTRAN_CT implementa la técnica de correlated sampling generalizado: las historias de fotones se construyen inicialmente en agua homogénea, luego se recalculan los pesos de las partículas para la geometría heterogénea. En lugar de puntuar dosis absoluta, el código puntúa la diferencia entre la dosis en la geometría heterogénea y la dosis TG-43, aumentando la eficiencia por factores de 2 a 40. Se reportaron tiempos de cálculo de unos 3 segundos para implantes de próstata con incertidumbre del 2% en voxels de 2 mm³. El código importa imágenes CT DICOM y usa el CTcreate del EGSnrc para asignación de secciones eficaces.
El BrachyDose es un código de usuario del EGSnrc que utiliza el multi-geometry package. Modela tanto fotones como electrones con energías cinéticas de 1 keV a MeV, incluyendo fuentes LDR y HDR de diversas energías, aplicadores de placas oculares y modelos virtuales de pacientes basados en CT. Fue extensivamente verificado generando parámetros TG-43 para múltiples fuentes comerciales de $^{125}$I, $^{103}$Pd y $^{192}$Ir.
El ALGEBRA (ALgorithm for heterogeneous dosimetry based on GEANT4 for BRAchytherapy) se basa en GEANT4 y el estándar DICOM-RT. Importa datos de planificación e imágenes CT, con un método semiautomático de segmentación. El scoring, usando la funcionalidad “parallel world” de GEANT4, es independiente de la geometría de transporte — las resoluciones de transporte y scoring pueden diferir.
El egs_brachy es la herramienta más moderna del grupo, distribuida como software libre y de código abierto. Utiliza egs++ (biblioteca C++ del EGSnrc) para modelado geométrico y emplea diversas técnicas de eficiencia: estimador de longitud de trayectoria para kerma de colisión, fuentes de phase-space, reciclaje de partículas y técnicas específicas de reducción de varianza para braquiterapia electrónica. Para implantes de próstata y mama con voxels de 2 mm³ y placas oculares con voxels de 1 mm³, los tiempos de simulación oscilan entre 13 y 39 segundos para 2% de incertidumbre promedio en el blanco. El código puede ejecutarse en múltiples núcleos para tiempos aún menores. Para más sobre simulaciones y herramientas de QA, consulta nuestro artículo sobre protones y QA avanzado con Monte Carlo.
El Papel de la Imagen en la Asignación de Tejidos para MC
La precisión del cálculo Monte Carlo en braquiterapia depende críticamente de la asignación voxel a voxel de las secciones eficaces de fotones, lo que requiere conocimiento detallado de la composición tisular. La tomografía computarizada (CT) es el input estándar porque su intensidad sigue aproximadamente el coeficiente de atenuación lineal relativo del tejido subyacente. La conversión de unidades Hounsfield (HU) a densidad electrónica o másica es un paso relativamente sencillo.
Para fuentes de alta energía, donde los efectos de composición tisular son menores y la dispersión Compton domina, las imágenes CT proporcionan información suficiente para calcular la dosis absorbida con pocos puntos porcentuales de error. Melhus y Rivard mostraron que las inhomogeneidades de composición tisular tienen efectos despreciables (<5%) para $^{192}$Ir en distancias clínicamente relevantes en tejidos blandos.
Para fuentes de baja energía, la situación cambia completamente. La fuerte dependencia $Z^{3-4}$ de la sección eficaz fotoeléctrica exige determinación precisa de la composición elemental — algo que la CT de energía única no proporciona directamente. Estudios recientes demuestran que la CT de doble energía (DECT) puede proporcionar estimaciones más precisas de la composición elemental, reduciendo incertidumbres en las simulaciones MC.
La resonancia magnética (MRI) ofrece contraste superior en tejidos blandos, particularmente ventajoso para la delineación de la próstata. Sin embargo, no proporciona directamente información de densidad electrónica. Las distorsiones geométricas debidas a inhomogeneidades del campo magnético, no linealidad de gradiente y efectos de susceptibilidad representan desafíos adicionales, aunque la braquiterapia puede ser menos sensible a estas distorsiones que la radioterapia externa.
La sensibilidad de las distribuciones de dosis a la composición tisular es significativa. Para implantes prostáticos con $^{125}$I, dos composiciones elementales de próstata de la literatura resultaron en variaciones de 3,5% en el $D_{w,m,90\%}$. Para mama, la variabilidad en la composición tisular resultó en variaciones de dosis de hasta 10%. Maughan et al. encontraron gran variación en el contenido de carbono (8%–32% en peso) y ceniza mineral (0,9%–3,0% en masa) en tumores de varios sitios, resultando en variaciones del 20% en $(\mu_{en}/\rho)_{tumor} / (\mu_{en}/\rho)_{agua}$ a 30 keV — evidenciando la necesidad de más estudios en esta área.
Especificación de Dosis: $D_{w,m}$ versus $D_{m,m}$
Un tema debatido en la transición a cálculos Monte Carlo en braquiterapia es la magnitud dosimétrica utilizada para reportar las dosis administradas. El TG-43 reporta dosis en agua en agua ($D_{w,w}$). Con MC, surgen dos opciones: dosis en medio en medio ($D_{m,m}$) — fotones transportados y dosis puntuada en el tejido real — y dosis en agua en medio ($D_{w,m}$) — fotones transportados en tejido real pero dosis convertida a agua.
La diferencia entre estas magnitudes depende de las dimensiones de la cavidad (volumen de interés) en relación con el alcance de los electrones secundarios. Carlsson-Tedgren y Carlsson aplicaron la teoría de cavidad de Burlin para evaluar cuándo las cavidades pueden considerarse pequeñas, intermedias o grandes. Para fuentes de baja energía, cavidades de dimensiones típicas de voxels de cálculo se comportan como cavidades grandes, simplificando la conversión. Para fuentes de alta energía, la situación es más compleja y los métodos MC se convierten en la única herramienta verdaderamente adecuada para resolver la cuestión.
El avance continuo de estas técnicas apunta hacia un futuro donde el cálculo Monte Carlo será una herramienta de rutina en la planificación de braquiterapia, ofreciendo dosimetría verdaderamente específica del paciente. Para conocer las tendencias emergentes, consulta nuestro artículo sobre IA y futuro del Monte Carlo en radioterapia.