La delineación en tumores de cavidad nasal y senos paranasales exige integrar imagen fina, anatomía y rutas de extensión hacia la base del cráneo y los nervios craneales. Para la visión completa de la serie, consulte el Target Volume Delineation and Field Setup – Complete Clinical Guide; si quiere comparar otro sitio complejo de cabeza y cuello, también puede revisar nuestro artículo dedicado al carcinoma nasofaríngeo.
El capítulo deja claro dónde está el riesgo. La cavidad nasal y los senos paranasales se comunican por múltiples ostios y están separados por septos delgados, de modo que la progresión hacia cavidades vecinas puede aparecer pronto. Por eso el contorneo sinonasal no debe basarse solo en la masa visible.
Principios generales de anatomía y patrones de diseminación
La respuesta breve es directa: estos casos obligan a pensar en un mapa anatómico amplio desde el primer corte. El capítulo incluye histologías muy distintas, como carcinoma escamocelular, adenocarcinoma de glándulas salivales menores, carcinoma adenoide quístico, estesioneuroblastoma, carcinoma sinonasal indiferenciado, carcinoma neuroendocrino de células pequeñas, melanoma y carcinoma NUT de línea media, pero todas comparten un problema práctico: la extensión rápida a través de cavidades conectadas.
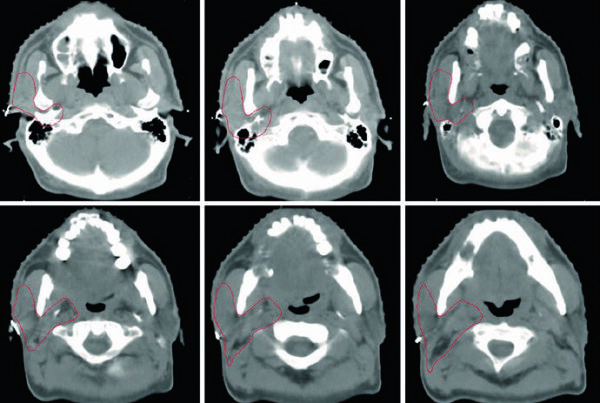
En tumores que nacen en la cavidad nasal superior, el capítulo destaca ENB, SNUC y SNEC porque pueden invadir con facilidad la lámina cribosa y avanzar hacia la fosa craneal anterior. Cuando ese patrón es plausible, esas regiones deben incluirse en el volumen objetivo.
Los tumores del seno maxilar siguen otra ruta, pero con la misma agresividad anatómica. Pueden invadir la cavidad nasal por la pared medial porosa, la encía maxilar por la pared lateral del antro, la fosa infratemporal o pterigopalatina por extensión posterior y la órbita por avance superior directo o a través de los senos etmoidales. El contorneo tiene que seguir esas rutas previsibles.
La extensión perineural requiere una actitud generosa. El texto recomienda cubrir nervios craneales aferentes y eferentes cuando existe propagación perineural, porque las metástasis microscópicas salteadas son frecuentes y el rescate puede ser difícil. Si un nervio está comprometido, la cobertura debe seguirlo hasta la base del cráneo. En carcinoma adenoide quístico, la cobertura neural se recomienda incluso sin invasión perineural patológica demostrada.
La irradiación ganglionar electiva se reserva para casos seleccionados. El capítulo la sugiere en ENB y en carcinoma escamocelular avanzado, sobre todo si el tumor se origina en el seno maxilar o compromete áreas con drenaje linfático abundante, como nasofaringe, mucosa, piel, mejilla, nariz anterior, encía maxilar o reborde alveolar.
Enfermedad macroscópica: volúmenes y dosis
La siguiente tabla resume la secuencia básica para enfermedad visible. El punto más práctico es que el CTV70 puede ser idéntico al GTV70 cuando la proximidad de estructuras críticas no permite una expansión cómoda.
| Volumen objetivo | Definición y descripción |
|---|---|
| GTV70 | Toda la enfermedad macroscópica en examen físico e imagen, incluyendo TC y RM. El PET puede ayudar a definir mejor la extensión tumoral, y la RM puede mostrar invasión perineural oculta en el PET. |
| CTV70 | Habitualmente idéntico al GTV70. Puede añadirse un margen de 3 a 5 mm si existe incertidumbre en la delimitación del tumor primario. Por la cercanía a estructuras críticas, ese margen puede reducirse a 0 mm; es decir, el GTV puede ser igual al CTV70. |
| PTV70 | CTV70 más 3 a 5 mm según la incertidumbre de posicionamiento. Ese margen puede reducirse a 1 mm cerca de estructuras normales críticas, como tronco encefálico y quiasma óptico. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 7.1). La enfermedad macroscópica se prescribe en fracciones de 1,8 a 2 Gy hasta 70 Gy.
Estudio diagnóstico relevante para la delineación
El capítulo es muy claro en este punto: la definición del volumen solo es fiable si la revisión diagnóstica es completa. Eso incluye historia y síntomas preoperatorios, examen neurológico con énfasis en nervios craneales, imágenes pre y posoperatorias, informe quirúrgico e informe anatomopatológico.
La endoscopia por fibra óptica sigue siendo importante, pero la localización tumoral depende de imagen diagnóstica de alta calidad. La erosión cortical ósea temprana se visualiza mejor en TC de alta resolución con contraste intravenoso y cortes finos de 1 a 2 mm de cavidad nasal y senos paranasales.
Cuando la pregunta clínica es extensión en tejidos blandos, invasión intracraneal, diseminación perineural o compromiso de forámenes y canales neurales, la técnica preferida es la RM fina con contraste intravenoso y secuencias con supresión grasa. El PET/CT ayuda a identificar ganglios y enfermedad metastásica. Esa combinación es la base real del GTV.
Simulación y localización diaria
La posición recomendada es concreta. El paciente debe simularse en decúbito supino, con apoyo cefálico y cuello extendido, usando una máscara Aquaplast personalizada de cinco puntos que inmoviliza cabeza, cuello y hombros.
El capítulo también incorpora detalles prácticos. Una tabla de tracción para hombros puede retirarlos del trayecto de los haces. El bite block puede desplazar la lengua en sentido inferior, lejos de la nasofaringe de alta dosis. En pacientes con muchas restauraciones metálicas, un protector oral a medida puede absorber dispersión electrónica y reducir mucositis relacionada con el tratamiento.
La TC de simulación debe utilizar cortes de 3 mm o menos con contraste intravenoso y abarcar desde el vértex hasta la carina. El isocentro suele ubicarse a nivel de los aritenoides. En casos posoperatorios conviene marcar las cicatrices con material radiopaco. Para IGRT, lo ideal es cone beam CT diario alineado a hueso; también es adecuado usar imágenes kilovoltaje diarias alineadas a hueso con cone beam semanal.
Delineación del blanco y volúmenes subclínicos
El GTV debe definirse con todas las fuentes clínicas relevantes y no con una sola modalidad. El capítulo cita de forma explícita endoscopia, TC, RM y PET. A partir de esa base, el CTV de alto riesgo debe cubrir todos los sitios iniciales de enfermedad y las rutas probables de extensión subclínica.
En el contexto posoperatorio, eso incluye el lecho de resección, las áreas de extensión ganglionar y todos los sitios iniciales de enfermedad preoperatoria, con consideración para cubrir todo el lecho posoperatorio y el colgajo. En el tratamiento definitivo, la recomendación es una expansión de 5 a 10 mm alrededor del tumor primario mientras se cubre el subsitio anatómico relevante y se respetan las barreras anatómicas. Los márgenes positivos o las áreas de extensión extranodal pueden justificar un CTV66, administrado de forma secuencial con 6 Gy en tres fracciones.
Regiones subclínicas de alto y bajo riesgo
Esta tabla separa los niveles de riesgo microscópico que guían la selección de dosis. Resume qué debe ir a 60-66 Gy y qué puede mantenerse en 50-54 Gy, incluyendo cuello no violado y cobertura profiláctica de nervios craneales.
| Volumen objetivo | Definición y descripción |
|---|---|
| CTV60-66 | Incluye regiones con alto riesgo de enfermedad microscópica. En el posoperatorio debe abarcar el lecho de resección, las áreas de extensión ganglionar y todos los sitios iniciales de enfermedad preoperatoria, considerando cubrir todo el lecho posoperatorio y el colgajo. En el contexto definitivo, incluye una expansión de 5 a 10 mm sobre el tumor primario y cobertura del subsitio anatómico relevante respetando límites anatómicos. |
| CTV66 | Debe considerarse para márgenes positivos o áreas de extensión extranodal. Puede administrarse de forma secuencial con 6 Gy en tres fracciones. |
| CTV50-54 | Incluye regiones subclínicas de bajo riesgo, como cuello no violado o cobertura profiláctica de nervios craneales. |
| PTV60-66 | CTV60-66 más 3 a 5 mm según la incertidumbre de posicionamiento y la técnica de imagen guiada. En áreas adyacentes a estructuras críticas, el margen puede reducirse a 1 mm. |
| PTV50-54 | CTV50-54 más 3 a 5 mm según la incertidumbre de setup y la técnica de IGRT utilizada. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 7.2). En casos posoperatorios, el CTV delineado puede ser una expansión del GTV preoperatorio y, cuando corresponda, del GTV posoperatorio según la extensión y localización tumoral.
Consideraciones anatómicas por subsitio para el CTV primario
La tabla 7.3 es la parte más operativa del capítulo. Convierte anatomía y patrones de diseminación en límites concretos para CTV60, CTV66 y CTV70 en cada subsitio sinonasal.
| Subsitio / histología | Eje anatómico o situación | Orientación de delineación |
|---|---|---|
| Carcinoma escamocelular del seno maxilar | Superior | Suelo orbitario y base del cráneo. La RM coronal puede ayudar a delimitar el compromiso del suelo orbitario. En casos con extensión intracraneal, considerar un margen dural de 5 mm. |
| Carcinoma escamocelular del seno maxilar | Inferior | Paladar duro, incluyendo al menos 10 mm de margen alrededor de la enfermedad macroscópica inicial. |
| Carcinoma escamocelular del seno maxilar | Medial | Tabique nasal en casos lateralizados. Si la extensión medial supera el tabique, considerar cobertura de toda la cavidad nasal. |
| Carcinoma escamocelular del seno maxilar | Lateral | Fosa infratemporal, incluyendo el espacio masticador. Si existe extensión lateral, considerar prolongar la cobertura a lo largo del músculo temporal. |
| Carcinoma escamocelular del seno maxilar | Posterior | Fosa pterigopalatina y base del cráneo, prestando atención a incluir la fisura infraorbitaria. El paladar duro posterior recibe inervación de una rama del CN V2. Si hay compromiso posterior, cubrir el trayecto de CN V2 y CN V3 hasta la cueva de Meckel. |
| Carcinoma escamocelular del seno maxilar | Nervios | Ramas de la segunda división del trigémino, nervio infraorbitario y nervios palatinos mayores. |
| Carcinoma escamocelular de cavidad nasal, ENB, SNUC, SNEC, melanoma | Superior | Lámina cribosa si está intacta; de lo contrario, incluir el injerto dural. Considerar un margen de 5 mm a lo largo de la duramadre cuando la lámina cribosa esté comprometida o exista extensión intracraneal macroscópica. |
| Carcinoma escamocelular de cavidad nasal, ENB, SNUC, SNEC, melanoma | Inferior | Paladar duro. |
| Carcinoma escamocelular de cavidad nasal, ENB, SNUC, SNEC, melanoma | Medial | Incluir toda la cavidad nasal. |
| Carcinoma escamocelular de cavidad nasal, ENB, SNUC, SNEC, melanoma | Lateral | Borde medial del seno maxilar ipsilateral en casos localizados. |
| Carcinoma escamocelular de cavidad nasal, ENB, SNUC, SNEC, melanoma | Posterior | Láminas pterigoideas, fosa pterigopalatina, seno etmoidal y seno esfenoidal. |
| Carcinoma escamocelular de cavidad nasal, ENB, SNUC, SNEC, melanoma | Nervios | Ramas del nervio olfatorio y de las dos primeras divisiones del trigémino, incluyendo nervios nasociliar y nasopalatino. |
| SNEC | Fraccionamiento y cuello electivo | Usar los volúmenes de cavidad nasal. Existe alto riesgo de enfermedad metastásica. Considerar fraccionamiento estándar o 45 Gy en 30 fracciones dos veces al día. La cobertura ganglionar electiva puede omitirse. |
| Melanoma mucoso de cavidad nasal | Fraccionamiento | Usar los volúmenes de cavidad nasal. Existe alto riesgo de enfermedad metastásica. Para tumores grandes, considerar fraccionamiento estándar. Para tumores pequeños, tratar solo el sitio primario con 30 a 36 Gy en fracciones de 6 Gy dos veces por semana. |
| Seno etmoidal | Superior | Seguir el mismo límite superior que en cavidad nasal. |
| Seno etmoidal | Inferior | Incluir un margen de 10 mm sobre la extensión tumoral inicial. En tumores tempranos, el cornete inferior puede ser suficiente. En enfermedad más avanzada, incluir el paladar duro. |
| Seno etmoidal | Medial / lateral | Incluir cavidad nasal, senos etmoidales y seno maxilar ipsilateral. Si la lámina papirácea está violada, incluir el recto medial. Un compromiso orbitario más avanzado puede requerir cobertura adicional. |
| Seno etmoidal | Posterior | Base del cráneo y seno esfenoidal. Los ganglios retrofaríngeos deben incluirse si el tumor compromete la nasofaringe o existe enfermedad N1. |
| Seno etmoidal | Cobertura ganglionar electiva | Las metástasis ganglionares son infrecuentes. Considerar irradiación electiva en tumores grandes T4 o enfermedad de alto grado, como carcinoma escamocelular o adenocarcinoma. |
| Seno etmoidal | Nervios | Ramas de la primera y segunda división del trigémino. La inervación parasimpática sigue el nervio vidiano. |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 7.3).
Dos recordatorios del texto merecen quedar subrayados. Los carcinomas adenoides quísticos son marcadamente neurotrópicos, por lo que los volúmenes deben abarcar nervios aferentes y eferentes locales hasta la base del cráneo. El ENB nace en la cavidad nasal superior y suele invadir pronto la lámina cribosa y la fosa craneal anterior; por eso esas regiones forman parte del CTV de alto riesgo.
Diseño de campos, drenaje ganglionar y estrategia de dosis
El plan final debe reflejar tanto la vía quirúrgica como el patrón esperado de drenaje. El capítulo menciona abordajes como degloving mediofacial, rinotomía lateral, resección craneofacial y resección endoscópica. Si se realizó una resección craneofacial, el injerto frontal debe incluirse en el volumen objetivo y los marcadores fiduciales quirúrgicos pueden ayudar a definir el lecho tumoral.
La irradiación electiva del cuello depende del criterio del médico tratante, pero el texto aporta una guía concreta: el drenaje regional incluye ganglios retrofaríngeos y niveles IB a IV; el nivel V debe cubrirse si existe compromiso nasofaríngeo; los ganglios faciales deben considerarse en tumores de cavidad nasal; la irradiación bilateral es habitual porque muchos primarios son de línea media; y los tumores del seno maxilar suelen tratarse de forma unilateral.
Las figuras clínicas muestran cómo esa lógica se traduce en dosis. Un caso posoperatorio de SNUC T4aN0M0 recibió 60 Gy en el lecho tumoral primario con cobertura de alto riesgo para lámina cribosa, seno etmoidal, seno esfenoidal y paladar duro, además de irradiación electiva bilateral a ganglios retrofaríngeos y niveles 1B a 4 con 54 Gy. Otro caso, un carcinoma escamocelular irresecable T4bN1M0 del seno maxilar izquierdo, recibió quimiorradioterapia definitiva con 70 Gy al tumor macroscópico y al ganglio comprometido, y CTV50 para suelo orbitario, fisura infraorbitaria, foramen redondo, fosa pterigopalatina, fosa infratemporal y espacio masticador.
El capítulo también muestra un caso adyuvante de carcinoma escamocelular de cavidad nasal anterior con cobertura de bajo riesgo para cavidad nasal, ganglios retrofaríngeos y ganglios faciales, un ENB Kadish C con cobertura de alto riesgo hasta duramadre, seno maxilar medial, etmoides, esfenoides, cavidad nasal, fosa pterigopalatina y foramen redondo, y un carcinoma adenoide quístico del seno maxilar con tumor residual posoperatorio y cobertura explícita de trayectos neurales, sin tratamiento electivo del cuello por la histología. Esos ejemplos no reemplazan las tablas, pero muestran cómo aplicarlas.
En cuanto a la técnica, los autores expresan una preferencia clara: enfoque secuencial con cone down. El plan inicial, en 30 fracciones y con dose painting, entrega 54 Gy a 1,8 Gy por fracción a regiones subclínicas de bajo riesgo y 60 Gy a 2 Gy por fracción a regiones subclínicas de alto riesgo. Después se agrega un cone down de 5 fracciones con 10 Gy adicionales solo para enfermedad macroscópica, completando 70 Gy en 35 fracciones.