No sarcoma pediatrico, o delineamento de volume alvo e o planejamento de campos comecam antes do primeiro contorno: histologia, sitio primario e resposta a quimioterapia de inducao mudam diretamente o volume final, a dose e ate a forma de simular o paciente. Sarcoma de Ewing e rabdomiossarcoma exigem integracao estreita entre CT, MRI, PET e anatomia regional, porque a diferenca entre tumor que apenas desloca estruturas e tumor que realmente as invade altera o campo de modo concreto. Para uma visao completa do tema, confira nosso Target Volume Delineation and Field Setup – Complete Clinical Guide.
Contexto Clinico, Anatomia e Disseminacao
O primeiro passo pratico e lembrar que os sarcomas pediatricos formam um grupo heterogeneo. Os algoritmos de tratamento variam por histologia, estagio, grupo de risco e, segundo o capitulo, ate pelo local geografico da pratica, como Europa versus Estados Unidos. Entre os tumores osseos, o sarcoma de Ewing e o segundo mais frequente na infancia; o primeiro e o osteossarcoma, no qual a radioterapia costuma ter papel menos central. Entre os sarcomas de partes moles, o rabdomiossarcoma e o subtipo predominante.
Em Ewing e em RMS, o tratamento local costuma ser combinado com quimioterapia sistemica. Quando a doenca e irressecavel, a radioterapia isolada costuma ser a estrategia definitiva; em cenarios de maior risco, ela tambem entra no pos-operatorio. A distribuicao anatomica ajuda a antecipar dificuldades. O Ewing aparece mais na pelve, em cerca de 25% dos casos, seguido pelo femur, com 16%. Isso importa porque tumores pelvicos frequentemente nao sao bons candidatos a resseccao e acabam seguindo para radioterapia definitiva.
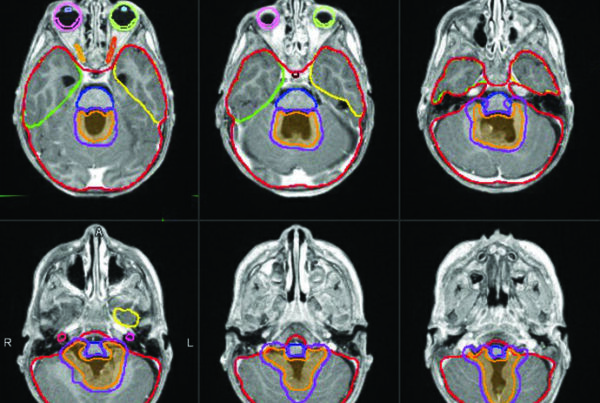
No RMS, a distribuicao e mais espalhada: cabeca e pescoco respondem por 35% dos sitios primarios, sistema geniturinario por 20% e extremidades por outros 20%. Dentro dos tumores de cabeca e pescoco, o texto separa lesoes parameningeas, orbitarias e de outras localizacoes. As parameningeas representam 15% de todos os casos de RMS e as orbitarias 10%; os outros sitios de cabeca e pescoco respondem por mais 10%. Essa divisao nao e burocratica. Lesoes parameningeas, situadas em uma das oito regioes resumidas pelo mnemnico MMNNOOPP, carregam risco maior de extensao direta ao sistema nervoso central e entram no grupo de sitio primario desfavoravel.
Na leitura da extensao local, os limites anatomicos reais seguem mandando no desenho do campo. Osso nao acometido e membranas intraossea funcionam como barreiras para disseminacao microscopica, embora erosao e invasao ossea nao sejam raras e devam ser checadas principalmente no CT. Outro ponto util do capitulo e a diferenca entre tumor que empurra e tumor que invade. Se a imagem pre-quimioterapia mostra massa apenas deslocando pulmao, bexiga ou alcas, a reducao volumetrica apos inducao pode justificar encolhimento do alvo. Ja a invasao verdadeira de estruturas vizinhas deve manter pelo menos alguma cobertura nos campos apos a quimioterapia.
A disseminacao nodal nao e dominante na maioria dos sarcomas pediatricos, mas ela aparece em contextos bem definidos. RMS de extremidade tem taxa nodal mais alta e frequentemente pede pesquisa por linfonodo sentinela. Em doenca geniturinaria, especialmente paratesticular, alguns pacientes podem passar por disseccao retroperitoneal ipsilateral com preservacao neural, em geral reservada para maiores de 10 anos. Mesmo assim, cobertura eletiva de cadeias nao costuma ser recomendada para a maior parte dos casos de RMS e Ewing. Quando ha metastase nodal documentada, o texto e claro: nao basta cobrir o linfonodo acometido; e prudente incluir ao menos parte de toda a bacia nodal envolvida.
Imagem Diagnostica para Definicao do Volume Alvo
Para definir GTV e CTV em sarcoma pediatrico, nao existe exame unico que resolva tudo. O capitulo trata CT e MRI como ferramentas complementares, enquanto o PET ganhou espaco tanto para estadiamento quanto para documentar os sitios inicialmente envolvidos antes da quimioterapia de inducao.
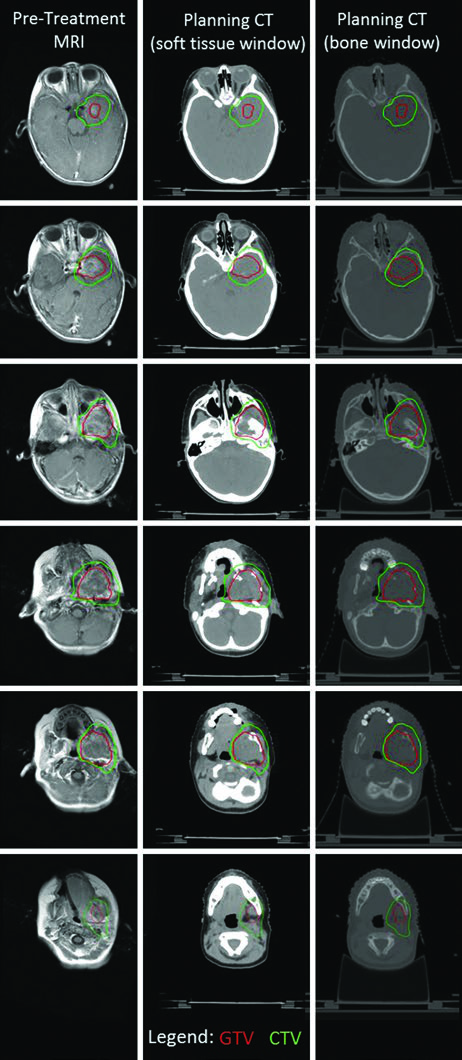
O CT tem papel mais forte quando a duvida principal e erosao, destruicao ou infiltracao ossea. O MRI oferece melhor separacao de partes moles e fica especialmente importante para estimar extensao intracraniana, como nos tumores parameningeos de cabeca e pescoco. O PET, por sua vez, vem sendo adotado com mais frequencia tanto em RMS quanto em Ewing no estadiamento inicial, com literatura de apoio para preferi-lo a tecnicas como cintilografia ossea em varios cenarios. Na pratica, ele ajuda a marcar o mapa da doenca antes da quimioterapia e evita que um local inicialmente metabolico, mas depois parcialmente resolvido, desapareca do raciocinio do planejamento.
Esse raciocinio vale ainda mais quando o tratamento local depende de distinguir contato, deslocamento e invasao. Uma lesao parameningea com erosao do assoalho craniano ou uma massa toracica que ocupava espaco depois retomado pelo pulmao normal nao pode ser interpretada apenas pela simulacao tardia. O alvo precisa nascer da fusao entre a anatomia de apresentacao e a anatomia residual.
Delineamento do Volume Alvo e Planejamento do Tratamento
Em Ewing, a logica pratica e trabalhar com dois momentos da doenca: o volume de apresentacao e o volume residual apos a inducao. No RMS, o tratamento pode usar dose unica ou dois niveis de dose, mas a decisao continua girando em torno da mesma pergunta: houve apenas efeito de massa sobre estruturas vizinhas ou existia invasao verdadeira?
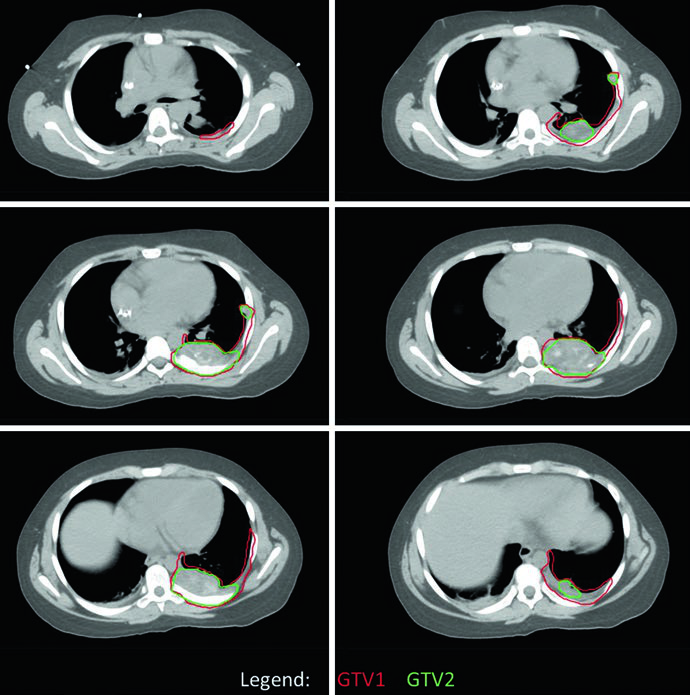
Volume-alvo em sarcoma de Ewing
A tabela abaixo resume como o capitulo organiza os volumes iniciais e os volumes reduzidos no Ewing. O ponto mais importante e que o GTV2 nao segue apenas o residual visivel: toda a extensao ossea pre-quimioterapia costuma permanecer dentro do volume reduzido.
| Volume-alvo | Definicao e descricao |
|---|---|
| Volumes iniciais (pre-inducao) | |
| GTV1 | Extensao macroscopia pre-quimioterapia da doenca inicial, incluindo osso, partes moles e linfonodos aumentados ou suspeitos nao ressecados. O GTV1 pode ser ajustado se o tumor inicial se estendia para cavidades ou espacos, como pelve e torax, e depois regrediu com a quimioterapia. |
| CTV1 | GTV1 + 1.0-1.5 cm. O CTV1 inclui bacias nodais envolvidas clinica ou patologicamente. |
| PTV1 | CTV1 + margem de setup especifica da instituicao e do tipo de guiagem por imagem, frequentemente de 3-5 mm. |
| Volumes reduzidos (pos-inducao) | |
| GTV2 | Tumor residual apos quimioterapia de inducao. Mesmo assim, toda a extensao ossea pre-quimioterapia costuma ser incluida no GTV2. No pos-operatorio, o GTV2 corresponde a doenca residual em osso ou partes moles e aos locais de margem positiva. |
| CTV2 | GTV2 + 1.0-1.5 cm. |
| PTV2 | CTV2 + margem de setup especifica da instituicao e do tipo de guiagem por imagem, frequentemente de 3-5 mm. |
Fonte: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Tabela 33.1)
Doses para Ewing sarcoma
As doses abaixo seguem o esquema descrito no protocolo COG AEWS1031, sempre em fracoes diarias de 1.8 Gy. O capitulo usa essa tabela como referencia objetiva para separar cenarios definitivos e pos-operatorios.
| Cenario | PTV1 (Gy) | PTV2 (Gy) |
|---|---|---|
| Radioterapia definitiva em todos os sitios, exceto vertebral | 45.0 | 10.8 |
| Radioterapia definitiva em localizacao vertebral | 45.0 | 5.4 |
| Ewing extraosseo com resposta completa a quimioterapia | 50.4 | 0 |
| Pos-operatorio com doenca residual microscopica (resseccao R1) e necrose tumoral >90% na patologia | 0 | 50.4 |
| Pos-operatorio com doenca residual microscopica (resseccao R1) e necrose tumoral <90% na patologia | 50.4 | 0 |
| Pos-operatorio com doenca residual macroscopica (resseccao R2) | 45.0 | 10.8 |
Fonte: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Tabela 33.2)
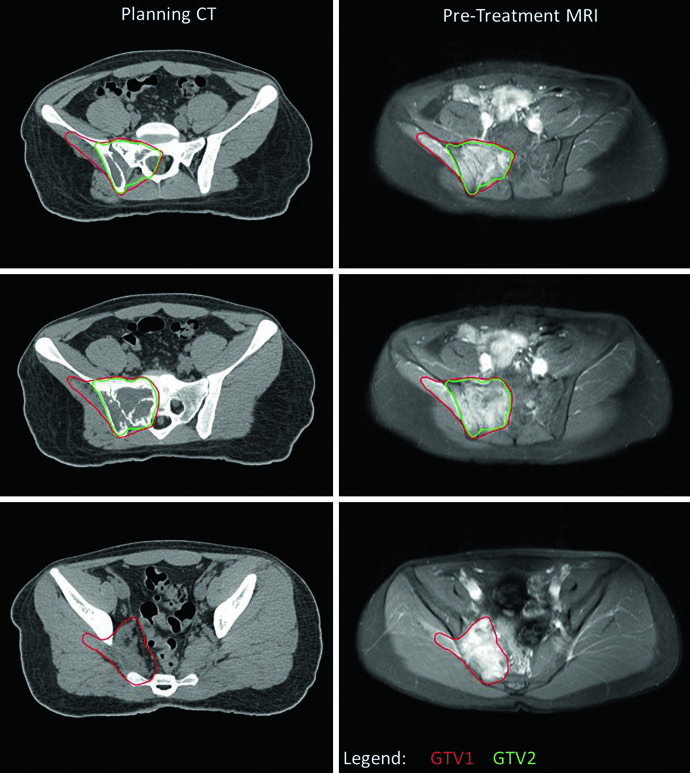
Os casos ilustrados no capitulo mostram bem como essa adaptacao funciona. No caso pelvico, os CTVs foram desenhados como GTV + 1.5 cm; em um dos cortes inferiores nao havia mais doenca residual e, por isso, o GTV2 desaparecia naquele nivel. O PTV1 recebeu 45.0 Gy e o PTV2 mais 10.8 Gy, totalizando 55.8 Gy. No exemplo toracico, uma simulacao em quatro dimensoes foi usada para captar a excursao respiratoria completa. Ali, os CTVs foram feitos com expansao de 1 cm, e o GTV1 foi adaptado para respeitar o espaco agora reocupado por pulmao normal apos a inducao, mantendo cobertura de todos os pontos de contato do tumor original.
No RMS, o capitulo chama atencao para uma mudanca conceitual relevante: a classificacao histologica isolada vem cedendo espaco a uma leitura molecular do risco. Protocolos atuais do COG usam status de fusao em vez da divisao classica entre embrionario e alveolar. Fusoes envolvendo FOX01, geralmente PAX3-FOX01 em t(2;13) e PAX7-FOX01 em t(1;13), definem historia natural de maior risco. Ja tumores alveolares sem fusao tendem a se comportar de forma mais proxima do RMS embrionario.
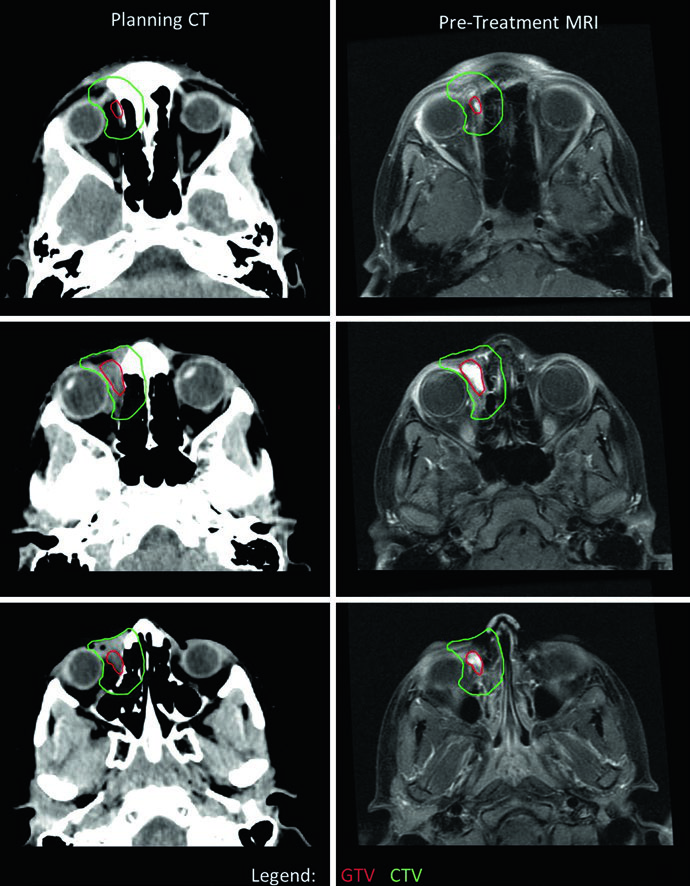
Volume-alvo em rabdomiossarcoma
No RMS, a reducao volumetrica para boost so e segura quando a imagem inicial mostrava deslocamento de estruturas como torax ou pelve. Lesao invasiva, sobretudo parameningea, costuma exigir cobertura mais fiel da extensao pre-quimioterapia ate a dose maxima.
| Volume-alvo | Definicao e descricao |
|---|---|
| GTV1 | Extensao macroscopia pre-quimioterapia da doenca inicial, incluindo osso, partes moles e linfonodos aumentados ou suspeitos nao ressecados. |
| CTV1 | GTV1 + 1 cm. O CTV1 inclui bacias nodais com envolvimento clinico ou patologico. |
| PTV1 | CTV1 + margem de setup especifica da instituicao e do tipo de guiagem por imagem, frequentemente de 3-5 mm. |
| GTV2 | Tumor residual apos quimioterapia de inducao, excluindo areas em que o tumor inicial apenas empurrava estruturas vizinhas, como torax ou pelve. Doenca invasiva pre-quimioterapia, principalmente no RMS parameningeo de cabeca e pescoco, deve em geral permanecer no GTV2 independentemente da resposta. |
| CTV2 | GTV2 + 1 cm. |
| PTV2 | CTV2 + margem de setup especifica da instituicao e do tipo de guiagem por imagem, frequentemente de 3-5 mm. |
Fonte: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Tabela 33.3)
Doses para rabdomiossarcoma
O capitulo sintetiza o fracionamento do RMS em funcao de grupo cirurgico, estado nodal, resposta e status de fusao. O quadro abaixo organiza essas indicacoes, sempre em fracoes diarias de 1.8 Gy.
| Grupo | Status de fusao | Dose (Gy) |
|---|---|---|
| I (resseccao R0) | Negativo (embrionario) | 0 |
| I (resseccao R0) | Positivo (alveolar) | 36.0 |
| II, N0 com R1 microscopico | Qualquer | 36.0 para a doenca pre-quimioterapia |
| II, N+ com linfonodo envolvido e ressecado | Qualquer | 41.4 para o sitio pre-quimioterapia e a regiao nodal |
| III, nao orbitario e orbitario com resposta incompleta apos inducao | Qualquer | 50.4* |
| III, orbitario com resposta completa apos inducao | Qualquer | 45.0** |
| Consideracoes especiais | ||
| III, no ARST1431, tumor >5 cm pre-quimioterapia sem resposta completa apos inducao | Qualquer | 59.4* |
| III, no ARST1431, resposta completa radiologica ou confirmada por biopsia na semana 9 | Qualquer | 36.0*** |
| RMS de extremidade, N0 clinico e patologico, apos amputacao | Qualquer, incluindo alveolar/fusao-positiva | 0 |
Fonte: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Tabela 33.4)
* No ARST1431, a reducao de volume pode ser feita apos 36.0 Gy, de modo que o PTV1 receba 36.0 Gy e o PTV2 receba o cone-down adicional de 14.4 Gy ou 23.4 Gy, conforme o tamanho tumoral e o contexto clinico.
** No ARST1431, doenca de grupo III com resposta completa na reavaliacao da semana 9 pode ser tratada com dose unica de 36.0 Gy em PTV1, sem boost adicional. Por isso, primarios orbitarios com resposta completa podem receber 36.0 Gy; o capitulo mantem 45.0 Gy como referencia geral da tabela.
*** Resposta completa radiologica por CT/MRI e metabolica por FDG-PET, ou ausencia de doenca residual em biopsia na semana 9, permite tratamento em dose unica de 36.0 Gy no PTV1.
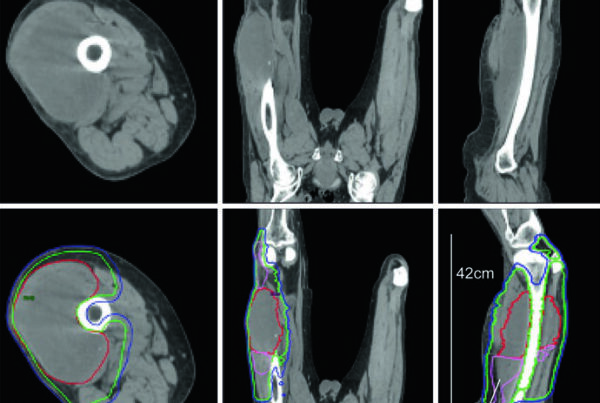
Os exemplos clinicos reforcam onde essa logica falha ou precisa ser mantida integralmente. O RMS parameningeo da fossa infratemporal com extensao intracraniana e erosao ossea foi tratado desde o inicio com dose unica de 50.4 Gy, porque nao havia margem segura para esperar reducao volumetrica antes da radioterapia. O caso orbitario, com resposta incompleta a quimioterapia, tambem seguiu para volume unico de 50.4 Gy; o CTV foi desenhado como GTV + 1 cm e chegou a ultrapassar a orbita ossea em alguns cortes por suspeita de erosao. O detalhe tecnico mais interessante foi o desvio ocular para a direita, usado para melhorar poupanca de lente e nervo optico. Ja no RMS de extremidade com adenopatia axilar, a equipe preferiu contornar toda a bacia axilar como GTV para nao subdosar uma disseminacao nodal extensa vista no PET. Como o sitio primario respondeu pouco e a axila so parcialmente, tanto a mao quanto a bacia axilar foram conduzidas com 50.4 Gy em dose unica. O texto ainda destaca que nao havia doenca em transito entre a mao direita e a axila, motivo pelo qual o braco entre esses pontos nao foi irradiado.
Simulacao, Imobilizacao, Dispositivos e Localizacao Diaria
O setup em sarcoma pediatrico precisa seguir a anatomia tratada, nao um molde universal. O capitulo e direto: mascara termoplastica para cabeca e pescoco, bracos elevados com VacLok ou cradle semelhante e wingboard para torax, imobilizacao de pelve e coxas proximais com VacLok para lesoes pelvicas, e dispositivos personalizados para extremidades, incluindo em alguns casos posicao feet-first ou mesmo nao supina.
Quando existe suspeita de movimento respiratorio relevante, a simulacao em quatro dimensoes entra como ferramenta de decisao, e nao como detalhe opcional. Esse principio aparece no caso toracico de Ewing e conversa bem com o raciocinio usado em nosso artigo sobre cancer de pulmao: delineamento e campos, onde a excursao respiratoria tambem redefine o alvo tratado. Em lesoes pelvicas, sobretudo geniturinarias, o enchimento vesical pode alterar a posicao do alvo. O capitulo sugere considerar ultrassom diario para reproduzir enchimento de bexiga em prostata e bexiga, e em criancas com pouca previsibilidade pode ser util simular tanto com bexiga cheia quanto vazia para capturar toda a excursao possivel.
Ha ainda detalhes bem praticos. Em meninos com sarcomas pelvicos ou de coxa proximal, a posicao em frog-leg pode ser usada se houver protecao testicular. A frequencia e o tipo de guiagem por imagem definem a expansao de CTV para PTV; muitas instituicoes usam imagem kV diaria e, por isso, trabalham com margens de 3-5 mm. Em casos muito proximos de estruturas criticas, especialmente cabeca e pescoco, margens menores podem ser consideradas se a rotina de IGRT for robusta. O texto tambem lembra que simulacao com MRI em posicao de tratamento pode complementar a simulacao por CT. Para pacientes pequenos, geralmente abaixo de 8 anos, a equipe deve antecipar a necessidade de sedacao ou anestesia diaria tanto na simulacao quanto durante o tratamento.
Avaliacao do Plano
Na avaliacao final do plano, a meta de cobertura e objetiva: pelo menos 95% do PTV, ou dos PTVs, deve receber a dose prescrita. O capitulo tambem recomenda limitar hotspots acima de 110%, idealmente com no maximo 10% do PTV recebendo 110% ou mais.
Restricoes convencionais de tecido normal
As restricoes abaixo resumem os limites convencionais citados para Ewing e RMS. O proprio texto avisa que elas devem ser ponto de partida, nao teto complacente, porque os riscos tardios da radioterapia pediatrica sao profundos.
| Orgao/tecido | Volume (%) | Dose (Gy) |
|---|---|---|
| Tronco encefalico | Point max | 54 |
| Quiasma optico/nervo optico | Point max | 54 |
| Medula espinhal | Point max | 45 |
| Cristalino | Point max | 6 |
| Coclea | Point max | 35 |
| Coracao | 100 | 30 |
| Pulmoes bilaterais | 20 | 20 |
| Pulmoes bilaterais | 100 | 15 |
| Figado | 100 | 23.4 |
| Figado | 50 | 30 |
| Rins bilaterais | 50 | 24 |
| Rins bilaterais | 100 | 14.4 |
| Intestino delgado | 50 | 45 |
| Bexiga | 100 | 45 |
| Reto | 100 | 45 |
Fonte: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Tabela 33.5)
Esse cuidado com OAR vale ainda mais em pediatria. O capitulo sugere buscar poupanca mais agressiva que a minima tabelada e abre espaco para considerar protonterapia, embora detalhes de tecnica, incerteza de alcance e arranjo de feixes fiquem fora do escopo. Na conversa com familia e paciente, a analise do plano precisa antecipar efeitos agudos e tardios do sitio tratado. Em cabeca e pescoco, entram dentofaciais, xerostomia, xerophthalmia, queda de acuidade visual, catarata, assimetria facial, endocrinopatias e disfuncao neurocognitiva. Em extremidades, preocupam fechamento epifisario e reducao do crescimento osseo. Em irradiacao vertebral, o texto lembra risco de menor estatura, cifose, lordose e escoliose, reduzido quando se cobre o corpo vertebral completo em criancas pre-puberes. Em torax, surgem pneumonite, fibrose pulmonar e cardiotoxicidade. Em pelve, ganham peso cistite, incontinencia ou estenose urinaria e infertilidade, risco que ainda deve ser lido ao lado da quimioterapia utilizada, especialmente ciclofosfamida.
Na pratica, este capitulo mostra que planejamento de sarcoma pediatrico nao premia rigidez. O melhor plano costuma nascer da combinacao entre imagem de apresentacao, resposta biologica e setup reproduzivel. Se voce quiser revisar o contexto maior da serie, vale retornar ao guia completo, que conecta este raciocinio a outros cenarios de delineamento em radioterapia.