Introducción a la Protonterapia y Monte Carlo
La protonterapia se ha consolidado como una de las técnicas más precisas de radioterapia externa, aprovechando el pico de Bragg para concentrar la dosis en el volumen blanco con una caída abrupta en la región distal. Sin embargo, la precisión que hace a los protones tan atractivos clínicamente también exige modelos de cálculo de dosis a la altura — y ahí es donde Monte Carlo se vuelve indispensable.
A diferencia de los fotones — cuyas interacciones están dominadas por el efecto Compton y el fotoeléctrico — los protones pierden energía mediante ionizaciones, dispersión múltiple de Coulomb e interacciones nucleares. Cada proceso depende de modelos físicos distintos, secciones eficaces y constantes de materiales que los algoritmos analíticos simplifican considerablemente. Monte Carlo rastrea cada partícula individualmente y aplica distribuciones de probabilidad reales para cada interacción, alcanzando una precisión en dosis de aproximadamente 1%–2%, frente a incertidumbres potencialmente mayores de los algoritmos de pencil beam.
Para una visión completa de todas las aplicaciones de Monte Carlo, consulte nuestra guía completa sobre Monte Carlo en Radioterapia.
Entrega del Haz: Dispersión Pasiva vs. Barrido
Existen dos paradigmas fundamentales en la entrega de protones, y la complejidad de la simulación Monte Carlo varía drásticamente entre ambos.
En la dispersión pasiva, el haz se ensancha mediante un sistema de doble dispersión y se modula con una rueda moduladora rotatoria que crea el spread-out Bragg peak (SOBP). Colimadores (aperturas) conforman lateralmente el campo, y compensadores de rango moldean el borde distal a la forma del blanco. Cada campo posee una configuración única del cabezal — energía, dispersores, modulador, apertura y compensador — lo que hace que los phase spaces sean poco reutilizables y las simulaciones computacionalmente costosas.
En el barrido de haz (beam scanning), dos imanes deflectan pencil beams individuales en las direcciones $x$ e $y$, mientras la energía se ajusta capa por capa antes de que el haz entre en la sala. No se requiere hardware específico para el paciente (aunque pueden usarse aperturas para mejorar la penumbra). Esta simplicidad permite construir modelos de fuente analíticos y phase spaces reutilizables, haciendo viable el uso clínico rutinario de Monte Carlo en barrido.
Como regla práctica, aproximadamente el 1% de los protones primarios sufre una interacción nuclear por centímetro de alcance del haz. Estas interacciones generan un halo nuclear alrededor de cada pencil beam, con contribución significativa cuando múltiples beamlets se superponen. Las simulaciones Monte Carlo deben predecir este halo correctamente para obtener dosis precisas — algo que los algoritmos analíticos típicamente ignoran o tratan de forma simplificada.
Caracterización del Haz en la Entrada del Cabezal
El punto de partida de cualquier simulación Monte Carlo en protonterapia es la parametrización del haz en la entrada del cabezal de tratamiento. Las variables clave son: energía del haz ($E$), dispersión de energía ($\Delta E$), tamaño del spot ($\sigma_x$, $\sigma_y$) y distribución angular ($\sigma_{\theta x}$, $\sigma_{\theta y}$).
El tamaño típico de un haz de protones está en el rango de 2–8 mm en $\sigma$, mientras que la dispersión angular es del orden de 2–5 mm-mrad para haces provenientes de un ciclotrón. Para dispersión pasiva, la dispersión angular en la entrada del cabezal tiene poca influencia en el haz de salida, ya que el material dispersor domina. Para beam scanning, la correlación entre la posición de la partícula dentro del spot y su momento angular necesita ser modelada — una parametrización completa del espacio de fases puede derivarse de la línea de haz magnética o por ajuste a datos medidos.
La dispersión de energía de un ciclotrón es típicamente menor al 1% ($\Delta E/E$), mientras que los sincrotrones pueden extraer haces con dispersión de energía dos órdenes de magnitud menor. Medir la energía con precisión suficiente involucra análisis de curvas de Bragg en agua o técnicas de dispersión elástica.
Modelado Monte Carlo del Cabezal de Tratamiento
La fidelidad con que se modela el cabezal depende del objetivo de la simulación. Para cálculo de dosis en el paciente, basta incluir los principales dispositivos de conformación del haz. En beam scanning, son los imanes de barrido y eventuales aperturas. En dispersión pasiva, incluye el sistema de doble dispersión, rueda moduladora, apertura y compensador.
La rueda moduladora — un componente mecánico rotativo con pistas de diferentes espesores — puede tratarse en Monte Carlo como múltiples geometrías estáticas o aplicando técnicas 4D que cambian la geometría dinámicamente. Los materiales comunes de las pistas incluyen polietileno (lexan) y plomo; una variación del 10% en la densidad de estos materiales puede causar cambios de alcance del orden de 1 mm.
Las aperturas deben modelarse explícitamente debido a la radiación secundaria y efectos de edge scattering. Los compensadores con geometría irregular requieren importación CAD o definición por puntos de contorno. Para simular patrones de barrido, las técnicas Monte Carlo 4D permiten estudiar detalles de los parámetros de entrega.
Monte Carlo también se utiliza para diseñar detectores de gamma prompt para verificación de alcance, optimizar reconstrucción de imágenes para tomografía computarizada con protones y estudiar dispersión en colimadores multiláminas como alternativa a aperturas específicas por paciente. Las simulaciones pueden además apoyar programas de QA clínico, reduciendo la necesidad de estudios experimentales repetitivos al definir tolerancias para parámetros del haz.
Phase Spaces y Modelos de Fuente
Un phase space registra tipo, energía, dirección y posición de típicamente decenas a cientos de millones de partículas en un plano perpendicular al eje central del haz. Para dispersión pasiva, los phase spaces en la salida del cabezal son poco útiles — cada campo tiene configuración única. Sin embargo, para beam scanning, las variaciones se limitan a energía y configuraciones de imanes, y los phase spaces se vuelven altamente reutilizables.
Más allá de los phase spaces, los modelos de fuente analíticos son viables para beam scanning: cada pencil beam se parametriza por posición ($x$, $y$), energía, peso, divergencia y dispersión angular, derivados de mediciones de fluencia en aire y curvas dosis-profundidad en agua. Las partículas secundarias generadas en el cabezal típicamente pueden despreciarse.
Una precaución importante: caracterizar cada beamlet con una distribución Gaussiana simple sobreestima la fluencia en el centro, ya que ignora el halo de protones dispersados en gran ángulo. Una segunda Gaussiana en el formalismo suele ser necesaria para la corrección. Este hecho tiene implicación directa en la viabilidad del Monte Carlo clínico — dado que la mayor parte del tiempo computacional en dispersión pasiva se gasta rastreando partículas por el cabezal, el barrido de haz es órdenes de magnitud más eficiente para simulación.
Conversión CT y Asignación de Materiales
En el cálculo de dosis con Monte Carlo, cada vóxel CT debe convertirse en composición material, densidad de masa y potencial de ionización. A diferencia de los algoritmos analíticos que usan stopping power relativo, Monte Carlo opera con propiedades materiales explícitas.
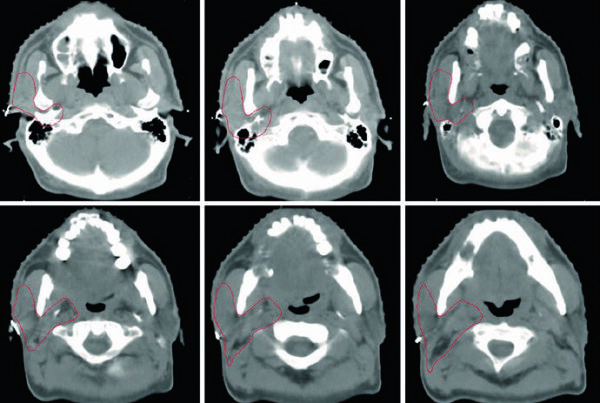
Los esquemas de conversión CT agrupan tejidos en 5–30 grupos que comparten composición material. Sin embargo, tejidos blandos en el rango de 0–100 unidades Hounsfield (HU) se distinguen pobremente — números CT similares pueden representar composiciones elementales distintas. Un cambio de método de conversión puede influir en el alcance del haz en 1–2 mm en tratamientos de cabeza y cuello.
| Parámetro de Conversión | Impacto Típico | Observación |
|---|---|---|
| Composición elemental | Efecto más significativo | Diferencias en H, C, O, Ca entre métodos (Schneider vs Rogers) |
| Densidad de masa | Papel menor en región blanco | Más relevante en hueso e interfaces |
| Energía media de excitación | 5%–15% de incertidumbre | Impacta directamente la predicción de alcance |
| CT dual-energy | Mejora asignación material | Proporciona dos mapas de atenuación para composiciones más precisas |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
Las energías medias de excitación para tejidos poseen incertidumbres del 5%–15%, reflejadas directamente en la predicción de alcance. El CT dual-energy mejora significativamente la asignación material al proporcionar dos mapas de atenuación diferentes, permitiendo determinar densidades electrónicas relativas y números atómicos efectivos con mayor precisión.
Dosis Absoluta y Dosis-en-Agua vs. Dosis-en-Tejido
Los sistemas de planificación prescriben dosis en Gy por GigaProtones o en cGy por unidad monitora (MU). Monte Carlo puede simular directamente la carga recolectada en la cámara de ionización de transmisión del cabezal — pero esto requiere muchas historias y un modelo detallado del nozzle. Alternativamente, se puede relacionar el número de protones en la entrada del cabezal con la dosis en un SOBP en agua, método equivalente cuando el modelo del cabezal es preciso.
Una distinción fundamental: los algoritmos analíticos calculan dosis-en-agua (la experiencia clínica, mediciones y constraints se basan en esto), mientras que Monte Carlo calcula intrínsecamente dosis-en-tejido. La diferencia puede alcanzar 10%–15% en anatomía ósea, pero es del orden de ~2% en tejidos blandos. En la práctica, una conversión retroactiva multiplicando por stopping powers relativos independientes de energía alcanza precisión de ~1%.
Interacciones Nucleares e Impacto en la Dosis
Las interacciones nucleares contribuyen con bastante más del 10% de la dosis total, especialmente en la región de entrada de la curva de Bragg, donde protones secundarios causan buildup por emisión predominantemente frontal. La reducción de fluencia primaria por colisiones nucleares también es notable.
La energía media en el pico de Bragg es aproximadamente el 10% de la energía inicial. La sección eficaz de interacciones nucleares alcanza su máximo en ~20 MeV y decrece rápidamente, haciendo despreciable la contribución nuclear cerca de la posición del pico de Bragg prístino. Para un SOBP, sin embargo, las contribuciones proximales al pico mantienen relevancia, causando una inclinación (tilt) en el plateu del SOBP si se desprecian.
Para cálculos de dosis en el paciente, solo los protones secundarios de interacciones protón-núcleo necesitan rastrearse — la energía de otras partículas secundarias puede depositarse localmente cuando su alcance proyectado es menor que el tamaño del vóxel. Conozca más sobre estos principios en nuestro artículo sobre fundamentos de Monte Carlo en radioterapia.
Monte Carlo vs. Algoritmos Analíticos: Diferencias Clínicas
La mayoría de los planes de tratamiento en protonterapia aún utiliza algoritmos analíticos de pencil beam, y Monte Carlo se ha usado tanto para validación como para commissioning. Las diferencias son clínicamente significativas en regiones con heterogeneidades tisulares pronunciadas.
Diferencias en Alcance Predicho
El alcance de un campo clínico de protones se define como $R_{90}$ — la posición del nivel de 90% de dosis en la caída distal del SOBP. Globalmente, las diferencias de alcance entre analítico y Monte Carlo son pequeñas (ambos comisionados en agua). Localmente, sin embargo, discrepancias significativas ocurren donde el haz atraviesa heterogeneidades.
En la práctica clínica, márgenes de alcance del orden de 3,5% + 1 mm se aplican comúnmente. Con Monte Carlo, estos márgenes podrían reducirse uniformemente a 2,4% + 1,2 mm, independientemente de la complejidad geométrica del paciente. Para geometrías homogéneas (como hígado), los márgenes pueden ser tan bajos como 2,7% + 1,2 mm, pero para geometrías con heterogeneidades laterales (cabeza y cuello, pulmón), el analítico puede requerir hasta 6,3% + 1,2 mm.
| Geometría | Margen con Analítico | Margen con Monte Carlo |
|---|---|---|
| Homogénea (hígado) | 2,7% + 1,2 mm | 2,4% + 1,2 mm |
| Heterogeneidades laterales (cabeza/cuello, pulmón) | Hasta 6,3% + 1,2 mm | 2,4% + 1,2 mm |
| Genérica (práctica corriente) | 3,5% + 1 mm | 2,4% + 1,2 mm |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
Diferencias en la Dosis Predicha
La mayor dispersión múltiple predicha por Monte Carlo causa un ensanchamiento de la distribución de dosis y consecuentemente menor dosis en la región de alto-medio dose. La dosis en el blanco por Monte Carlo es generalmente ligeramente menor que la predicha por el analítico. Para pacientes de cabeza y cuello y pulmón, diferencias en la dosis media del blanco pueden alcanzar el 4%. En mama e hígado, se mantienen alrededor del 2%. Campos pequeños son aún más sensibles.
Casos extremos incluyen implantes metálicos — como implantes dentales en cáncer de cabeza y cuello — que causan perturbaciones de dosis significativas, típicamente no predichas con precisión por algoritmos analíticos debido a la naturaleza de alto-Z de estos materiales. Para detalles sobre cálculo de dosis en escenarios complejos, vea nuestro artículo sobre cálculo de dosis Monte Carlo en el paciente.
Implementación Clínica y Planificación Basada en Monte Carlo
Implementar Monte Carlo en la clínica de protonterapia implica transferir información del sistema de planificación al código Monte Carlo vía interfaz DICOM-RTion. Los principales centros de protones ya operan con sistemas Monte Carlo in-house para verificación de dosis o investigación. La interfaz necesita traducir ángulo de gantry, ángulo de mesa, posición de isocentro, dimensiones de vóxel y dosis prescrita.
Para planificación inversa con Monte Carlo (IMPT), los requisitos computacionales son más estrictos — cada beamlet posible debe precalcularse con alta precisión estadística antes de la optimización. Herramientas rápidas de Monte Carlo son esenciales. En la práctica, la optimización puede basarse en el algoritmo analítico y usar Monte Carlo solo para ajustes finos o en checkpoints limitados durante el proceso iterativo.
Los principales proveedores de sistemas de planificación trabajan actualmente en la incorporación de Monte Carlo. Mejoras tanto en la eficiencia computacional del software como en el hardware han hecho viable su uso rutinario.
QA Avanzado con Monte Carlo en Protonterapia
El control de calidad en protonterapia se beneficia enormemente de Monte Carlo de varias formas:
Primero, las simulaciones pueden definir tolerancias para parámetros del haz. Variando sistemáticamente parámetros de entrada y observando el impacto en las distribuciones de dosis, se establecen límites aceptables para tamaño de spot, energía y alineación del cabezal sin necesidad de mediciones extensivas.
Segundo, Monte Carlo se usa para recalcular planes a partir de log files de tratamiento, permitiendo verificación dosis-entrega que considera lo que realmente se entregó, no solo lo planificado.
Tercero, aplicaciones de verificación de alcance usan simulaciones Monte Carlo para modelar la emisión de gamas prompt — fotones emitidos durante interacciones nucleares que portan información sobre la posición del pico de Bragg in vivo. Monte Carlo es esencial para diseñar detectores y optimizar algoritmos de reconstrucción.
Cuarto, simulaciones de distribuciones de LET (transferencia lineal de energía) son fundamentales para consideraciones radiobiológicas. El LET varía considerablemente a lo largo de la profundidad en protonterapia, con implicaciones directas para la efectividad biológica relativa (RBE). Monte Carlo permite mapear estas distribuciones con precisión espacial que las mediciones experimentales difícilmente alcanzan.
Finalmente, simulaciones de track structure a escala nanométrica — usando extensiones como TOPAS-nBio basado en Geant4-DNA — permiten investigar daños al ADN y clustering de ionizaciones en volúmenes subcelulares, conectando la física del transporte de partículas directamente con la radiobiología.
Códigos Monte Carlo para Protonterapia
Diversos códigos están disponibles para simulaciones en protonterapia:
| Código | Base | Características |
|---|---|---|
| TOPAS | Geant4 | Interfaz amigable, sin necesidad de programación; apoyado por NCI |
| GATE | Geant4 | Framework para aplicaciones de radioterapia e imagen |
| GAMOS | Geant4 | Framework de simulación con interfaz simplificada |
| PTsim | Geant4 | Dedicado a protonterapia |
| FICTION | FLUKA | Wrapper para FLUKA orientado a radioterapia |
| FLUKA | Standalone | Código multipropósito con modelos nucleares detallados |
| MCNPX | Standalone | Amplia biblioteca de secciones eficaces |
| VMCpro | Standalone | Optimizado para velocidad en protonterapia |
| Shield-Hit | Standalone | Enfocado en iones pesados y protones |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
TOPAS merece mención especial: diseñado dentro de la iniciativa ‘Informatics Technologies for Cancer Research’ del NCI, permite que no-expertos y no-físicos realicen simulaciones Monte Carlo complejas sin necesidad de programación. Para más sobre códigos y aplicaciones en diferentes modalidades, vea nuestro artículo sobre Monte Carlo para haces de iones.
Eficiencia Computacional y Perspectivas
La eficiencia de Monte Carlo en protonterapia depende de varios factores: número de historias, tamaño de paso (limitado por el vóxel CT, típicamente 0,5–5 mm), y algoritmos de tracking en geometría voxelizada. Técnicas de re-segmentación de la geometría y denoising (suavizado) de distribuciones de dosis permiten reducir el número de historias necesarias, aunque deben aplicarse con cautela — los métodos de suavizado tienden a suavizar gradientes de dosis, lo cual es especialmente problemático en protonterapia.
La incertidumbre estadística deseada es típicamente menor al 2% en el volumen blanco. Se necesitan menos protones para alcanzar esta precisión comparado con fotones, ya que los protones son directamente ionizantes con mayor LET. La interpolación de la grid CT a vóxeles mayores no es recomendada antes de la simulación (el promedio de composiciones materiales no está bien definido), pero el re-sampling puede hacerse después del cálculo de dosis con ponderación volumétrica adecuada.
Con la evolución simultánea de software (códigos más eficientes, GPUs) y hardware, Monte Carlo para protonterapia avanza firmemente hacia convertirse en el estándar de cálculo de dosis — reemplazando progresivamente los algoritmos analíticos que dominaron las últimas décadas. Para entender cómo la inteligencia artificial puede acelerar aún más esta transición, consulte nuestro artículo sobre IA y el futuro de Monte Carlo en radioterapia.