El Monte Carlo dejó de ser exclusivo de centros de investigación. Hoy, sistemas de planificación como Monaco (Elekta), iPlan (BrainLab) y opciones dentro de Eclipse (Varian) ofrecen cálculo de dosis basado en simulación estocástica — y la alternativa determinística Acuros XB ofrece precisión comparable con tiempos de cálculo drásticamente menores. En este artículo, exploramos cómo funciona el método Monte Carlo en el contexto clínico, qué códigos MC sustentan los TPS comerciales y por qué la ecuación de transporte de Boltzmann resuelta por Acuros XB representa un cambio de paradigma para la rutina del físico médico.
Para una visión completa de la evolución de los algoritmos — desde los métodos empíricos hasta las técnicas de convolución — consulte nuestra guía completa sobre algoritmos de cálculo de dosis por fotones.
Monte Carlo en Radioterapia: ¿Por Qué Simular Partícula por Partícula?
El Monte Carlo resuelve numéricamente la ecuación de transporte de Boltzmann rastreando millones de partículas individuales. A diferencia de los algoritmos analíticos que aproximan el transporte con kernels o pencil beams, el MC reproduce cada interacción fotón–electrón según las secciones eficaces conocidas. El resultado es la distribución de dosis más precisa que se puede obtener computacionalmente.
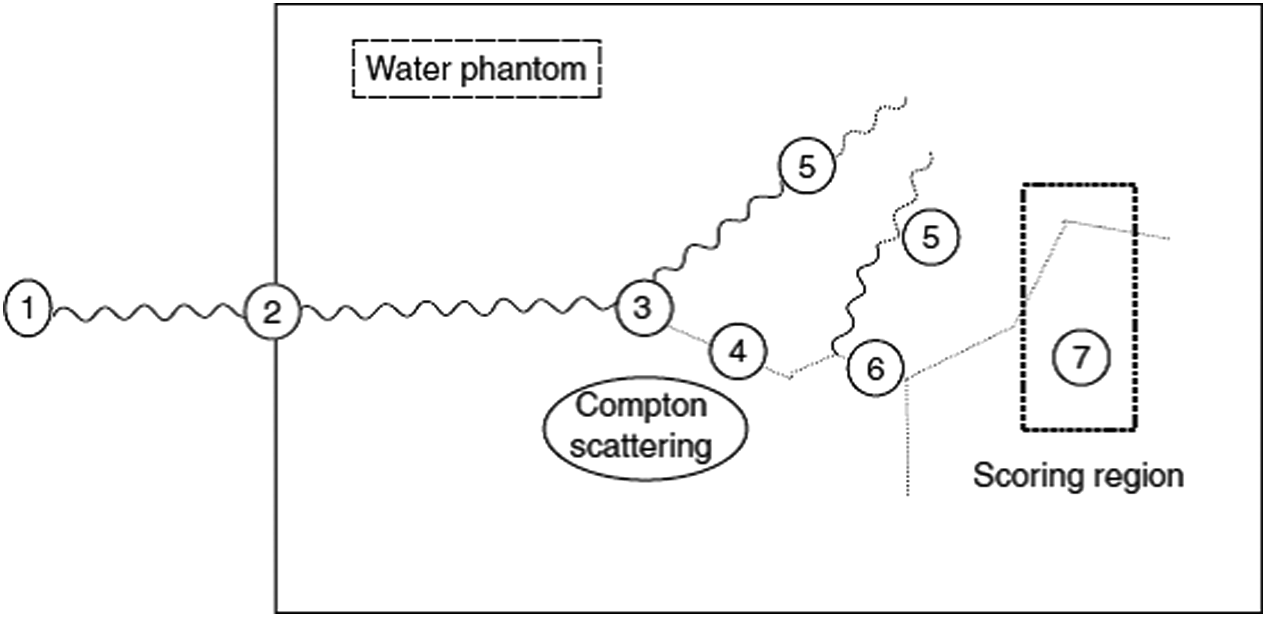
La simulación comienza con el espacio de fase (phase-space) — energía, posición y dirección de cada partícula. Un fotón de 1 MeV sufre en promedio 14–15 interacciones en agua antes de la absorción fotoeléctrica. Cada interacción se selecciona por muestreo aleatorio de la función de distribución de probabilidad acumulativa (CPD): producción de pares, dispersión Compton, absorción fotoeléctrica y dispersión Rayleigh. La distancia hasta la próxima interacción sigue:
$$x = -\frac{1}{\mu_{tot}} \ln(1 – R)$$
Donde:
- $\mu_{tot}$ = coeficiente de atenuación total del medio (suma de todos los procesos de interacción)
- $R$ = número aleatorio uniformemente distribuido entre 0 y 1
Para electrones, la situación cambia radicalmente. Un electrón de 10 MeV en oxígeno tiene alcance CSDA de 5,6 g/cm² y sufre entre $10^5$ y $10^6$ interacciones antes de perder toda su energía cinética. Simular cada una individualmente sería computacionalmente prohibitivo.
Transporte de Electrones por Historia Condensada
La solución vino con Berger (1963): el método de historia condensada. La idea es agrupar miles de interacciones de pequeño efecto en pocos «pasos» virtuales de gran efecto. En la práctica, entre las llamadas colisiones «catastróficas» — creación de rayos delta y fotones de bremsstrahlung por encima de ciertos umbrales — el electrón pierde energía continuamente según el stopping power restringido.
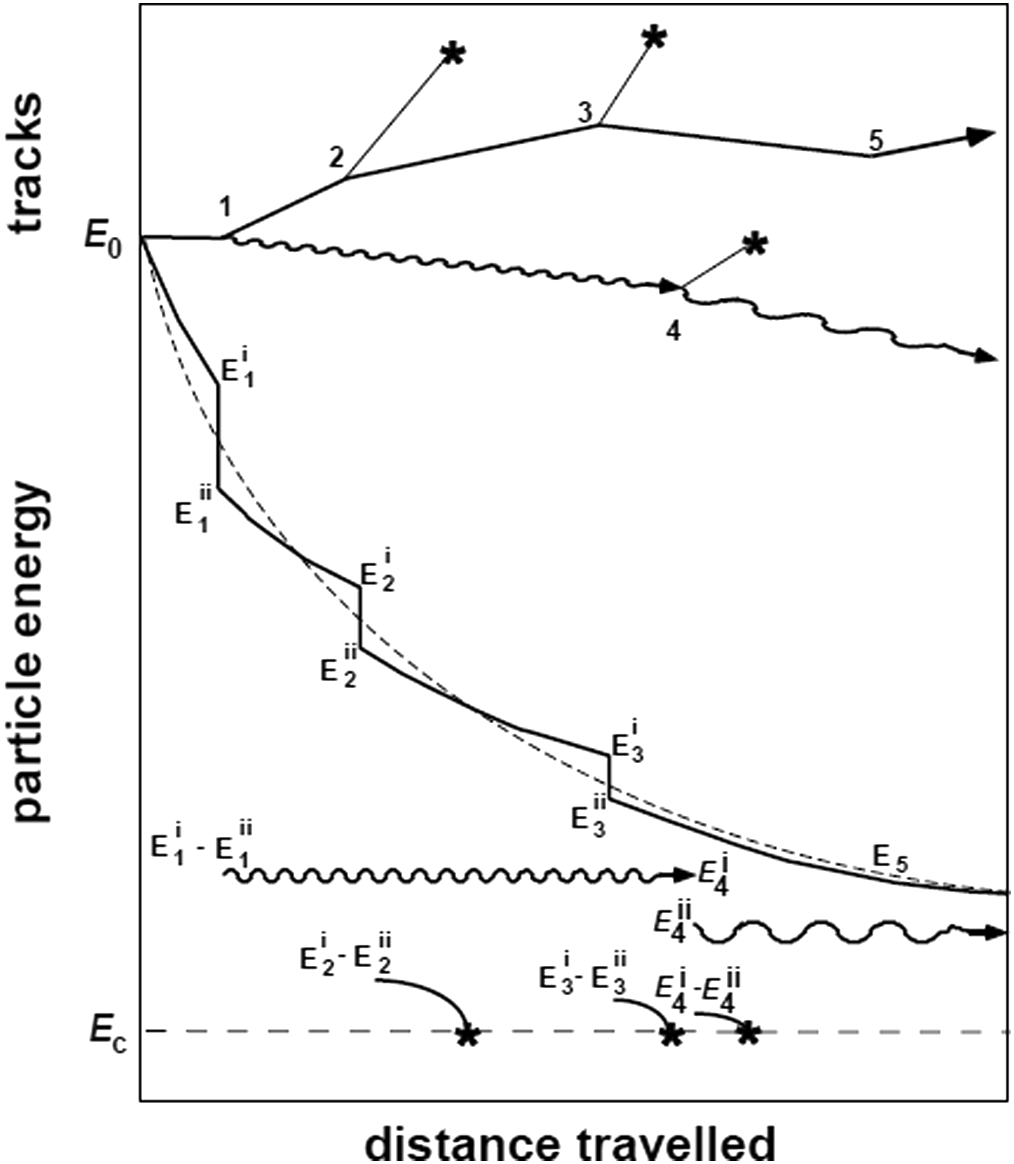
Berger clasificó este enfoque como simulación «Clase II»: híbrida entre transporte continuo y muestreo analógico de eventos discretos. Los cutoffs de energía controlan el balance entre precisión y velocidad. En EGSnrc, el parámetro ECUT define la energía cinética por debajo de la cual el electrón es «absorbido localmente» — típicamente elegido para que el alcance CSDA a esa energía sea aproximadamente 1/3 de la menor dimensión del vóxel. El ESTEPE limita la fracción máxima de pérdida de energía por paso condensado (valor típico: 4%).
Sin historia condensada, el transporte de partículas cargadas requeriría recursos del orden de teraflops ($10^{12}$ operaciones/segundo) para la mayoría de los problemas prácticos. En la práctica, la historia condensada es la técnica de reducción de varianza más importante en aplicaciones de radioterapia.
Transporte Acoplado Fotón–Electrón
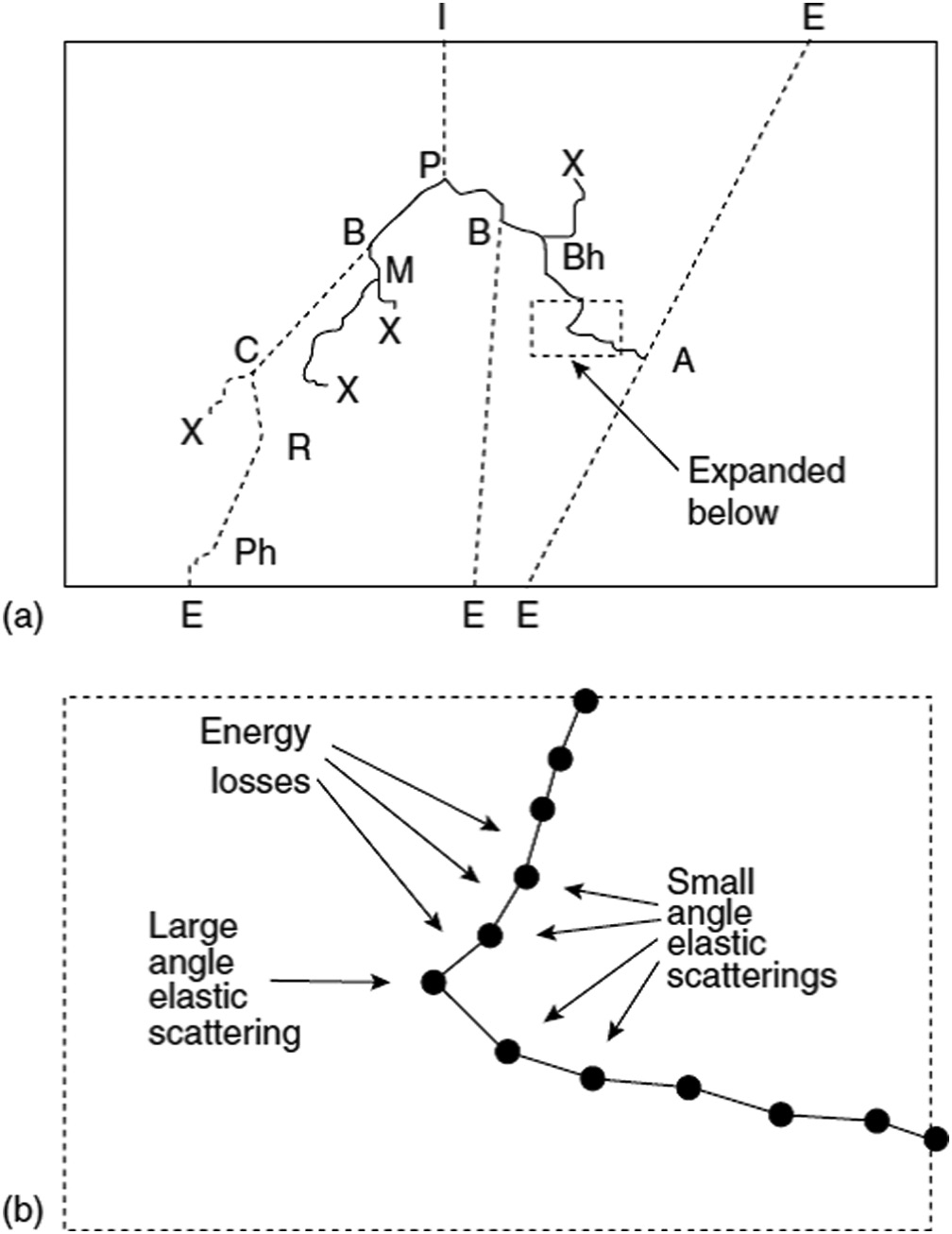
Los fotones transfieren energía a través de electrones secundarios — por lo tanto, el transporte de ambos tipos de partícula debe estar acoplado. La Figura 30.5 ilustra una historia completa: un fotón entra en la geometría y sufre producción de pares (P). El electrón resultante genera bremsstrahlung (B), mientras el fotón dispersado sufre Compton (C), Rayleigh (R) y absorción fotoeléctrica (Ph). El positrón se aniquila (A) generando dos fotones de 511 keV que escapan de la geometría.
En la práctica clínica, este acoplamiento permite al Monte Carlo capturar correctamente efectos como la falta de equilibrio de partículas cargadas en campos pequeños e interfaces de densidad — situaciones donde algoritmos como pencil beam y AAA pueden fallar significativamente.
Técnicas de Reducción de Varianza en Monte Carlo
La incertidumbre estadística de una simulación MC disminuye con $1/\sqrt{N}$, donde $N$ es el número de historias. Duplicar la precisión requiere cuadruplicar el tiempo de cálculo. Las técnicas de reducción de varianza (VRT) superan este cuello de botella modificando la simulación para obtener menor varianza sin aumentar el número de historias.
La eficiencia $\varepsilon$ de una simulación se define como:
$$\varepsilon = \frac{1}{[s(N)]^2 \cdot T(N)}$$
Donde $[s(N)]^2$ es la varianza estimada y $T(N)$ el tiempo total de cálculo. El objetivo de las VRTs es aumentar $\varepsilon$ reduciendo $s(N)$, $T(N)$, o ambos.
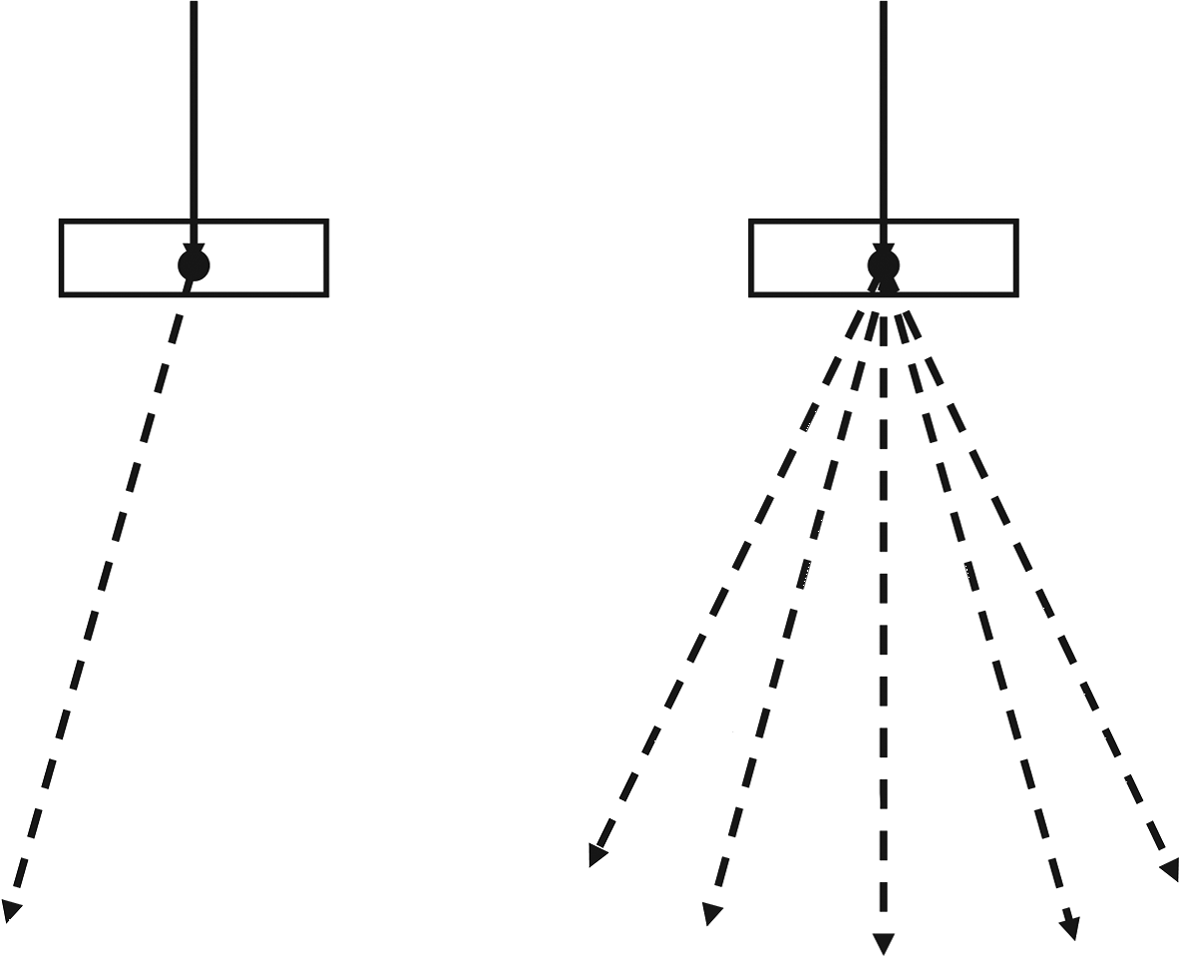
Las VRTs más utilizadas en la simulación de cabezales de aceleradores incluyen:
- Splitting uniforme de partículas: en vez de generar 1 fotón de bremsstrahlung con peso $w = 1$, se generan $N_{split}$ fotones independientes con peso $w = 1/N_{split}$ cada uno. La Figura 30.7 muestra el concepto con $N_{split} = 5$.
- Forzamiento de interacción: los fotones son forzados a interactuar dentro de la región de interés. El número de caminos libres medios $\lambda$ hasta el punto de interacción es: $\lambda = -\ln\left[1 – R(1 – e^{-\Lambda})\right]$, donde $\Lambda = \sum_{Start}^{Stop} \mu_i s_i$.
- Muestreo correlacionado: se precalcula el transporte en la región externa (constante) y se repite solo el transporte en la región variable para cada geometría diferente.
- Ruleta rusa: elimina partículas de bajo peso estadístico, compensando con aumento proporcional del peso de las sobrevivientes.
Códigos MC e Implementaciones en TPS Comerciales
El físico médico moderno no necesita escribir su propio código MC. Décadas de desarrollo han producido paquetes poderosos, muchos de ellos gratuitos. La tabla siguiente resume los principales códigos utilizados en física médica.
Principales Códigos Monte Carlo en Física Médica
| Código | Características Principales | Aplicación |
|---|---|---|
| EGSnrc / BEAMnrc | Código más citado en física médica; control fino del transporte condensado electrón–fotón | Investigación; modelado de cabezales (BEAMnrc); dosis en paciente (DOSXYZnrc) |
| MCNP | Incluye transporte de neutrones; uso extensivo en industria nuclear | Física médica; blindaje; braquiterapia |
| GEANT4 | Toolkit multi-partícula integral; creciente uso médico | Investigación; protonterapia; PET/SPECT |
| VMC++ / XVMC | Optimizado para velocidad con «electron-track repeating» | Oncentra/Masterplan (Elekta); Monaco; XiO |
| PENELOPE | Transporte electrónico sofisticado | Investigación; PRIMO (verificación libre) |
| DPM | Pasos condensados grandes cruzando interfaces de materiales | TPS Pinnacle (Philips) |
| MMC (Macro MC) | Semi-numérico, transporte híbrido rápido de electrones | Eclipse (Varian) — haces de electrones |
| PEREGRINE | Desarrollado para planificación en radioterapia | Corvus (Best NOMOS) |
Fuente: Handbook of Radiotherapy Physics: Theory and Practice, 2nd Ed. (CRC Press, 2020) (Table 30.1)
TPS Comerciales con Monte Carlo
| TPS / Sistema | Tipo | Simulación del LINAC | Dosis en Paciente | Disponibilidad |
|---|---|---|---|---|
| Monaco (Elekta) | Planificación | VSM | XVMC (rápido) | Comercial |
| Eclipse — electrones (Varian) | Planificación | VSM | MMC (precalculado) | Comercial |
| iPlan (BrainLab) | Planificación | VSM | XVMC (rápido) | Comercial |
| Oncentra (Elekta) | Planificación | VSM | VMC++ (rápido) | Comercial |
| Pinnacle (Philips) | Planificación | — | DPM (rápido) | Comercial |
| XiO (Elekta) | Planificación | VSM | XVMC (rápido) | Comercial |
| PRIMO | Verificación | PENELOPE (completo) | PENELOPE | Gratuito |
| PLanUNC | Verificación | EGSnrc (completo) | EGSnrc | Gratuito |
Fuente: Handbook of Radiotherapy Physics: Theory and Practice, 2nd Ed. (CRC Press, 2020) (Table 30.2, adaptada)
Monte Carlo Clínico: Dosis por MU y Dose-to-Medium
Dos cuestiones prácticas distinguen el MC clínico del MC de investigación. La primera es la relación dosis por unidad monitora (MU). En MC, la dosis se calcula por partícula simulada — para convertir a Gy/MU, es necesario normalizar usando la dosis en condiciones de referencia (campo 10×10 cm², profundidad de referencia, SSD o SAD definida). Esta calibración garantiza consistencia con la dosimetría absoluta del servicio.
La segunda cuestión es la elección entre dose-to-medium ($D_m$) y dose-to-water ($D_w$). El MC naturalmente calcula $D_m$ — la dosis depositada en el material real del vóxel (hueso, pulmón, tejido blando). Para convertir a $D_w$, se aplica la razón de stopping powers agua/medio:
$$D_w = D_m \cdot \left(\frac{S}{\rho}\right)_{medio}^{agua}$$
En la práctica, la diferencia entre $D_w$ y $D_m$ es clínicamente significativa solo en hueso (hasta 5–10%) y puede influir en la interpretación de DVHs en casos de cabeza y cuello o columna.
¿Por Qué el MC Aún No Domina la Rutina Clínica?
Precisión sin precedentes tiene un precio: tiempo de cálculo. Alrededor de 1990, se estimaba que un plan de tratamiento por fotones llevaría cientos de horas con el hardware disponible. Hoy, con procesadores multicore y GPUs, el MC clínico es viable para haces de electrones y se acerca a la viabilidad plena para fotones.
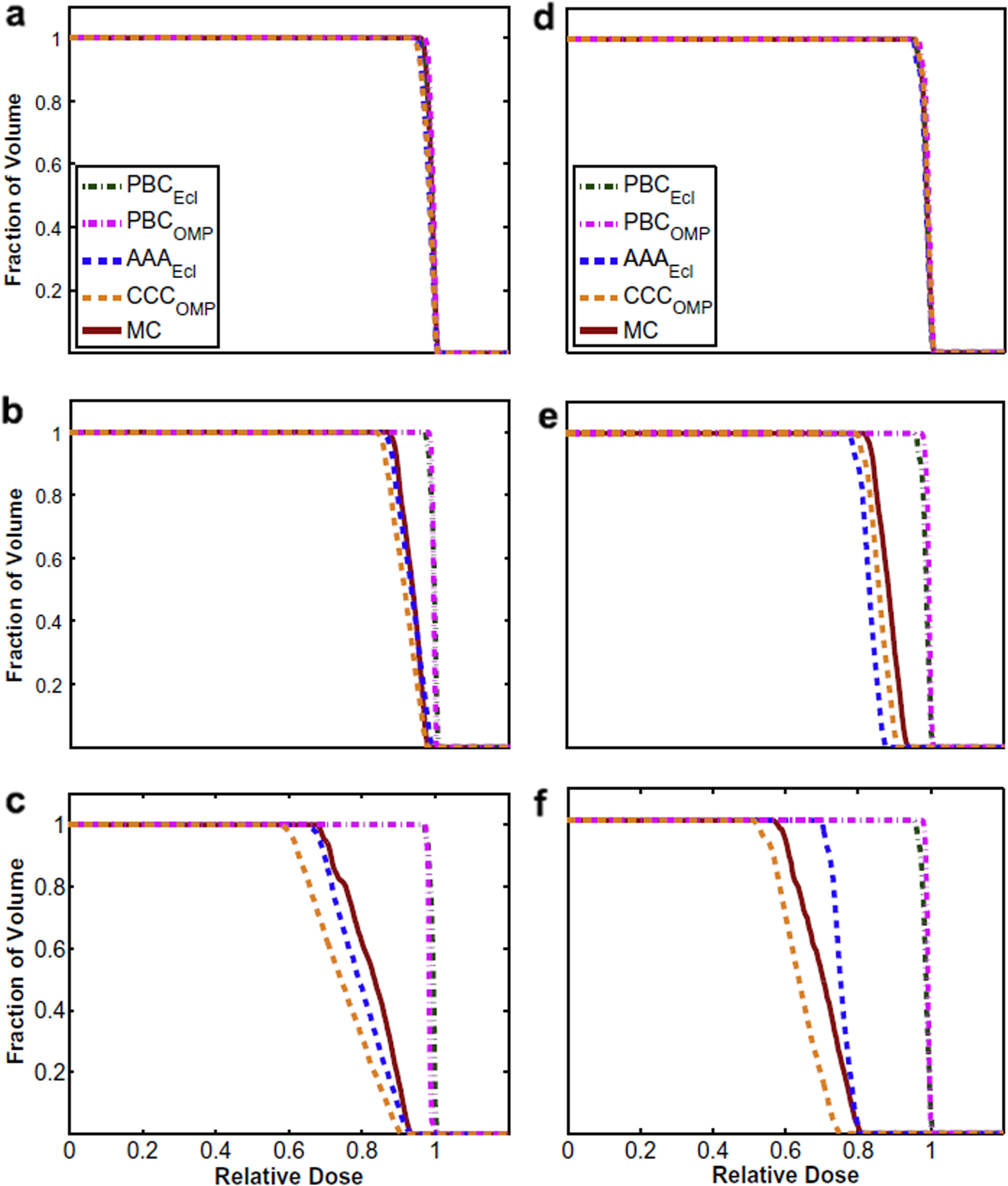
La Figura 30.13 muestra DVHs para un tumor pulmonar calculados con diferentes algoritmos. Con densidad pulmonar de 1,0 g/cm³, todos coinciden. A medida que la densidad baja a 0,4 y luego 0,1 g/cm³, los algoritmos pencil beam sobreestiman severamente la dosis tumoral, mientras MC y Collapsed Cone Convolution convergen al mismo resultado. En 18 MV y densidad 0,1 g/cm³, la discrepancia del pencil beam supera el 20%.
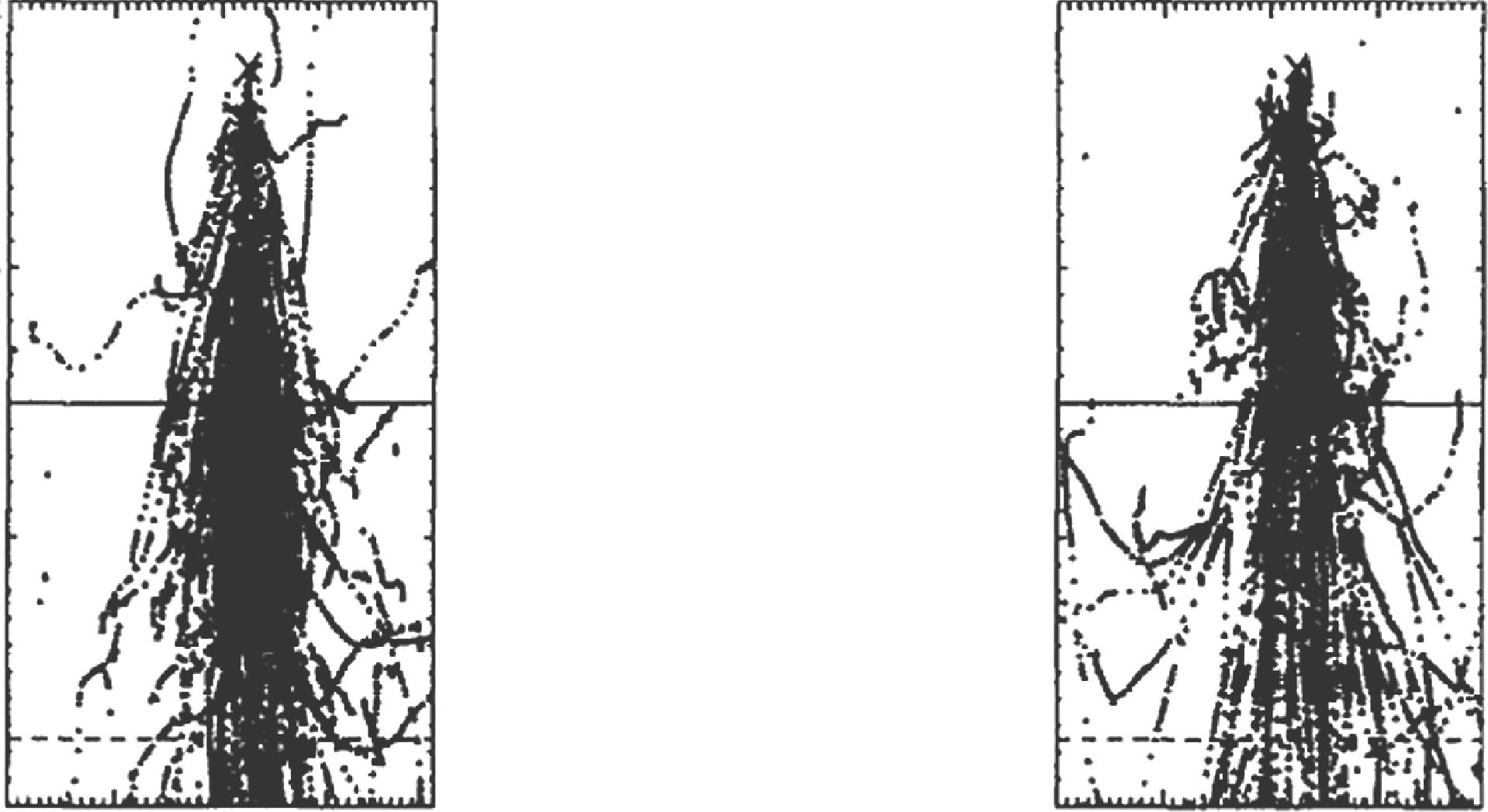
La razón fundamental de esta superioridad está en la Figura 30.12: el scaling rectilíneo de kernels (usado por algoritmos de convolución) asume que la distribución de dosis depende solo de la densidad media entre el punto de interacción y el de deposición. El MC muestra que el orden de las densidades importa — un fotón que cruza primero tejido denso y luego pulmón genera un patrón de electrones diferente del camino inverso. Para conocer más sobre los fundamentos de la superposición y TERMA, consulte nuestro artículo dedicado.
La Ecuación Lineal de Transporte de Boltzmann (LBTE): Fundamentos Matemáticos
Mientras el Monte Carlo resuelve la ecuación de transporte de forma estocástica — simulando historias individuales de partículas —, el Acuros XB adopta el enfoque determinístico: resuelve la LBTE directamente sobre una grilla computacional. Para comprender el Acuros, es esencial entender la ecuación que resuelve.
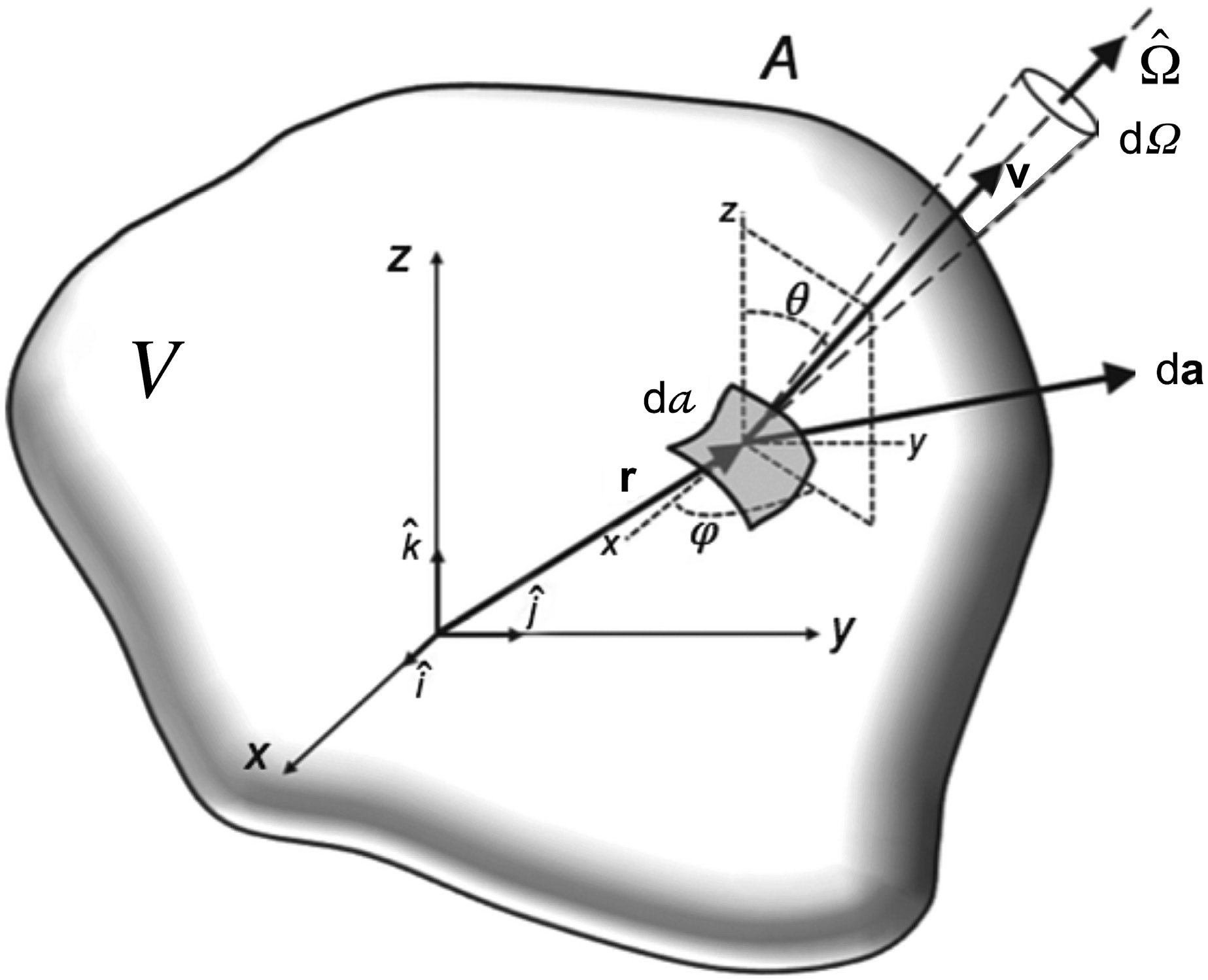
La ecuación lineal de transporte de Boltzmann describe la conservación de partículas en un medio. En su forma más general, para una partícula de tipo $p$ con energía $E$ viajando en la dirección $\hat{\Omega}$ desde la posición $\vec{r}$:
$$\hat{\Omega} \cdot \nabla \psi_p(\vec{r}, E, \hat{\Omega}) + \sigma_{t,p}(\vec{r}, E)\, \psi_p(\vec{r}, E, \hat{\Omega}) = q_p(\vec{r}, E, \hat{\Omega})$$
Donde:
- $\psi_p(\vec{r}, E, \hat{\Omega})$ = fluencia angular de la partícula tipo $p$ (fotones o electrones) en la posición $\vec{r}$, energía $E$ y dirección $\hat{\Omega}$
- $\sigma_{t,p}(\vec{r}, E)$ = sección eficaz macroscópica total (probabilidad de interacción por unidad de recorrido)
- $q_p(\vec{r}, E, \hat{\Omega})$ = término fuente total, que incluye dispersión entrante (scattering-in), producción de partículas secundarias y fuentes externas
- $\hat{\Omega} \cdot \nabla$ = operador de streaming (derivada espacial a lo largo de la dirección de vuelo)
El primer término ($\hat{\Omega} \cdot \nabla \psi$) describe el transporte libre de partículas a lo largo de la dirección $\hat{\Omega}$. El segundo término ($\sigma_t \psi$) representa las pérdidas por interacción — tanto absorción como dispersión fuera del haz angular considerado. El lado derecho ($q_p$) agrupa todas las fuentes de partículas en ese punto del espacio de fase.
El término fuente es la pieza más compleja de la ecuación, ya que acopla diferentes tipos de partículas y diferentes energías:
$$q_p(\vec{r}, E, \hat{\Omega}) = \sum_{p’} \int_0^{\infty} \int_{4\pi} \sigma_{s,p’ \to p}(\vec{r}, E’ \to E, \hat{\Omega}’ \to \hat{\Omega})\, \psi_{p’}(\vec{r}, E’, \hat{\Omega}’)\, d\hat{\Omega}’\, dE’ + q_{ext,p}(\vec{r}, E, \hat{\Omega})$$
Aquí, $\sigma_{s,p’ \to p}$ es el kernel de dispersión diferencial que describe la probabilidad de que una partícula de tipo $p’$ con energía $E’$ y dirección $\hat{\Omega}’$ produzca una partícula de tipo $p$ con energía $E$ y dirección $\hat{\Omega}$. La sumatoria sobre $p’$ acopla fotones y electrones: fotones Compton generan electrones, electrones generan bremsstrahlung, y así sucesivamente.
Transporte Acoplado Fotón–Electrón en la LBTE
Para haces clínicos de megavoltaje, la LBTE se desdobla en un sistema acoplado. El transporte de fotones sigue:
$$\hat{\Omega} \cdot \nabla \psi_\gamma + \sigma_{t,\gamma}\, \psi_\gamma = \int_0^{\infty} \int_{4\pi} \sigma_{s,\gamma \to \gamma}\, \psi_\gamma\, d\hat{\Omega}’\, dE’ + \int_0^{\infty} \int_{4\pi} \sigma_{s,e \to \gamma}\, \psi_e\, d\hat{\Omega}’\, dE’ + q_{ext,\gamma}$$
El primer término integral del lado derecho representa fotones dispersados (Compton, Rayleigh). El segundo representa bremsstrahlung y aniquilación — fotones creados por electrones. El transporte de electrones es análogo, con términos fuente provenientes de las interacciones fotoeléctrica, Compton y producción de pares:
$$\hat{\Omega} \cdot \nabla \psi_e + \sigma_{t,e}\, \psi_e = \int_0^{\infty} \int_{4\pi} \sigma_{s,e \to e}\, \psi_e\, d\hat{\Omega}’\, dE’ + \int_0^{\infty} \int_{4\pi} \sigma_{s,\gamma \to e}\, \psi_\gamma\, d\hat{\Omega}’\, dE’$$
Este acoplamiento bidireccional fotón-electrón es lo que hace a la LBTE tan poderosa — y tan difícil de resolver. El Monte Carlo resuelve este sistema muestreando historias aleatorias; el Acuros XB lo resuelve discretizando todas las variables e iterando numéricamente.
De la Fluencia a la Dosis
Una vez resuelta la fluencia angular $\psi_e(\vec{r}, E, \hat{\Omega})$, la dosis absorbida en el material real del vóxel se calcula integrando la fluencia electrónica sobre todas las energías y direcciones, ponderada por el stopping power másico de colisión:
$$D_m(\vec{r}) = \int_0^{\infty} \left(\frac{S_{col}(E)}{\rho}\right)_m \phi_e(\vec{r}, E)\, dE$$
Donde $\phi_e(\vec{r}, E) = \int_{4\pi} \psi_e(\vec{r}, E, \hat{\Omega})\, d\hat{\Omega}$ es la fluencia escalar de electrones y $(S_{col}/\rho)_m$ es el stopping power másico de colisión en el material $m$ del vóxel. Para obtener $D_w$, se sustituye el stopping power del material por el del agua:
$$D_w(\vec{r}) = \int_0^{\infty} \left(\frac{S_{col}(E)}{\rho}\right)_w \phi_e(\vec{r}, E)\, dE$$
Esta formulación es idéntica a la usada por el Monte Carlo para reportar dosis — la diferencia radica únicamente en cómo se obtuvo la fluencia $\phi_e$: por muestreo estocástico (MC) o por solución determinística (Acuros XB).
Monte Carlo vs. LBTE: Dos Caminos para la Misma Ecuación
Es fundamental comprender que Monte Carlo y Acuros XB resuelven la misma ecuación física — la LBTE. La diferencia es metodológica:
- Monte Carlo (estocástico): genera historias aleatorias de partículas, muestrea interacciones según distribuciones de probabilidad y acumula dosis en vóxeles de scoring. La precisión depende del número de historias ($N$) — la incertidumbre estadística cae con $1/\sqrt{N}$. Cada historia es independiente, haciendo el algoritmo naturalmente paralelizable.
- Acuros XB (determinístico): discretiza el espacio de fase en variables angulares, energéticas y espaciales, y resuelve el sistema de ecuaciones resultante por iteración. No hay ruido estadístico — la solución converge al resultado exacto de la LBTE discretizada conforme la malla se refina. El error es puramente de discretización, no estadístico.
En la práctica, ambos producen resultados concordantes dentro de 1–2% en escenarios clínicos típicos. La elección entre ellos está guiada por consideraciones de velocidad, tipo de problema e infraestructura disponible.
Acuros XB: Implementación y Discretización de la LBTE
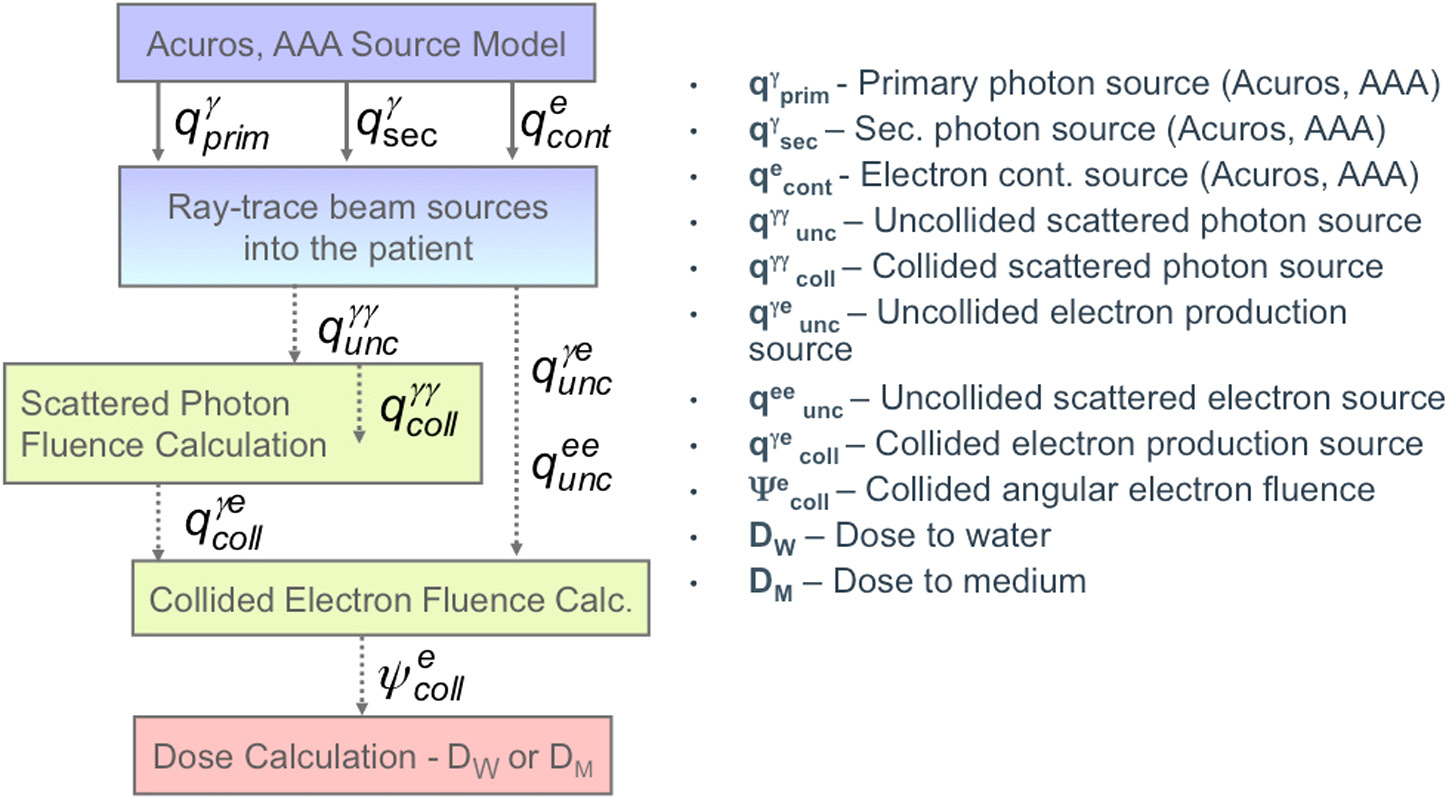
El Acuros XB (External Beam), desarrollado originalmente por Transpire Inc. y adquirido por Varian para su integración en Eclipse, resuelve la LBTE a través de una cascada de etapas cuidadosamente ordenadas. La implementación descompone el problema de transporte en componentes que se resuelven secuencialmente.
Etapa 1: Transporte de Fotones No Colisionados
La fluencia primaria — fotones que no han sufrido ninguna interacción — se calcula por ray-tracing analítico a partir del modelo de fuente del acelerador. Cada rayo se atenúa exponencialmente conforme atraviesa los vóxeles del paciente, usando las secciones eficaces macroscópicas del material asignado a cada vóxel. La atenuación sigue:
$$\psi_\gamma^{unc}(\vec{r}, E, \hat{\Omega}) = \psi_\gamma^{src}(E, \hat{\Omega}) \cdot \exp\left(-\int_0^s \sigma_{t,\gamma}(\vec{r}’, E)\, ds’\right)$$
Donde $s$ es la distancia recorrida a lo largo de la dirección $\hat{\Omega}$ desde la fuente hasta el punto $\vec{r}$.
Etapa 2: Discretización Angular — Ordenadas Discretas ($S_N$)
La variable angular $\hat{\Omega}$ se discretiza usando el método de ordenadas discretas ($S_N$). La esfera unitaria de direcciones se subdivide en un conjunto finito de direcciones $\hat{\Omega}_n$ con pesos de cuadratura $w_n$, de modo que las integrales sobre el ángulo sólido se aproximan por:
$$\int_{4\pi} f(\hat{\Omega})\, d\hat{\Omega} \approx \sum_{n=1}^{N_{dir}} w_n\, f(\hat{\Omega}_n)$$
El Acuros XB utiliza típicamente conjuntos de cuadratura con 80 a 128 direcciones discretas — suficiente para capturar la anisotropía del transporte en haces de radioterapia, incluyendo dispersión lateral y retrodifusión.
Etapa 3: Discretización Energética — Método Multigrupo
El espectro continuo de energía se divide en grupos discretos ($G$ grupos típicamente). Para cada grupo $g$, las secciones eficaces se precalculan y tabulan como constantes $\sigma_{t,g}$ y $\sigma_{s,g’ \to g}$. La ecuación de transporte para el grupo $g$ en la dirección $\hat{\Omega}_n$ se convierte en:
$$\hat{\Omega}_n \cdot \nabla \psi_g^n(\vec{r}) + \sigma_{t,g}(\vec{r})\, \psi_g^n(\vec{r}) = \sum_{g’=1}^{G} \sum_{n’=1}^{N_{dir}} w_{n’}\, \sigma_{s,g’ \to g}(\vec{r}, \hat{\Omega}_{n’} \to \hat{\Omega}_n)\, \psi_{g’}^{n’}(\vec{r}) + q_{ext,g}^n(\vec{r})$$
La estructura multigrupo de las secciones eficaces se deriva de bibliotecas nucleares estándar (similares a las usadas en física de reactores nucleares), adaptadas para las energías de interés en radioterapia (keV a MeV). Los materiales del paciente se asignan a partir de densidades CT usando tablas de conversión HU-a-material con composiciones químicas conocidas.
Etapa 4: Discretización Espacial — Diferencias Finitas en la Grilla del Paciente
El volumen del paciente se discretiza en la grilla de cálculo del Eclipse (típicamente 2,5 mm de resolución, aunque resolución fina de hasta 1 mm está disponible). Para cada vóxel, las ecuaciones multigrupo de ordenadas discretas se resuelven usando esquemas de diferencias finitas que garantizan conservación de partículas y positividad de la fluencia.
El barrido (sweep) espacial procede octante por octante: para cada dirección discreta $\hat{\Omega}_n$, los vóxeles se barren en secuencia upstream-to-downstream, de modo que la fluencia incidente en cada vóxel ya fue calculada en los vóxeles precedentes. Este procedimiento es altamente eficiente y puede paralelizarse por octante.
Etapa 5: Transporte de Fotones Dispersados
La fuente de fotones dispersados se calcula a partir de la fluencia de fotones no colisionados (Etapa 1). Fotones Compton, Rayleigh y de aniquilación se transportan iterativamente: en cada iteración, la nueva fluencia dispersada contribuye a una nueva fuente de dispersión, hasta que se alcanza la convergencia.
Etapa 6: Fuente de Electrones y Transporte Electrónico
Las interacciones fotoeléctrica, Compton y producción de pares generan electrones secundarios. El Acuros XB calcula esta fuente de electrones a partir de la fluencia total de fotones y luego resuelve la LBTE para electrones, incluyendo la pérdida continua de energía (CSDA) y la producción de bremsstrahlung. La fluencia electrónica resultante se integra para producir la distribución de dosis final.
Modelo de Fuente y Commissioning
El Acuros XB utiliza el mismo modelo de fuente de múltiples fuentes virtuales (multi-source model) del AAA: fuente primaria (blanco), fuente de dispersión extraprimaria (filtro aplanador, colimadores) y fuente de transmisión de los jaws/MLC. Los parámetros se ajustan durante el commissioning a partir de datos dosimétricos medidos — PDDs, perfiles y factores de campo. Esto significa que clínicas que ya comisionaron el AAA pueden migrar al Acuros XB sin necesidad de medidas adicionales.
Comparación Detallada: Monte Carlo vs. Acuros XB
La tabla siguiente presenta una comparación directa entre Monte Carlo y Acuros XB en los aspectos más relevantes para la práctica clínica:
| Aspecto | Monte Carlo | Acuros XB |
|---|---|---|
| Método | Estocástico — muestreo aleatorio de historias de partículas | Determinístico — solución numérica de la LBTE en grilla discreta |
| Ruido estadístico | Presente; disminuye con $1/\sqrt{N}$. Requiere ~$10^9$ historias para incertidumbre < 1% | Ausente. Error es de discretización (tamaño del vóxel, cuadratura angular, grupos de energía) |
| Tiempo de cálculo (IMRT típico) | 5–30 min (acelerado por GPU) a horas (CPU) | 1–5 min (CPU multi-core estándar) |
| Precisión en medio homogéneo | Referencia (gold standard) | Equivalente al MC (< 1% diferencia) |
| Precisión en pulmón | Referencia | Dentro de 1–2% del MC en la mayoría de los escenarios |
| Precisión en hueso | Referencia | Dentro de 1–2% del MC |
| Interfaces aire–tejido | Excelente (resuelve desequilibrio CPE) | Excelente (resuelve LBTE explícitamente) |
| Campos pequeños (< 3×3 cm²) | Excelente | Excelente |
| Reporte $D_w$ / $D_m$ | Ambos (nativo $D_m$) | Ambos (nativo $D_m$) |
| Implantes metálicos | Excelente (composición real del material) | Bueno (asignación de material limitada a materiales de la biblioteca) |
| Efecto de campo magnético (MR-LINAC) | Excelente (EGSnrc, GEANT4 con extensión magnética) | Soportado en Acuros XB v15.6+ para Unity (Elekta) |
| Geometrías muy complejas | Superior (sin aproximaciones de discretización angular) | Bueno (resolución angular finita puede suavizar detalles) |
| Investigación y escenarios no estándar | Flexibilidad total (geometrías arbitrarias, scoring personalizado) | Limitado a lo que el TPS ofrece |
| TPS comerciales | Monaco, iPlan, Oncentra, XiO, Pinnacle | Eclipse (Varian) — exclusivo |
Aplicaciones Clínicas Avanzadas del Acuros XB
Estereotaxia Pulmonar (SBRT)
En la SBRT de pulmón, los campos son pequeños, las heterogeneidades son extremas (aire a tumor a aire) y el equilibrio de partículas cargadas (CPE) no existe en los bordes del tumor. Estudios como Bush et al. (2011) y Fogliata et al. (2011) demostraron que el Acuros XB concuerda con el Monte Carlo dentro de 1–2% en estas condiciones, mientras el AAA puede sobreestimar la cobertura tumoral en hasta 5–10% dependiendo de la densidad pulmonar y el tamaño del campo. El Acuros XB reportando dose-to-medium ($D_m$) captura correctamente la reducción de dosis en las interfaces aire–tumor.
Planificación con MR-LINAC
Sistemas MR-LINAC como Unity (Elekta) y ViewRay MRIdian generan un campo magnético de 0,35–1,5 T que desvía la trayectoria de los electrones secundarios vía fuerza de Lorentz. Esto altera la distribución de dosis, especialmente en interfaces aire–tejido — el llamado efecto de retorno electrónico (electron return effect, ERE). El Acuros XB versión 15.6+ para Eclipse incluye extensión para campos magnéticos, resolviendo la LBTE con términos adicionales de deflexión. La fuerza de Lorentz modifica el operador de transporte electrónico:
$$\hat{\Omega} \cdot \nabla \psi_e + \sigma_{t,e}\, \psi_e + \frac{e}{p}(\vec{v} \times \vec{B}) \cdot \nabla_{\hat{\Omega}} \psi_e = q_e$$
Donde $\vec{B}$ es el campo magnético, $\vec{v}$ la velocidad del electrón, $e$ la carga elemental y $p$ el momento. El término adicional $\nabla_{\hat{\Omega}}$ representa la rotación de la dirección de vuelo en el espacio angular — esencial para capturar el ERE correctamente.
Implantes Metálicos de Alta Densidad
Prótesis de cadera (titanio, cromo-cobalto), implantes dentales y marcadores fiduciales introducen heterogeneidades extremas ($Z$ efectivo alto, densidad 4–8 g/cm³). El Acuros XB asigna composiciones de material a partir de tablas HU-a-material y calcula secciones eficaces específicas para cada material. Para implantes con densidad muy alta (por encima del rango típico del CT), la asignación puede estar limitada por la biblioteca de materiales del Acuros. En esos casos, el Monte Carlo con geometría explícita del implante puede ser preferible.
Cabeza y Cuello: Interfaces Hueso–Aire
Tumores en cavidades nasales, senos paranasales y base de cráneo involucran interfaces frecuentes entre hueso, aire y tejido blando. El Acuros XB captura los efectos de retrodifusión y pérdida de equilibrio en estas interfaces con precisión muy superior a la del AAA — y con tiempo de cálculo compatible con la optimización inversa de IMRT/VMAT.
Por Qué el Acuros XB Está Reemplazando al AAA en Eclipse
Desde la versión 13.6 de Eclipse, Varian posiciona al Acuros XB como el algoritmo preferencial para fotones. Las razones son claras:
- Precisión: resuelve la LBTE explícitamente, capturando heterogeneidades con precisión de MC.
- Velocidad: 2–5x más rápido que MC para planes VMAT típicos.
- Sin ruido: resultado determinístico, sin artefactos de submuestreo.
- Dose-to-medium: reporta $D_m$ nativamente, alineado con recomendaciones actuales.
- Commissioning simplificado: usa el mismo modelo de fuente del AAA.
En la práctica, servicios que migran del AAA al Acuros XB frecuentemente observan diferencias clínicamente relevantes (2–5%) en planes de pulmón, especialmente en SBRT con campos pequeños. Esta diferencia puede afectar la cobertura del PTV y los límites de dosis en OAR, justificando la recalibración de protocolos institucionales.
Comparación Completa: Monte Carlo vs. Acuros vs. Algoritmos Analíticos
| Característica | Monte Carlo | Acuros XB (LBTE) | AAA/CCC | Pencil Beam |
|---|---|---|---|---|
| Principio | Simulación estocástica | Solución determinística de la LBTE | Convolución/Superposición | Convolución 1D + correcciones |
| Precisión en heterogeneidades | Referencia (gold standard) | Excelente (~1–2% del MC) | Buena (CCC > AAA) | Limitada |
| Campos pequeños | Excelente | Excelente | Buena (con limitaciones) | Pobre |
| Tiempo de cálculo | Minutos–horas | Minutos | Segundos–minutos | Segundos |
| Ruido estadístico | Presente (disminuye con más historias) | Ausente | Ausente | Ausente |
| $D_w$ vs $D_m$ | Ambos (nativo $D_m$) | Ambos | $D_w$ (nativo) | $D_w$ (nativo) |
| TPS disponibles | Monaco, iPlan, Oncentra, XiO | Eclipse (Varian) | Eclipse (AAA), Oncentra (CCC) | Varios (legado) |
Compilación basada en el Handbook of Radiotherapy Physics: Theory and Practice, 2nd Ed. (CRC Press, 2020)
El Futuro del Cálculo de Dosis en Radioterapia
La convergencia de hardware cada vez más económico — GPUs con miles de núcleos, procesadores multithread, cloud computing — está haciendo viable el MC clínico para la rutina diaria. El informe TG-157 de la AAPM (2020) ya considera el MC como estándar de oro para haces de electrones y próximo a la viabilidad plena para fotones.
En la práctica, dos escenarios coexisten. Para clínicas que utilizan Eclipse, el Acuros XB ofrece el mejor equilibrio entre precisión y velocidad para cálculo de dosis en fotones — especialmente en pulmón, cabeza y cuello y estereotaxia. Para servicios con Monaco u otros TPS basados en XVMC/VMC++, el Monte Carlo ya forma parte de la rutina con tiempos de cálculo aceptables.
El informe TG-268 de la AAPM (2018) estableció directrices para reportar estudios basados en MC, estandarizando la documentación de parámetros como cutoffs de energía, VRTs utilizadas e incertidumbres estadísticas. Esta estandarización es esencial para garantizar reproducibilidad y comparabilidad entre estudios — y para que los resultados de investigación se traduzcan de forma confiable en la práctica clínica.
El futuro apunta hacia algoritmos híbridos que combinan la robustez determinística del Acuros con aceleración por GPU y técnicas de deep learning para estimación inicial de dosis, reduciendo aún más el tiempo de cálculo sin comprometer la precisión. Proyectos de investigación en Monte Carlo acelerado por GPU (como gDPM y ARCHER) ya demuestran cálculos de planes VMAT completos en menos de 1 minuto, acercando el MC a la viabilidad en tiempo real para radioterapia adaptativa.
Para explorar otros aspectos del Monte Carlo en radioterapia, incluyendo aplicaciones en protonterapia, braquiterapia y QA avanzado, consulte nuestros artículos dedicados. Para una introducción completa al método Monte Carlo en radioterapia, vea nuestra guía completa sobre Monte Carlo. Y para entender cómo los métodos empíricos de cálculo de dosis allanaron el camino para estas técnicas sofisticadas, lea nuestro análisis de la evolución de los algoritmos.
Este artículo forma parte de nuestra serie sobre algoritmos de cálculo de dosis por fotones.




