Los métodos empíricos de cálculo de dosis — conocidos también como métodos broad-beam — constituyeron la base de la planificación computarizada en radioterapia durante décadas. Antes de que los algoritmos de convolución y Monte Carlo se volvieran prácticos, el físico médico dependía de datos tabulados y correcciones semi-analíticas para estimar la dosis en el paciente. Este artículo recorre cada técnica en detalle: desde la representación tabular de Bentley-Milan hasta las correcciones de heterogeneidad de Batho, ETAR y sustracción de haz.
Para una visión panorámica de todos los algoritmos de cálculo de dosis por fotones — desde los empíricos hasta Monte Carlo — consulte nuestro guía completa sobre algoritmos de cálculo de dosis por fotones.
Componentes de Dosis en Haces Clínicos de Fotones
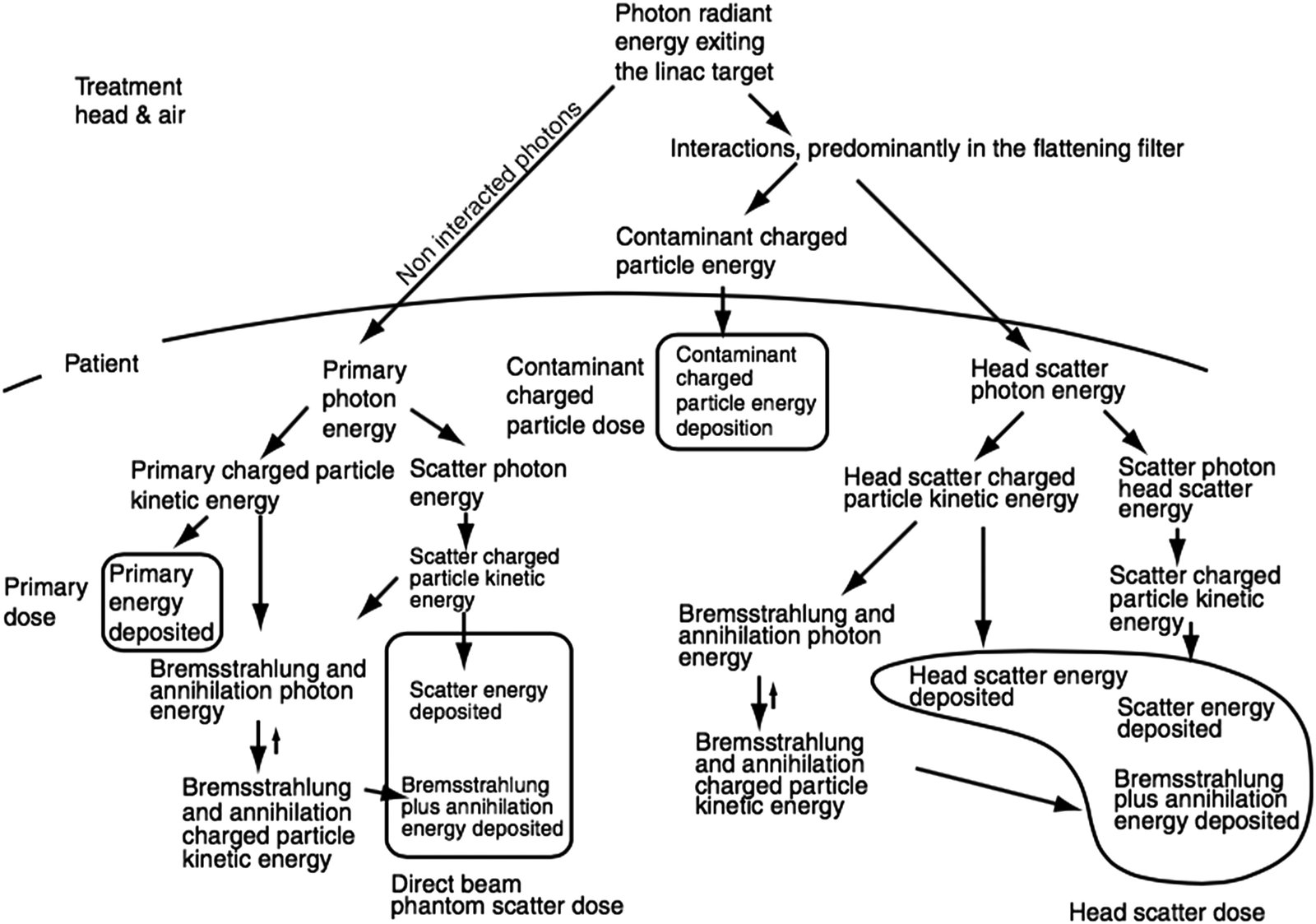
La dosis total en cualquier punto del paciente resulta de cuatro componentes. La dosis primaria, originada por fotones que no sufrieron interacción adicional, representa generalmente más del 70% del total. La dispersión en el fantoma (phantom scatter) aporta hasta un 30%, dependiendo del tamaño de campo y la profundidad.
Menos evidentes pero clínicamente relevantes, la dispersión en el cabezal — fotones dispersados en el filtro aplanador y colimador — puede alcanzar el 5–10% de la dosis total. Finalmente, la contaminación por partículas cargadas, predominantemente electrones, afecta la región de build-up (típicamente los primeros 4 cm).
Los métodos broad-beam tratan estos componentes de forma implícita. Esta simplificación es tanto su fortaleza — velocidad de cálculo — como su debilidad fundamental.
Representaciones Tabulares: El Modelo Bentley-Milan
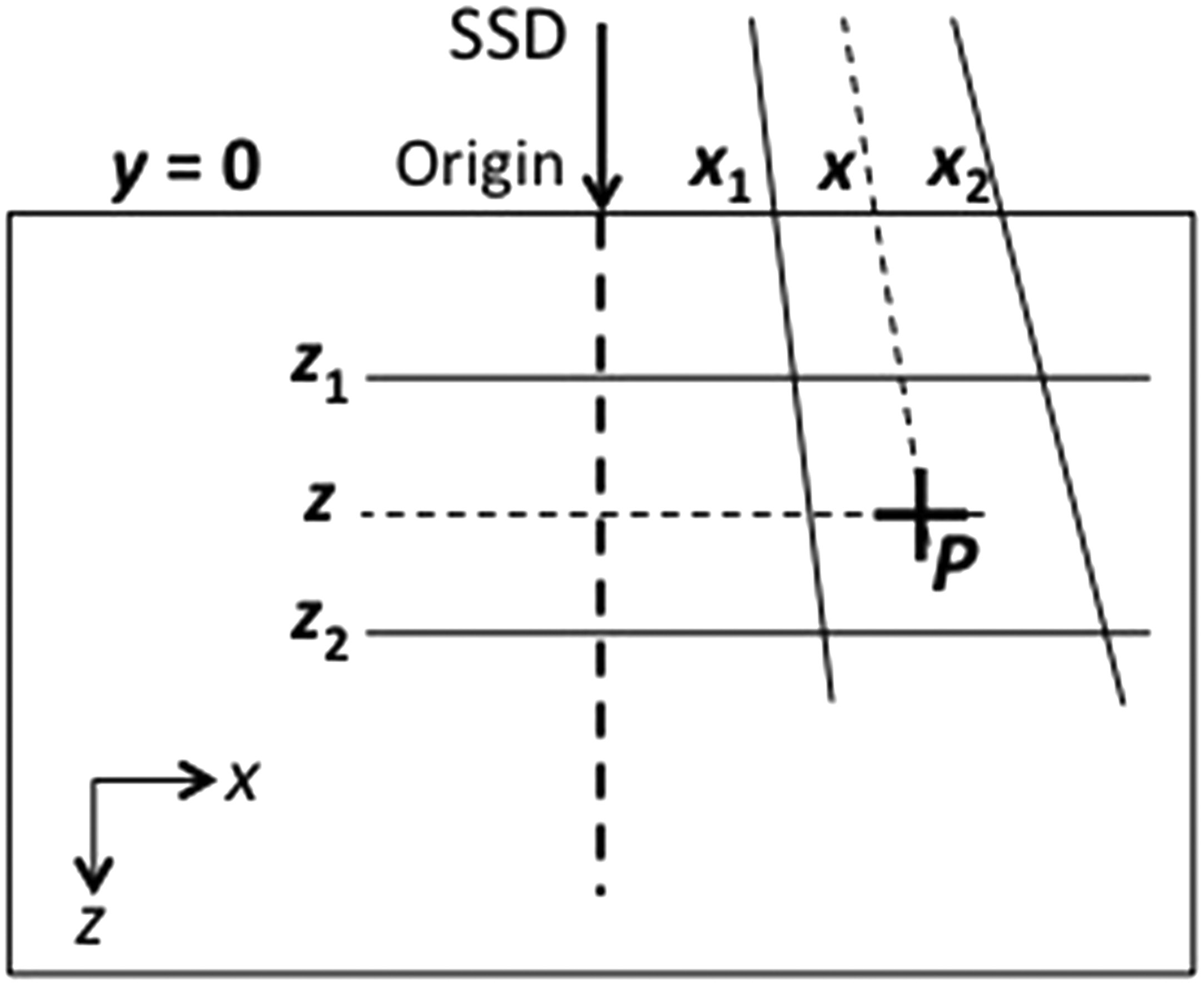
En la década de 1970, Bentley y Milan desarrollaron uno de los primeros sistemas digitales de planificación. El modelo almacenaba datos de haz como curvas de dosis en profundidad en el eje central y razones off-axis (OAR). Para economizar memoria, se utilizaban cuadrados equivalentes para reducir campos rectangulares arbitrarios a datos de campos cuadrados.
Cada campo cuadrado tenía curvas de PDD almacenadas en solo 17 profundidades, igualmente espaciadas desde $z_{max}$. La región de build-up recibía un tratamiento simplificado: la dosis a una profundidad $z < z_{max}$ se interpolaba linealmente entre la dosis superficial y la dosis máxima, usando una profundidad modificada $z_B$:
$$z_B = z_{max} – \frac{(z_{max} – z)^3}{z_{max}^2}$$
Las razones off-axis dependían principalmente del ancho in-plane del campo. La implementación original cabía en 255 ítems de datos — exactamente $2^8 – 1$.
Representaciones Analíticas y Correcciones de Cuña
Una alternativa a las tablas fueron las funciones analíticas. El modelo de van de Geijn (1965, 1970, 1972) separaba la representación en dosis en el eje central y razones off-axis, cada parte modelada por una función matemática. Solo siete mediciones bastaban para caracterizar las curvas de PDD para una energía dada.
Para filtros de cuña, dos enfoques coexistían. El primero incluía distribuciones de dosis con cuña directamente en el dataset experimental. El segundo derivaba un perfil de transmisión a partir de mediciones con y sin cuña en campo grande, tabulándolo como factor de corrección. Este perfil también podía calcularse a partir de las dimensiones y composición del filtro, siempre que el coeficiente de atenuación fuera verificado experimentalmente.
Corrección de Forma del Paciente: SSD Efectiva y TPR
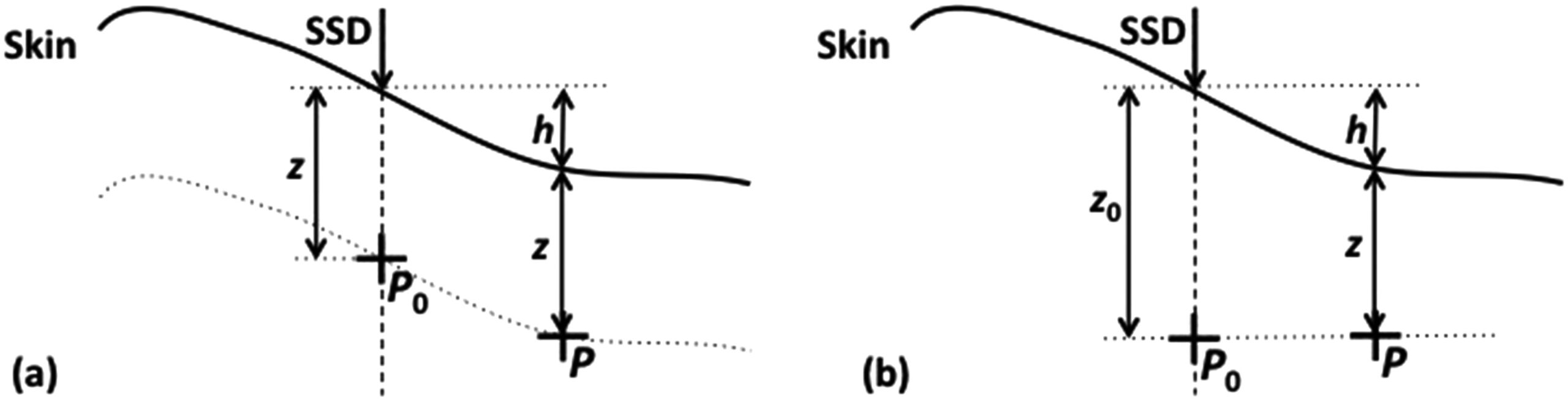
El cuerpo humano no es un bloque plano de agua. Corregir la dosis para la curvatura real de la superficie requiere métodos dedicados.
Método de la SSD Efectiva
El método SSD efectiva aplica una corrección de ley del inverso del cuadrado. Si la SSD en el eje central es $SSD$ y el incremento de distancia para un punto off-axis es $h$, el factor de corrección es:
$$C_{SSD} = \left(\frac{SSD + z}{SSD + h + z}\right)^2$$
Método de la Razón TPR
Una alternativa es el método de la razón TPR. El factor de corrección es la razón de dos tissue phantom ratios, independientes de la SSD:
$$C_{TPR} = \frac{TPR(z, ESQ_{z_0})}{TPR(z + h, ESQ_{z_0})}$$
En ambos casos, se necesita una corrección off-axis adicional para el filtro aplanador y la cuña.
Corrección de Heterogeneidades: De la Profundidad Efectiva a Batho
La presencia de pulmón, hueso y aire en el trayecto del haz altera tanto la atenuación como la dispersión.
Profundidad Efectiva (TAR)
El método más simple sustituye la profundidad real por una profundidad efectiva $z_{eff}$:
$$z_{eff} = \sum_{i=1}^{n} t_i \, \rho_i$$
$$C_{het}^{TPR} = \frac{TPR(z_{eff}, ESQ_z)}{TPR(z, ESQ_z)}$$
Es una corrección unidimensional que ignora cambios en la dispersión lateral.
Corrección Power-Law de Batho
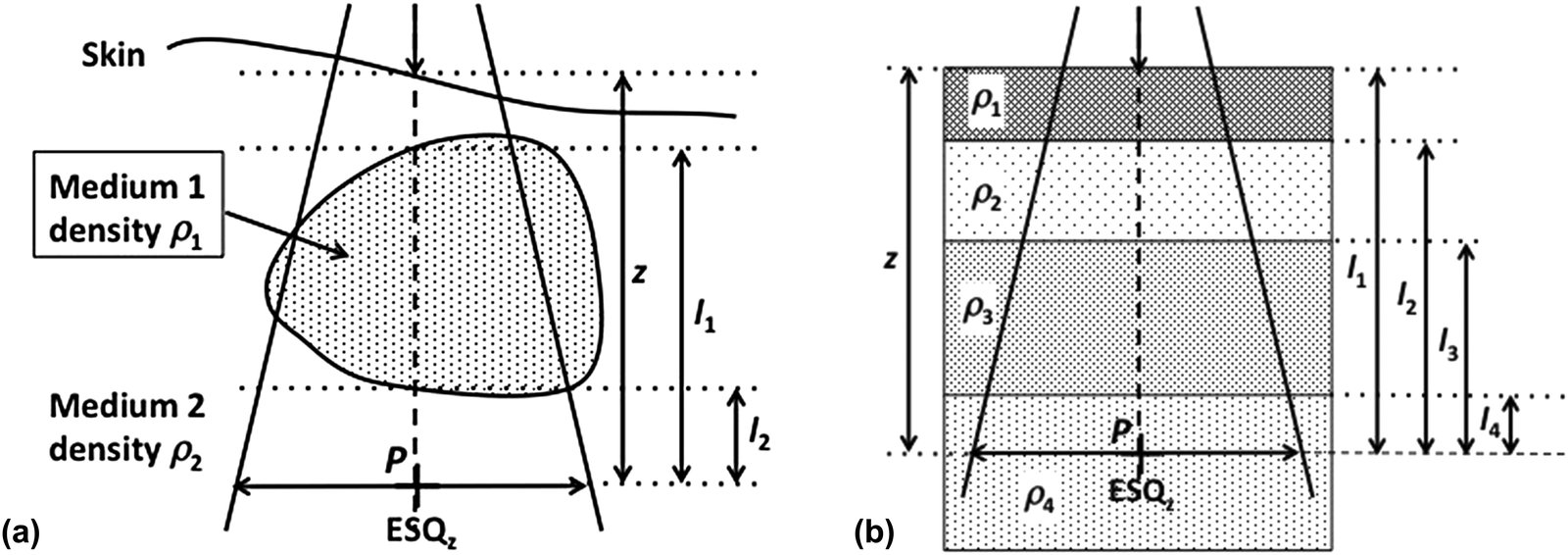
El método power-law, propuesto por Batho (1964) y generalizado por Sontag y Cunningham (1977), eleva el TAR a la potencia de la densidad relativa del medio. Para un punto $P$ en medio de densidad $\rho_2$ debajo de una heterogeneidad de densidad $\rho_1$:
$$C_{het}^{Batho} = TAR(l_2, ESQ_z)^{(\rho_2 – \rho_1)} \cdot TAR(l_1, ESQ_z)^{(1 – \rho_1)}$$
Para múltiples capas superpuestas (Webb y Fox, 1980):
$$C_{het}^{Batho} = \prod_{i=1}^{n} TAR(l_i, ESQ_z)^{(\rho_i – \rho_{i-1})}$$
Comparación Experimental de Métodos
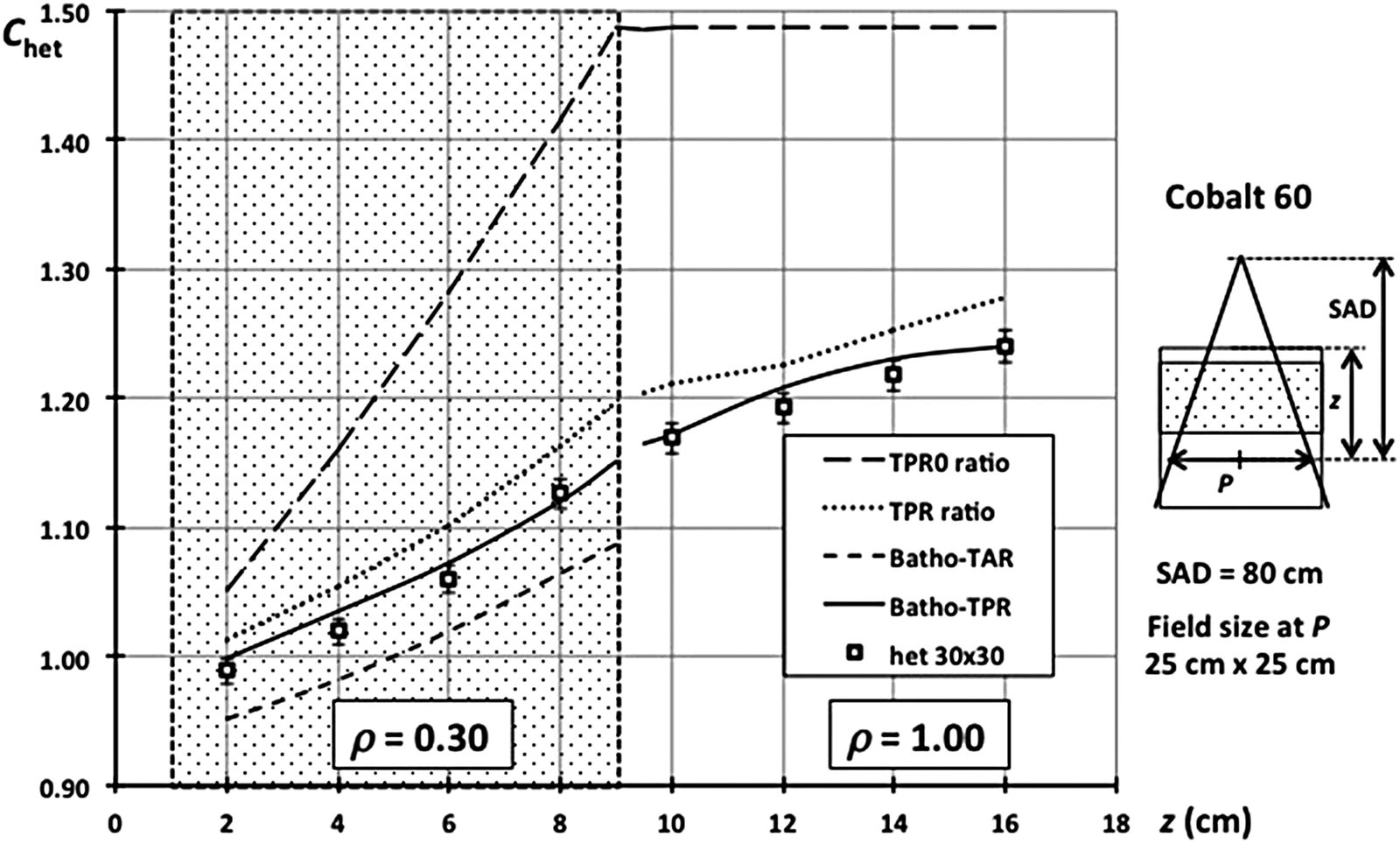
La Figura 28.5 muestra resultados para una heterogeneidad de 8 cm ($\rho = 0{,}3$) a 1 cm de profundidad en haz de cobalto-60. El método TPR0 sobreestima fuertemente. El Batho-TAR original funciona bien por debajo de la heterogeneidad pero subestima dentro de ella. La formulación Batho-TPR ofrece el mejor compromiso, con errores típicamente menores al 2%.
| Método | Dentro de la heterogeneidad | Debajo de la heterogeneidad | Limitación principal |
|---|---|---|---|
| Profundidad efectiva (TAR/TPR ratio) | Sobreestima corrección | Sobreestima corrección | Ignora modificación de dispersión |
| Batho original (TAR) | Subestima dosis | Buena precisión (~2%) | No contabiliza retrodispersión |
| Batho-TPR modificado | Mejor resultado | Buena precisión (~2%) | Asume geometría de capas |
| Batho-TPR (campo cero) | Equivalente a TAR ratio | Equivalente a TAR ratio | Solo válido para campo pequeño |
Fuente: Handbook of Radiotherapy Physics, 2nd Ed., Capítulo 28
Beam Subtraction y ETAR: Refinamientos 3D
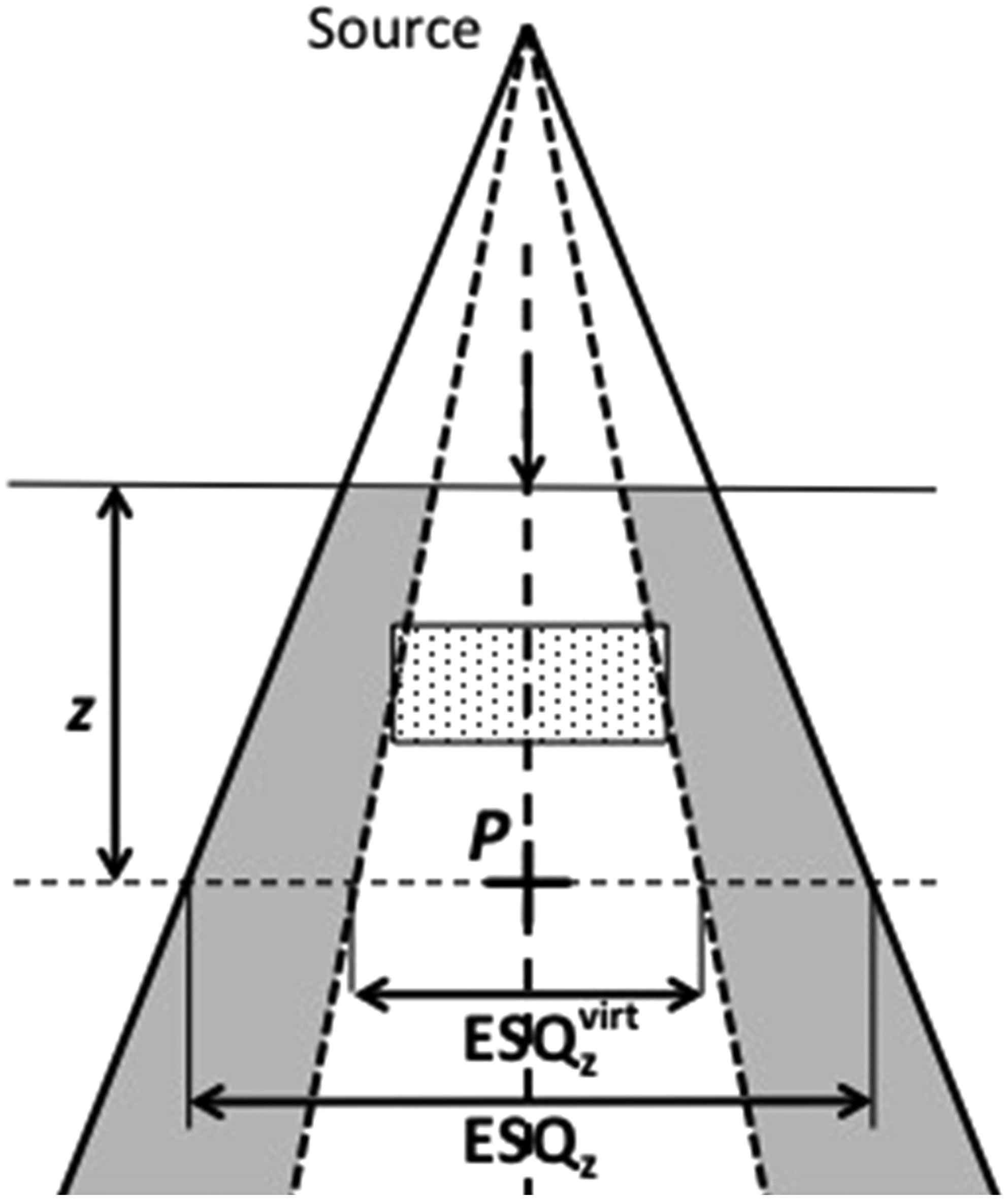
Método Beam Subtraction
Cuando la heterogeneidad es menor que el campo, el método de Batho falla. El beam subtraction (Lulu y Bjärngard, 1982; Kappas y Rosenwald, 1982) usa un haz virtual ($ESQ_z^{virt}$) que cubre exactamente la heterogeneidad:
$$C_{het}^{Batho-subt} = 1 + \frac{TPR(z, ESQ_z^{virt})}{TPR(z, ESQ_z)} \times (C_{het}^{Batho} – 1)$$
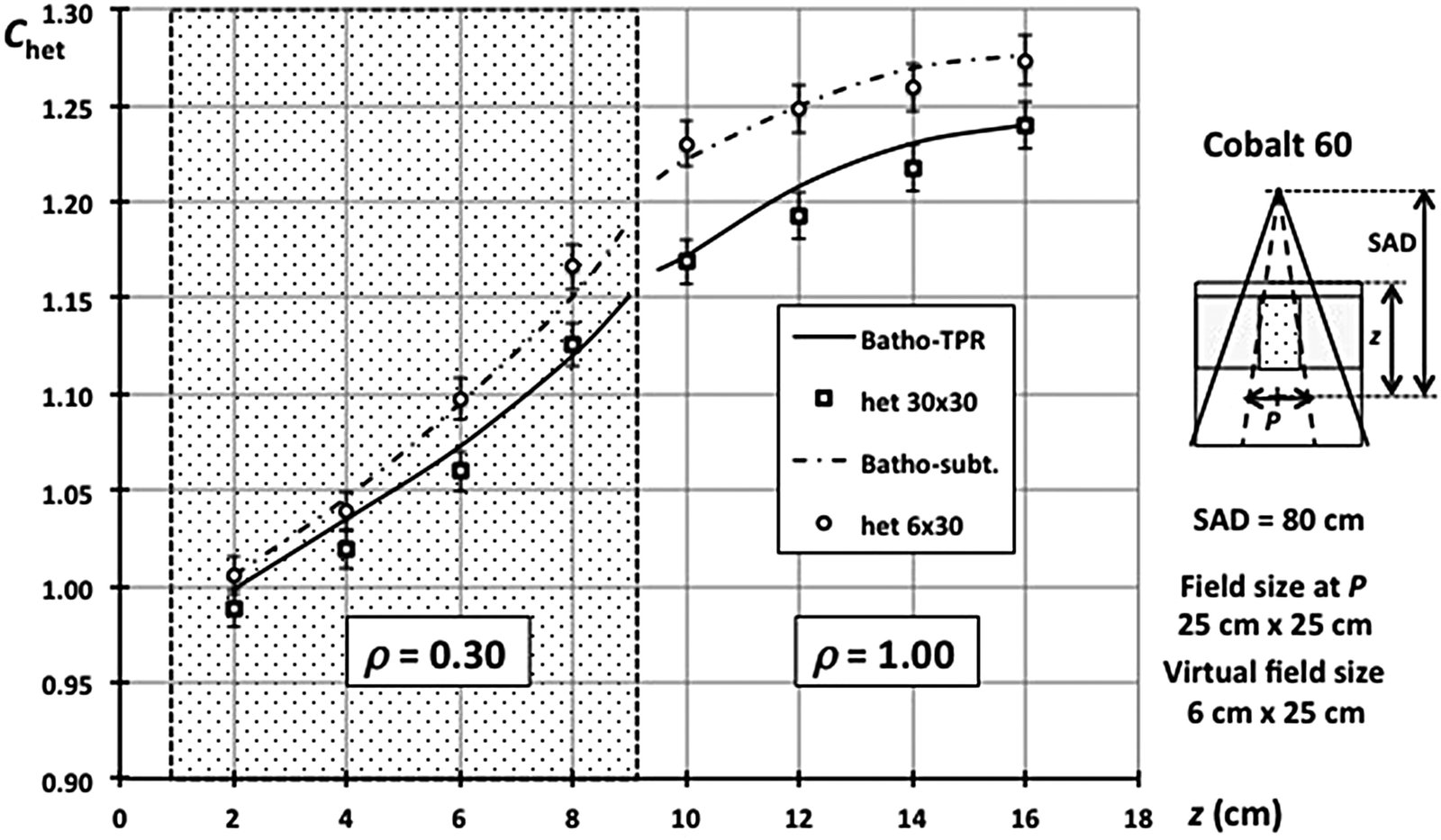
La Figura 28.7 confirma la eficacia: para una heterogeneidad de 6 cm ($\rho = 0{,}3$) en campo de 25×25 cm², la curva de beam subtraction coincide con los datos experimentales.
Método ETAR (Equivalent Tissue-Air Ratio)
El método ETAR (Sontag y Cunningham, 1978) va más allá, escalando no solo la profundidad sino también el tamaño de campo:
$$C_{het}^{ETAR} = \frac{TPR(z_{eff}, ESQ_z^{eff})}{TPR(z, ESQ_z)}$$
donde $ESQ_z^{eff}$ resulta de escalar el radio del campo circular equivalente por la densidad efectiva $\bar{\rho}$:
$$\bar{\rho} = \frac{\sum_{i,j,k} \rho_{ijk} W_{ijk}}{\sum_{i,j,k} W_{ijk}}$$
En la época, el cálculo 3D completo era prohibitivo, así que Sontag y Cunningham redujeron el array de densidades a 2D, colapsando píxeles con las mismas coordenadas X,Z.
Limitaciones de los Métodos Broad-Beam
Después de recorrer toda la cadena de correcciones queda claro por qué los métodos broad-beam fueron progresivamente reemplazados. Cada corrección agrega aproximaciones sobre aproximaciones. Funcionaron razonablemente para campos rectangulares durante décadas, pero resultan inadecuados para escenarios modernos: campos no rectangulares, IMRT, VMAT y estereotaxia.
La limitación fundamental es tratar la dispersión de forma global, sin ray-tracing explícito del componente de scatter. Los algoritmos de Monte Carlo y convolución/superposición ofrecen hoy una precisión fundamentalmente superior con tiempos de cálculo aceptables en la práctica clínica. Para una visión completa de esta evolución, vea nuestra guía sobre algoritmos de cálculo de dosis por fotones.




