WBRT versus Radiocirugía en Metástasis Cerebrales
La decisión entre irradiación cerebral total (WBRT) y radiocirugía estereotáxica (SRS) depende de factores como número y volumen de las metástasis, estado funcional y perfil molecular. Herramientas pronósticas como el Graded Prognostic Assessment (GPA) molecular permiten estratificar pacientes incorporando histología, estado mutacional y número de lesiones en una puntuación pronóstica más refinada que las escalas antiguas basadas únicamente en RPA.
En la práctica clínica, la SRS preserva mejor la función neurocognitiva y la calidad de vida, mientras que la WBRT mejora las tasas de control intracraneal distante y global. Estos compromisos tienen consecuencias reales en los desenlaces funcionales a largo plazo y merecen una discusión cuidadosa con el paciente y el equipo multidisciplinario antes de definir la estrategia de tratamiento.
Para una revisión completa de las técnicas de delineación en radioterapia, consulte nuestra guía completa sobre delineación de volumen blanco.
WBRT: Principios de Planificación y Delineación del Blanco
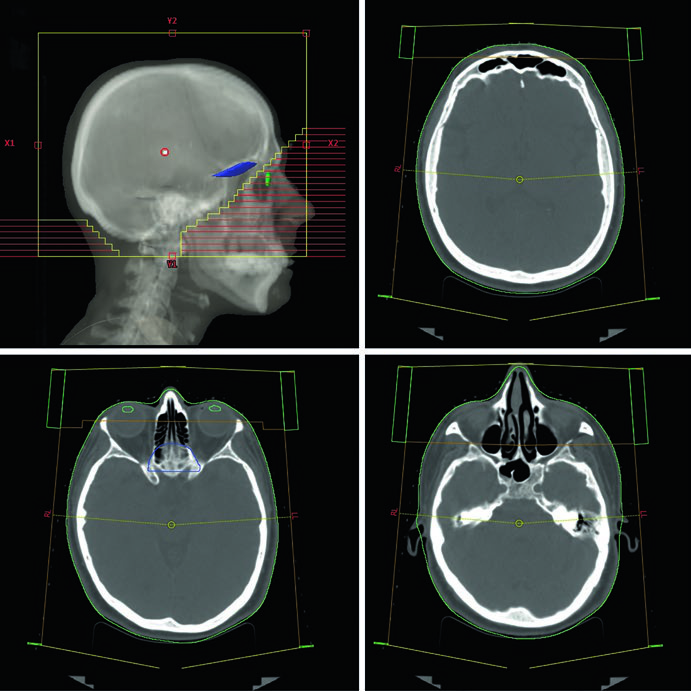
La planificación convencional de WBRT utiliza 3D-CRT con haces laterales opuestos de fotones de 6 MV. Los haces se rotan ligeramente en oblicuo anterior derecho e izquierdo (RAO/LAO) para evitar la divergencia hacia los cristalinos. El colimador multiláminas (MLC) bloquea los cristalinos mientras asegura cobertura adecuada de la placa cribiforme y los lóbulos temporales. Un detalle técnico que marca diferencia en la práctica diaria: el isocentro puede colocarse en la línea media a nivel del canto del ojo, eliminando la divergencia del haz hacia los ojos y cristalinos sin necesidad de rotar los haces.
La TC de planificación sin contraste abarca desde el vértex hasta la columna cervical superior, con espesor de corte axial ≤2,5 mm. El paciente se posiciona en decúbito supino con la cabeza en posición neutral, inmovilizado con máscara termoplástica y campo de visión de 600 mm. La verificación del posicionamiento se realiza semanalmente con películas ortogonales e imagen MV en la WBRT convencional. La imagen kV diaria se reserva para WBRT basada en IMRT, donde la precisión de entrega exige verificación más frecuente.
Los bordes de campo en la WBRT convencional siguen un protocolo definido: superiormente, flash de 2 cm por encima del vértex; posteriormente, flash de 2 cm con posible extensión cervical posterior; inferiormente, base de C1; y anteriormente, el MLC bloquea desde el flash de 2 cm hasta la cara anterior de C1, protegiendo las parótidas y los cristalinos. La cobertura de los lóbulos temporales y la placa cribiforme es obligatoria en todos los escenarios clínicos.
Escenarios Clínicos y Campos Sugeridos
La planificación varía según la indicación clínica. Las metástasis difusas (numerosas o «incontables») y la irradiación craneal profiláctica (PCI) para carcinoma de pulmón de células pequeñas (SCLC) reciben campos convencionales estándar. La enfermedad leptomeníngea requiere cobertura adicional de los nervios ópticos, la región retroorbitaria y la lámina cribosa, con márgenes expandidos de 8–10 mm para penumbra y posicionamiento diario en los lóbulos temporales y placa cribiforme. La leucemia y el linfoma del SNC exigen inclusión de la retina y, cuando hay compromiso ocular confirmado por examen con lámpara de hendidura, cobertura de los globos oculares completos.
| Escenario | Campos | Volúmenes Blanco | Bordes de Campo |
|---|---|---|---|
| WBRT Convencional | 3D-CRT lateral opuesto (RAO/LAO) | Contenido craneal completo | Sup: 2 cm flash; Post: 2 cm flash; Inf: base de C1; Ant: MLC bloquea parótida y cristalinos |
| Enfermedad Leptomeníngea | 3D-CRT lateral opuesto | Contenido craneal + nervios ópticos + región retroorbitaria + lámina cribosa | Lóbulos temporales y placa cribiforme con margen adicional de 8–10 mm para penumbra y setup |
| Linfoma/Leucemia del SNC | 3D-CRT lateral opuesto | Contenido craneal + nervios ópticos + región retroorbitaria + retina ± globos completos | 1/3 posterior de los globos si no hay compromiso ocular; globos completos si compromiso confirmado |
| Preservación de cuero cabelludo | 3D-CRT lateral opuesto | Contenido craneal completo | Borde del MLC en la tabla externa de la calota |
| HA-WBRT | IMRT/VMAT | CTV: parénquima cerebral hasta el foramen magno; PTV: CTV menos (hipocampos + 5 mm) | Sin margen de setup adicional |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.1)
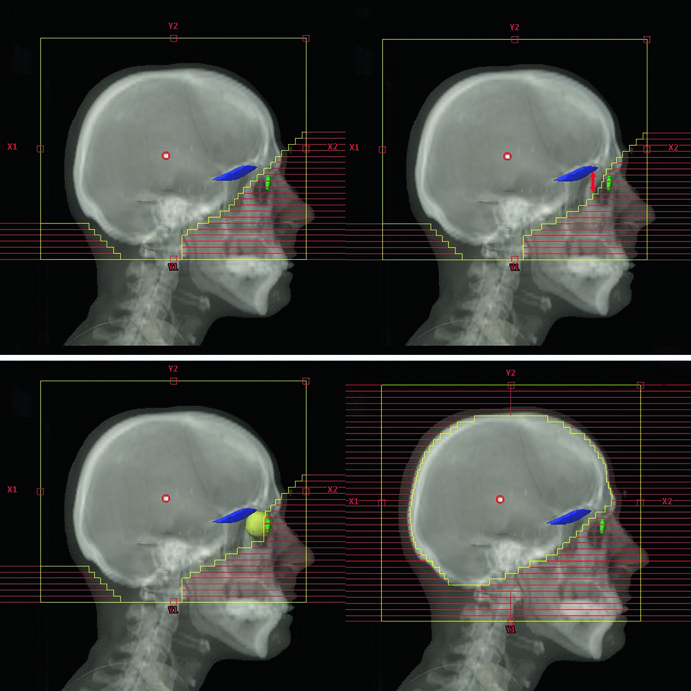
La técnica de preservación de cuero cabelludo merece mención especial. El resultado cosmético es la prioridad, pero el método puede producir un patrón de alopecia en «Mohawk invertido» — algo que conviene discutir con el paciente antes del tratamiento para alinear expectativas. El borde del MLC se posiciona en la tabla externa de la calota en lugar del flash convencional de 2 cm, reduciendo la dosis en el cuero cabelludo pero manteniendo cobertura adecuada del parénquima cerebral.
Dosis y Fraccionamiento en WBRT
El fraccionamiento varía según la indicación clínica y el pronóstico del paciente. El esquema más frecuente para metástasis cerebrales y enfermedad leptomeníngea es 30 Gy en 10 fracciones. La reirradiación con WBRT es factible con 20–25 Gy en 10 fracciones, pero requiere un intervalo mínimo de 4–6 meses entre los cursos para permitir la recuperación del tejido neural.
| Escenario Clínico | Dosis y Fraccionamiento |
|---|---|
| WBRT / Enfermedad leptomeníngea | 30 Gy / 10 fx (más común), 37,5 Gy / 15 fx (RTOG), 30 Gy / 12 fx, 20 Gy / 5 fx (mal pronóstico) |
| WBRT reirradiación | 20–25 Gy / 10 fx (intervalo mínimo de 4–6 meses) |
| PCI para SCLC | 25 Gy / 10 fx (más común) |
| Profilaxis SNC para LLA | 12 Gy / 8 fx |
| Leucemia SNC (alto riesgo) | ≥18 Gy / 9–10 fx (dosis basada en la intensidad de la terapia sistémica) |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.2)
Preservación Hipocampal en WBRT (HA-WBRT)
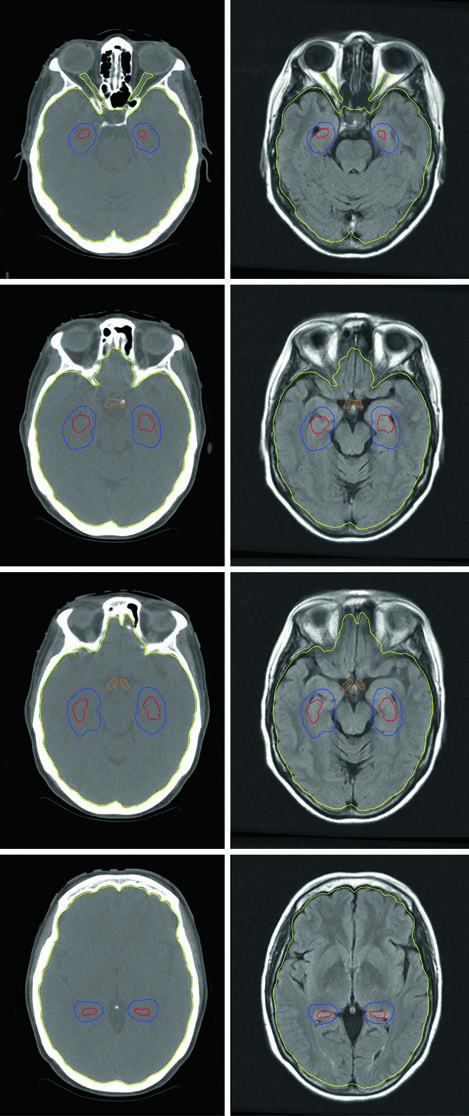
Las estrategias para preservar la función neurocognitiva incluyen la adición de memantina y/o la técnica de HA-WBRT. La preservación hipocampal es particularmente relevante porque la neurogénesis adulta ocurre en la zona subgranular (SGZ) del hipocampo — la irradiación de esta región contribuye significativamente al deterioro cognitivo post-WBRT, especialmente en memoria y aprendizaje verbal.
La planificación de HA-WBRT requiere IMRT con planificación inversa, utilizando TC de planificación fusionada con RM contrastada con gadolinio. La secuencia utilizada es spoiled gradient tridimensional con espesor de corte axial de 1,25–1,5 mm para definir la región de exclusión hipocampal con la precisión necesaria. Según las directrices de contorno del RTOG 0933, solo la porción SGZ de los hipocampos se contornea (no la estructura completa), y se aplica una expansión volumétrica de 5 mm para crear la zona de exclusión. El PTV consiste en todo el tejido cerebral (parénquima hasta el foramen magno) menos los hipocampos expandidos, sin margen de setup adicional.
Las restricciones de dosis son estrictas y varían según la indicación. Para metástasis cerebrales: hipocampos D100% ≤9 Gy, Dmax ≤16 Gy; nervios ópticos y quiasma Dmax ≤30 Gy. Para PCI de SCLC con preservación hipocampal, los límites se estrechan aún más: hipocampos D100% ≤7,5 Gy, Dmax ≤13,5 Gy; nervios ópticos y quiasma Dmax ≤25 Gy. Un criterio de exclusión fundamental: las lesiones ubicadas a menos de 5 mm del hipocampo descalifican al paciente para HA-WBRT.
SRS: Principios de Planificación y Delineación del Blanco
La radiocirugía estereotáxica abarca escenarios de fracción única y SRS fraccionada (2–5 fracciones) tanto para metástasis intactas como para cavidades posresección. Los instrumentos disponibles incluyen sistemas con marco o sin marco con Gamma Knife (cobalto-60) y sistemas basados en LINAC. Cada plataforma tiene particularidades prácticas: en Gamma Knife, PTV = CTV sin expansión adicional; en sistemas LINAC, puede ser necesario un pequeño margen de PTV dependiendo de la precisión mecánica del sistema y del protocolo de verificación de imagen.
La delineación del volumen blanco y la planificación utilizan RM volumétrica contrastada ponderada en T1 con cortes de 1–2 mm preferentemente. Cuando el paciente no tolera RM o tiene un dispositivo implantado incompatible, se recurre a TC contrastada como alternativa. Para SRS basada en LINAC, se adquiere una TC de corte fino y se corregistra con la RM para el cálculo dosimétrico. La imagen diaria es obligatoria en sistemas LINAC.
Delineación del Volumen Blanco en SRS
La delineación difiere sustancialmente entre metástasis intactas y cavidades posquirúrgicas. Para lesiones intactas, el proceso es directo: el GTV es la lesión captante de contraste en la secuencia T1 de la RM, y el CTV equivale al GTV más 0 mm — sin margen adicional. Para cavidades posresección existen dos métodos bien establecidos en la literatura, cada uno con una filosofía de margen distinta.
| Blanco | GTV | CTV |
|---|---|---|
| Metástasis no resecadas | Lesión captante de contraste en RM T1 | GTV + 0 mm |
| Cavidad posresección (Método 1 — Soltys et al.) | n/a | Expansión uniforme de 2 mm alrededor de los bordes de la cavidad de resección en RM poscontraste |
| Cavidad posresección (Método 2 — Soliman et al.) | n/a | Toda la región captante + cavidad + trayecto quirúrgico en RM postoperatoria; 5–10 mm a lo largo del colgajo óseo si contacto dural preoperatorio; 1–5 mm si sin contacto dural; 1–5 mm a lo largo del seno venoso si contacto previo |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.3)
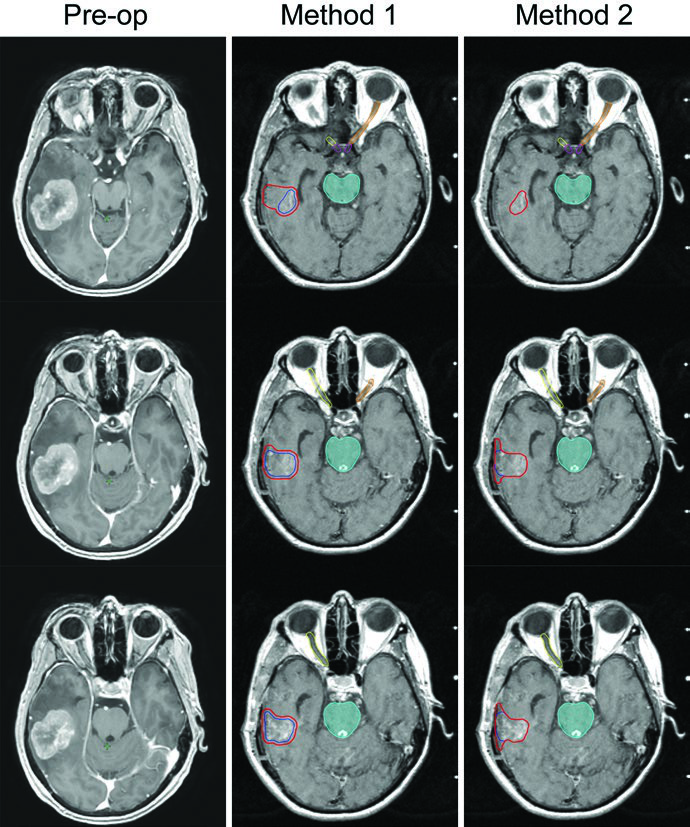
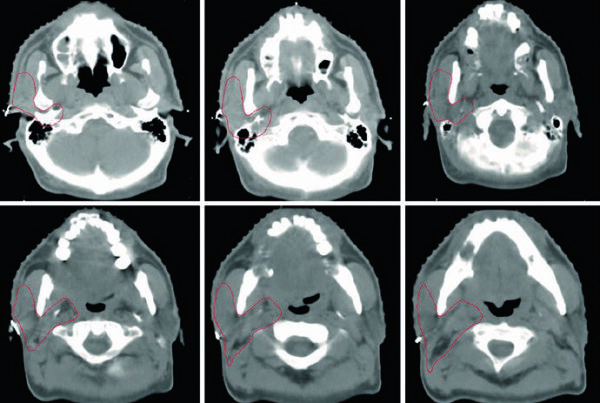
El Método 2 de Soliman et al. es más conservador y tiende a generar volúmenes de CTV mayores. En el ejemplo ilustrado, una cavidad de 24 mm en el lóbulo temporal izquierdo — tras resección total de metástasis de 33 mm de cáncer rectal primario con contacto dural preoperatorio pero sin contacto con seno venoso — recibiría un margen de 10 mm a lo largo del colgajo óseo. Se eligió fracción única por el tamaño pequeño de la cavidad (<3 cm) y distancia suficiente de estructuras cerebrales delicadas. Con Gamma Knife, PTV = CTV sin expansión adicional. El Método 1 de Soltys aplica simplemente 2 mm uniformes alrededor de la cavidad en la RM T1 posgadolinio, generando un volumen menor y potencialmente menos toxicidad.
Dosis y Restricciones de Órganos en Riesgo en SRS
La dosis en SRS depende del tamaño o volumen de la lesión y de la distancia a estructuras críticas. Los esquemas de fraccionamiento a continuación se basan en el protocolo Alliance A071801, que ofrece orientación para cavidades postoperatorias y metástasis intactas en 1, 3 o 5 fracciones.
| Parámetro | 1 Fracción | 3 Fracciones | 5 Fracciones |
|---|---|---|---|
| Dosis PTV — cavidad postop | 20 Gy (<4,2 cm³), 18 Gy (4,2–8,0 cm³), 17 Gy (8,0–14,4 cm³), 15 Gy (14,4–20 cm³), 14 Gy (20–30 cm³), 12 Gy (≥30 cm³ a <5 cm) | 27 Gy (<30 cm³) | 30 Gy (≥30 cm³ a <5 cm) |
| Dosis PTV — metástasis intactas | 24 Gy (<1 cm), 22 Gy (1,0–2,0 cm), 18 Gy (2,0–3,0 cm), 15 Gy (3,0–4,0 cm) | 27 Gy | 30 Gy |
| Tronco cerebral | V12 Gy < 1 cm³ | 23,1 Gy máx; V18 Gy < 0,5 cm³ | 28 Gy máx; V23 Gy < 0,5 cm³ |
| Aparato óptico | 9 Gy máx | 17,4 Gy máx; V13,8 Gy < 0,2 cm³ | 23 Gy máx; V20 Gy < 0,2 cm³ |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 28.4 — basado en el protocolo Alliance A071801)
La elección entre fracción única y fraccionada depende fundamentalmente del tamaño de la lesión y de la proximidad a estructuras nobles. Las lesiones pequeñas (<3 cm) con distancia suficiente de estructuras delicadas reciben fracción única con dosis más altas. Las cavidades mayores (≥30 cm³) y lesiones próximas al tronco cerebral o aparato óptico se benefician del fraccionamiento en 3–5 fracciones, que permite la entrega de una dosis total efectiva elevada respetando los límites de tolerancia de los órganos en riesgo mediante la reparación celular entre fracciones.
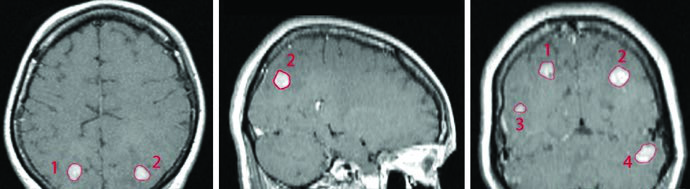
La SRS de múltiples isocentros permite tratar simultáneamente lesiones en diferentes localizaciones cerebrales — como lóbulos parietales, temporal y cerebelo — en una sola sesión de tratamiento. En el ejemplo del libro, cuatro metástasis de cáncer de mama (volúmenes de 0,07 a 1,92 cm³, diámetros de 6 a 20 mm) fueron tratadas con fracción única en una paciente que ya había recibido WBRT previa de 30 Gy en 10 fracciones. El GTV de cada lesión fue definido por la captación de contraste en la RM T1 posgadolinio y, con Gamma Knife, PTV y CTV utilizaron expansión de 0 mm desde el GTV.
Para profundizar en otros temas de delineación cerebral, consulte los artículos sobre tumores benignos del SNC y tumores malignos del SNC de la misma serie.