En cáncer de esófago, la delineación de volumen objetivo y el diseño de campos empiezan en la simulación. Este capítulo organiza un flujo práctico con planificación basada en tomografía para IMRT y 3D-CRT, y después baja al detalle de movimiento respiratorio, cobertura ganglionar y márgenes para tumores cervicales, torácicos y de la unión gastroesofágica. Para revisar el panorama completo de la serie, consulte el Target Volume Delineation and Field Setup – Complete Clinical Guide.
Principios generales de planificación y delineación de volumen objetivo
El estándar que describen los autores usa planificación basada en tomografía computarizada con técnicas conformacionales. IMRT y 3D-CRT trabajan con múltiples ángulos de haz y permiten distintos grados de conformidad de dosis, pero ambas dependen del mismo requisito: contornear con precisión los volúmenes blanco, las estructuras normales y los órganos en riesgo, y después revisar los histogramas dosis-volumen antes de aprobar el plan.
La anatomía del esófago explica por qué esa disciplina no es opcional. El órgano comienza en el cuello, en el borde inferior del cartílago cricoides y por delante de la sexta vértebra cervical, desciende por el mediastino, atraviesa el diafragma y llega al abdomen. Por eso el plan exige conocer bien el cuello, el plexo braquial, el mediastino, los pulmones, el corazón, la médula espinal y el esófago normal. El capítulo además remite a un atlas de contorneo para estas estructuras torácicas.
Simulación
La posición ideal de simulación coloca los brazos por encima de la cabeza. Así se amplía la cantidad de arreglos de haz disponibles y se evita irradiar a través de los brazos. En tumores distales o de la unión gastroesofágica, el capítulo recomienda incluir control del movimiento respiratorio con tomografía 4D, gating respiratorio o técnicas de apnea, porque el desplazamiento del blanco modifica la forma en que se expanden los volúmenes.
También hay una medida operativa concreta para mejorar la reproducibilidad. Los pacientes con tumores distales o de la unión gastroesofágica deben permanecer en ayuno por al menos 2 a 3 horas antes de la simulación y antes de cada tratamiento. El objetivo es limitar la variación diaria provocada por gas gástrico o intestinal. Si se utiliza IMRT, el contraste intravenoso durante la simulación puede definir mejor los campos ganglionares.
Subdivisiones anatómicas del esófago
Tomando una distancia estándar de 40 cm entre los incisivos y la unión gastroesofágica, el capítulo divide el esófago en cuatro segmentos prácticos. El esófago cervical llega aproximadamente hasta 15 a 20 cm. El segmento torácico superior o proximal va de 18 a 20 cm hasta cerca de 25 cm. El torácico medio o distal cubre de 25 cm a 30 a 32 cm. El esófago abdominal va de 30 a 32 cm hasta 40 cm. Esta referencia endoscópica ayuda a ubicar el tumor y a decidir qué drenaje ganglionar debe incluirse de forma electiva.
Los autores proponen abordar las neoplasias por subconjuntos anatómicos: tumores de esófago superior y medio, tumores torácicos y tumores de la unión gastroesofágica. Si la enfermedad cruza más de una subdivisión, el contorneo puede seguir las guías de todos los grupos implicados. En cualquier localización, ambos pulmones deben delinearse completos para analizar el DVH. En tumores altos conviene delinear plexo braquial y laringe. En tumores bajos, la atención se mueve hacia corazón, hígado, riñones, estómago y asas intestinales vecinas.
Delineación de volumen objetivo en cáncer de esófago
El capítulo utiliza GTV, CTV y PTV, pero aclara que en la institución de los autores se define de rutina un ITV entre el GTV y el CTV. Ese ITV recoge el movimiento interno del tumor observado en la CT 4D. Luego se expande a CTV y después a PTV. En la práctica, esa capa intermedia es especialmente útil en tumores distales y de la unión gastroesofágica, donde el movimiento respiratorio puede ser relevante.
El GTV debe delinearse con apoyo de CT, PET, endoscopia digestiva alta y ultrasonido endoscópico. El ultrasonido endoscópico mejora la valoración de la profundidad de invasión y ayuda a clasificar pequeños ganglios peri-esofágicos difíciles de interpretar solo con CT o PET. Si el tumor se ubica por encima de la carina, el capítulo recomienda broncoscopia para descartar una fístula traqueoesofágica, ya que ese hallazgo puede retrasar la radioterapia.
Márgenes entre ITV, CTV y PTV
La expansión estándar de ITV a CTV es de 1 cm en sentido radial para abarcar los ganglios peri-esofágicos y de 3 a 4 cm en dirección superior e inferior a lo largo de la mucosa esofágica, con el fin de cubrir diseminación submucosa y posibles lesiones discontinuas. Cuando el volumen se superpone con el corazón o con hígado sano, ese margen puede reducirse a 0,5 cm si el manejo del movimiento es adecuado.
En tumores distales y de la unión gastroesofágica, una expansión caudal de 4 cm incluiría demasiado estómago o vísceras abdominales. Por eso la recomendación es 2 cm a lo largo de mucosa gástrica clínicamente no comprometida. La excepción aparece en tratamientos con intención preoperatoria y dosis de hasta 4500 cGy, donde puede ser razonable un margen gástrico de 4 cm o más, sobre todo con extensión gástrica importante. Los cuerpos vertebrales no comprometidos y los riñones se excluyen del CTV. Los ganglios francamente comprometidos pueden recibir un margen de 0,5 a 1,0 cm desde GTV a CTV, y si existen ganglios peri-esofágicos macroscópicamente positivos, el CTV debe cubrir al menos 1 cm en sentido cefálico por encima de ellos. El margen recomendado de CTV a PTV es de 0,5 cm, con la salvedad de que puede ajustarse según la técnica usada para valorar movimiento y la confianza clínica en la extensión real de la enfermedad.
Cobertura ganglionar electiva según la localización del tumor
La cobertura ganglionar electiva cambia con el nivel del tumor primario. En tumores cervicales y torácicos proximales se incluyen ambas cadenas supraclaviculares. Su límite craneal es el borde inferior del cartílago cricoides, y los límites anterior, posterior y lateral están dados por el músculo esternocleidomastoideo. En tumores torácicos proximales también se agregan ganglios mediastínicos además de los peri-esofágicos, cubriendo toda la tráquea, los niveles 2 y 4, con extensión hacia el esternón y las cabezas claviculares para abarcar el nivel 3.
Los tumores distales deben incluir los ganglios celíacos. El capítulo los delimita con precisión: aspecto lateral de T12 a la derecha, 0,5 a 1 cm más allá del borde lateral de la aorta a la izquierda, cuerpos vertebrales por detrás y páncreas por delante. En este grupo no hace falta irradiar de forma electiva las estaciones mediastínicas superiores, salvo la porción que ya quede incluida por la expansión craneal del primario. En tumores de la unión gastroesofágica, el CTV debe incluir ganglios paraaórticos y del ligamento gastrohepático en un volumen limitado por el hígado a la derecha y el estómago a la izquierda.
Unión gastroesofágica y clasificación de Siewert-Stein
Cuando un tumor de la unión gastroesofágica se superpone de manera marcada con la cardias gástrica, puede ser difícil decidir si el origen es más gástrico que esofágico. Para resolver esa zona gris, el capítulo usa la clasificación de Siewert-Stein. Las lesiones tipo I tienen su epicentro entre 1 y 5 cm por encima de la unión. Las tipo II se ubican desde 1 cm proximal hasta 2 cm distal. Las tipo III tienen epicentro entre 2 y 5 cm por debajo de la unión. El texto considera razonable usar el tipo II como punto de corte para cáncer de esófago y añade que la octava edición del AJCC define como esofágicos los tumores cuyo epicentro no se extiende más de 2 cm dentro de la cardias gástrica.
En tumores Siewert tipo II puede incluirse parte o toda la región del hilio esplénico y de la curvatura mayor. Además, siguiendo las guías vigentes para cáncer gástrico, se puede considerar laparoscopia diagnóstica, colocación de yeyunostomía en Y, quimiorradioterapia preoperatoria o quimiorradioterapia posoperatoria.
Resumen de recomendaciones por segmento esofágico
La Tabla 14.1 resume las recomendaciones de contorneo en cuatro escenarios anatómicos. Reúne la definición del segmento, el margen de ITV a CTV, el margen de CTV a PTV, la cobertura ganglionar electiva y la dosis señalada por los autores.
Tabla 14.1. Recomendaciones de contorneo en cáncer de esófago
| Subdivisión | Definición | Margen ITV a CTV | Margen CTV a PTV | Cobertura ganglionar electiva | Dosis |
|---|---|---|---|---|---|
| Cervical | Incisivos hasta aproximadamente 15–20 cm | 3 cm superior e inferior a lo largo de la mucosa, con 1 cm radial | 0,5 cm | Peri-esofágica, supraclavicular y ± mediastino anterior | 50,4 Gy en fracciones de 1,8 Gy, con consideración de refuerzo de dosis hasta 60–70 Gy para SCC |
| Torácico superior | De 18–20 cm hasta aproximadamente 25 cm | 3 cm superior e inferior a lo largo de la mucosa, con 1 cm radial | 0,5 cm | Peri-esofágica, supraclavicular y ± mediastino anterior | 50,4 Gy en fracciones de 1,8 Gy |
| Torácico inferior | De 25 cm hasta aproximadamente 37 cm | 3 cm superior e inferior a lo largo de la mucosa, con 1 cm radial | 0,5 cm | Peri-esofágica | 50,4 Gy en fracciones de 1,8 Gy en tratamiento definitivo; 41,4–50,4 Gy en fracciones de 1,8 Gy en tratamiento preoperatorio |
| Abdominal (unión gastroesofágica) | De aproximadamente 37 a 42 cm | 3 cm superior a lo largo de la mucosa esofágica y 1–2 cm inferior a lo largo de la mucosa gástrica para 50,4 Gy; con dosis de intención preoperatoria (≤4500 cGy), un margen gástrico ≥4 cm puede ser apropiado | 0,5 cm | Peri-esofágica, ligamento gastrohepático (estaciones paracárdica y gástrica izquierda), eje celíaco y ± hilio esplénico | 50,4 Gy en fracciones de 1,8 Gy en tratamiento definitivo; 41,4–50,4 Gy en fracciones de 1,8 Gy en tratamiento preoperatorio |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 14.1)
Ejemplos clínicos del capítulo
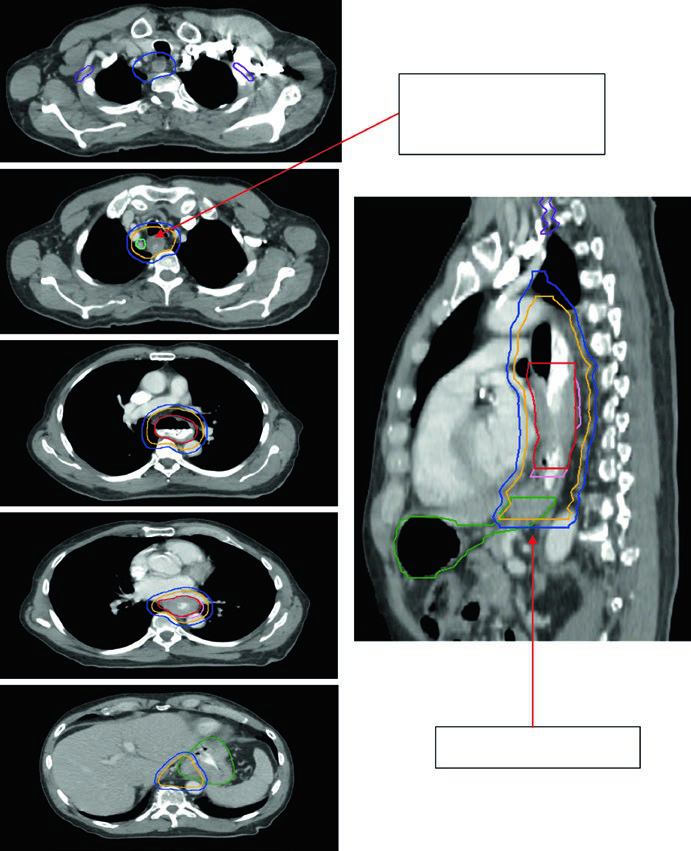
Las figuras muestran cómo estas reglas se convierten en contornos reales. La Figura 14.1 presenta a un paciente de 69 años con carcinoma escamoso del esófago cervical o torácico superior. El PET muestra un primario captante y ganglios paratraqueales levemente ávidos, mientras que la endoscopia describe una masa ulcerada y submucosa entre 15 y 23 cm desde los incisivos. El conjunto final incluye plexo braquial, laringe, GTV esofágico, GTV ganglionar, CTV, PTV de 54 Gy y PTV de 60 Gy. La continuación del caso subraya un punto práctico: la cobertura supraclavicular bilateral es electiva, pero el CTV no sobrepasa el cartílago cricoides.
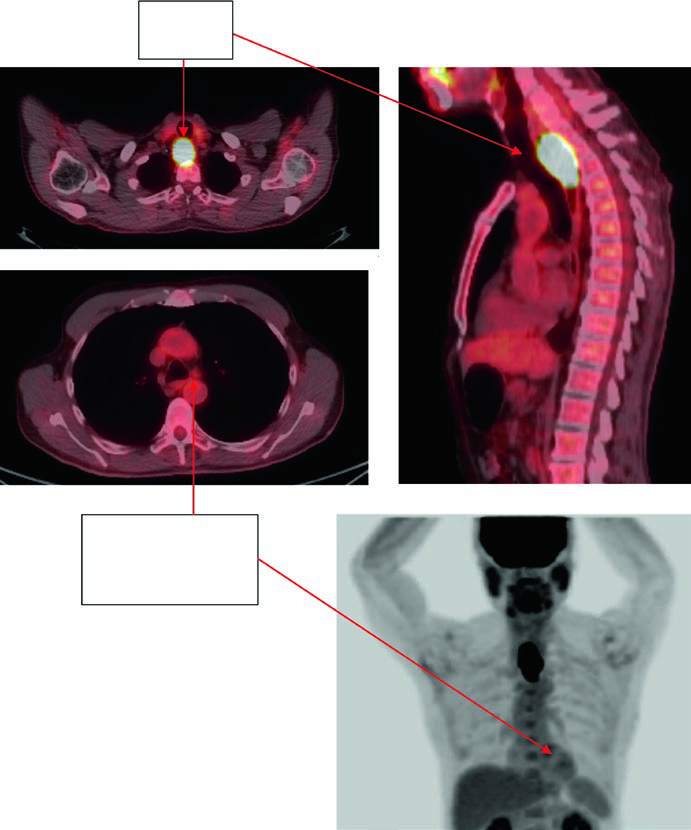
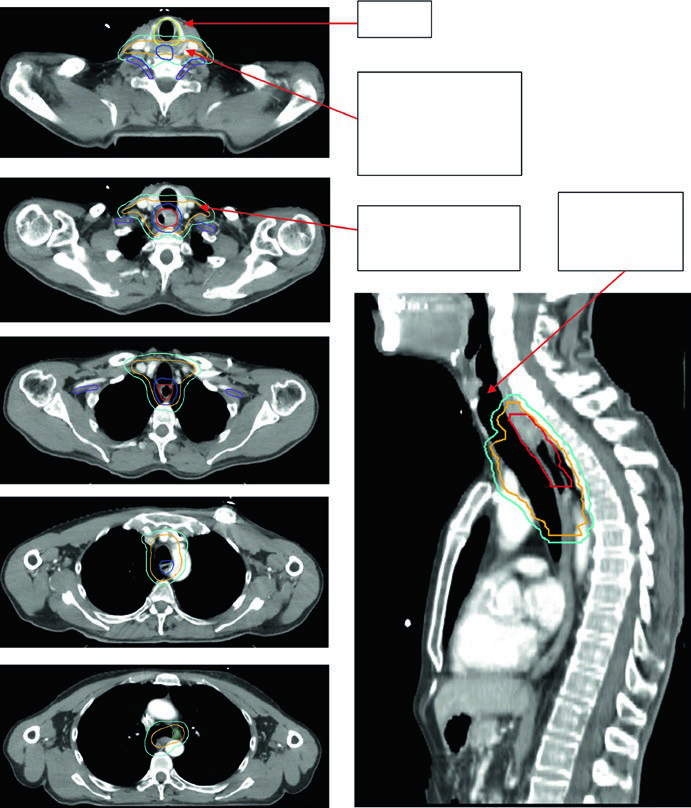
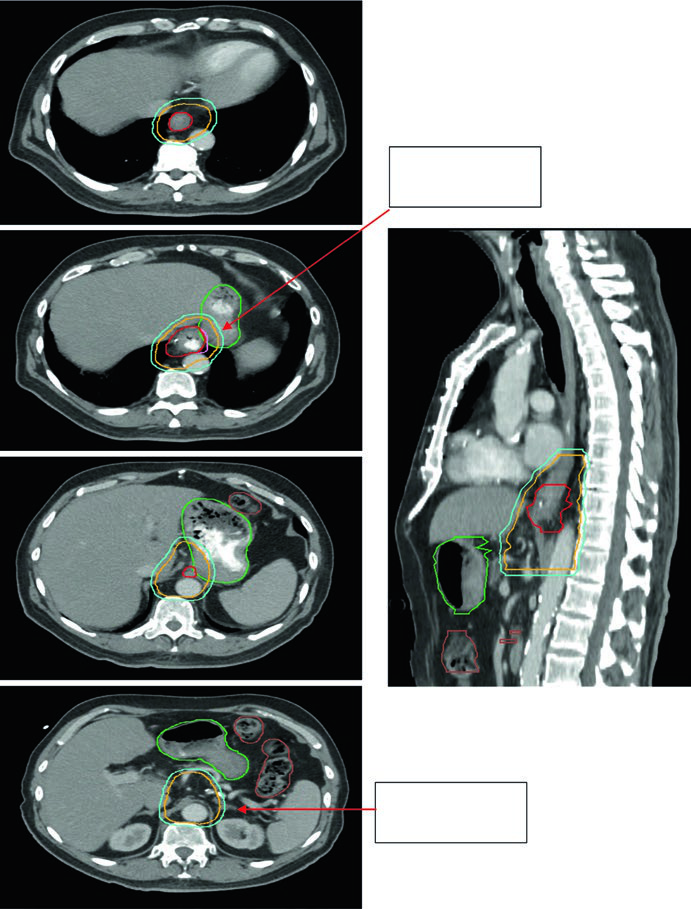
La Figura 14.2 sigue a un paciente de 81 años con adenocarcinoma esofágico torácico inferior uT3N1. El PET muestra el primario y un ganglio 4R. La endoscopia describe un adenocarcinoma circunferencial y parcialmente obstructivo entre 31 y 35 cm desde los incisivos, y el ultrasonido endoscópico apoya enfermedad T3 con sospecha en el mismo 4R. La imagen de continuación fija dos números centrales del capítulo: 0,5 cm desde GTV a CTV para el ganglio comprometido y 3 a 4 cm de cobertura inferior.
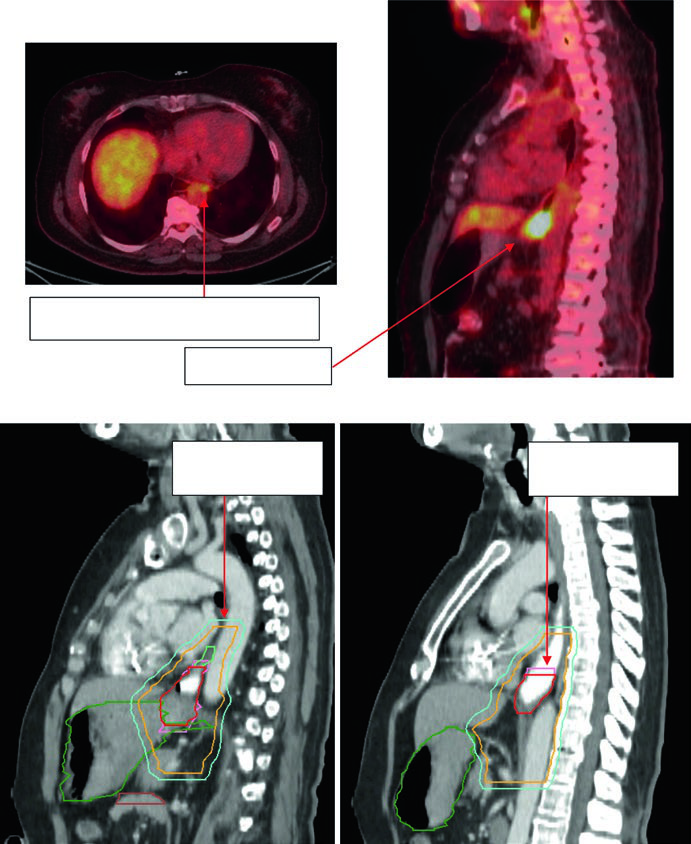
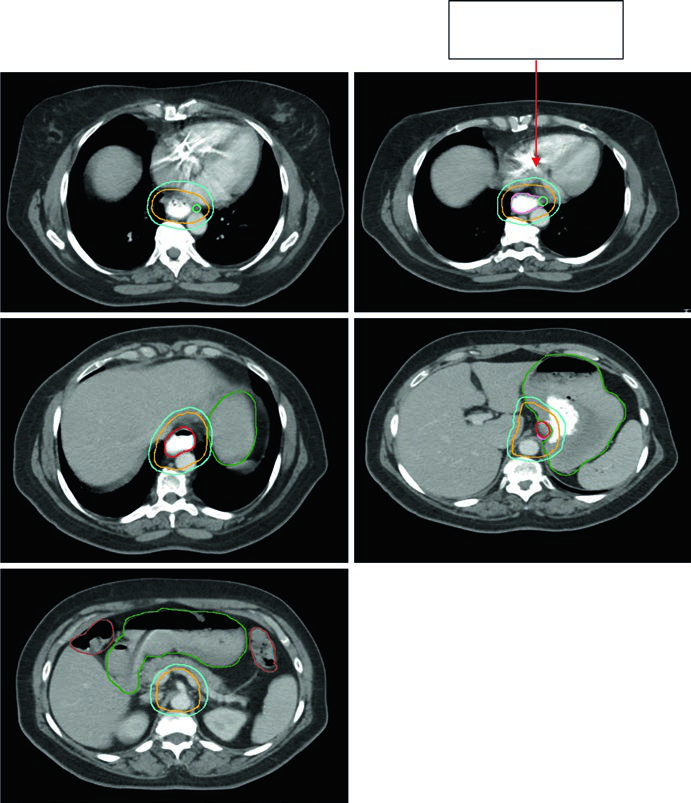
Las Figuras 14.3 y 14.4 se concentran en la unión gastroesofágica. En la Figura 14.3, un paciente de 75 años con adenocarcinoma uT3N0 muestra un CTV que se extiende al estómago proximal y al eje celíaco. En la Figura 14.4, un paciente de 59 años con adenocarcinoma uT3N2 localizado entre 36 y 40 cm desde los incisivos presenta primario y ganglio paraesofágico captantes en PET. La tomografía sagital de planificación muestra el movimiento del GTV dentro del ITV, la cobertura de 3 a 4 cm por encima del ITV y la inclusión explícita del ganglio paraesofágico dentro del CTV.
El cierre del capítulo es muy concreto. Hay que seguir el eje mucoso, medir bien el movimiento, adaptar la cobertura electiva al nivel anatómico del primario y evitar expansiones distales automáticas sobre estómago o vísceras no comprometidas. Si quiere comparar esta lógica con otros sitios anatómicos de la serie, vuelva a la guía completa de delineación de volumen objetivo y planificación de campos.