Delineación del cáncer de páncreas en radioterapia
El adenocarcinoma pancreático representa uno de los desafíos más exigentes en la planificación de radioterapia abdominal. La proximidad íntima de órganos luminales radiosensibles — estómago, duodeno e intestino delgado — al volumen blanco obliga a un equilibrio constante entre cobertura tumoral y protección de órganos en riesgo (OARs). La IMRT se ha convertido en la técnica estándar para tratar el cáncer de páncreas en escenarios neoadyuvante, adyuvante y definitivo, mientras que los enfoques ablativos requieren SBRT o técnicas guiadas por imagen.
Para una visión integral de todos los sitios anatómicos abordados en este libro, consulte nuestra guía completa sobre delineación de volumen blanco y campos en radioterapia.
Simulación y manejo del movimiento respiratorio
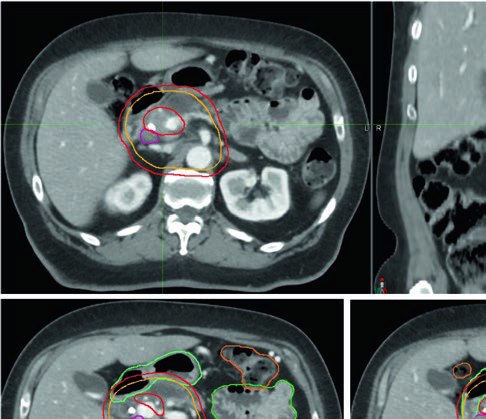
La TC de simulación con contraste IV en protocolo pancreático resulta indispensable para la delineación precisa del blanco y los OARs. El protocolo estándar utiliza 150 cc de contraste yodado a 5 cc/s, con adquisición en dos fases: arterial tardía (35 s de retraso) y portal venosa (90 s de retraso). Este enfoque bifásico permite delimitar tanto el tumor primario — típicamente hipointenso — como la extensión vascular, crítica para dosis superiores a 50 Gy en EQD2.
El manejo del movimiento respiratorio reduce las dosis a los OARs y maximiza la cobertura del blanco. Para cualquier enfoque ablativo, el control de movimiento es obligatorio. El gating — ya sea en inspiración profunda sostenida (DIBH) o gating espiratorio — es preferible, pero requiere fiduciales metálicos o stent metálico como referencias. Cuando el gating no es viable, la alternativa es el volumen blanco interno (ITV), delineando el GTV en todas las fases del 4D-CT. El paciente se inmoviliza en alpha-cradle personalizado con brazos elevados sobre la cabeza cuando sea tolerable.
Volúmenes blanco en el escenario neoadyuvante (borderline resecable)
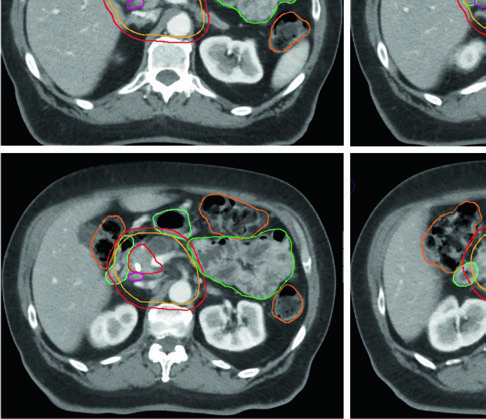
El tratamiento preoperatorio de enfermedad borderline resecable o resecable de alto riesgo utiliza dosis más bajas y, por tanto, tecnología menos compleja. Sin embargo, los márgenes deben ser suficientemente generosos para englobar toda la enfermedad microscópica y la extensión radiográficamente oculta a lo largo de la vasculatura.
Definición de volúmenes neoadyuvantes
| Volumen | Definición y descripción |
|---|---|
| GTV | Toda enfermedad macroscópica en imagen, incluyendo el tumor primario (típicamente hipointenso), con atención especial a la extensión a lo largo de los vasos y todos los ganglios sospechosos |
| ITV (opcional) | Si se utiliza enfoque ITV, delinear el GTV en todas las fases del 4D-CT |
| CTV | Expansión uniforme de al menos 1 cm sobre toda la enfermedad macroscópica + cobertura de cadenas del tronco celíaco (CA) y arteria mesentérica superior (AMS) + margen adicional a lo largo de vasos en caso de incertidumbre + cobertura del hilio esplénico (lesiones de cuerpo/cola) + cobertura opcional de porta hepatis (lesiones de cabeza) |
| PTV | Margen basado en técnica de control de movimiento, mínimo 0,5 cm. Sin ITV y en respiración libre, expansión de 1–1,5 cm en dirección craneocaudal |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.1)
Los esquemas de fraccionamiento apropiados incluyen 25 Gy en 5 fracciones, 30 Gy en 10 fracciones, 36 Gy en 12 fracciones y 50,4 Gy en 28 fracciones. La elección depende de la intención terapéutica, la anatomía del paciente y la tecnología disponible.
Tratamiento definitivo de enfermedad irresecable: dosis ablativas
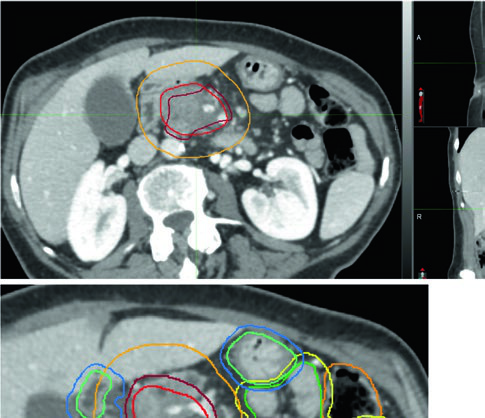
Los tumores irresecables deben recibir dosis ablativas ($\text{BED}_{10} \geq 100\ \text{Gy}$) siempre que estén disponibles técnicas de control de movimiento y guía por imagen. La tendencia hacia menos fracciones — impulsada en parte por la naturaleza intensiva de la planificación estereotáctica — debe equilibrarse con consideraciones radiobiológicas y dosimétricas que garanticen una dosis realmente ablativa.
La proximidad de los OARs luminales radiosensibles frecuentemente exige esquemas hipofraccionados con más de cinco fracciones. La recomendación práctica: 75 Gy en 25 fracciones para tumores a menos de 1 cm de los OARs, y 67,5 Gy en 15 fracciones para tumores a más de 1 cm. El esquema de 50 Gy en 5 fracciones puede usarse selectivamente cuando el tumor está a más de 2 cm de los OARs. Cuando el contacto extenso tumor-OAR impide cobertura adecuada con dosis ablativa, las alternativas no ablativas de 50,4–56 Gy en 28 fracciones o 33 Gy en 5 fracciones son opciones razonables.
Volúmenes blanco en el escenario definitivo
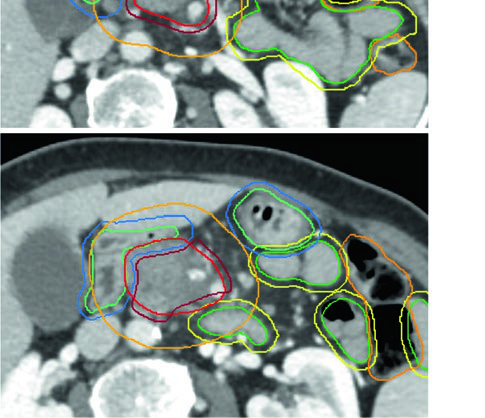
| Volumen | Definición y descripción |
|---|---|
| GTV | Toda enfermedad macroscópica en imagen, incluyendo el tumor primario y la extensión vascular |
| ITV (opcional) | Si se utiliza enfoque ITV, delinear el GTV en todas las fases del 4D-CT |
| CTV alta dosis | Corresponde al GTV (o ITV si se utiliza) sin margen adicional |
| CTV dosis microscópica | Expansión uniforme ≥ 1 cm sobre toda la enfermedad macroscópica + cadenas CA y AMS + hilio esplénico (cuerpo/cola) + margen vascular adicional + porta hepatis opcional (cabeza) |
| PTV alta dosis | Expansión 0–0,5 cm, sustrayendo OARs críticos superpuestos con margen de seguridad: • 56 Gy/28 fx o 33 Gy/5 fx: sustraer estómago e intestino delgado sin margen adicional • 50 Gy/10 fx, 67,5 Gy/15 fx o 75 Gy/25 fx: sustraer con expansión de 0,5 cm (0,7 cm para interfaz larga) |
| PTV microscópico | Mínimo 0,5 cm; sin ITV en respiración libre, 1–1,5 cm craneocaudal |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.2)
Un detalle práctico que a menudo se subestima: dada la naturaleza infiltrativa del PDAC, el sobre-contorneo del GTV para incluir el parénquima pancreático circundante puede ser razonable, especialmente cuando se respalda con imagen diagnóstica adicional. En regiones de contacto directo entre GTV y OAR crítico, el PTV debe excluir el OAR con un margen de seguridad que exceda la expansión del PRV.
PRVs para esquemas de dosis ablativa
| Estructura | Definición del PRV |
|---|---|
| Estómago/duodeno proximal PRV | Estómago y segmentos 1–2 del duodeno + 0,3 cm (0,5 cm para interfaz larga con el blanco) |
| Intestino delgado PRV | Resto del intestino delgado + 0,3 cm (0,5 cm para interfaz larga) |
Aplicable para dosis ≥ 60 Gy en 25 fracciones o equivalente en BED. Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.2)
Planificación adyuvante post-pancreatectomía
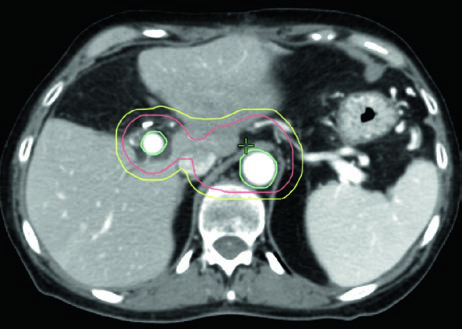
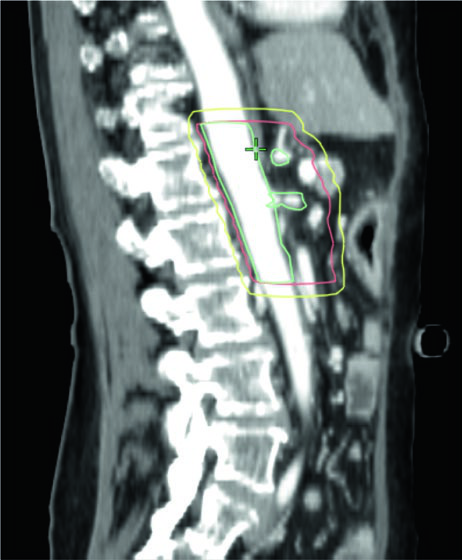
El diseño de campos adyuvantes sigue el atlas de contorneo del RTOG 0848, construido alrededor de regiones de interés (ROIs) seleccionadas por facilidad de identificación y reproducibilidad. Campos más pequeños dirigidos al lecho quirúrgico, CA y AMS pueden ser apropiados en escenarios con OARs limitantes de dosis.
Volúmenes blanco adyuvantes (atlas RTOG 0848)
| Volumen | Definición y descripción |
|---|---|
| GTV | No aplica |
| CTV | Lecho quirúrgico y pancreaticoyeyunostomía (PJ) + cadenas ganglionares peripancreáticas, CA, AMS, paraaórticas, vena porta (tumores de cabeza) y esplénicas (cuerpo/cola). ROIs escalonados del RTOG 0848: • CA (1–1,5 cm proximal) • AMS (2,5–3 cm proximal) • Vena porta (VP: inicio en confluencia VMS/vena esplénica) • PJ • Aorta (superiormente al más cefálico de CA, VP o PJ; inferiormente a L2, o L3 para cubrir GTV preoperatorio) • Lecho tumoral (basado en imagen preoperatoria, informe patológico, clips quirúrgicos) |
| Expansiones | VP, PJ, CA, AMS: 1,0 cm. Aorta: 2,5–3,0 cm derecha, 1,0 cm izquierda, 2–2,5 cm anterior, 0,2 cm posterior. CTV = unión de expansiones, confirmando cobertura del lecho tumoral |
| PTV | Mínimo 0,5 cm; sin ITV en respiración libre, 1–1,5 cm craneocaudal |
Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.3)
Restricciones de dosis para órganos en riesgo
Las restricciones de dosis varían según el esquema de fraccionamiento. La tabla siguiente resume los límites más relevantes para los principales OARs en la planificación pancreática, organizados por número de fracciones. La distinción entre Límite (L — nunca superar) y Guideline (G — restricción sugerida cuando la cobertura no se compromete) resulta clave para la optimización del plan.
| OAR | 5 fracciones | 10 fracciones | 15–25 fracciones |
|---|---|---|---|
| Estómago/duodeno | Dmax ≤ 23 Gy (G); D2cc ≤ 23 Gy (G) | Dmax ≤ 28 Gy (G); D2cc ≤ 28 Gy (G) | Dmax ≤ 40 Gy (G); D2cc ≤ 40 Gy (G) |
| Intestino delgado | Dmax ≤ 23 Gy (G); D5cc ≤ 21 Gy (L) | Dmax ≤ 28 Gy (G); D5cc ≤ 25 Gy (L) | Dmax ≤ 40 Gy (G); D5cc ≤ 25 Gy (L) |
| Intestino grueso | Dmax ≤ 25 Gy (G); D5cc ≤ 25 Gy (L) | Dmax ≤ 30 Gy (G); D5cc ≤ 30 Gy (L) | Dmax ≤ 45 Gy (L) |
| Hígado* | Dmean < 15 Gy; V15 < 700 cc (L) | Dmean < 16 Gy; V16 < 700 cc (L) | Dmean < 20 Gy; V20 < 700 cc (L) |
| Riñones (cada uno) | V10 < 50%; D < 10 cc (L) | V10 < 50%; D < 10 cc (L) | V20 < 50%; Dmean (L) |
| Riñón único | D5cc < 16 Gy (L) | D5cc < 16 Gy (L) | D5cc < 20 Gy (L) |
| Médula espinal | Dmax < 18 Gy (L) | Dmax < 18 Gy (L) | Dmax < 35–45 Gy (L) |
| Conductos hepáticos/biliares | Dmax ≤ 40 Gy (G) | Dmax ≤ 55 Gy (G) | Dmax ≤ 70–80 Gy (G) |
| Esófago | Dmax ≤ 25 Gy (G) | Dmax ≤ 30 Gy (G) | Dmax ≤ 45–65 Gy (G) |
L = Límite (no debe superarse); G = Guideline (restricción sugerida). *Hígado: si no hay cirrosis, usar restricciones inferiores. Fuente: Target Volume Delineation and Field Setup, 2nd Edition (Table 16.4)
Un matiz importante: cuando el PTV se superpone a un OAR crítico, entra en vigor la restricción «si hay solapamiento». Para el estómago, por ejemplo, el D5cc con solapamiento puede limitarse a 30 Gy en 5 fracciones o 33 Gy en 10 fracciones. Este nivel de detalle marca la diferencia entre un plan que entrega dosis ablativa y uno que se queda corto.
Integración práctica: del diagnóstico al plan final
La selección del fraccionamiento en cáncer pancreático nunca es puramente académica. Tres factores determinan el esquema óptimo: la intención de tratamiento (preoperatorio, adyuvante o definitivo), la tecnología disponible (gating, CBCT, fiduciales) y la anatomía específica del paciente — en particular, la extensión de la interfaz tumor-OAR.
En la práctica, el flujo de trabajo comienza con la evaluación de resecabilidad. Los tumores borderline reciben esquemas de dosis más baja (25–50,4 Gy) con márgenes CTV generosos de al menos 1 cm y cobertura de cadenas vasculares. Los tumores irresecables son candidatos a dosis ablativa (BED₁₀ ≥ 100 Gy), pero la viabilidad depende directamente de la capacidad de excluir OARs del PTV de alta dosis con márgenes de seguridad adecuados. El escenario adyuvante, sin GTV a delinear, sigue el atlas estandarizado del RTOG 0848 con sus expansiones específicas por ROI.
Para quienes planifican casos de cáncer gástrico o hepatocarcinoma, muchas de las restricciones de OARs y principios de control de movimiento se solapan significativamente — la consulta cruzada resulta valiosa.
Referencias
- Reyngold M, Parikh P, Crane CH. Ablative radiation therapy for locally advanced pancreatic cancer: techniques and results. Radiat Oncol. 2019;14(1):95.
- Goodman KA, Regine WF, Dawson LA, et al. Radiation Therapy Oncology Group consensus panel guidelines for the delineation of the clinical target volume in the postoperative treatment of pancreatic head cancer. Int J Radiat Oncol Biol Phys. 2012;83(3):901–8.